文档内容
2023—2024 学年度(上)阶段性考试(一)
理科综合
高 2021 级
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 K-39 Cu-64 Cl-35.5 Mn-55 Al-27
一、选择题:本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只
有一项是符合题目要求的。
1.葡萄糖、氨基酸、核苷酸是细胞生命活动离不开的重要物质。下列有关叙述错误的
是( )
A.葡萄糖是细胞呼吸最常用的能源物质
B.氨基酸不能与双缩脲试剂成紫色反应
C.核苷酸是细胞内遗传信息的携带者
D.细胞内三种物质都不具有物种特异性
2.沙眼衣原体是一类原核生物,有较复杂的、能进行一定代谢活动的酶系统,但不能
合成高能化合物,营严格的细胞内寄生。下列说法正确的是( )
A.沙眼衣原体是独立的生命系统,其系统的边界是细胞壁
B.沙眼衣原体细胞内含有DNA,以无丝分裂方式繁殖
C.沙眼衣原体细胞内的某些蛋白质可通过核孔进入细胞核
D.沙眼衣原体不能合成高能化合物的原因可能是无相关的酶
3.将洋葱鳞片叶外表皮细胞置于0.3g/mL的蔗糖溶液中会发生质壁分离,然后再置于
清水中会发生质壁分离的复原。在上述全过程中,下列说法错误的是( )
A.细胞液浓度先变大再变小,细胞吸水能力先变大再变小
B.若采用更高浓度的蔗糖溶液进行实验,置于清水中可能不会发生复原现象
C.发生质壁分离的过程中,细胞液浓度小于细胞质基质浓度小于蔗糖溶液浓度
D.若将0.3 g/mL的蔗糖溶液更换为0.3 g/mL的葡萄糖溶液,则实验开始时质壁分离
的速率更慢
4.胃内的酸性环境是通过质子泵维持的,质子泵催化1分子的ATP水解所释放的能量,
可驱动1个H+从胃壁细胞进入胃腔和1 个K+从胃腔进入胃壁细胞,K+又可经通道蛋白顺
浓度进入胃腔。下列相关叙述正确的是( )
A.K+进入胃腔消需要耗能量
B.H+从胃壁细胞进入胃腔的方式是主动运输
C.胃壁细胞内K+的含量不会影响细胞内液渗透压的大小
D.K+进出胃壁细胞的跨膜运动运输方式是相同的
5.下列关于科学研究的叙述中,错误的是( )
A.萨顿采用类比推理法,证明了基因位于染色体上
B.运用对比实验法,来探究酵母菌的细胞呼吸方式
C.用荧光标记法,来证明细胞膜具有一定的流动性
D.用差速离心法,来研究细胞器的组成成分及功能
6.荠菜的果实形状由两对独立遗传的等位基因控制,已知三角形基因(B)对卵形基因(b)
高三理科综合试卷第1页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}为显性,但当另一圆形显性基因(A)存在时,基因 B 和 b 都不能表达。现有一对亲本杂
交,后代的分离比为圆形∶三角形∶卵形=4∶3∶1,则该亲本的基因型可能为( )
A. aabb×Aabb B.AaBb×Aabb C.AaBb×aaBb D.AaBb×aabb
7、化学与生活密切相关,下列有关说法错误的是
A.电子跃迁到激发态过程中释放能量产生紫色光—钾盐可用作紫色烟花的原料
B.75%浓度的酒精、含氯消毒剂、过氧乙酸均可以有效灭活新型冠状病毒
C.“嫦娥五号”着陆器在月面展示的国旗主要材料为国产高性能芳纶纤维,属于新型
有机高分子材料
D.海水资源的综合利用涉及制盐、制取镁和溴等,其过程中部分涉及氧化还原反应
8、N 为阿伏伽德罗常数的值。下列说法正确的是
A
A.1molCH中含电子数目为10N
3 A
B.l mol S和l mol Cu反应,电子转移数是2N
A
C.在电镀铜的过程中,当阳极质量减轻32g时,转移电子数目为N
A
D.标准状况下,22.4L新戊烷含有的共价键总数为16N
A
9、离子方程式正确的是
A.硫氰化铁溶液中加NaOH溶液产生沉淀:Fe3++3OH—=Fe(OH) ↓
3
B.1mol 乙酸(忽略挥发损失)与足量的 C H 18OH 在浓硫酸作用下加热,充分反应可生
2 5
成N 个 CH CO18OCH
A 3 2 5
C.少量SO 通入Ca(ClO) 溶液中:Ca2++ClO—+SO+H O=CaSO ↓+Cl-+2H+
2 2 2 2 4
D.向1LamolL1的FeBr 溶液中通入amolCl 充分反应:
2 2
2Fe22Cl 2Br 2Fe34ClBr
2 2
10、W、X、Y、Z 为原子序数依次增大的四种短周期元素,A、B、C、D 为上述四种元素
中的两种或三种所组成的化合物,E为单质。已知室温下,0.1molL1A的水溶液pH为
1,B 分子中含有10 个电子,D 具有漂白性,可以用B 的浓溶液去检验E 是否泄漏,五
种化合物间的转化关系如图所示。下列说法正确的是
A.X、Y形成的二元化合物只有两种
B.Z元素在同周期元素中半径最小
C.D中各原子均满足最外层8e稳定结构
D.W、Y组成化合物的沸点一定低于W、Z组成化合物的沸点
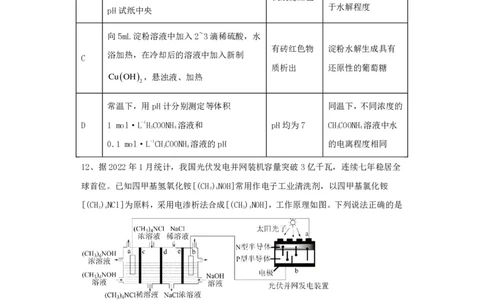
11、化学是以实验为基础的科学。下列实验的操作、现象和结论都正确的是
选
实验操作 实验现象 实验结论
项
高三理科综合试卷第2页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}导体左端下
将等质量镁丝、 沉,右端上
A 升,并且溶 金属性:Mg>Al
液中在铝上
铝丝和导体按图示连接好,放入NaOH溶液
有气泡冒出
中,并使导体处于平衡状态
剪一小段pH试纸放在洁净的玻璃片上,用
溶液呈酸性,说明
液滴周围pH
B 洁净干燥的玻璃棒蘸取NaHSO 溶液点在 HSO的电离程度大
3 3
试纸变红色
于水解程度
pH试纸中央
向5mL淀粉溶液中加入2~3滴稀硫酸,水
有砖红色物 淀粉水解生成具有
浴加热,在冷却后的溶液中加入新制
C
质析出 还原性的葡萄糖
CuOH ,悬浊液、加热
2
常温下,用pH计分别测定等体积 同温下,不同浓度的
D 1 mol·L-1HCOONH 溶液和 pH均为7 CHCOONH 溶液中水
3 4 3 4
0.1 mol·L-1CHCOONH 溶液的pH 的电离程度相同
3 4
12、据2022年1月统计,我国光伏发电并网装机容量突破3亿千瓦,连续七年稳居全
球首位。已知四甲基氢氧化铵[(CH )NOH]常用作电子工业清洗剂,以四甲基氯化铵
3 4
[(CH )NCl]为原料,采用电渗析法合成[(CH) NOH],工作原理如图。下列说法正确的是
3 4 3 4
A.c为阳离子交换膜,d、e均为阴离子交换膜
B.光伏并网发电装置中N 型半导体为正极
C.制备182g (CH)NOH,两极共产生33.6L气体(标准状况)
3 4
D.保持电流恒定,升高温度可加快合成四甲基氢氧化铵的速率
13、湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒
n(AgCl-)
的分布系数δ [如δ (AgCl)= 2 ] 随lgc(Cl-)的变化曲线如图所示。已知:
2 n (含Ag微粒)
总
lg[K (AgCl)]=-9.75。下列叙述错误的是
sp
高三理科综合试卷第3页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}A.AgCl溶解度随c(Cl-)增大而不断减小
B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1
C.25℃时,AgCl+Cl- AgCl2的平衡常数K=100.2
2 3
D.当c(Cl-)=10-2mol•L-1时,溶液中c(AgCl)>c(Ag+)>c(AgCl2)
2 3
二、选择题:本题共8小题,每小题6分,共48分。在每小题给出的四个选项中,第
14~18题只有一项符合题目要求,第19~21题有多项符合题目要求。全部选对的得 6分,
选对但不全的得3分,有选错或不答的得0分。
14.关于开普勒行星运动定律,下列说法正确的是( )
A.太阳系所有的行星都绕太阳做匀速圆周运动
a3
B.在 k中,k 是与太阳质量有关的常量
T2
C.对任意一个行星,它在远日点的速度都要大于近日点的速度
D.开普勒行星运动定律仅适用于行星绕太阳运动
15.每个工程设计都蕴含一定的科学道理。如下图的两种家用燃气炉架都有四个爪,若
将总质量为m的锅放在图乙所示的炉架上,忽略爪与锅之间的摩擦力,设锅为半径为R
的球面,则每个爪与锅之间的弹力( )
1 1
A.等于 mg B.小于 mg
4 4
C.R越大,弹力越大 D.R越大,弹力越小
16.如图所示,在粗糙水平地面上放着一个截面为四分之一圆弧的柱状物体A,A的左
侧紧靠竖直墙,A与竖直墙之间放一光滑圆球B,整个装置处于静止状态。若把A向右
移动少许后,它们仍处于静止状态,则( )
A.墙受到的压力大小不变 B.A与B之间的作用力减小
C.A受到的摩擦力增大 D.A与地面之间的压力减小
17.滑雪运动是2022年北京冬季奥运会主要的比赛项目。如图所示,水平滑道上运动
员A、B间距x 10m。运动员A以速度v 5m/s向前匀速运动。同时运动员B以初
0 0
速度v 8m/s向前匀减速运动,加速度的大小a2m/s2,运动
1
员A在运动员B继续运动x后追上运动员B,则x的大小为( )
1 1
高三理科综合试卷第4页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}A.4 m B.10 C.16 m D.20 m
18.长为L的细线一端系一质量为m的小球(可视为质点),另一端固定在一光滑锥顶
上,光滑锥顶角为2,轴线在竖直方向,如图甲所示。使小球在水平面内做角速度为
的匀速圆周运动,线的张力为F ,经分析可得F 2关系图像如图乙所示,已知重力
T T
加速度为g,则( )
g
A.amgsin B.b
Lcos
m
C.图线1的斜率k mLsin D.图线2的斜率k
1 2 L
19.如图所示,劲度系数不同的两个轻质弹簧a、b悬挂了质量为m 和m 两块橡皮泥,
1 2
整个装置保持静止时,弹簧a的长度与弹簧b的长度相等;已知m 3m ,重力加速度
2 1
为g,则( )
A.弹簧a的弹力比弹簧b的弹力大
B.在m 上取△m粘在m 处,弹簧a长度变短,弹簧b长度变长
1 2
C.剪断弹簧a瞬间,质量为m 和m 的橡皮泥的加速度大小都为g,方向竖直向下
1 2
D.剪断弹簧b瞬间,质量为m 的橡皮泥加速度大小为3g,方向竖直向上,质量为m 的
1 2
橡皮泥加速度大小为g,方向竖直向下
20.如图,A、B两个物体相互接触,但并不黏合,放置在水平面上,水平面与物体间
的摩擦力可忽略,已知m 4kg,m 6kg。从t0开始,推力F 和拉力F 分别作用
A B A B
于A、B上,F 、F 随时间的变化规律为:F 82tN,
A B A
F 22tN。则( )
B
A.t0时,A物体的加速度为2m/s2 B.t0时,A、B之间的相互作用力为4N
C.t2s时,A、B开始分离 D.A、B开始分离时的速度为3m/s
21.如图甲所示,足够长的水平传送带以v=2 m/s的
1
速度沿顺时针方向运行,滑块(视为质点)以某一初速
度v水平滑上传送带的右端。若滑块在传送带上向左运
2
动的过程中,位移与时间比值-时间的图象如图乙所示,
则下列说法正确的是( )
A.v的大小为4 m/s B.滑块在传送带上的加速度大小为2 m/s2
2
C.物块向左的位移为2 m D.滑块在传送带上运动的总时间为2.25 s
高三理科综合试卷第5页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}三、非选择题:共174分,第22~32题为必考题,每个试题考生都必须作答。第33~38
题为选考题,考生根据要求作答。
(一)必考题:共129分。
22.(6分)某同学想通过测绘小灯泡的I-U图像来研究小灯泡的电阻随电压变化的规
律,要求小灯泡两端的电压由零逐渐增加到2.5V,并便于操作。已选用的器材有:
待测小灯泡一只(额定电压为2.5V,电阻约为几欧);
电池组(电动势为3.0V,内阻约1Ω);
电压表一个(量程0~3V,内阻约为3kΩ);
电流表一个(量程0~0.6A,内阻约为0.1Ω);
开关一个、导线若干。
(1)实验中所用的滑动变阻器应选下列中的 。
A.滑动变阻器(最大阻值为10Ω,额定电流为2A)
B.滑动变阻器(最大阻值为1500Ω,额定电流为0.5A)
(2)实验的电路图应选用下列的图( )
(3)实验得到小灯泡的I-U图像如图所示,则可知随着电压的增大,小灯泡的电阻
(填“增大”“减小”或“不变”)。如果将这个小灯泡接到电动势为2.5V,内阻不计
的电源两端,小灯泡消耗的功率为 W。(结果保留2位有效数字)
23.(9分)如图为孙华和刘刚两位同学设计的一个实验装置,用来探究一定质量的小
车其加速度与力的关系。其中电源为50Hz的交流电,一质量为m的光滑滑轮用一轻质
0
细杆固定在小车的前端,小车的质量为M,砂和砂桶的质量为m。
(1)此实验中正确的操作是
A.实验需要用天平测出砂和砂桶的质量m
B.实验前需要将带滑轮的长木板右端垫高,以平衡摩擦力
C.小车靠近打点计时器,应先接通电源,再释放小车
D.为减小系统误差,实验中一定要保证砂和砂桶的质量m远小于小车的质量M
(2)孙华同学以小车的加速度a为纵坐标,力传感器的示数F为横坐标,画出的a—F
图线与横坐标的夹角为θ ,且斜率为k,则小车的质量为
1 2 2 2
A. B. m C. m D.
tan tan 0 k 0 k
(3)刘刚同学实验中测得,拉力传感器显示的示数为4N,打出的部分计数点如图所示
高三理科综合试卷第6页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}(每相邻两个计数点间还有4个点未画出),其中,s = 4.79cm,s = 5.61cm,s = 6.39cm,
1 2 3
s = 7.17cm,s = 7.98cm,s = 8.84cm,则小车的加速度a = m/s²,此
4 5 6
次实验中砂和砂桶的质量m = kg。(重力加速度取9.8m/s²,结果均保留2
位有效数字)
24.(14分)如图,水平桌面上一个质量m0.01kg的物体(视为质点)将弹簧压缩至
A点后由静止释放,在弹力作用下物体获得一向右速度后脱离弹簧,之后从桌子边缘B
点平抛出去,并从C点沿CD方向进入竖直平面内,由斜直轨道CD和圆弧形轨道DEFGH
平滑连接而成的光滑轨道上运动,CD与水平面成37角,EG为竖直直径,FH为水平
直径。已知物块刚好能沿圆轨道经过最高点G,AB间的距离l4m,物体与桌面间的动
摩擦因数0.25,C点距离桌面的水面距离x1.2m,B、C两点间的高度差h 0.45m,
1
C、D两点间的高度差h 1.05m,重力加速度g取10m/s2,sin370.6,cos370.8,
2
求:
(1)弹簧被压缩至A点时的弹性势能E ;
p
(2)圆弧轨道半径R;
(3)当物体从D点进入圆弧轨道后,撤去斜直轨道CD,物体从H点落到水平面的时间
t。
25.(18分)疫情防控期间的“亲子游戏”对家庭成员的身心有很好的调节作用,某家
庭利用新型材料设计了一项户外“亲子游戏”,装置如图所示。新型材料板放置在水平
地面上,质量m 2kg的木块位于材料板的最右端。新型材料板质量m 1kg,长
1 2
L12m,上表面平均分为AB、BC、CD三段,BC段光滑,AB、CD段与木块间的动摩擦
因数均为0.40,材料板与地面间动摩擦因数 0.20,开始材料板和木块均静止。
1 2
家庭成员两人一组,在相等时间内施加外力拉动木块,比较哪组能使木块在材料板上滑
行得更远且不脱离木板。某次游戏中,爸爸用F 12N的水平力向左拉木块,作用2s后
1
撤去,紧接着儿子用竖直向上的力F 20N作用在木块上,2s后再撤去。将木块视为
2
质点,重力加速度g取10m/s2,最大静摩擦力等于滑动摩擦力。求:(计算结果可用分
式表示)
(1)撤掉F 时木块的速度大小v ;
1 1
高三理科综合试卷第7页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}(2)木块在材料板上发生相对滑动的时间t;
(3)整个过程中,材料板在地面上滑行的总距离s。
26.(15分)高锰酸钾具有强氧化性,广泛应用于化工、医药、金属冶炼等领域。实验
室可通过固体碱溶氧化法制备高锰酸钾。回答下列问题:
(1)称取2. 5 Cl (Mr=122.5)和5.0 (Mr=56),置于铁坩埚中并混合均匀,
加热混合物至熔融。加热铁坩埚时,除图中的部分仪器外,还需要_______(填仪器名称),
不使用瓷坩埚的原因是_______________________。
(2)将 . 8 (Mr=87)分多次加入熔融物中,继续加热,反应剧烈,最终得到墨绿
2
色 。该步反应的化学方程式为__________________________,分多次加入 的
2 2
原因是___________________。
(3)待铁坩埚冷却后,将其置于蒸馏水中共煮至固体全部溶解。趁热向浸取液中通入C ,
2
使 歧化为 与 ,该反应的化学方程式为___________。静置片刻,抽滤。
2 2
该步骤若用 Cl代替C ,可能的后果是_______________________。
2
(4)水浴加热滤液至出现 晶膜,冷却后抽滤、干燥晶体。在该实验中采用水浴加热
的主要优点是___________。下表是部分化合物溶解度随温度变化的数据,步骤(3)中C
2
不宜通入过多,目的是___________,产品经纯化后称重,质量为3.60g。本实验中 的
产率为_______%。
温度/℃ 20 30 40 50
C / 110 114 117 121
2
C / 33.7 39.9 47.5 65.6
/ 6.4 9.0 12.6 16.9
27.锑(Sb)可用作阻燃剂、电极材料、催化剂等物质的原材料。一种以辉锑矿(主要成
分为Sb S ,还含有FeO 、AlO 、SiO 等)为原料提取锑的工艺如下:
2 3 2 3 2 3 2
高三理科综合试卷第8页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}已知:溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Al3+ Fe2+
开始沉淀时(c=0.01mol·L-1)的pH 2.2 3.7 7.5
完全沉淀时(c=1.0×10-5mol·L-1)的pH 3.2 4.7 9.0
回答下列问题:
(1)“溶浸”时氧化产物是S,Sb S 被氧化的化学方程式为_____________________。
2 3
(2)“还原”时加入Sb的目的是将_____________________还原,提高产物的纯度。
( )“水解”时需控制溶液pH=2.5。
①Sb3+发生水解的离子方程式为_____________________。
②为避免水解产物中混入Fe(OH),Fe3+浓度应小于______mol·L-1。
3
( )“滤液”中含有的金属阳离子有______。向“滤液”中通入足量______ (填化学式)
气体,再将滤液pH调至3.5,可析出Fe(OH) 沉淀。将沉淀溶于浓盐酸后,产物可返回
3
_______________工序循环使用。
(5)Sb可由SbCl —电解制得,阴极的电极反应式为_____________________。
4
28.碳达峰、碳中和是现在需要继续完成的环保任务,C 的综合利用成为热点研究对
象,C 作为碳源加氢是再生能源的有效方法,C 加氢可以合成甲醇,Olah提出“甲醇
经济”概念,认为甲醇会在不久的将来扮演不可或缺的角色,通过C 加氢生产甲醇是
有希望的可再生路线之一,该过程主要发生如下反应:
反应Ⅰ:C C
反应Ⅱ:C C =- 1.1 mol
2
(1)①相关键能如下表,则 = ,该反应的活化能 (填“大
1 (正) (逆)
于”“小于”或“等于”)。
化学键 C C
键能 mol 436 1071 464 803
高三理科综合试卷第9页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}②若K、K分别表示反应Ⅰ、反应Ⅱ的平衡常数,则C C 的平衡
1 2
常数K=______ (用含K、K的代数式表示)。
1 2
③已知C C 的正反应速率 = c C c ( k为正反
正 2 2
应的速率常数),某温度时测得数据如下:
C mol L mol L mol L m
正
1 0.02 0.01
2 0.02 0.02 a
则此温度下表中a=______。
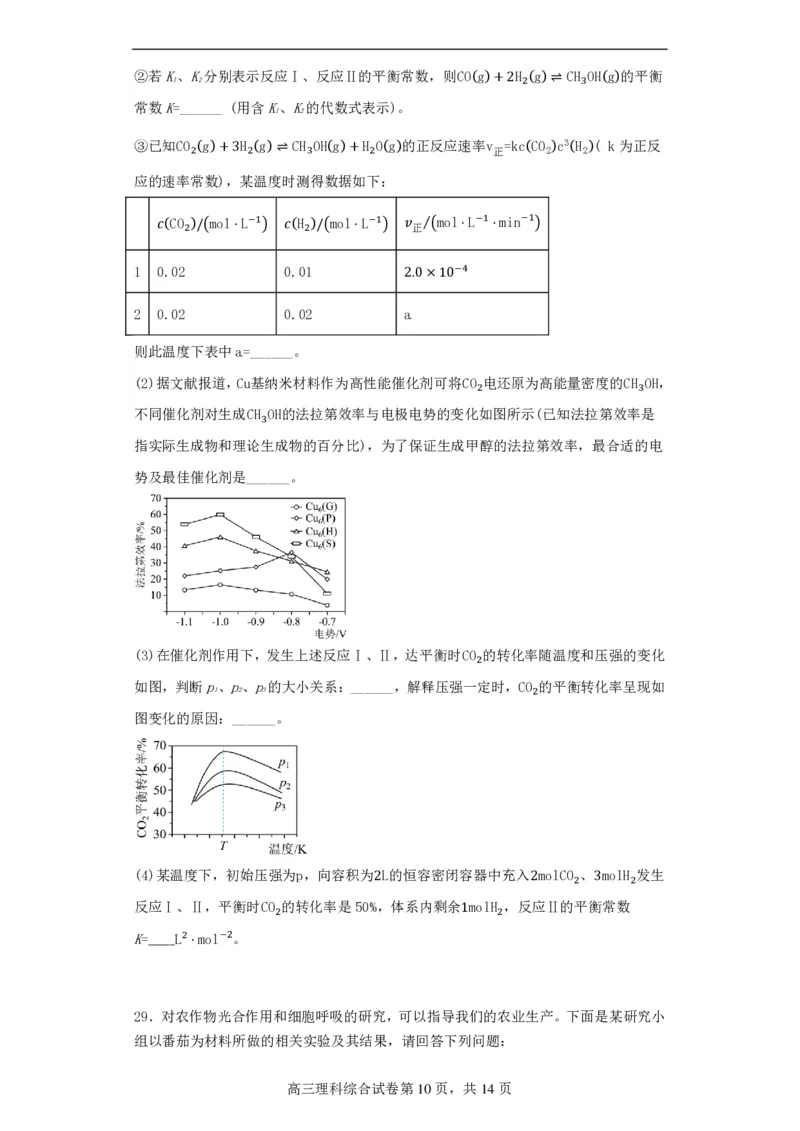
(2)据文献报道,C 基纳米材料作为高性能催化剂可将C 电还原为高能量密度的C ,
不同催化剂对生成C 的法拉第效率与电极电势的变化如图所示(已知法拉第效率是
指实际生成物和理论生成物的百分比),为了保证生成甲醇的法拉第效率,最合适的电
势及最佳催化剂是______。
(3)在催化剂作用下,发生上述反应Ⅰ、Ⅱ,达平衡时C 的转化率随温度和压强的变化
如图,判断p、p、p的大小关系:______,解释压强一定时,C 的平衡转化率呈现如
1 2 3
图变化的原因:______。
(4)某温度下,初始压强为 ,向容积为 L的恒容密闭容器中充入 molC 、 mol 发生
反应Ⅰ、Ⅱ,平衡时C 的转化率是50%,体系内剩余 mol ,反应Ⅱ的平衡常数
K= L mol 。
29.对农作物光合作用和细胞呼吸的研究,可以指导我们的农业生产。下面是某研究小
组以番茄为材料所做的相关实验及其结果,请回答下列问题:
高三理科综合试卷第10页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}(1) 由图甲可推知,与 P 点相比,Q 点限制单株光合作用强度的外界因素是
_______________(写出两种),甲实验给我们的启示是在栽培农作物时要注意
__________。
(2) 种植番茄的密闭大棚内一昼夜空气中的CO 含量变化如图乙所示。C~F段,叶绿体
2
内ADP含量最高的地方是______ _,叶绿体内O 的含量将________ ,一昼夜
2
内植株显示出生长现象。依据是
___________________________________________________________________________。
图乙给我们的启示是在密闭大棚内种植作物时要注意__________________。
(3) 将对称叶片左侧遮光、右侧曝光(如图丙),并采用适当的方法阻止两部分之间的物
质和能量的转移。在适宜光照下照射 12 小时后,从两侧截取同等面积的叶片,烘干称
重,分别记为a和b(单位:g)。则(b-a)所代表的是12小时内从右侧截取的部分叶
片 _______________的质量。
(4) 装置丁(如图丁)可用来探究光照强度对光合作用强度的影响。根据该图的材料及设
置,可以确定该实验的因变量应该是____________________ ,而
自变量可以是__________;
30.(9分除标注外每空1分)图1表示细胞内某些有机物的元素组成和功能关系,其
中甲代表图中有机物共有的元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ是生物大分子,X,Y、Z、P分
别为构成生物大分子的基本单位;图2为核酸的部分结构示意图。回答下列问题:
(1)图中甲代表的元素是________。
(2)纤维素是构成________的主要成分;脂质中除Ⅰ外,还包括________。相同质量
的Ⅴ和Ⅰ彻底氧化分解,Ⅰ释放的能量更多的原因是________(2分)。
(3)Y和Z在组成上的不同主要体现在图2 中________(填序号)上。若图2 为Ⅱ的
部分结构,则④的中文名称是________。
(4)染色体的主要组成成分是图1中的________。SARS病毒的遗传信息储存在图1的
________中。(两空选填Ⅰ~Ⅴ)
31.图1、图2分别表示某种二倍体动物细胞分裂过程中某时期的模式图,图3 表示该
种动物分裂过程中不同时期每条染色体上DNA分子数的变化,图4表示该种动物不同时
期染色体和DNA的数量关系。请据图回答下列问题:
高三理科综合试卷第11页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}(1)图1 细胞名称是____________________,含有________条染色单体;图 2 细胞产生
的子细胞名称是__________________。
(2)图 3 中 CD 段形成的原因________________________,发生的分裂方式及时期是
________或__________。
(3)图 2 细胞分裂时期对应图 3 的________段;基因的自由组合定律发生在图 3 的
________段。
(4)有丝分裂过程中不会出现图4中的____________(填字母)。
32 .已知小麦茎秆的高和矮是一对相对性状,由 A/a 控制,且显隐性未知,抗锈病与
感锈病是另一对相对性状,由B/b控制,且抗锈病性状为显性。但两对基因的位置均未
知。育种工作者在试验田中发现甲、乙两株小麦,经自交实验,结果如下表所示。回答
下列问题:
在子一代中的性状及其比例
亲本自交 高秆 矮秆 抗锈病 感锈病
甲:高秆(易倒伏)抗锈病 3/4 1/4 1 0
乙:矮秆(抗倒伏)感锈病 0 1 0 1
(1)通过甲组实验结果可推知:控制性状高秆、矮秆的基因符合分离定律,其依据是
______ ,甲的基因型为________。
(2)判定植株乙是纯合体,因为________________________。
(3)请以子一代为材料,设计杂交实验来确定这两对基因是否位于一对同源染色体上。
简要写出实验思路、预期结果及结论:
实验思路:让子一代中 杂交(1分),
选取杂交子代中的 植株自交(1分),统计自交子代 (1
分)。
预期结果及结论:
① 若自交子代出现 ,则这两对基因位于两对同源
染色体上(2分);② 若自交子代出现 ,则这两对
基因位于一对同源染色体上(2分)。
(二)选考题:共45分。请考生从2道物理题、2道化学题、2道生物题中每科任选一
题作答。如果多做,则每科按所做的第一题计分。
34.[物理——选修3–4](15分)
(1).(5分)一列向左传播的简谐横波,传播速度大小为v=0.6m/s,t=1.9s时波刚传到
高三理科综合试卷第12页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}O点,波形图如图所示,x轴上的P质点横坐标x0.96m,则下列说法中正确的是( )
A.图中O质点运动的方向沿y轴负方向
B.P质点刚开始振动时运动方向沿y轴正方向
C.P质点刚开始振动的时间为t 0.3s
p
D.P质点第一次到达波谷的时间为0.6s
E.P质点的振动周期为0.3s
(2).(10分)某三棱镜的横截面为一直角三角形,如图所示,
6
A90,B30,C60 ,棱镜材料的折射率为 ,入射光沿平行于底面BC
2
的方向射向AB面,经AB面和AC面折射后射出。
(1)求出射光线和AC边的夹角。
(2)为使从AB边入射的光线恰好不能从AC面出射,入射光线的入射角为多少?
35.铝离子电池能量密度高、成本低且安全性高,是有前景的下一代储能电池。铝离子
电池一般采用离子液体作为电解质,几种离子液体的结构如下。
回答下列问题:
(1)基态铝原子的核外电子排布式为_______________________。
(2)基态氮原子的价层电子排布图为__________________________________。
(3)化合物I中碳原子的杂化轨道类型为,化合物II中阳离子的空间构型为__________。
(4)化合物III中O、F、S电负性由大到小的顺序为_______________________。
(5)传统的有机溶剂大多易挥发,而离子液体有相对难挥发的优点,原因是___________。
(6)铝离子电池的其中一种正极材料为AlMn O ,其晶胞中铝原子的骨架如图所示。
2 4
高三理科综合试卷第13页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}① 晶体中与Al距离最近的Al的个数为__________。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐
标,如图中原子1的坐标为( , , ),原子2的坐标为( , , ),则原子3的坐标为
_________。
③已知该晶体属于立方晶系,晶胞参数为apm,阿伏加德罗常数的值为N ,则晶体的密
A
度为__________ ·cm-3(列出计算式)。
37.酵母的蛋白质含量可达自身干重的一半,可作为饲料蛋白的来源。有些酵母可以利
用工业废中醇作为碳源进行培养,这样既可减少污染又可降低生产成本。研究人员拟从
土壤样品中分离该类酵母,并进行大量培养。下图所示为操作流程,请回答下列问题:
(1)配制培养基时,按照培养基配方准确称量各组分,将其溶解、定容后,调节培养
基的 ,及时对培养基进行分装,并进行 灭菌。
(2)取步骤②中不同梯度的稀释液加入标记好的无菌培养皿中,在步骤③中将温度约
(在25℃、50℃或80℃中选择)的培养基倒入培养皿混匀,冷凝后倒置培养。
(3)挑取分离平板中长出的单菌落,按步骤④进行划线。下列叙述合理的有 。
a.为保证无菌操作,接种针、接种环使用前都必须灭菌
b.划线时应避免划破培养基表面,以免不能形成正常菌落
c.挑取菌落时,应挑取多个菌落,分别测定酵母细胞中甲醇的含量
d.可以通过逐步提高培养基中甲醇的浓度,获得甲醇高耐受株
(4)分离培养酵母菌通常使用 (填“牛肉膏蛋白胨”“ S”或“麦芽汁琼
脂”)培养基,步骤⑤中,为使酵母数量迅速增加,培养过程中需保证充足的营养和
供应。为监测酵母的活细胞密度,将发酵液稀释1 000倍后,经等体积台盼蓝染液染色,
用25×16型( 即中格25,每一个中格有16个小格 ,计数室体积为1mm×1mm×0.1mm)
血细胞计数板计数5个中格中的细胞数,理论上 色细胞的个数应不少
于 ,才能达到每毫升 ×109个活细胞的预期密度。
高三理科综合试卷第14页,共14页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}高三理综试题 第15页共 页
{#{QQABLYCUgggoAABAAAhCAwmwCEGQkBGACIoGwFAEIAAAABNABAA=}#}