文档内容
第一章 原子结构与性质
第一节 原子结构
第2课时 构造原理与电子排布式 电子云与原子轨道
培优第一阶——基础过关练
1.(2022·江苏苏州·高二期末)符号“2p”没有给出的信息是
A.能级 B.电子层
C.电子云形状 D.电子云在空间的伸展方向
2.(2022·吉林油田第十一中学高二期末)表示一个原子在M能层上有10个电子,可以写成
A.3p6 B.3d10 C.3s23p63d2 D.3s23p64s2
3.(2022·浙江·高二期末)下列属于基态Na原子的电子排布式的是
A.1s22s22p6 B.1s22s22p53s2
C.1s22s22p33p1 D.1s22s22p63s1
4.(2022·天津东丽·高二期末)图A和图B分别是1s电子的概率密度分布图和电子云轮廓图。下列有关
说法正确的是
A.图A中的每个小黑点表示1个电子
B.图B表示1s电子只能在球体内出现
C.图A中的小黑点的疏密表示电子在核外空间某处单位体积内出现机会的多少
D.图B表明1s电子云轮廓图呈圆形,有无数对称轴
5.(2022·陕西西安·高二期末)下列说法不正确的是
A.原子核外电子排布,先排满 层再排 层、先排满 层再排 层
B.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道
C.2p、3p、4p的轨道形状均为哑铃形
D.各能层含有的原子轨道数为 (n为能层序数)
6.(2022·四川省绵阳第一中学高二阶段练习)下列电子排布中,原子处于激发状态的是
A.
B.
C.
D.7.(2022·河南·周口市文昌中学高二阶段练习)某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法中
不正确的是
A.该元素原子中共有25个电子 B.该元素原子核外有4个能层
C.该元素原子最外层共有7个电子 D.该元素原子M能层共有13个电子
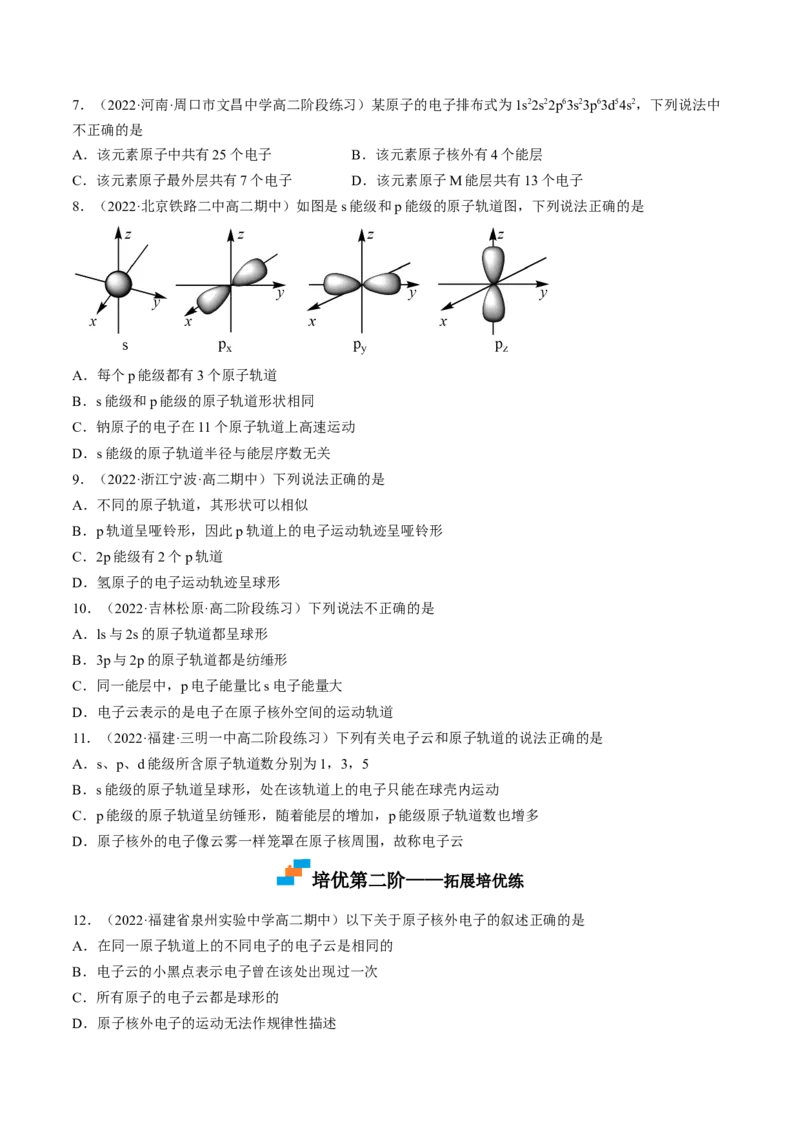
8.(2022·北京铁路二中高二期中)如图是s能级和p能级的原子轨道图,下列说法正确的是
A.每个p能级都有3个原子轨道
B.s能级和p能级的原子轨道形状相同
C.钠原子的电子在11个原子轨道上高速运动
D.s能级的原子轨道半径与能层序数无关
9.(2022·浙江宁波·高二期中)下列说法正确的是
A.不同的原子轨道,其形状可以相似
B.p轨道呈哑铃形,因此p轨道上的电子运动轨迹呈哑铃形
C.2p能级有2个p轨道
D.氢原子的电子运动轨迹呈球形
10.(2022·吉林松原·高二阶段练习)下列说法不正确的是
A.ls与2s的原子轨道都呈球形
B.3p与2p的原子轨道都是纺缍形
C.同一能层中,p电子能量比s电子能量大
D.电子云表示的是电子在原子核外空间的运动轨道
11.(2022·福建·三明一中高二阶段练习)下列有关电子云和原子轨道的说法正确的是
A.s、p、d能级所含原子轨道数分别为1,3,5
B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
C.p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道数也增多
D.原子核外的电子像云雾一样笼罩在原子核周围,故称电子云
培优第二阶——拓展培优练
12.(2022·福建省泉州实验中学高二期中)以下关于原子核外电子的叙述正确的是
A.在同一原子轨道上的不同电子的电子云是相同的
B.电子云的小黑点表示电子曾在该处出现过一次
C.所有原子的电子云都是球形的
D.原子核外电子的运动无法作规律性描述13.(2022·湖北·高二阶段练习)某基态原子的所有含电子的能层中,其最高能层所含电子最少,且基态
原子核外有15种不同空间运动状态的电子,则该原子的元素符号可能是
A.K B.Sc C.Cu D.Ga
14.(2022·河南·许昌市普通教育教学研究室高二期末)下列基态电子排布式中错误的是
A.Ne、1s22s22p6 B. S2-、1s22s22p63s23p6
C.Ca2+、1s22s22p63s23p6 D.F、1s22s12p6
15.(2022·四川自贡·高一期末)已知某元素的基态原子的价电子排布式为 ,则下列说法正确的是
A.该元素的基态原子的最外层电子数是4
B.该元素的原子序数为6
C.该元素的基态原子的轨道数为4
D.该元素的基态原子的M层上共有6种不同运动状态的电子
16.(2021·福建·上杭县才溪中学高二期中)某元素原子的外围电子排布是4s24p5,该元素或其化合物不可
能具有的性质是
A.该元素单质能与水发生反应 B.该元素的最高化合价呈+7价
C.该元素最高价氧化物的水化物显酸性 D.该元素气态氢化物的热稳定性比HCl强
17.(2022·云南省通海县第三中学高二期末)下列给出的基态原子的电子排布式,其中正确的是
A. Na:1s22s22p7 B. Ag:1s22s22p63s23p63d104s24p64d95s2
11 47
C. Ca:1s22s22p63s23p63d2 D. Br:[Ar]3d104s24p5
20 35
18.(2022·黑龙江·双鸭山一中高二阶段练习)下列表述正确的是
A.各能级的原子轨道数按s、p、d、f的顺序依次为1、3、5、7
B.基态Se的价电子排布式:3d104s24p4
C.基态铍原子最外层电子的电子云图为:
D.电子仅在激发态跃进到基态时才会产生原子光谱
19.(2022·陕西·周至县第四中学高二阶段练习)请根据构造原理,按要求写出下列电子排布式或原子结
构示意图:
(1) S的电子排布式_______。
16
(2) Na的次外层电子排布式_______。
10
(3) Ca的最高能层的电子排布式_______。
20
(4) Fe的简化电子排布式_______。
26
(5) Co的原子结构示意图_______。
27
(6) Fe3+的电子排布式_______。
26
(7) As的简化电子排布式为_______。
3320.(2021·吉林·长春市第二十九中学高二期末)(1)s电子的原子轨道呈___________形,每个s能级有
___________个原子轨道;p电子的原子轨道呈___________形,每个p能级有___________个原子轨道。
(2) 基态铝原子核外共有___________种不同能级的电子,有___________种不同运动状态的电子。
21.(2022·福建省宁化第六中学高二阶段练习)某元素的基态原子外层的电子排布为4s1。
(1)若该元素为主族元素,则该元素的元素符号为_______,写出该元素基态原子的电子排布式_______。
(2)若该元素的原子中3d轨道上有5个电子,则该元素符号为_______,其价电子排布式为_______,位于
周期表中第_______周期_______族。
22.(2021·四川省安岳县兴隆中学高二阶段练习)回答下列问题:
(1)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为
_______;其最高价氧化物对应水化物的化学式是_______。
(2)s电子的原子轨道呈_______形,每个s能级有_______个原子轨道;p电子的原子轨道呈_______形,每
个p能级有_______个原子轨道。
(3)元素X的基态原子最外层电子排布式为nsnnpn+1,其p电子云在空间有3个互相_______(填“垂直”或
“平行”)的伸展方向;元素X的名称_______,它的最低价氢化物的电子式是_______。
(4)元素Y的基态原子电子排布式为nsn-1npn+1,则Y的元素符号为_______。