文档内容
第二章 分子结构与性质
第一节 共价键
第2课时 键参数——键能、键长与键角
培优第一阶——基础过关练
1.(2022·陕西西安·高二期末)关于键长、键能和键角,下列说法不正确的是
A.键长越长,键能越大,共价化合物越稳定
B.通过反应物和生成物分子中键能数据可以粗略预测反应热的大小
C.键角是确定多分子立体结构的重要参数
D.同种原子间形成的共价键键长:三键<双键<单键
2.(2022·河南·南阳中学高二阶段练习)下列各组粒子不属于等电子体的是
A.CH 和 B.O 和NO C.NO和CO D.PCl 和
4 3 2 2 2 3
3.(2022·广东·广州市真光中学高二阶段练习)关于键长、键能、键角,下列说法错误的是
A.键角是描述分子空间结构的重要参数
B.键长是形成共价键的两原子的核间距
C.键能:H-I>H-Br>H-Cl
D.键角的大小与键长、键能的大小无关
4.(2022·吉林·高二期末)能够用键能的大小作为主要依据来解释的是
A.稀有气体一般难发生化学反应
B. 分子比 稳定
C.常温常压下氯气呈气态而溴单质星液态
D.C-H键的键能为 ,解离 分子中C-H,需要放出能量为
5.(2022·山西英才学校高二期中)下列有关共价键的键参数的说法不正确的是
A. 、 、 分子中的键角依次增大
B.HF、 、 分子中的键长依次增长
C. 、 、 分子中的键能依次减小
D.分子中共价键的键能越大,分子的熔、沸点越高
6.(2021·四川省南充市嘉陵第一中学高二阶段练习)下列叙述正确的是
A.分子中的键角:CO >HO>CH>NH
2 2 4 3
B.共价键一定有方向性和饱和性
C.两个原子形成共价键时有1个σ键,可能有π键
D.在双键中,σ键的键能小于π键的键能
7.(2021·四川省安岳县兴隆中学高二阶段练习)下列说法中正确的是
A.分子中键能越大,键角越大,则分子越稳定B.元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子可能形成共价键
C.水分子可表示为H-O-H,分子中键角为180°
D.H-O键键能为463KJ/mol,即18gHO分解成H 和O 时,消耗能量为926kJ
2 2 2
8.(2022·陕西·宝鸡市金台区教育体育局教研室高二期中)原子数目和价电子总数都相等的分子或离子互
为等电子体,等电子体具有相似的空间构型。下列各组分子或离子的空间构型相似的是
A.CH 和 B.NO和O C.NO 和O D.HCl和HO
4 2 2 3 2
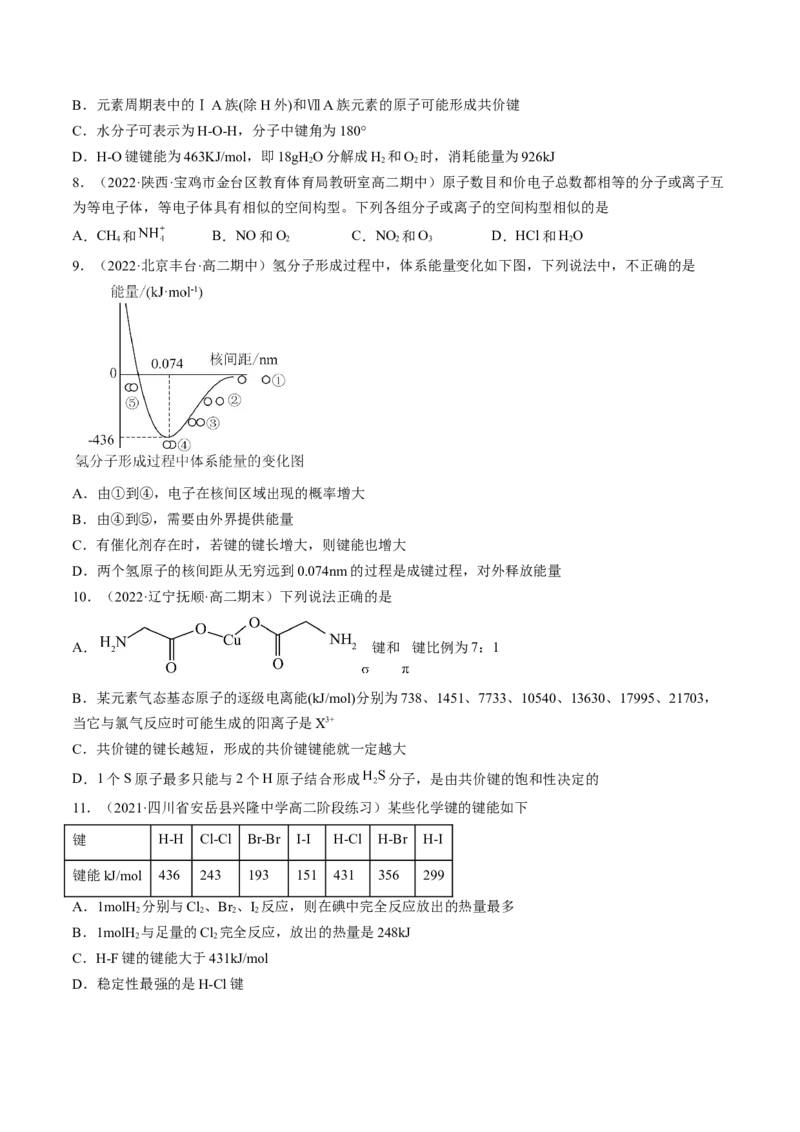
9.(2022·北京丰台·高二期中)氢分子形成过程中,体系能量变化如下图,下列说法中,不正确的是
A.由①到④,电子在核间区域出现的概率增大
B.由④到⑤,需要由外界提供能量
C.有催化剂存在时,若键的键长增大,则键能也增大
D.两个氢原子的核间距从无穷远到0.074nm的过程是成键过程,对外释放能量
10.(2022·辽宁抚顺·高二期末)下列说法正确的是
A. 键和 键比例为7:1
B.某元素气态基态原子的逐级电离能(kJ/mol)分别为738、1451、7733、10540、13630、17995、21703,
当它与氯气反应时可能生成的阳离子是X3+
C.共价键的键长越短,形成的共价键键能就一定越大
D.1个S原子最多只能与2个H原子结合形成 分子,是由共价键的饱和性决定的
11.(2021·四川省安岳县兴隆中学高二阶段练习)某些化学键的键能如下
键 H-H Cl-Cl Br-Br I-I H-Cl H-Br H-I
键能kJ/mol 436 243 193 151 431 356 299
A.1molH 分别与Cl、Br 、I 反应,则在碘中完全反应放出的热量最多
2 2 2 2
B.1molH 与足量的Cl 完全反应,放出的热量是248kJ
2 2
C.H-F键的键能大于431kJ/mol
D.稳定性最强的是H-Cl键培优第二阶——拓展培优练
12.(2022·安徽·青阳第一中学高二阶段练习)根据键能数据(H-Cl 431 kJ/mol,H-I 297 kJ/mol),可得出的
结论是
A.溶于水时,HI比HCl更容易电离
B.HI比HCl熔沸点高
C.HI比HCl稳定
D.拆开等物质的量的HI和HCl,HI消耗的能量多
13.(2022·重庆九龙坡·高二期末)下列排列顺序错误的是
A.键能:C=C>C-C B.键长:Br-Br>Cl-Cl
C.键角: D.极性:F-C>Cl-C
14.(2022·黑龙江·双鸭山一中高二期末)下列说法不正确的是
A.H-F是p-pσ键 B.Cl、Br 、I 的键能依次下降,键长依次增大
2 2 2
C.NH 的键角大于HO的键角 D.共价键的成键原子可以有金属原子
3 2
15.(2022·黑龙江·汤原县高级中学高二期末)下列说法中正确的是
A.单晶硅为分子晶体
B.乙烯分子中,碳原子的sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
C.键长H-F