文档内容
第二章 分子结构与性质
第二节 分子的空间结构
第2课时 杂化轨道理论
培优第一阶——基础过关练
1.在以下的分子或离子中,空间结构的几何形状是三角锥形的是
A.SO B.CH C.CO D.PCl
4 2 3
2.乙烯是石油化学工业的重要原料,其产量可以用来衡量一个国家石油化学工业的发展水平。下列关于
乙烯的说法不正确的是
A.含σ键、π键 B.化学键均为非极性共价键
C.碳原子均采取sp2杂化 D.所有原子均位于同一平面
3.下列叙述中正确的是
A.CS 为V形的极性分子,形成分子晶体
2
B.SiF 和SO 的中心原子均为sp3杂化,SiF 呈正四面体,SO 呈三角锥形
4 4
C.氯化硼(BCl )的熔点为-107 ℃,氯化硼液态时能导电而固态时不导电
3
D.ClO 的空间结构为平面三角形
4.下列分子的中心原子是 杂化的是
A. B. C. D.
5.下列分子中的中心原子杂化轨道的类型相同的是
A.CO 与SO B.C H 与C H C.BeCl 与HO D.CH 与NH
2 2 2 2 2 4 2 2 4 3
6.下列分子的中心原子采用 杂化,但分子的空间结构不同的一组是
① ;② ;③ ;④ ;⑤ ;⑥
A.①②③ B.①⑤⑥ C.②③④ D.③⑤⑥
7.下列关于原子轨道和电子云的表述正确的是
A.s能级和p能级的原子轨道形状相同
B.用原子轨道描述氢分子中化学键的形成:
C. 分子中心原子杂化轨道的电子云轮廊图:
D.乙烯中 键电子云模型:8.下列分子中中心原子的杂化方式和分子的空间构型均正确的是
A.C H:sp2、直线形 B. :sp3、三角锥形
2 2
C.BF:sp3、三角锥形 D.HO:sp3、V形
3 2
9.下列有关分子结构的描述正确的是
A.NH 中心原子为sp2杂化,分子呈三角锥形
3
B.HCHO分子为平面三角形,分子中含3个σ键和一个π键
C.HO的VSEPR模型为V形,能与H+形成配位键
2
D.CH 为正四面体形分子,能与水分子形成分子间氢键
4
10.下列说法正确的是
A.SO 的VSEPR模型与分子的空间结构相同
2
B.HS、NF 、CH 这一组粒子的中心原子杂化类型相同,分子或离子的键角不相等
2 3 4
C. 的电子式为 ,离子呈平面正方形结构,SF 分子是正八面体形
6
D.SO 中心S原子的孤电子对数为0,故其结构为平面三角形
11.科学家从化肥厂生产的(NH )SO 中检出化学式为NH(SO ) 的物质,该物质的晶体中含有SO 和NH
4 2 4 4 4 4 2 4
两种离子,当NH 遇到碱性溶液时,会生成N 分子。下列说法正确的是
4 4
A.14N、N 与N 互为同位素
4 2
B.N 为正四面体结构,键角为109°28′
4
C.NH 与SO 中心原子的杂化方式均为“sp3”杂化
D.(NH )SO 中只含有共价键,不含离子键,属于共价化合物
4 2 4
培优第二阶——拓展培优练
12.甲烷中的碳原子是sp3杂化,下列用*表示碳原子的杂化和甲烷中的碳原子杂化状态一致的是
A.CH≡C*CH B.C*H=CHCH C.CH=C*HCH D.CH=CHC*H
3 2 3 2 3 2 3
13.次氯酸具有很强的氧化性,下列有关说法正确的是
A.该分子的电子式是H:O:Cl B.氧原子与H、Cl都形成π键
C.氧原子发生sp杂化 D.该分子为V形分子
14.下列有关苯分子中的描述不正确的是
A.碳原子均以sp2杂化轨道形成正六边形的碳环,键角为120°
B.每个碳原子还有一个与碳环平面垂直的未参与杂化的2p轨道,相互间以“肩并肩”方式相互重叠,形
成一个大π键
C.6条碳碳键完全等同,共有6个原子处于同一平面
D.每个碳原子的一个 sp2杂化轨道分别与6个H原子的1s轨道重叠形成6条σ键15.下列分子中,杂化类型相同,空间结构也相同的是
A. 、 B. 、 C. 、 D. 、
16.价层电子对互斥理论和杂化轨道理论都可以判断、解释分子或离子的空间构型,下列说法正确的是
A. 和 的键角相同 B. 、 的中心原子价层电子对数相同
C. 、 中S原子的杂化方式相同 D. 、 都是直线形的分子
17.氯化亚砜( )是一种很重要的化学试剂,可以作为氯化剂和脱水剂。下列关于氯化亚砜分子的空
间结构和(S)采取何种杂化方式的说法正确的是
A.三角锥形、 B.三角形、
C.平面三角形、 D.三角锥形、
18.X、Y、Z、Q、E五种元素中,X原子的基态价电子排布式为 ,Y位于元素周期表第二周期第ⅢA
族,Z的两种同位素原子常用于测定文物的年代,Q是元素周期表中电负性最大的元素,E的阳离子通常
存在于明矾和草木灰中。下列说法正确的是
A.第一电离能:
B. 中阴离子中心原子的杂化方式为 杂化
C. 的空间构型为V形
D.原子半径:
19.用VSEPR 理论判断:
物质 孤对电子对数 轨道杂化形式 空间构型
SO _______ _______ _______
3
_______ _______ _______
PO
NCl _______ _______ _______
3
CO _______ _______ _______
2
20.推广磷酸亚铁锂电池的新能源汽车对减少二氧化碳排放和大气污染具有重要意义。工业上用FeCl 、
3
NH HPO 、LiCl及苯胺( )为原料制磷酸亚铁锂材料。回答下列问题:
4 2 4
(1)基态铁原子核外电子运动状态有____种;基态Fe3+较基态Fe2+稳定的原因是____。
(2)在NH HPO 中的N、P、O三种元素的电负性由大到小的顺序是____;NH 的空间构型为____;已知
4 2 4
HPO 与PO 中P原子的杂化方式相同,则HPO 杂化轨道类型为____。
2 2
21.根据物质结构的基本理论,原子之间通过原子轨道的重叠方式,以不同类型的化学键结合,形成具有
不同空间结构的分子或离子,按照已学的物质结构知识填写下列空白。
(1)在 分子中,硼原子的杂化轨道类型为_______,F-B-F的键角是_______, 为_______分子(极性分子或非极性分子)。
(2) 可与 形成 , 中氧原子采用_______杂化。 的立体构型为_______。
(3) 中H-O-H键角比 中H-O-H键角大,原因为_______。
22.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是 )
为原料经合成气(主要成分为 制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、
煤、焦炭为原料制合成气,常因含羰基铁 等而导致以合成气为原料合成甲醇和合成氨等生产过
程中的催化剂产生中毒。请回答下列问题:
(1) 中铁的化合价为0,写出铁原子的基态电子排布式:_______。
(2)与 互为等电子体的分子和离子分别为_____和_______(各举一种即可,填化学式), 分子的电子式
为_______, 分子的结构式可表示成_______。
(3)在 中,碳原子采取 杂化的分子有_______。
(4) 分子中, 中的碳原子采用杂化_______方式, 中的碳原子采取杂化方式_______。
23.钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)基态铜原子的价电子排布式为_______。
(2)CaCO 高温分解可制得CaO。CaO与C在一定条件下可生成电石(CaC ),电石与水反应生成Ca(OH) 和
3 2 2
一种4原子气体分子。
①写出电石与水反应的化学方程式_______;反应制得的气体中通常会含有硫化氢等杂质气体,可用
_______吸收。
②CaCO 中阴离子的空间构型为_______。
3
③该气体分子中σ键与π键的数目之比为_______。
④写出2种与 互为等电子体的分子的化学式_______。
(3)工业上电解CaCl 制Ca而不采用电解CaO的原因是_______。
2
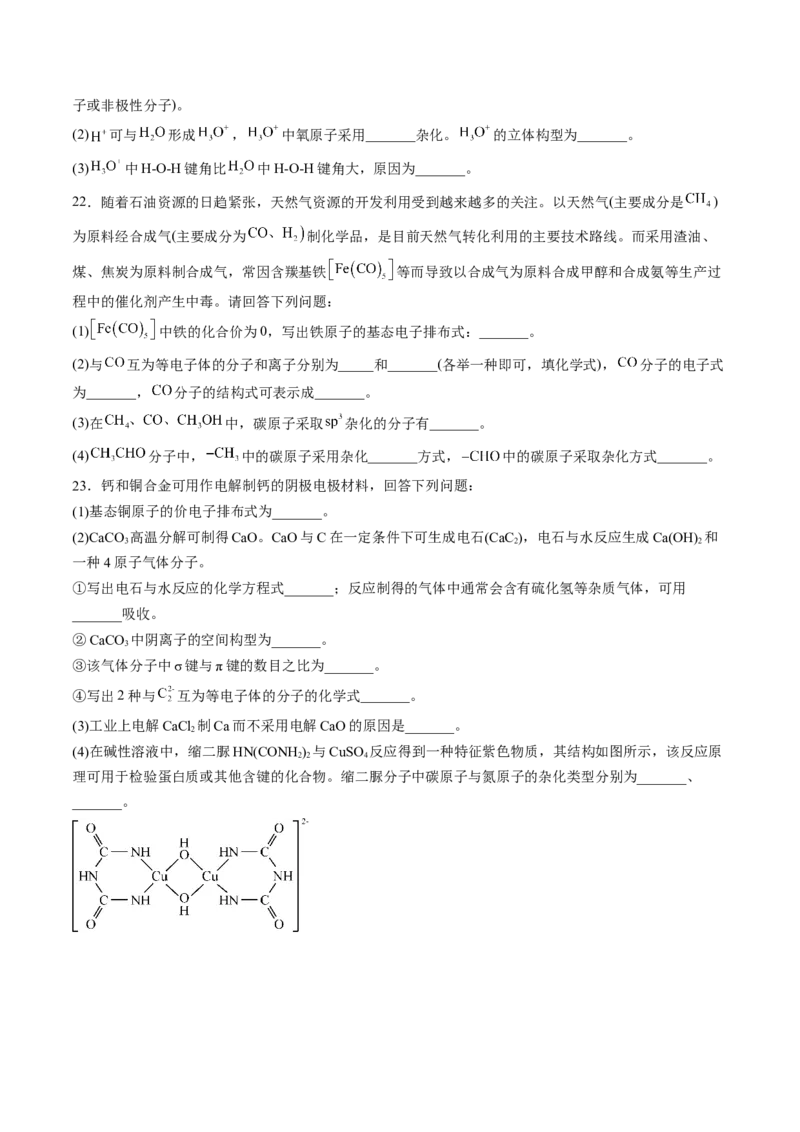
(4)在碱性溶液中,缩二脲HN(CONH ) 与CuSO 反应得到一种特征紫色物质,其结构如图所示,该反应原
2 2 4
理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为_______、
_______。