文档内容
第2章 分子结构与性质
2.3.2 分子间作用力
一.选择题(共11小题)
1.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主
要的相互作用依次是
A.分子间作用力;分子间作用力;非极性键
B.分子间作用力;分子间作用力;极性键
C.分子间作用力;极性键;分子间作用力
D.分子间作用力;分子间作用力;非极性键
【答案】B
【解析】固态水中和液态水中含有氢键和分子间作用力,当雪花→水→水蒸气主要是氢键和分子间作用力被破
坏,但属于物理变化,共价键没有破坏,水蒸气→氧气和氢气,为化学变化,破坏的是极性共价键,故选B。
2.以下关于分子间作用力的叙述不正确的是
A.是一种较弱的化学键
B.分子间作用力较弱,破坏它所需能量较少
C.分子间作用力对物质的熔、沸点有影响
D.稀有气体液化后分子间存在分子间作用力
【答案】A
【解析】
A.分子间作用力不属于化学键,A错误;
B.分子间作用力较弱,破坏它所需能量较少,B正确;
C.分子间作用力不属于化学键,一般对物质熔、沸点有影响,C正确;
D.稀有气体分子间存在分子间作用力,D正确。
答案选A。
3.有下列两组命题
A组 B组
Ⅰ 键键能小于 键键能 比HF稳定
Ⅱ 键键能小于 键键能 比HI稳定
Ⅲ 分子间作用力大于HF分子间作用力 沸点比HF高
Ⅳ 分子间作用力小于HCl分子间作用力 沸点比HCl低B组中命题正确,且能用A组命题加以正确解释的是
A.Ⅰ① B.Ⅱ② C.Ⅲ③ D.Ⅳ④
【答案】B
【解析】
原子半径 ,原子半径越大,键长越长,键能越小,
A. 键键能答于 键键能,HF较稳定,故A错误;
B.HCl比HI稳定,是由于 键键能大于 键键能,故B正确;
C.HF分子间存在氢键,沸点较高,故C错误;
D.HI相对分子之间较大,分子间作用力较强,沸点较高,故D错误.
故选:B。
4.CO 气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO 气体,这两个变化过程中需要克
2 2
服的作用分别是
A.分子间作用力,离子键 B.化学键,分子间作用力
C.化学键,化学键 D.分子间作用力,分子间作用力
【答案】B
【解析】试题分析:CO 气体在一定条件下可与金属镁反应生成氧化镁和碳,属于化学变化,克服的是化学键;
2
干冰在一定条件下也可以形成CO 气体,属于状态的变化,需要克服的是分子间作用力,答案选B。
2
5.CO 气体在一定条件下可与金属镁反应,干冰在一定条件下可以形成CO 气体,这两个变化过程中CO 需要
2 2 2
克服的作用分别是
A.共价键,共价键 B.共价键,分子间作用力
C.分子间作用力,共价键 D.分子间作用力,分子间作用力
【答案】B
【解析】
试题分析:CO 气体在一定条件下可与金属镁反应,生成氧化镁和碳,属于化学变化,需要克服的作用力是共
2
价键、金属键。干冰在一定条件下可以形成CO 气体,属于物理化学,需要克服的作用力是分子间作用力,因
2
此正确的答案选B。
6.下列说法正确的是( )
A.一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越小
B.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作用,称为分子间作用力
C.分子间作用力主要影响物质的化学性质
D.分子间作用力的大小远大于化学键,是一种很强的作用力【答案】B
【解析】
A.一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,A错误;
B.分子内部的相邻原子之间强烈的相互作用称为化学键,而分子之间也存在相互作用,这种作用力比较微弱,
称为分子间作用力,B正确;
C.分子间作用力主要影响物质的物理性质,如熔沸点、溶解性等,C错误;
D.分子间作用力的大小远小于化学键,是一种比较弱的作用力,D错误;
故合理选项是B。
7.下列说法正确的是( )
A. 和NaH中的化学键类型完全相同
B. 、 中,每个原子都满足8电子稳定结构
C.HCl比 稳定是因为分子间作用力前者强于后者
D. 晶体加热熔化时需克服共价键和分子间作用力
【答案】A
【解析】
A. 和NaH都是仅含离子键的离子化合物,A正确;
B. 中B最外层有6个电子,B错误;
C. HCl和 的稳定性与分子内化学键强弱有关,与分子间作用力无关,C错误;
D. 晶体是共价晶体,熔化时需克服共价键,D错误;
答案选A。
8.下列说法正确的是
A.水分子间存在氢键,所以水分子比较稳定
B.HSO 溶于水能电离出H+和SO 2-,所以硫酸是离子化合物
2 4 4
C.I 加热升华过程中只需克服分子间作用力
2
D.SiO 熔化破坏共价键和分子间作用力
2
【答案】C
【解析】
A. 水分子间存在氢键,但氢键影响水的物理性质,不能影响水的化学性质,所以不能由此判断水分子比较稳定,故错误;B. HSO 溶于水能电离出H+和SO 2-,但硫酸是共价化合物,故错误;C. I 加热升华过程中只需克服碘
2 4 4 2
分子之间的分子间作用力,故正确;D. SiO 熔化破坏共价键,故错误;故选C。
2
9.下列说法正确的是
A.CO 溶于水,既破坏了分子间作用力又破坏了共价键
2
B.常温、常压下以液态存在的物质一定都是由分子构成,该液体肯定不导电
C.NH 和Cl 两种分子中,每个原子的最外层都具有8电子稳定结构
3 2
D.HO、HS、HTe分子间作用力依次增大
2 2 2
【答案】A
【解析】A、CO 溶于水,发生CO+HO=HCO,因此即破坏了分子间作用力,又破坏了共价键,故A正确;
2 2 2 2 3
B、Hg常温下为液体,Hg为金属单质,该液体能够导电,故B错误;C、NH 中H原子最外层2个电子,故C
3
错误;D、水分子间存在分子间氢键,分子间用作用力更大,HS、HTe分子间不存在分子间氢键,相对分子质
2 2
量越大,分子间作用力越大,即分子间作用力顺序是HO>HTe>HS,故D 错误。
2 2 2
10.关于氢键,下列说法正确的是
A.氢键比分子间作用力强,所以它属于化学键
B.冰中存在氢键,水中不存在氢键
C.分子间形成的氢键使物质的熔点和沸点升高
D.氢键可以增大物质的化学性质
【答案】C
【解析】
A、氢键比分子间作用力强,比化学键弱很多,选项A错误;
B、冰中存在氢键,水中也存在氢键,选项B错误;
C、氢键较一般的分子间作用力强,含有氢键的物质具有较高的熔沸点,选项C正确;
D、化学性质是由化学键决定的,与氢键无关,选项D错误;
答案选C。
11.中科院国家纳米科学中心科研员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的
本质”这一化学界争论了80多年的问题提供了直观证据。下列有关氢键说法中不正确的是( )
A.由于氢键的存在,冰能浮在水面上
B.由于氢键的存在,乙醇比甲醚更易溶于水
C.由于氢键的存在,沸点:HF>HCl>HBr>HI
D.由于氢键的存在,影响了蛋白质分子独特的结构
【答案】C
【解析】
A.冰中水分子排列有序,含有氢键数目增多,使体积膨胀,密度减小,因此冰能浮在水面上,是分子间存在氢键所致,A正确;
B.乙醇与水分子间存在氢键,增加乙醇在水中的溶解度,所以由于氢键的存在,乙醇比甲醚更易溶于水,B正
确;
C.卤素的氢化物中只有HF含有氢键,卤素的氢化物的沸点:HF>HI>HBr>HCl,C错误;
D.氢键具有方向性和饱和性,所以氢键的存在,影响了蛋白质分子独特的结构,D正确;
故合理选项是C。
二、填空题(共3题)
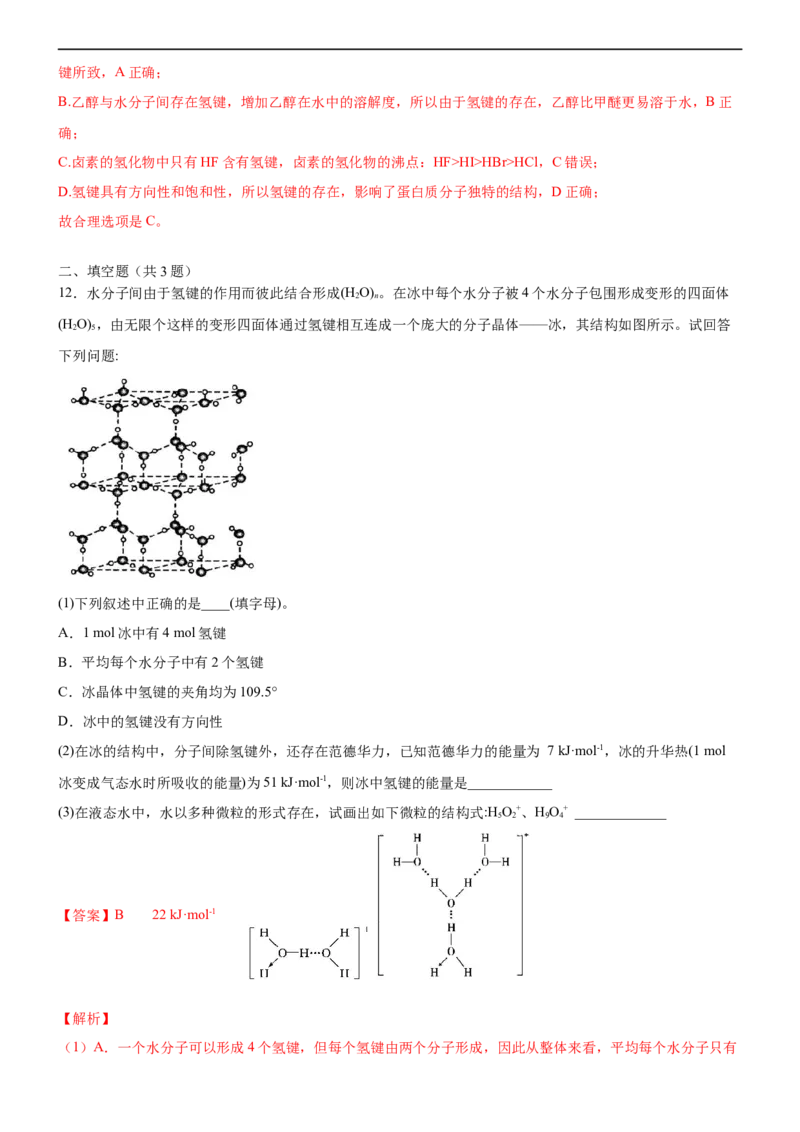
12.水分子间由于氢键的作用而彼此结合形成(H O) 。在冰中每个水分子被4个水分子包围形成变形的四面体
2 n
(H O) ,由无限个这样的变形四面体通过氢键相互连成一个庞大的分子晶体——冰,其结构如图所示。试回答
2 5
下列问题:
(1)下列叙述中正确的是____(填字母)。
A.1 mol冰中有4 mol氢键
B.平均每个水分子中有2个氢键
C.冰晶体中氢键的夹角均为109.5°
D.冰中的氢键没有方向性
(2)在冰的结构中,分子间除氢键外,还存在范德华力,已知范德华力的能量为 7 kJ·mol-1,冰的升华热(1 mol
冰变成气态水时所吸收的能量)为51 kJ·mol-1,则冰中氢键的能量是____________
(3)在液态水中,水以多种微粒的形式存在,试画出如下微粒的结构式:H O+、HO+ _____________
5 2 9 4
【答案】B 22 kJ·mol-1
【解析】
(1)A.一个水分子可以形成4个氢键,但每个氢键由两个分子形成,因此从整体来看,平均每个水分子只有2个氢键,1 mol冰中有2 mol氢键,选项A错误;
B.一个水分子可以形成4个氢键,但每个氢键由两个分子形成,因此从整体来看,平均每个水分子只有2个氢
键,选项B正确;
C、正四面体的夹角为109.5°,但冰中水分子形成的是变形四面体,故冰晶体中氢键的夹角不是109.5°,选项C
错误;
D、由于氢键具有方向性和饱和性,选项D错误;
答案选B;
(2)冰的升华热是51kJ/mol,水分子间还存在范德华力(7kJ/mol),1mol水中含 有2mol氢键,升华热=范德华力
+氢键,代入具体数值,即51kJ/mol=7kJ/mol+2×氢键键能,所以冰晶体中氢键的“键能”是
51kJ/mol-7kJ/mol
=22kJ/mol;
2
(3) H O+可以写成两个水分子以氢键相连,其中一个水分子的O再以氢键连结一个氢离子,书写时将所有原子
5 2
看为一个整体用方括号括起来,“+”放在方括号右上角,即结构式为 ,同理HO+可写成4
9 4
个水分子以氢键相连,其中一个水分子的O再以氢键连结一个氢离子,书写时将所有原子看为一个整体用方括
号括起来,“+”放在方括号右上角,即结构式为 。
13.根据下列要求回答相关问题:
(1)下列物质沸点递变顺序正确的是________(填字母,下同)。
A.SnH >GeH >SiH>CH B.SbH >AsH >PH >NH
4 4 4 4 3 3 3 3
C.HI>HBr>HCl>HF D.HTe>HSe>HS>HO
2 2 2 2
(2)下列过程中:①冰融化成水②HNO 溶于水③NH Cl受热分解,依次克服作用力的类型分别是_______。
3 4
A.氢键、范德华力、离子键 B.氢键、极性键、离子键
C.范德华力、氢键、非极性键 D.范德华力、非极性键、极性键
(3)下列说法正确的是________。
A.氨、氯化氢与水分子都能形成氢键,故极易溶于水B.由于氢键存在,卤化氢中HF最稳定
C.冰的密度小于水,是由于水分子间存在氢键
D.NH 、HO、HF相对分子质量增大,沸点升高
3 2
【答案】A B C
【解析】
(1)A.氢化物的相对分子质量越大,沸点越高,则沸点SnH >GeH >SiH>CH,A正确;
4 4 4 4
B.氢化物的相对分子质量越大,沸点越高,含有氢键的沸点较高,氨气分子间存在氢键,所以沸点:NH >
3
SbH >AsH >PH ,B错误;
3 3 3
C.氢化物的相对分子质量越大,沸点越高,含有氢键的沸点较高,HF分子间存在氢键,所以沸点:HF>HI>
HBr>HCl,C错误;
D.氢化物的相对分子质量越大,沸点越高,含有氢键的沸点较高,水分子间存在氢键,所以沸点:HO>HTe
2 2
>HSe>HS,D错误;
2 2
故选A。
(2)①冰中水分子间存在氢键,所以冰融化成水克服氢键;②HNO 溶于水发生电离,破坏了共价键,所以克
3
服极性键;③NH Cl属于离子晶体,含有离子键,NH Cl受热分解克服离子键;故答案为:B。
4 4
(3)A.氯化氢与水分子之间不形成氢键,氨气与水分子间能形成氢键,A错误;
B.氢化物的稳定性与共价键有关,共价键越强,氢化物越稳定,与氢键无关,B错误;
C.在冰中,由于氢键的作用,水分子间形成正四面体结构,使得水分子间的空隙变大,所以水变冰后体积增
大,密度变小,C正确;
D.NH 、HO、HF分子间存在氢键,沸点高低与氢键有关,所以不能根据相对分子质量大小来判断沸点,D
3 2
错误;
故选C。
14.(1)水分子间存在一种“氢键”(介于范德华力与化学键之间)的作用,彼此结合而形成(HO) 。在冰中每个
2 n
水分子被4个水分子包围形成变形的正四面体,通过氢键相互连接成庞大的分子晶体,其结构示意图如图(1)表
示:①1 mol冰中有______mol 氢键。
②在冰的结构中,每个水分子与相邻的 4个水分子以氢键相连接。在冰晶体中除氢键外,还存在范德华力(11
kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰晶体中氢键的能量是________kJ ·mol-1。
③氨气极易溶于水的原因之一也与氢键有关。请判断 NH 溶于水后,形成的 NH·HO 的合理结构是
3 3 2
__________[填图 (2)中的序号]。
(2)图(3)折线c可以表达出第________族元素氢化物的沸点的变化规律。两位同学对某主族元素氢化物的沸点
的变化趋势画出了两条折线a和b,你认为正确的是:________(填“a”或“b”);部分有机物的熔沸点见下
表:
CH
3
烃 CH CHCH 硝基苯酚
4 3 3
(CH)CH
2 2 3
沸点/℃ -164 -88.6 -0.5 熔点/℃ 45 96 114
由这些数据你能得出的结论是:______________________,______________(至少写2条)。
【答案】 2 20 b ⅣA b 有机物相对分子质量越大,分子间作用力越强,故沸点越高;当有机物能形成
分子内氢键时,分子间作用力减弱,熔点变低 当分子间能形成氢键时,分子间作用力增强,熔点升高
【解析】(1)①根据冰的结构示意图,每个HO分子通过氢键与4个HO分子结合,平均每个HO分子含有氢
2 2 2
键数目为4× =2个,故1mol冰中含2mol氢键,故答案为:2;
②冰的升华热是51kJ/mol,水分子间还存在范德华力(11kJ/mol),1mol水中含有2mol氢键,升华热=范德华力
+氢键,所以冰晶体中氢键的“键能”是20kJ/mol,故答案为:20;
③NH 溶于水后,形成的NH •H O中,NH •H O的电离方程式为NH •H O NH ++OH-,可知结构中含有
3 3 2 3 2 3 2 4
铵根和氢氧根的基本结构,NH •H O的合理结构是b,故答案为:b;
3 2
(2) 折线a和b都由有沸点先小后大,则开始物质的沸点高,与氢键有关,而a中原子序数大的氢化物沸点高于
含氢键的物质,与事实不符,故a错误,b正确;只有c曲线中的物质间没有氢键,则c为碳族元素氢化物,即
折线c可以表达出第ⅣA族元素氢化物的沸点的变化规律;根据表中所给的物质可以看出:有机物的相对分子
质量越大、分子间作用力越强,沸点越高,并且是当有机能形成分子内氢键时,分子间作用力减弱,熔点变低;
当分子间能形成氢键时,分子间作用力增强,熔点升高,故答案为:ⅣA;b;有机物的相对分子质量越大、分
子间作用力越强,故沸点越高;当有机能形成分子内氢键时,分子间作用力减弱,熔点变低或当分子间能形成
氢键时,分子间作用力增强,熔点升高。