文档内容
雅礼中学 2024 届高三综合自主测试(一)
化学参考答案
一、选择题(本题共14小题,每小题3分,共42分)
1、B【解析】“常恐秋节至,焜黄华叶衰”,树叶由绿变黄是树叶中叶绿素分解,被叶绿素
掩盖的红色素、黄色素露出而显红色、黄色,有新物质产生,发生了化学变化,故A正确;
碳纤维是一种新型无机非金属材料,是含碳量在90%以上的高强度高模量纤维,主要成分是
碳的单质,“心忧炭贱愿天寒”中的炭,炭黑的主要成分也为碳,不能互称为同素异形体,
故B错误;酒放置时间长,少量的乙醇被氧化为乙酸,乙酸与乙醇生成乙酸乙酯,乙酸乙酯
等酯类物质具有香味,所以产生香味主要是因为美酒含有酯类物质,故C正确;氮气跟氧气
能直接化合生成无色的一氧化氮气体;一氧化氮不溶于水,在常温下易跟空气中的氧气化合,
生成红棕色的二氧化氮气体;二氧化氮易溶于水,它溶于水后生成硝酸和一氧化氮,硝酸进
一步转化为可以为植物吸收的硝酸盐,增加土壤中氮肥含量,有利于作物生长,故D正确。
V 16.8 L
2、A【解析】A.标准状况下,16.8 L CH 物质的量为n= = =0.75 mol,甲
4 V 22.4 L·mol-1
m
烷和氯气反应除了生成CHCl,还生成CHCl、CHCl 和CCl,故反应生成的CHCl分子数小
3 2 2 3 4 3
m 56 g
于0.75N,故A正确;B.56g铁的物质的量为n= = =1mol,与足量的盐酸反应
A M 56 g/mol
生成1 mol亚铁离子,失去2 mol电子,转移的电子数为2N,故B错误;C.过氧化钠和二
A
氧化碳的反应为过氧化钠的歧化反应,氧元素由-1价歧化为-2价和0价,故1.05molNaO
2 2
转移1.05N个电子;而过氧化钠和SO 反应后氧元素由-1价变为-2价,故1.05 mol过氧
A 2
化钠转移2.1N个电子,故C错误;D.50 mL 18 mol/L浓硫酸的物质的量n=cV=18 mol/L
A
×50×10-3 L=0.9 mol,浓硫酸与足量铜共热,随着反应进行硫酸浓度降低变为稀硫酸,
稀硫酸与铜不反应,所以产生SO 的分子数小于0.45N,故D错误。
2 A
3、A【解析】A.CH CH(CH )CH COOH是羧酸,用系统命名法命名为3-甲基丁酸,故A
3 3 2
正确;B. 可以表示甲烷分子,但是不能表示CCl 分子,因为Cl原子的半径比C原
4
子大,与比例模型中的原子大小不符,故B错误;C.甲醇分子中C原子sp3杂化,O原子
sp3杂化,CHOH分子中,碳原子与氧原子之间形成的共价键类型为sp3-sp3σ键,故C错误;
3
D.基态铍原子电子排布式为1s22s2,最外层电子在s轨道,电子云轮廓是球形的,故D错
误。
4、B【解析】由流程可知,制备冰铜的反应物为CuFeS 和O,产物为CuS、FeO、SO,则方
2 2 2 2
程式为2CuFeS+2O CuS+2FeO+SO,A项正确;铜为29号元素,其基态电子排布式为
2 2 2 2
[Ar]3d104s1,B项错误;电解精炼铜时粗铜为阳极,粗铜中比Cu活泼的金属如Fe等先失电
子发生氧化反应、后Cu失电子发生氧化反应,即阳极反应式为Fe−2e−=Fe2+等、Cu−2e−=Cu2+(主
要),精铜为阴极,阴极电极反应式为Cu2++2e−=Cu,C项正确;SO 的价层电子数为6,价层
2
电子对数为3,价层电子对互斥模型为平面三角形,D项正确。
化学(YL)答案 (第 1 页,共 6 页)
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}5、B【解析】A.根据有机物的结构简式,可知该物质分子式为C H O ,故A不正确;B.该
27 30 16
物质分子中含有多个亲水性的酚羟基、醇羟基,有良好的水溶性,故B正确;C.该物质分
子结构中含有酚羟基和碳碳双键,与溴水能发生苯环上酚羟基的邻对位取代反应和碳碳双键
的加成反应,故C不正确;D.根据该物质分子结构和手性碳原子的定义可知,1分子该物质
含有10个手性碳原子(两个椅式环上的共10个碳原子都是手性碳原子),故D不正确。
6、D【解析】X、Y、Z、Q、R位于同一周期原子序数依次递增,结合图示可知,R形成1个
共价键,Q形成2个共价键,Z、Q的核电荷数之和等于R的最外层电子数的2倍,R不可能
为H,若R为F,Z、Q的核电荷数之和为7×2=14,五种元素位于同一周期,则X为Li、Z
为C、Q为O;若R为Cl,Z、Q的核电荷数之和为17×2=34(舍弃),Y形成4个共价键、
且得到1个电子形成阴离子,其原子序数小于C,Y为B,以此来解答。A.电子层数越多离
子半径越大,电子层数相同时原子序数越大的离子半径越小,则离子半径:X(Li+)<R(F-)
<Q(O2-),正确;B.ZQ 为CO,固态的二氧化碳是干冰,利用CO 晶体易升华的物理性质,
2 2 2
使用CO 跨临界可直接制冰,正确;C.主族元素同周期从左向右非金属性逐渐增强,则元素
2
的非金属性:Z(C)<Q(O)<R(F),正确;D.Y与R形成的化合物为BF,B的最外层电子数为
3
3+3=6,不满足8电子稳定结构,错误。
7、A【解析】A.装置乙为制备氮气的装置,其化学方程式为NaNO+NHCl N↑+NaCl+
2 4 2
2HO,A正确;B.乙装置制备氮气,氮气中混有水蒸气,通过甲装置干燥氮气,干燥的氮气
2
在丙中与BaH 反应制备BaN,BaN 遇水反应,最后用丁防止空气中的水蒸气进入丙中,故
2 3 2 3 2
气流由左向右的字母连接顺序为c→b→a→d→e→g→f或c→b→a→e→d→f→g,B错误;
C.BaN 遇水反应;BaH 在潮湿空气中能自燃,遇水反应,所以用装置甲中的浓硫酸干燥氮气,
3 2 2
用装置丁中的碱石灰吸收空气中的水蒸气,防止水蒸气进入装置丙中,C错误;D.实验时,
先点燃装置乙中的酒精灯,反应一段时间,目的是将用生成的氮气赶走装置中的空气,再点
燃装置丙中的酒精喷灯进行反应,D错误。
8、B【解析】A.NO-在酸性条件下有强氧化性,能将Fe2+氧化为Fe3+,因此选项中加KSCN
3
溶液,溶液变红的原因不一定是Fe(NO) 试样已变质,可能是NO-在酸性条件下将Fe2+氧化
3 2 3
为Fe3+所致,A错误;B.NaCO+CO+HO===2NaHCO,由于NaCO 溶解度大于NaHCO,当NaCO
2 3 2 2 3 2 3 3 2 3
饱和时NaHCO 过饱和,因此向饱和NaCO 溶液中通入CO,溶液变浑浊,是因为产生(析出)
3 2 3 2
NaHCO 晶体,B正确;C.HSO 是蔗糖水解的催化剂,水浴加热5min后所得溶液含HSO,加
3 2 4 2 4
入的少量新制Cu(OH) 与HSO 反应生成CuSO 和HO,即水解液中直接加新制Cu(OH) 悬浊液
2 2 4 4 2 2
不能检验水解产物中是否还有葡萄糖,应在加新制Cu(OH) 悬浊液之前先加入过量的NaOH
2
溶液,C错误;D.向NaHCO 溶液中滴加NaAlO 溶液,因AlO-结合H+能力强于CO2-,故而会
3 2 2 3
发生AlO-+HCO-+HO===Al(OH)↓+CO2-,产生白色沉淀,不产生气体,二者发生的也不是
2 3 2 3 3
双水解反应,D错误。
9、B【解析】A.由反应机理图可知化合物Ⅰ是反应的催化剂,A正确;B.该催化循环过程中
N原子的成键数目始终为3,未发生改变,B错误;C.由机理图可知该催化历程的总反应为
催化剂
2CH+O ===== 2CH+2HO,C正确;D.化合物Ⅶ→化合物Ⅰ的反应中O 转化成HO,属于氧
3 8 2 3 6 2 2 2
化还原反应,D正确。
化学(YL)答案 (第 2 页,共 6 页)
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}10、A【解析】A.氧化石墨烯分子中,有一部分碳原子形成了C—C、C—O键,形成大π键
的电子(自由电子)数减少,所以比石墨烯导电性弱,A错误;B.氧化石墨烯中含有碳碳双
键和羟基,易被氧化,故抗氧化能力比石墨烯弱,B项正确;C.氧化石墨烯中含有羧基、
羟基,能与水分子形成分子间氢键,故氧化石墨烯在水中的溶解度大于石墨烯,故C正确;
D.氧化石墨烯中含有碳碳双键能发生氧化反应和加成反应,含有羟基、羧基能发生酯化反
应,故D正确。
11、C【解析】抽掉玻璃板后,甲盛二氧化氮的集气瓶较快变浅,说明甲中二氧化氮向下扩
散速率比乙中空气向上扩散速率快,证明二氧化氮的密度比空气大,故A正确;气体混合时
混乱度增大的熵增的过程,则抽掉玻璃板后,乙盛空气的集气瓶出现红棕色,说明熵增的方
向是自发的,故B正确;抽掉玻璃板后,甲乙的体积均增大,二氧化氮浓度减小,所有集气
瓶中气体颜色变浅,二氧化氮转化为四氧化二氮的反应为气体体积减小的反应,压强减小,
平衡向逆反应方向移动,不是正向移动,故C错误;经过足够长的时间,甲和乙中均达到相
同的平衡状态,因为状态相同,所以瓶中气体颜色相同,故D正确。
12、D【解析】反应历程中最慢的一步是整个反应的决速步,结合图示可知,反应①为该反
应的决速步,A错误;反应①断开了酯基的碳氧双键结合18OH-,反应②断裂出原酯基中的—
OR′,反应③转移了氢离子得到醇R′OH,反应④生成羧酸钠没有转移氧原子,故反应结束
后醇中均不存在18O,B错误;反应①酯基中的碳从sp2杂化转变为sp3杂化,后经过反应②
又生成羧基,恢复sp2杂化,故该反应历程中碳原子杂化方式发生改变,C错误;反应①中
OH-带负电,攻击电负性较弱的碳原子,D正确。
13、B【解析】“水滴石穿”是指石头在水滴或雨滴的长期侵蚀作用下发生了的物理变化和
化学变化而溶解,从而使石头穿孔,故A符合;同主族元素所表现的性质体现了矛盾既有普
遍性也有特殊性,例如同主族元素的最高正化合价相同,但是氧和氟没有正价,故B不符合;
NaHCO 溶液中HCO−既发生电离:HCO− H++CO2−,也发生水解:HCO−+HO HCO−+OH−,
3 3 3 3 3 2 3
能体现对立统一,故C符合;苯硝化时生成硝基苯而甲苯硝化时生成三硝基甲苯,这体现了
甲基对苯环的影响,甲基的邻对位活泼,故D符合。
c HX ·c OH- K
14、B【解析】HX-的水解常数K= 2 = w≈6×10-7>K,溶液显碱性,A
h c HX- K a2
a1
c2 H+ ·c X2-
项正确;BaX+2H+===Ba2++HX,则 c(Ba2+)≈c(HX),K ·K = =
2 2 a1 a2 c HX
2
c2 H+ ·c X2- c2 Ba2+ ·K·K
,K(BaX)=c(Ba2+)·c(X2-)= a1 a2≈6.18×10-23,B项
c Ba2+ sp c2 H+
错误;b点时,由电荷守恒:2c(Ba2+)+c(H+)=c(HX-)+c(OH-)+2c(X2-)+c(Y-),C项正
确;BaX溶于HY溶液中的反应:BaX+2H+===Ba2++HX,0.01 mol BaX消耗0.02 mol H+,c
2
0.38 mol+0.02 mol
点溶液中n(H+)= 0.144 4mol=0.38 mol,则c(HY)= =0.4 mol·L-1,
1 L
D项正确。
二、非选择题(本题共4小题,共58分)
15、(1)恒压滴液漏斗 饱和NaHS溶液
(2)HS+Ni2++2NH===NiS↓+2NH+ (3)b
2 3 4
(4)4NiS+O+2HO=== 4Ni(OH)S
2 2
0.182V
(5)① % ②偏高
m
【解析】
化学(YL)答案 (第 3 页,共 6 页)
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}(1)装置Ⅱ中的试剂为饱和NaHS溶液,用于除去硫化氢气体中挥发的氯化氢气体杂质。
(3)抽滤洗涤时,洗涤水进入装置Ⅲ,然后通过抽气装置抽出达到洗涤目的,故连有抽气
泵的装置Ⅳ接在b处以便能够抽出洗涤水。
(4)已知,NiS在潮湿的空气中可转化为碱式硫化高镍[Ni(OH)S],从而降低除铜离子能
力,故随时间延长残留铜离子增加的原因是:4NiS+O+2HO===4Ni(OH)S。
2 2
0.020 0V×10-3×91
(5)①n(NiS)=n(NaHY)=0.0200V×10-3mol,则样品的纯度为 ×
2 2 m
0.182V
100%= %。②滴定过程中,缓冲溶液pH过低,Ni2++HY2- NiY2-+ 2H+,导致平衡
m 2
逆向移动,则需要更多的标准液参与反应,导致测得的产品纯度偏高。
16、(1)3d74s2
(2)Na[Al(OH)](或NaAlO)
4 2
(3)CH CH OHNa RuO 2H OCH CHORuOH 2NaOH
3 2 2 4 2 3 4
(4)2∶1
(5)低压低温蒸发,避免RuCl ·6H O分解
3 2
(6)0.167mol⋅ L-1
(7)H C O Co2 xH OCoC O ·xH O2H
2 2 4 2 2 4 2
(8)还原
【解析】(1)Co是27号元素,核外电子排布式为[Ar]3d74s2,则价电子排布式为3d74s2;
(2)“焙烧”过程Co、Ru分别被氧化为CoO、NaRuO,NaNO 被还原为NaNO,同时AlO
2 4 3 2 2 3
与NaOH反应生成Na[Al(OH)](或NaAlO),则“焙烧”后所得固体主要成分为CoO、NaRuO、
4 2 2 4
NaNO 和Na[Al(OH)](或NaAlO);
2 4 2
(3)“还原”过程乙醇被氧化为CHCHO,NaRuO 被还原生成Ru(OH)沉淀,同时产生NaOH,
3 2 4 4
则该反应的化学方程式为:
CH CH OHNa RuO 2H OCH CHORuOH 2NaOH ;
3 2 2 4 2 3 4
(4)“酸溶”过程中,先加入盐酸溶解Ru(OH)得到RuCl,再加入盐酸羟胺(NHOH⋅ HCl)
4 4 2
与RuCl 反应得到RuCl 和N,则盐酸羟胺(NHOH⋅ HCl)与RuCl 反应的化学方程式为:
4 3 2 2 4
2RuCl 2NH OH·HCl 2RuCl N 4HCl2H O,所以产物RuCl 和N 的物质的量之
4 2 3 2 2 3 2
比为2∶1;
(5)“蒸发结晶”在真空度为40kPa时进行(此时水的沸点是28°C),即在低压低温下
蒸发结晶得到RuCl 晶体,其目的是低压低温蒸发,避免RuCl⋅ 6HO分解;
3 3 2
(6)c C O2
K
sp
CoC
2
O
4
6.3108
6.3103mol·L1,则
2 4
c
Co2 1105mol·L1
c HC O
c
C
2
O
4
2
·c
H
6.3103mol·L1102mol·L1
0.984mol· L 1,所以
2 4 K 6.4105
a2
c
HC
O2
·c
H
0.984mol·L1102mol·L1
cH C O 2 4 0.167mol· L1;
2 2 4 K 5.9102
a1
化学(YL)答案 (第 4 页,共 6 页)
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}(7)“沉钴”时,向含Co2+溶液中加入草酸溶液得到CoCO⋅ xHO晶体,则反应的离子方程
2 4 2
式为:H C O Co2 xH OCoC O ·xH O2H;
2 2 4 2 2 4 2
(8)“还原”后,过滤得到Ru(OH) 沉淀和含有Na[Al(OH)](或NaAlO)的滤液,此
4 4 2
时Co、Ru都已经提取,则可以从含有Na[Al(OH)](或NaAlO)的滤液中提取AlO,所
4 2 2 3
以在“还原”步骤后提取AlO 最合适。
2 3
17、(1)CHO*+OH*+3H*―→CHO*+OH*+2H*
2 3
(2)CO(g)+3H(g)===CHOH(g)+HO(g) ΔH=-46 kJ·mol-1
2 2 3 2
(3)①T>T>T ②5.33×10-4
3 2 1
(4)KCO 5.0×10-2
2 3
(5)CO+6e-+6H+===CHOH+HO 4 mol
2 3 2
(6)当温度高于250 ℃,催化剂活性降低,反应速率减慢,随着温度升高,反应速率主要
受温度影响,与催化剂无关,所以反应速率又增大
【解析】(2)由图可知,CO 和H 合成CHOH的化学方程式为CO(g)+3H(g)===CHOH
2 2 3 2 2 3
(g)+HO(g),根据ΔH=反应物的总键能-生成物的总键能得ΔH=(2×803+3×436)
2
kJ·mol-1-(414×3+464×3+326)kJ·mol-1=-46 kJ·mol-1。
(3)①因为该反应为放热反应,压强不变时,温度越高,平衡逆向移动,CO 的转化率越小,
2
所以T、T、T从高到低排序为T>T>T。②平衡常数只与温度有关,T时,压强为50 atm,
1 2 3 3 2 1 1
CO 的转化率为50%,根据三段式:
2
CO(g)+3H(g) CHOH(g)+HO(g)
2 2 3 2
n 1 3 0 0
0
Δn 0.5 1.5 0.5 0.5
n 0.5 1.5 0.5 0.5
平
0.5 0.5
×50× ×50
p CHOH ·p HO 3 3
n =0.5+1.5+0.5+0.5=3,K= 3 2 = atm-2≈5.33
总 p p CO ·p3 H 0.5 1.5
2 2 ×50× ×50 3
3 3
×10-4atm-2。
(4)根据图示,用KCO 溶液吸收CO,生成KHCO,KHCO 分解生成KCO,可以循环利用;
2 3 2 3 3 2 3
c H+ ·c CO2- c CO2- ·c H+
HCO 的电离常数K= 3 ,pH=9,c(H+)=10-9mol·L-1, 3
2 3 a2 c HCO- c HCO- ·c H+
3 3
K 5.0×10-11
= a2 = =5.0×10-2。
c H+ 1.0×10-9
(5)由图可知,玻碳电极产生O,为阳极,铂电极为阴极,发生反应的电极反应式为CO
2 2
+6e-+6H+===CHOH+HO,阳极的电极反应式为2HO-4e-===O↑+4H+,生成标准状况下
3 2 2 2
22.4 L O,有4 mol质子通过质子交换膜。
2
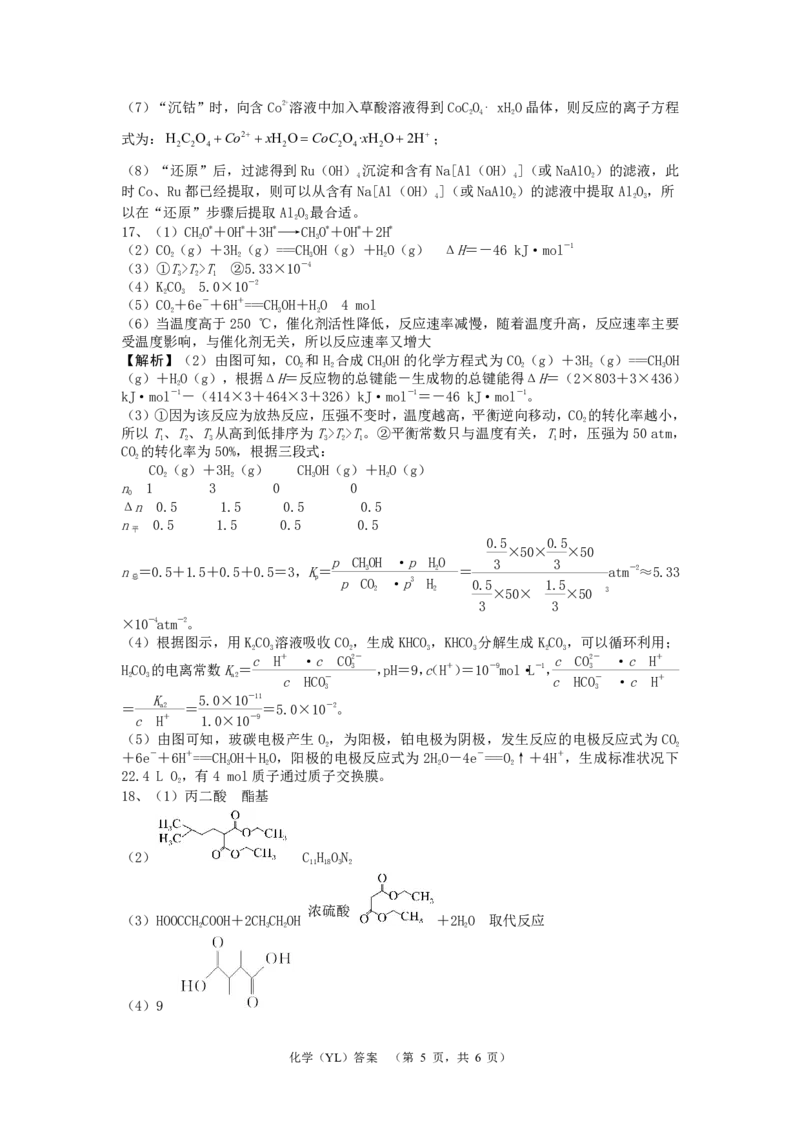
18、(1)丙二酸 酯基
(2) C H ON
11 18 3 2
浓硫酸
(3)HOOCCHCOOH+2CHCHOH +2HO 取代反应
2 3 2 2
(4)9
化学(YL)答案 (第 5 页,共 6 页)
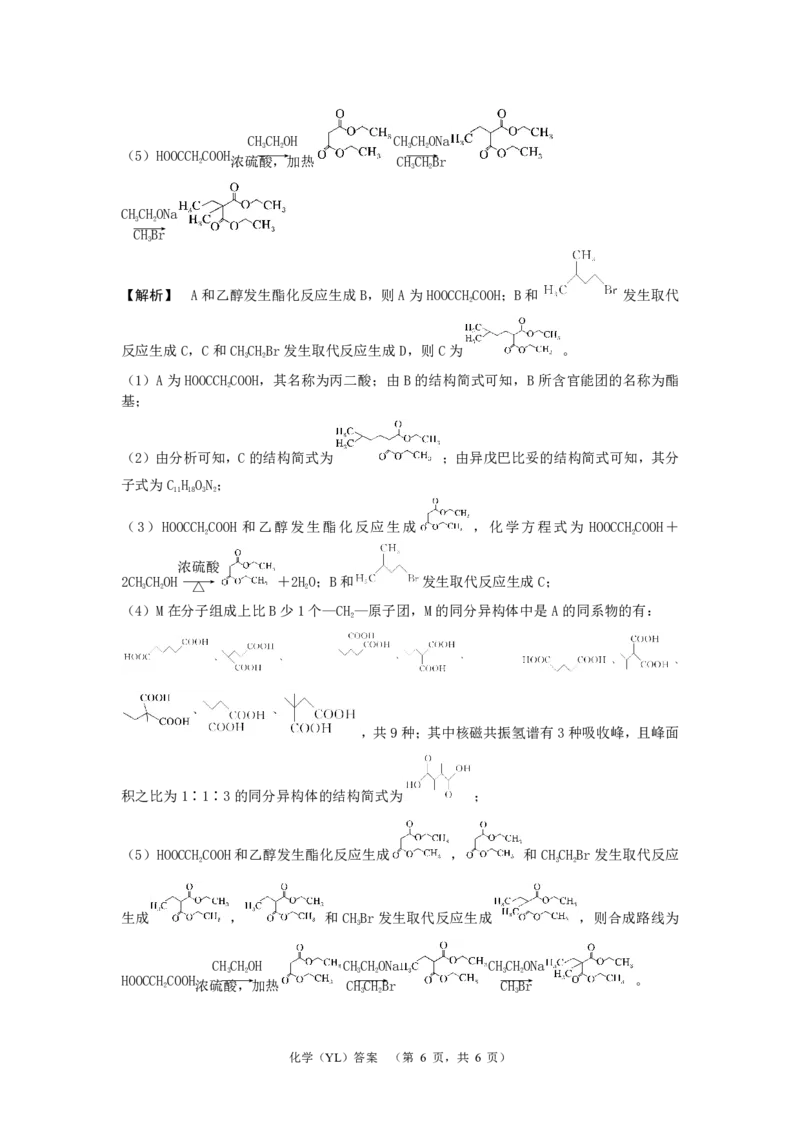
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}CHCHOH CHCHONa
3 2 3 2
(5)HOOCCHCOOH ――→ ――→
2 浓硫酸,加热 CHCHBr
3 2
CHCHONa
3 2
――→
CHBr
3
【解析】 A和乙醇发生酯化反应生成B,则A为HOOCCHCOOH;B和 发生取代
2
反应生成C,C和CHCHBr发生取代反应生成D,则C为 。
3 2
(1)A为HOOCCHCOOH,其名称为丙二酸;由B的结构简式可知,B所含官能团的名称为酯
2
基;
(2)由分析可知,C的结构简式为 ;由异戊巴比妥的结构简式可知,其分
子式为C H ON;
11 18 3 2
(3)HOOCCHCOOH 和乙醇发生酯化反应生成 ,化学方程式为 HOOCCHCOOH+
2 2
浓硫酸
2CHCHOH――→ +2HO;B和 发生取代反应生成C;
3 2 △ 2
(4)M在分子组成上比B少1个—CH—原子团,M的同分异构体中是A的同系物的有:
2
,共9种;其中核磁共振氢谱有3种吸收峰,且峰面
积之比为1∶1∶3的同分异构体的结构简式为 ;
(5)HOOCCHCOOH和乙醇发生酯化反应生成 , 和CHCHBr发生取代反应
2 3 2
生成 , 和CHBr发生取代反应生成 ,则合成路线为
3
CHCHOH CHCHONa CHCHONa
3 2 3 2 3 2
HOOCCHCOOH ――→ ――→ ――→ 。
2 浓硫酸,加热 CHCHBr CHBr
3 2 3
化学(YL)答案 (第 6 页,共 6 页)
{#{QQABTYwAggAgAIBAAAhCEQWACAKQkBECCAoOhEAAsAAACQFABAA=}#}