文档内容
班级 姓名 学号 分数
第 08 单元 化学与可持续发展
(A卷·夯实基础)
(时间:75分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分)
1.化学与环境密切相关,下列有关说法正确的是
A.CO、NO、NO 都是大气污染物,在空气中都能稳定存在
2
B.大气中SO 含量的增加会导致温室效应加剧
2
C.汽车尾气的主要污染成分包括NO、CO和N
2
D.NO可用于某些疾病的治疗
2.2022北京冬奥会是我国提出“2030碳达峰、2060碳中和”目标后的首个世界级体育盛会,冬奥会承诺
碳排放将全部中和。下列技术中不能促进碳中和的是
A.在火力发电中,对烟尘采用脱硫除尘处理减少空气污染
B.张北风电、太阳能发电实现绿色用电
C.“平原用电、山地用氢”的原则,在各赛区推广电动汽车、氢燃料电池汽车
D.中科院首次实现了从二氧化碳到淀粉的从头全合成
3.下列说法不正确的是
A.自然界中存在游离态的金属单质
B.金属活动性不同,冶炼方法也有所不同
C.地球上金属矿物资源是取之不尽的,因此,应加大开采金属矿物的速度,以满足经济发展的需要
D.废旧金属的回收利用,有利于环境保护
4.下列有关判断正确的是
A.金属阳离子被还原,一定会得到金属单质
B.金属冶炼过程中,金属化合物得到电子发生氧化反应
C.通过铝热反应可以在野外焊接钢轨
D.海带中含有碘单质,能使淀粉变蓝
5.下列有关金属的工业制法中正确的是
A.制钛:用金属钠置换氯化钛(TiCl )溶液中的钛
4
B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
学科网(北京)股份有限公司C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D.炼铜:电解硫酸铜溶液
6.我国在“煤变油”技术上已取得了重大突破,达到5吨煤可以合成1吨成品油的水平。下列有关叙述错
误的是( )
A.煤的组成元素主要是C,还含有少量的H、N、S、O等元素
B.“煤变油”的方法之一是使煤与H 作用生成液态有机物
2
C.煤之所以能变“油”,是因为煤中含有大量的汽油、柴油和煤焦油
D.煤变成成品油需要经过一系列工艺流程,发生复杂的物理、化学变化才能实现
7.下列说法正确的是
A.石油分馏塔从上到下的分馏产品依次是汽油、石油气、煤油、润滑油、柴油、重油
B.石油的各种分馏产品具有固定的沸点
C.石油裂化的目的是提高汽油等轻质油的产量和质量
D.石油裂解的主要目的是得到甲烷、丙烷等气态烷烃
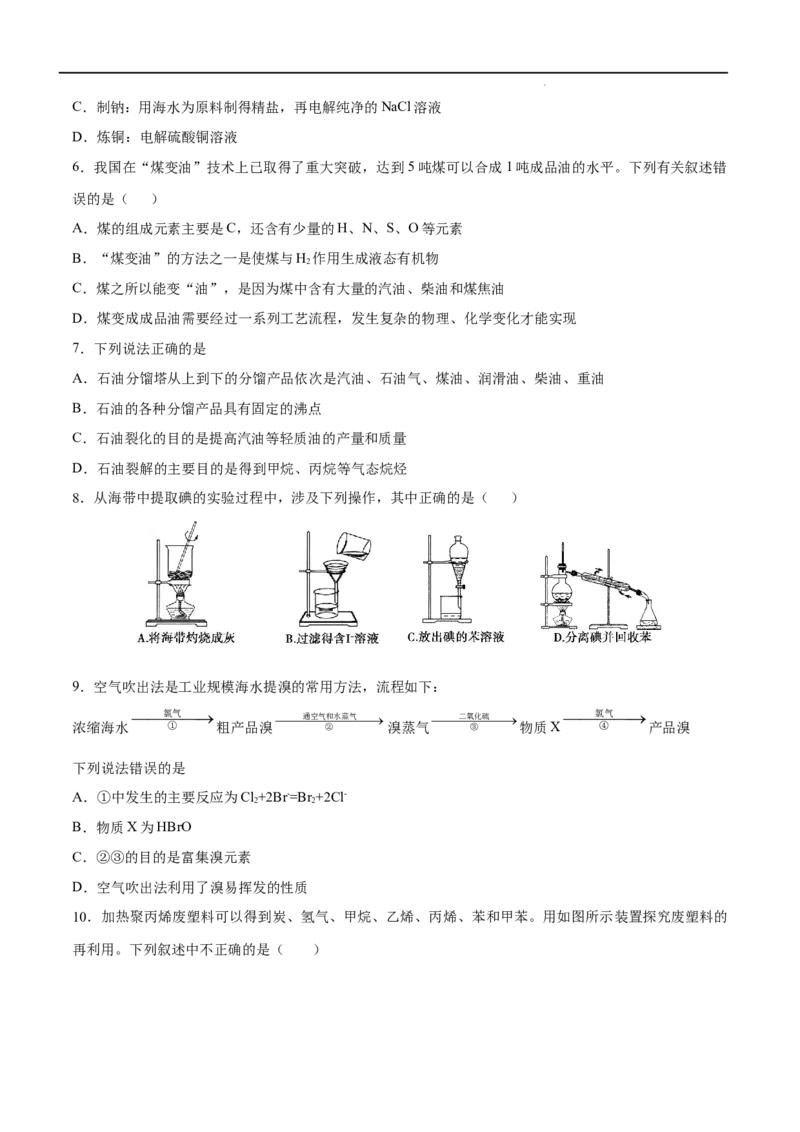
8.从海带中提取碘的实验过程中,涉及下列操作,其中正确的是( )
9.空气吹出法是工业规模海水提溴的常用方法,流程如下:
氯气 通空气和水蒸气 二氧化硫 氯气
浓缩海水 ① 粗产品溴 ② 溴蒸气 ③ 物质X ④ 产品溴
下列说法错误的是
A.①中发生的主要反应为Cl+2Br-=Br +2Cl-
2 2
B.物质X为HBrO
C.②③的目的是富集溴元素
D.空气吹出法利用了溴易挥发的性质
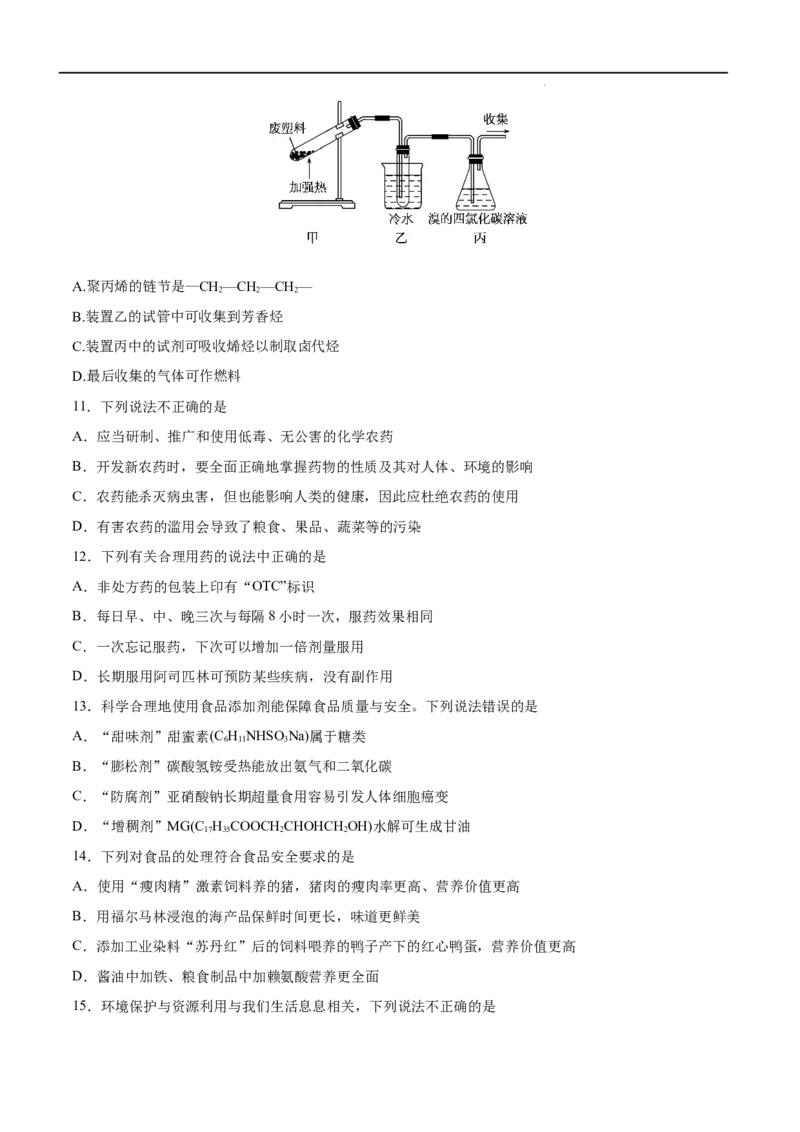
10.加热聚丙烯废塑料可以得到炭、氢气、甲烷、乙烯、丙烯、苯和甲苯。用如图所示装置探究废塑料的
再利用。下列叙述中不正确的是( )
学科网(北京)股份有限公司A.聚丙烯的链节是—CH—CH—CH—
2 2 2
B.装置乙的试管中可收集到芳香烃
C.装置丙中的试剂可吸收烯烃以制取卤代烃
D.最后收集的气体可作燃料
11.下列说法不正确的是
A.应当研制、推广和使用低毒、无公害的化学农药
B.开发新农药时,要全面正确地掌握药物的性质及其对人体、环境的影响
C.农药能杀灭病虫害,但也能影响人类的健康,因此应杜绝农药的使用
D.有害农药的滥用会导致了粮食、果品、蔬菜等的污染
12.下列有关合理用药的说法中正确的是
A.非处方药的包装上印有“OTC”标识
B.每日早、中、晚三次与每隔8小时一次,服药效果相同
C.一次忘记服药,下次可以增加一倍剂量服用
D.长期服用阿司匹林可预防某些疾病,没有副作用
13.科学合理地使用食品添加剂能保障食品质量与安全。下列说法错误的是
A.“甜味剂”甜蜜素(C H NHSONa)属于糖类
6 11 3
B.“膨松剂”碳酸氢铵受热能放出氨气和二氧化碳
C.“防腐剂”亚硝酸钠长期超量食用容易引发人体细胞癌变
D.“增稠剂”MG(C H COOCH CHOHCH OH)水解可生成甘油
17 35 2 2
14.下列对食品的处理符合食品安全要求的是
A.使用“瘦肉精”激素饲料养的猪,猪肉的瘦肉率更高、营养价值更高
B.用福尔马林浸泡的海产品保鲜时间更长,味道更鲜美
C.添加工业染料“苏丹红”后的饲料喂养的鸭子产下的红心鸭蛋,营养价值更高
D.酱油中加铁、粮食制品中加赖氨酸营养更全面
15.环境保护与资源利用与我们生活息息相关,下列说法不正确的是
学科网(北京)股份有限公司A.燃煤中加氧化钙可减少酸雨的形成及温室气体的排放
B.对含NO 、NO的废气处理后再排放
2
C.一定条件下,将CO 转化为淀粉,实现CO 的资源化利用
2 2
D.研发新型催化剂将CO 分解成碳和O,同时吸收热量
2 2
16.绿色化学的“原子经济性”是指在化学品合成过程中,合成方法和工艺应被设计成能把反应过程中所
用的所有原材科尽可能多的转化到最终产物中,以下反应最符合绿色化学的“原子经济性”要求的是
O SO
2 3
A.利用SO 与 反应制备 B.甲烷与氯气反应制取四氯化碳
2
C.以铜和浓硝酸为原科制取硝酸铜 D.一定条件下,用乙烯与水反应制取乙醇
二、非选择题(本题共5小题,共52分)
17.(10分)有四种常见药物:①阿司匹林( )②青霉素③胃舒平[Al(OH) ]④麻黄碱。
3
请回答:
(1)某同学胃酸过多,应选用的药物是_______(填序号),抗酸药的成分Al(OH) 中和胃酸过多的离子方程式
3
为________。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是___________(填序号,下同)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是___________。
(4)阿司匹林药品标签上贴有OTC,它表示___________。
(5)滥用药物会导致不良后果,如过量服用___________(填序号)会出现水杨酸中毒,应立即停药,并静脉注
射NaHCO 溶液,试写出该药物和NaHCO 反应的离子方程式:____________。
3 3
SO NO
18.(10分)酸雨的危害很大,能直接破坏农作物、腐蚀建筑物,还会危害人体健康。 2 、 x是形成
SO NO
酸雨的主要物质。研究 2 、 x等对减少酸雨,改善空气质量具有重要意义。请回答下列问题:
pH
(1)酸雨是指 小于_______的雨水。
(2)你认为减少酸雨的产生可采取的措施有_______(填序号)。
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰
(3)开发新能源可有效减少酸雨。下列能源不属于新能源的有_______(填序号)。
①太阳能 ②风能 ③地热能 ④海洋能 ⑤氢能 ⑥石油 ⑦无烟煤
学科网(北京)股份有限公司NO NO NO
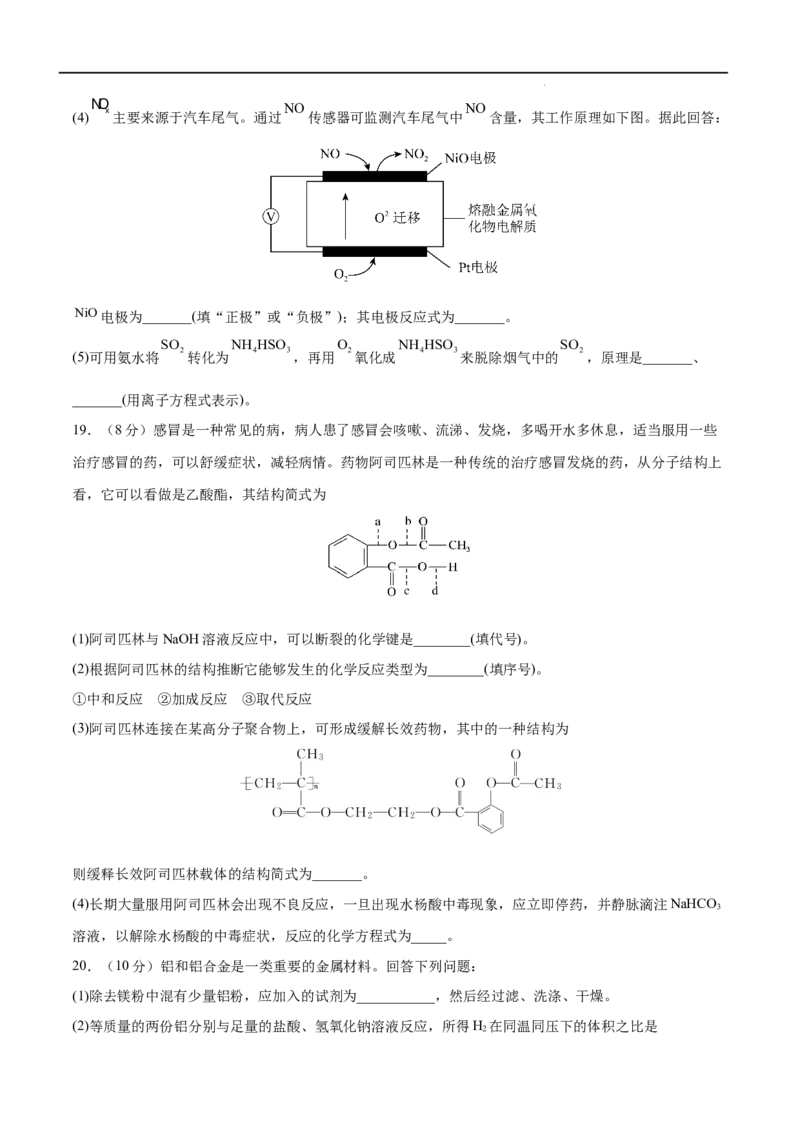
(4) x主要来源于汽车尾气。通过 传感器可监测汽车尾气中 含量,其工作原理如下图。据此回答:
NiO电极为_______(填“正极”或“负极”);其电极反应式为_______。
SO NH HSO O NH HSO SO
2 4 3 2 4 3 2
(5)可用氨水将 转化为 ,再用 氧化成 来脱除烟气中的 ,原理是_______、
_______(用离子方程式表示)。
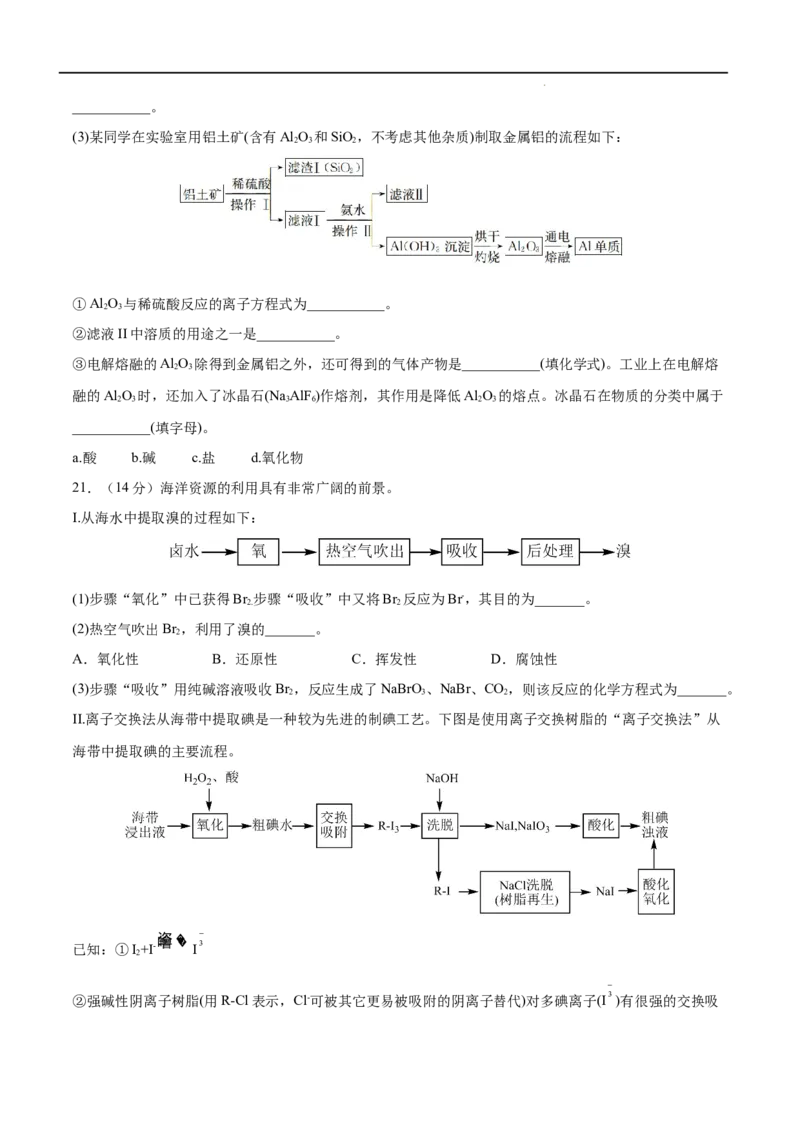
19.(8分)感冒是一种常见的病,病人患了感冒会咳嗽、流涕、发烧,多喝开水多休息,适当服用一些
治疗感冒的药,可以舒缓症状,减轻病情。药物阿司匹林是一种传统的治疗感冒发烧的药,从分子结构上
看,它可以看做是乙酸酯,其结构简式为
(1)阿司匹林与NaOH溶液反应中,可以断裂的化学键是________(填代号)。
(2)根据阿司匹林的结构推断它能够发生的化学反应类型为________(填序号)。
①中和反应 ②加成反应 ③取代反应
(3)阿司匹林连接在某高分子聚合物上,可形成缓解长效药物,其中的一种结构为
则缓释长效阿司匹林载体的结构简式为_______。
(4)长期大量服用阿司匹林会出现不良反应,一旦出现水杨酸中毒现象,应立即停药,并静脉滴注NaHCO
3
溶液,以解除水杨酸的中毒症状,反应的化学方程式为_____。
20.(10分)铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为___________,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H 在同温同压下的体积之比是
2
学科网(北京)股份有限公司___________。
(3)某同学在实验室用铝土矿(含有Al O 和SiO,不考虑其他杂质)制取金属铝的流程如下:
2 3 2
①Al O 与稀硫酸反应的离子方程式为___________。
2 3
②滤液II中溶质的用途之一是___________。
③电解熔融的Al O 除得到金属铝之外,还可得到的气体产物是___________(填化学式)。工业上在电解熔
2 3
融的Al O 时,还加入了冰晶石(NaAlF)作熔剂,其作用是降低Al O 的熔点。冰晶石在物质的分类中属于
2 3 3 6 2 3
___________(填字母)。
a.酸 b.碱 c.盐 d.氧化物
21.(14分)海洋资源的利用具有非常广阔的前景。
I.从海水中提取溴的过程如下:
(1)步骤“氧化”中已获得Br 步骤“吸收”中又将Br 反应为Br-,其目的为_______。
2. 2
(2)热空气吹出Br ,利用了溴的_______。
2
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤“吸收”用纯碱溶液吸收Br ,反应生成了NaBrO 、NaBr、CO,则该反应的化学方程式为_______。
2 3 2
II.离子交换法从海带中提取碘是一种较为先进的制碘工艺。下图是使用离子交换树脂的“离子交换法”从
海带中提取碘的主要流程。
已知:①I+I-
噲垐��
I3
2
②强碱性阴离子树脂(用R-Cl表示,Cl-可被其它更易被吸附的阴离子替代)对多碘离子(I3)有很强的交换吸
学科网(北京)股份有限公司附能力。
③步骤“交换吸附”发生的反应:R-Cl+I3=R-I +Cl-。
3
试回答下列问题:
(4)下列各步反应中,属于氧化还原反应的有:_______(填序号)
A.交换吸附 B.洗脱 C.酸化 D.NaCl洗脱
(5)酸性条件下,原料被HO 氧化时发生的反应有:
2 2
①_______;
②I+I-
噲垐��
I3
。
2
依据整个生产流程分析是否可以加过量HO;_______(填“是”或“否”)。并说明理由:_______。
2 2
(6)实验室模拟步骤“酸化氧化”,一般选用氯水。工业上生产企业可以按照自己的实际情况,选择合适的
氧化剂。若某企业在酸性条件下选择NaNO 为氧化剂,反应生成一种无色气体,遇空气立即变为红棕色,
2
则添加氧化剂与NaI的质量比应不少于_______。
学科网(北京)股份有限公司学科网(北京)股份有限公司