文档内容
人教版(2019)必修第一册第一章第三节 氧化还原反应
课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
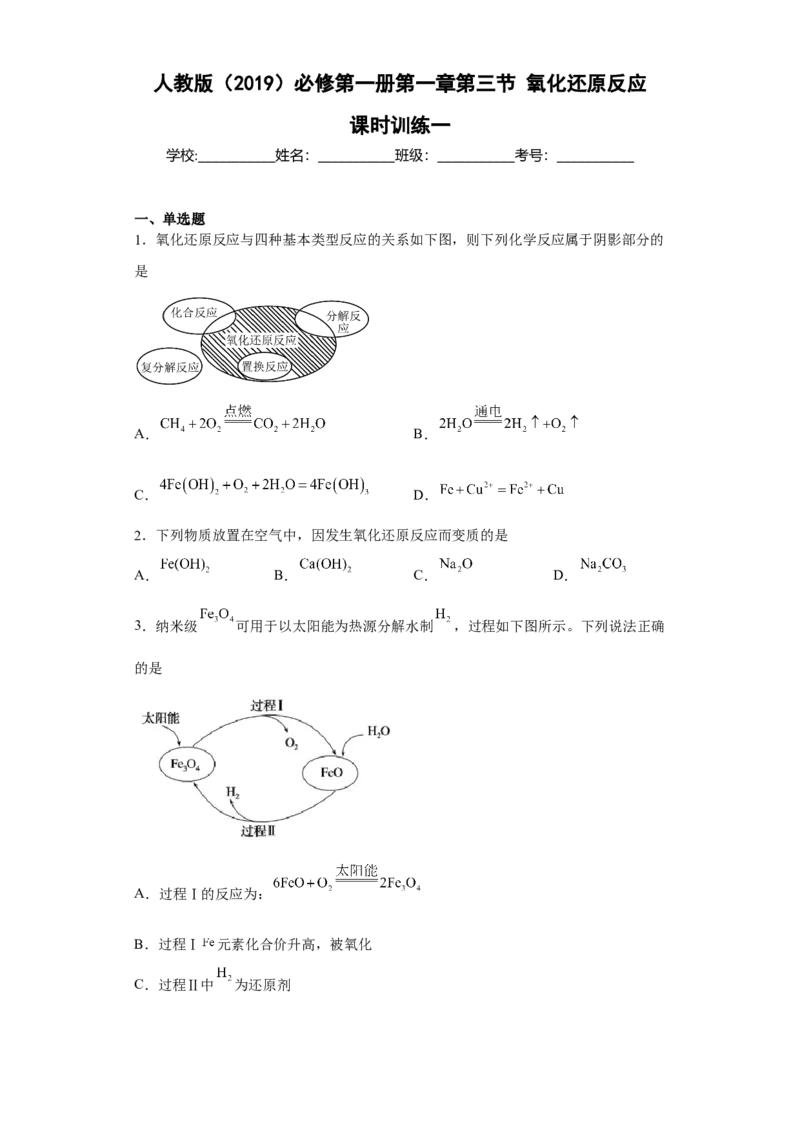
1.氧化还原反应与四种基本类型反应的关系如下图,则下列化学反应属于阴影部分的
是
A. B.
C. D.
2.下列物质放置在空气中,因发生氧化还原反应而变质的是
A. B. C. D.
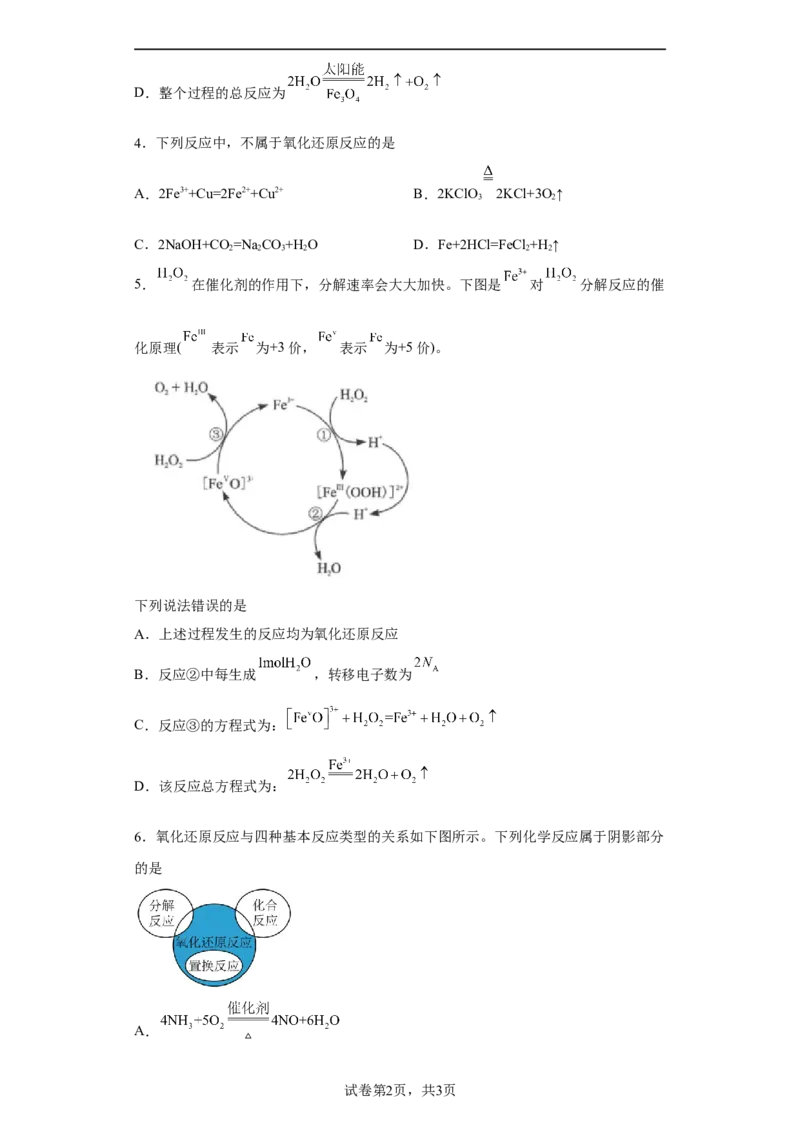
3.纳米级 可用于以太阳能为热源分解水制 ,过程如下图所示。下列说法正确
的是
A.过程Ⅰ的反应为:
B.过程Ⅰ 元素化合价升高,被氧化
C.过程Ⅱ中 为还原剂D.整个过程的总反应为
4.下列反应中,不属于氧化还原反应的是
A.2Fe3++Cu=2Fe2++Cu2+ B.2KClO 2KCl+3O ↑
3 2
C.2NaOH+CO =Na CO+H O D.Fe+2HCl=FeCl +H ↑
2 2 3 2 2 2
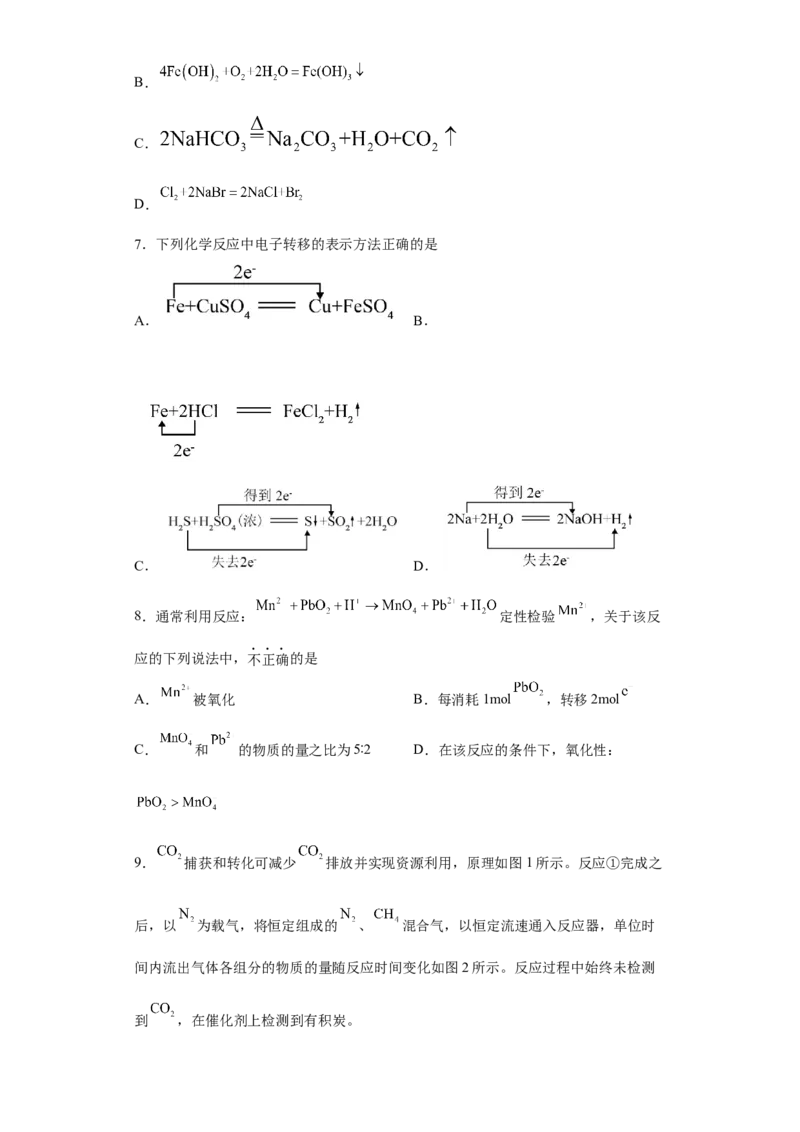
5. 在催化剂的作用下,分解速率会大大加快。下图是 对 分解反应的催
化原理( 表示 为+3价, 表示 为+5价)。
下列说法错误的是
A.上述过程发生的反应均为氧化还原反应
B.反应②中每生成 ,转移电子数为
C.反应③的方程式为:
D.该反应总方程式为:
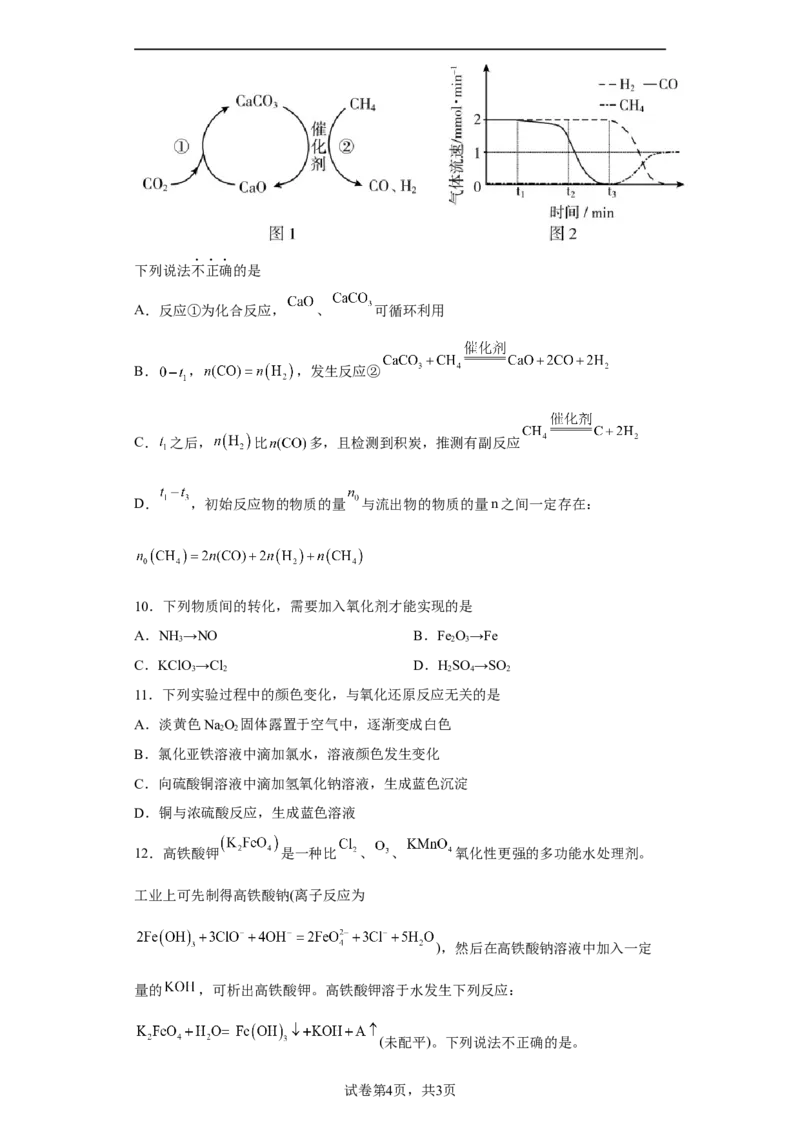
6.氧化还原反应与四种基本反应类型的关系如下图所示。下列化学反应属于阴影部分
的是
A.
试卷第2页,共3页B.
C.
D.
7.下列化学反应中电子转移的表示方法正确的是
A. B.
C. D.
8.通常利用反应: 定性检验 ,关于该反
应的下列说法中,不正确的是
A. 被氧化 B.每消耗1mol ,转移2mol
C. 和 的物质的量之比为5∶2 D.在该反应的条件下,氧化性:
9. 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之
后,以 为载气,将恒定组成的 、 混合气,以恒定流速通入反应器,单位时
间内流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测
到 ,在催化剂上检测到有积炭。下列说法不正确的是
A.反应①为化合反应, 、 可循环利用
B. , ,发生反应②
C. 之后, 比 多,且检测到积炭,推测有副反应
D. ,初始反应物的物质的量 与流出物的物质的量n之间一定存在:
10.下列物质间的转化,需要加入氧化剂才能实现的是
A.NH →NO B.Fe O→Fe
3 2 3
C.KClO→Cl D.HSO →SO
3 2 2 4 2
11.下列实验过程中的颜色变化,与氧化还原反应无关的是
A.淡黄色NaO 固体露置于空气中,逐渐变成白色
2 2
B.氯化亚铁溶液中滴加氯水,溶液颜色发生变化
C.向硫酸铜溶液中滴加氢氧化钠溶液,生成蓝色沉淀
D.铜与浓硫酸反应,生成蓝色溶液
12.高铁酸钾 是一种比 、 、 氧化性更强的多功能水处理剂。
工业上可先制得高铁酸钠(离子反应为
),然后在高铁酸钠溶液中加入一定
量的 ,可析出高铁酸钾。高铁酸钾溶于水发生下列反应:
(未配平)。下列说法不正确的是。
试卷第4页,共3页A.高铁酸钾中Fe为 价
B.工业上制备高铁酸钠时每生成1mol还原产物,转移3mol电子
C.物质A为
D. 处理水时,不仅能消毒杀菌,还能除去水中溶解的 等,并使悬浮杂质
沉降达到净水的目的
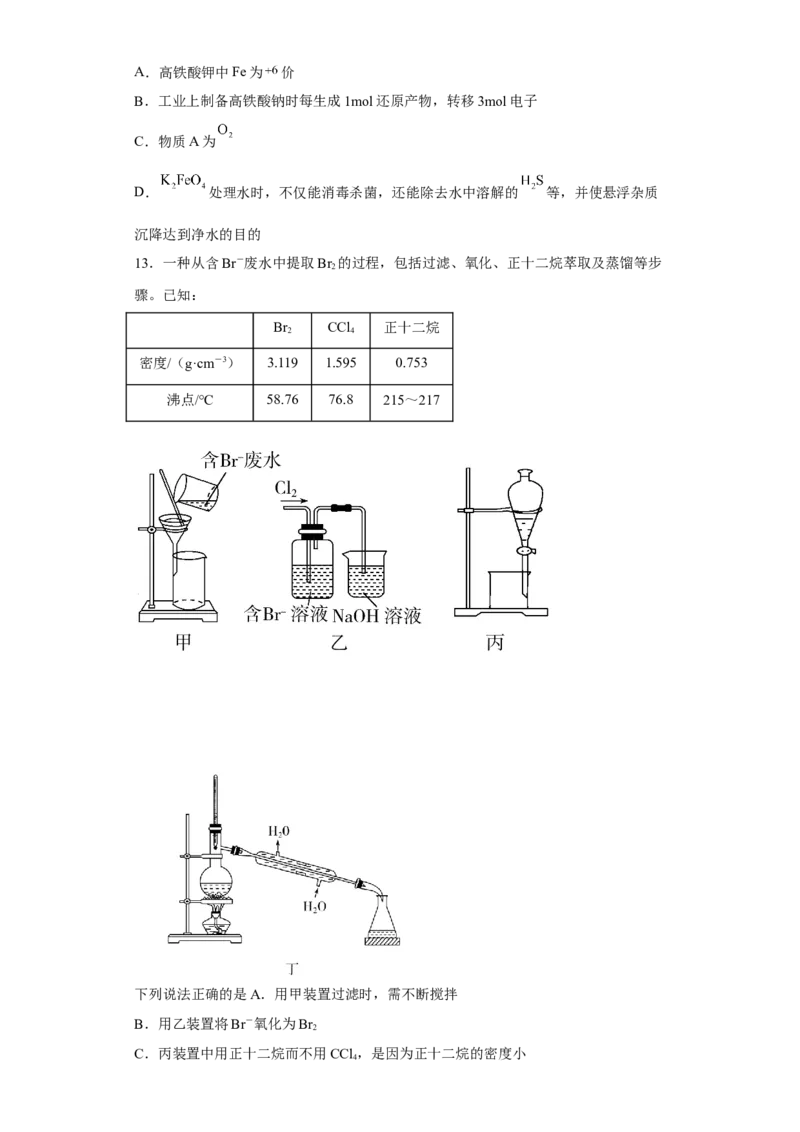
13.一种从含Br-废水中提取Br 的过程,包括过滤、氧化、正十二烷萃取及蒸馏等步
2
骤。已知:
Br CCl 正十二烷
2 4
密度/(g·cm-3) 3.119 1.595 0.753
沸点/℃ 58.76 76.8 215~217
下列说法正确的是A.用甲装置过滤时,需不断搅拌
B.用乙装置将Br-氧化为Br
2
C.丙装置中用正十二烷而不用CCl ,是因为正十二烷的密度小
4D.可用丁装置进行蒸馏,先收集正十二烷再收集Br
2
14. 是一种优良的饮用水处理剂,可用 、 、 混合共熔反应制
得: 。下列关于该反应的说法不正确
的是
A. 是还原剂, 为还原产物
B.在熔融条件下氧化性:
C.每生成 ,转移
D. 在处理饮用水过程中起氧化、杀菌、脱色、除自、净水等作用
15.2021年12月9日,神舟十三号航天员翟志刚、王亚平、叶光富在中国空间站进行
太空授课。火箭和飞船升空所需的巨大能量可由化学反应
提供,下列说法错误的是
A. 中氮元素的化合价为-2
B.该反应的优点之一是产物绿色环保
C.氧化剂与还原剂的质量比为16:23
D.反应瞬间产生的大量高温气体,推动火箭升空
二、填空题
16.请回答下列问题:
(1)CrO 是一种酸根离子,Fe(CrO ) 中铁元素的化合价为_______,Fe(CrO ) 属于
2 2 2 2
_______(填“酸”、“碱”、“盐”或“氧化物")。
(2)新型纳米材料氧缺位铁酸盐(MFe O,3氧化产物,,所以氧化性: ,B正确;
C. ,化合价升高3价,每生成 ,转移 ,C错误;
D. 具有强氧化性,在处理饮用水过程中起氧化、杀菌、脱色等,其还原产物
水解生成 胶体,具有吸附性,能达到净水的目的,D正确;
故选C。
15.C
【分析】 反应前后元素化合价发生了改变,是氧化还原反应,
NO 中氮元素化合价从+4 0,NO 做氧化剂;NH 中氢元素的化合价+1价,氮元素只能
2 4 2 4 2 4
是-2价,氮元素化合价从-2 0化合价升高,NH 是还原剂,据此分析解答.
2 4
【详解】A.NH 中氢元素的化合价+1价,氮元素只能是-2价,故A正确;
2 4
B.该反应产物是N 和HO,都不是污染气体,所以优点之一是产物绿色环保,故B正确;
2 2
C.氧化剂是NO,还原剂是NH,所以质量比是92:64,化简为23:16,故C错误;
2 4 2 4
D.反应瞬间产生的大量高温气体N 和HO,推动火箭升空,D正确;
2 2
故选D。16.(1) +2价 盐
(2) 胶体 氧化还原
(3) Fe O Cu O
2 2
(4)b
(5)+3
【详解】(1)根据CrO 可判断Fe(CrO ) 中铁元素的化合价为+2价,Fe(CrO ) 是金属阳
2 2 2 2
离子与酸根离子组成的盐类,故答案为:+2价;盐。
(2)将纳米材料氧缺位铁酸盐分散在蒸馏水中,所形成的分散系属于胶体,铁酸盐
MFe O 经过高温反应得到MFe O 的反应中因为M=Mn,Zn,Ni.且均为+2价,所以铁元素
2 4 2 x
一定变价,该反应属于氧化还原反应,故答案为:胶体;氧化还原。
(3)在酸性条件下。Fe O 容易转化为Fe2+,铁元素化合价降低,Fe O 作氧化剂,另应
2 2
该有元素化合价升高的元素,故6种粒子Fe O 、Fe3+、H+、HO、Cu O、Cu2+中应该选择
2 2 2
Cu O→Cu2+,则该反应中还原剂是Cu O,故答案为:Fe O ;Cu O。
2 2 2 2
(4)NaSO 中S的化合价为+2价,制备NaSO 时选用的反应物是含S元素,则根据氧
2 2 3 2 2 3
化还原反应中的“归中反应”规律,反应物中S元素的化合价应一个大于+2价、一个小于
+2价,只有NaSO +S符合,故答案为:b。
2 3
(5)S元素的化合价由+4价升高为+6价,Cr元素的化合价由+6价降低,设还原产物中Cr
元素的化合价为x,由电子守恒可知:0.024L0.05mol/L(6-4)=0.02L 0.02mol/L2(6-x),
解得x =+3,故答案为:+3。
17.(1)①、②
(2) 氧化和还原
(3)
(4)
答案第8页,共2页【分析】氮在自然界中的循环转化过程。是生物圈内基本的物质循环之一。如大气中的氮
经微生物等作用而进入土壤,为动植物所利用,最终又在微生物的参与下返回大气中,如
此反复循环,以至无穷。转化关系中大气中的氮气通过雷电作用生成一氧化氮,实现单质
变化为化合物,属于氮的固定,空气中的氮气在根瘤菌等微生物的作用下会形成硝酸盐作
为肥料被植物吸收。
【详解】(1)①、②、③中,属于氮的固定的是①和②属于非生物固氮,故答案为①、②。
(2)①N 和O 生成NO,化学方程式为 ;故答案为 。
2 2
②NO 转化为HNO,反应方程式为 ,N元素化合价从+4价变为+2
2 3
价和+5价;即表现出氧化性也表现出还原性;故答案为氧化和还原。
(3)N 也可以转化为NH ,工业合成氨的化学方程式为 ;
2 3
(4)稀硝酸为原料,制备KNO;可用稀硝酸与强氧化钾反应;化学方程式为
3
;故答案为 。
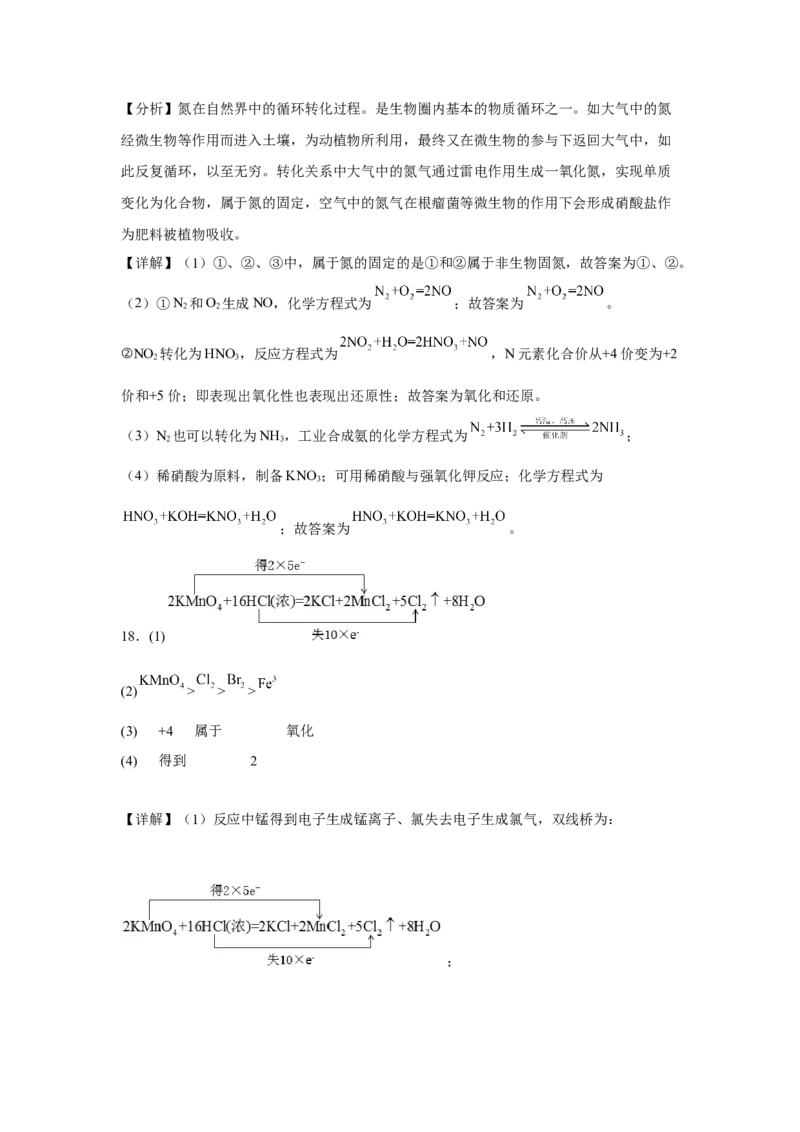
18.(1)
(2) > > >
(3) +4 属于 氧化
(4) 得到 2
【详解】(1)反应中锰得到电子生成锰离子、氯失去电子生成氯气,双线桥为:
;(2)氧化剂氧化性大于氧化产物,由①可知氧化性 ,②可知 ,
可知 ,故氧化性由强到弱
的顺序是 > > > ;
(3) 中氧为-2,则C元素的化合价为+4。一定条件下, 与H 反应生成CHOH(C
2 3
的化合价为-2)和HO,该反应中氢、碳元素化合价发生改变,属于氧化还原反应,CO 中
2 2
碳元素化合价降低,发生还原反应,在反应中作氧化剂;
(4)反应中硫元素化合价由0变为-2,则一个S参与反应时得到2个电子。
19.(1) 置换反应 Al Fe
(2) Cl Cl
【详解】(1)① 是一种单质和一种化合物反应生成另一种单
质和另一种化合物,属于置换反应;
② 反应中,Al元素化合价升高,发生氧化反应的是Al,
中Fe元素化合价降低,发生还原反应的 ;Al发生氧化反应生成 ,氧化产物是
, 发生还原反应生成Fe,还原产物是Fe。
(2) 反应,Cl 中Cl元素化合价由0升高为+1,被氧化
2
的元素是Cl;Cl 中Cl元素化合价由0降低为-1,被还原的元素是Cl;此反应的离子方程
2
式为 。
20.(1) Fe CuSO
4
答案第10页,共2页(2) 22.4 2
【详解】(1)反应①中,化合价升高的是Fe元素,被氧化,化合价降低的元素是Cu元素,
所在的反应物CuSO 是氧化剂,答案为Fe;CuSO ;
4 4
(2)反应②中若每消耗1 ,根据反应 可知,则生成 的
体积约是1mol 22.4L/mol=22.4L(标准状况),转移电子的物质的量为1mol 2=2 ;答案
为22.4;2。
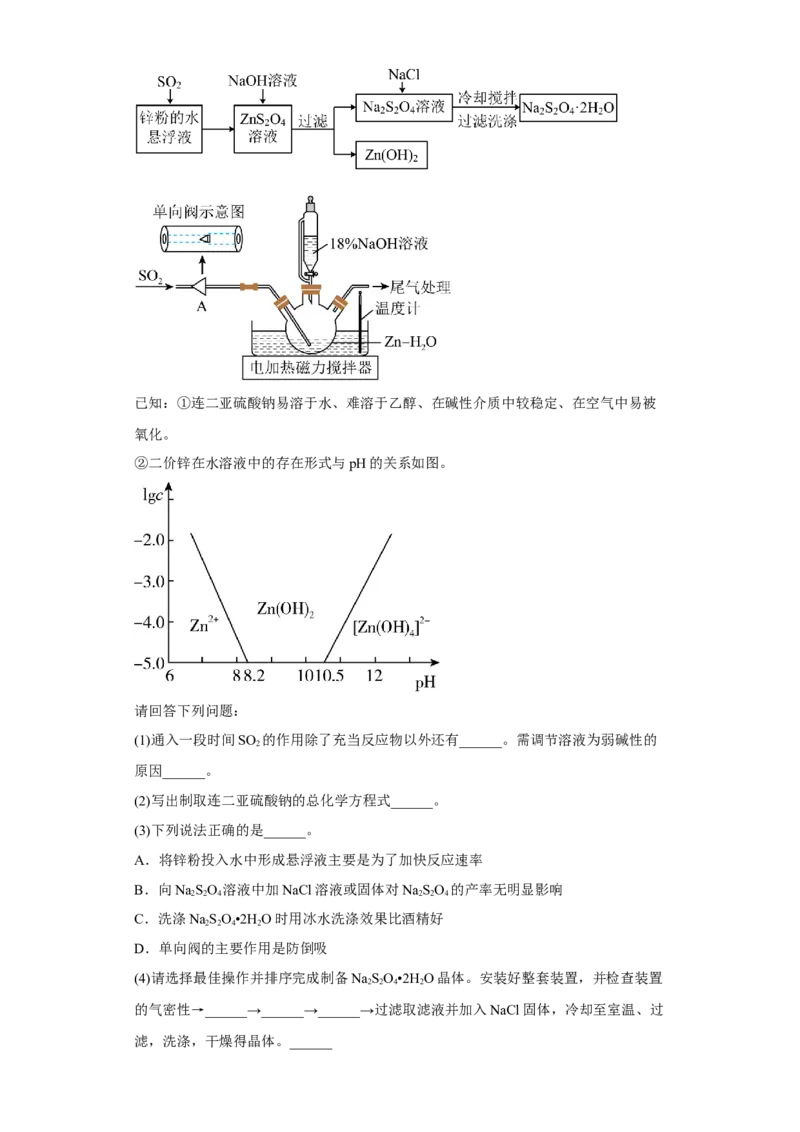
21.(1) 排除装置内的空气,防止连二亚硫酸钠没氧化; 碱性条件下,
能稳定存在;
(2)
(3)D
(4)a e g
(5) 66.7% 、
【详解】(1)连二亚硫酸钠空气中易被氧化、在碱性介质中较稳定,故通入 可以排除
装置内的空气,防止连二亚硫酸钠被氧化;溶液显碱性,使 能稳定存在。
(2) 的水溶液中通入 发生反应: 和
,制取连二亚硫酸钠的总化学方程式为:
(3)A. 将锌粉投入水中形成悬浮液主要是为了增大接触面,加快反应速率,A 正确;
B. 向 溶液中加 固体,使 增大,减小 的溶解量,促进
晶体析出,产率增大,加入 溶液, 减小,减少晶体析出,产率降低,B错误;
C. 连二亚硫酸钠易溶于水、难溶于乙醇,洗涤 时用酒精洗涤效果比冰水好,
C错误;
D. 单向阀的主要作用是防止氧气防倒吸进入装置中,将连二亚硫酸钠氧化,D正确;
故选D。
(4)制备 晶体,先安装好整套装置,并检查装置的气密性→将一定量的
Zn粉与蒸馏水混合搅拌成悬浊液→28~35℃加热条件下,向悬浊液中通入 至澄清→向
溶液中滴加 至pH在8.2~10.5之间,过滤取滤液并加入 固体,冷却至室温、过
滤,洗涤,干燥得晶体。故答案为:a→e→g;
(5) 与 发生反应,根据 升高6价,
,降1价,根据得失电子守恒,
,
, 晶体的纯度为:
; 可能被氧化成 ,结晶过程中可能含有 等杂质。
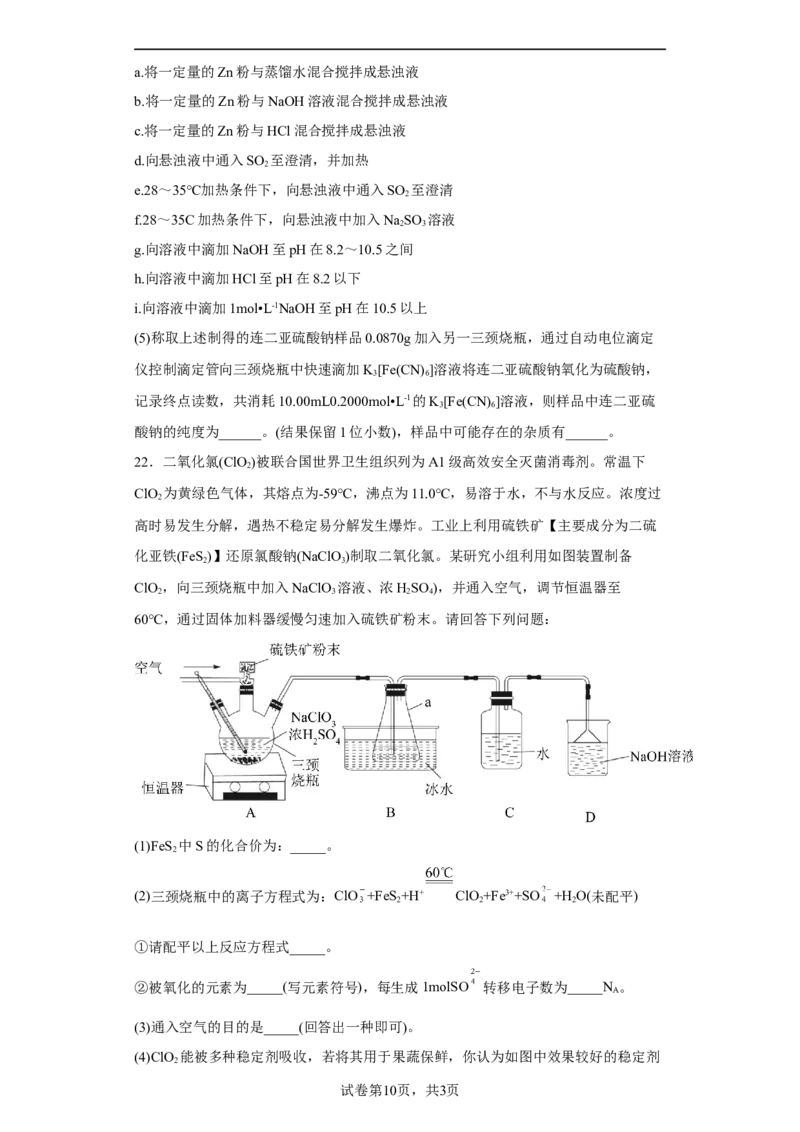
22.(1)-1
(2) 15ClO +FeS +14H+ 15ClO +Fe3++2SO +7H O Fe、S 7.5
2 2 2
(3)将生成的ClO 带出,在B装置中收集;稀释ClO ,防止发生爆炸
2 2
(4) 稳定剂Ⅱ 稳定剂Ⅱ可以缓慢释放ClO ,能较长时间维持保鲜所需的浓度
2
【分析】由实验装置图可知,装置A中二硫化亚铁与氯酸钠、浓硫酸共热反应制备二氧化
氯,装置B用于冷凝收集二氧化氯,装置C中盛有的水用于吸收挥发出的易溶于水的二氧
答案第12页,共2页化氯,装置D中盛有的氢氧化钠溶液用于吸收挥发出的二氧化氯,防止污染空气。
【详解】(1)由化合价代数和为0,亚铁离子中Fe元素化合价为+2可知,二硫化亚铁中
硫元素的化合价为-1价;
(2)①由未配平的离子方程式可知,反应中铁元素和硫元素的化合价升高被氧化,二硫化
亚铁为反应的还原剂,氯元素化合价降低被还原,氯酸钠是反应的氧化剂,反应生成
15mol二氧化氯转移15mol电子,反应的离子方程式为15ClO +FeS +14H+
2
15ClO +Fe3++2SO +7H O;
2 2
②由未配平的离子方程式可知,反应中铁元素和硫元素的化合价升高被氧化,被氧化的元
素为Fe、S,结合上述已配平的离子方程式15ClO +FeS +14H+ 15ClO +Fe3++2SO
2 2
+7H O可知,每生成1molSO 转移电子数为 =7.5N ,故答案为:Fe、S;
2 A
7.5;
(3)根据题给信息可知“常温下ClO 浓度过高时易发生分解,遇热不稳定易分解发生爆
2
炸。”所以通入空气,可稀释ClO ,防止爆炸,而且可将ClO 带出,便于在B装置中收集
2 2
(答案合理即可);
(4)根据示意图可判断稳定剂Ⅱ可以缓慢释放 ,能较长时间维持保鲜所需的浓度,
因此图中效果较好的稳定剂是稳定剂Ⅱ。答案第14页,共2页