文档内容
湖北省部分高中协作体2024--2025学年下学期期中联考
高一化学试题
本试卷共8页,19题,全卷满分100分,考试用时75分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答
题卡上,并将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B铅笔把答题卡上对应题目的
答案标号涂黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在
试卷、草稿纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共15小题,每题3分,共45分,每小题仅有一项是符
合题意。
1、下列离子方程式书写正确的是( )
A . 向 澄 清 石 灰 水 中 滴 加 少 量 Ca(HCO ) 溶 液 : Ca2+ + OH - +
3 2
HCO===CaCO ↓+H O
3 2
B.Na O 与稀硫酸反应:2O+4H+===O ↑+2H O
2 2 2 2
C.向饱和食盐水中先通足量NH ,再通过量CO :CO +OH-===HCO
3 2 2
D.Cl 溶于水:Cl +H O 2H++Cl-+ClO-
2 2 2
2、已知I-、Fe2+、SO 、Cl-和H O 均有还原性,它们在酸性溶液中还原
2 ⥫⥬ 2 2
性的强弱顺序为Cl-<Fe2+<H O <I-<SO ,则下列反应不能发生的是( )
2 2 2
A.2Fe3++SO +2H O===2Fe2++SO+4H+
2 2
B.I +SO +2H O===H SO +2HI
2 2 2 2 4
C.H O +H SO ===SO ↑+O ↑+2H O
2 2 2 4 2 2 2
D.2Fe2++Cl ===2Fe3++2Cl-
2
3、下列指定反应的离子方程式正确的是( )
A.往CaCl 溶液中通入少量CO :Ca2++H O+CO ===CaCO ↓+2H+
2 2 2 2 3
B.酸性介质中KMnO 氧化H O :2MnO+5H O +6H+===2Mn2++5O ↑
4 2 2 2 2 2+8H O
2
C.向 Ba(OH) 溶液中滴入少量 NaHSO 溶液:2H++SO+2OH-+Ba2+
2 4
===BaSO ↓+2H O
4 2
D.将稀盐酸滴在氧化铁上:2H++FeO===Fe2++H O
2
4、若20 g密度为ρ g·mL-1的Ca(NO ) 溶液中含有2 g Ca(NO ) ,则溶液中
3 2 3 2
NO的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
5、证明某溶液中含有Fe2+而不含有Fe3+的实验方法是( )
①先滴加氯水,再滴加KSCN溶液,溶液显红色
②先滴加KSCN溶液,溶液不显红色,再滴加氯水,溶液显红色
③滴加NaOH溶液,先产生白色絮状沉淀,后沉淀迅速变成灰绿色,最后
变成红褐色
④滴加KSCN溶液,溶液不显红色
A.①② B.②③
C.③④ D.①④
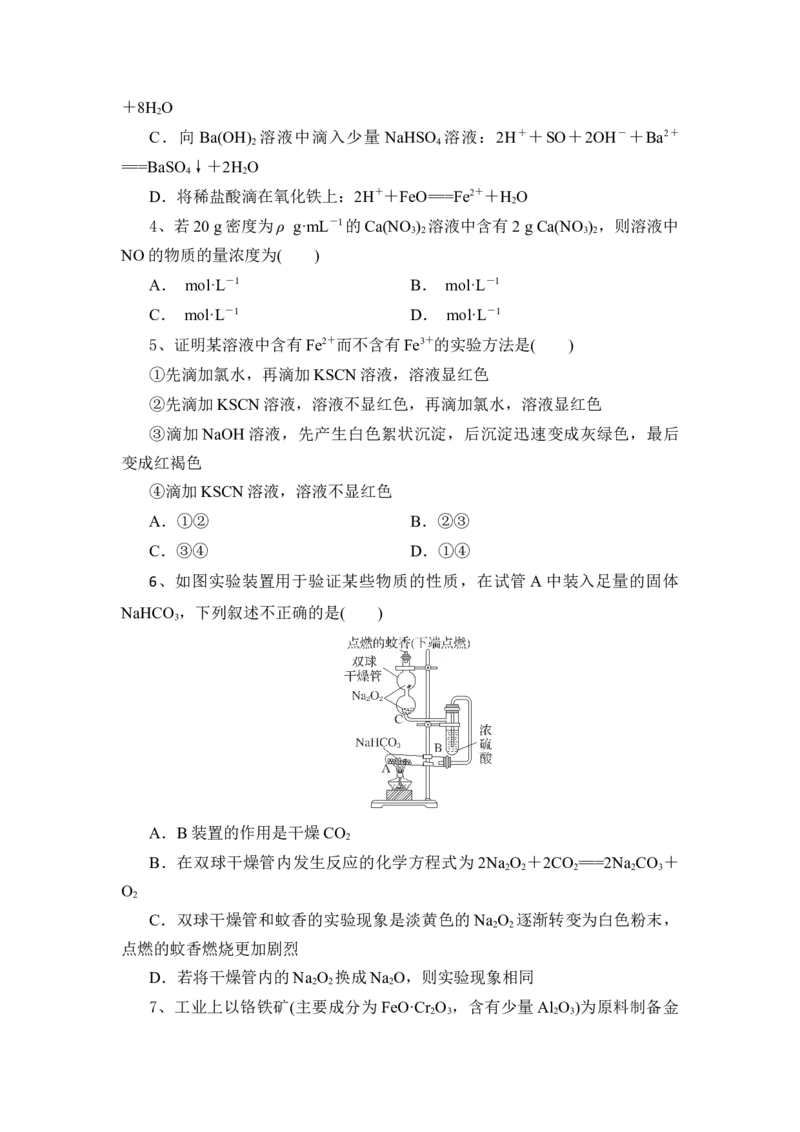
6、如图实验装置用于验证某些物质的性质,在试管A中装入足量的固体
NaHCO ,下列叙述不正确的是( )
3
A.B装置的作用是干燥CO
2
B.在双球干燥管内发生反应的化学方程式为 2Na O +2CO ===2Na CO +
2 2 2 2 3
O
2
C.双球干燥管和蚊香的实验现象是淡黄色的 Na O 逐渐转变为白色粉末,
2 2
点燃的蚊香燃烧更加剧烈
D.若将干燥管内的Na O 换成Na O,则实验现象相同
2 2 2
7、工业上以铬铁矿(主要成分为FeO·Cr O ,含有少量Al O )为原料制备金
2 3 2 3属铬的流程如下图。下列有关流程中的步骤说法错误的是( )
A.①需持续吹入空气作氧化剂
B.②需加入过量稀硫酸
C.③X一般为硫酸
D.④发生了铝热反应
8、下列说法错误的是( )
A.石墨晶体中层内导电性强于层间导电性
B.基态Cr3+的最高能层中成对电子与未成对电子的数目比为8∶3
C.ClO的空间结构为平面三角形
D.(CH COO) Ni·4H O的空间构型为八面体,中心离子的配位数为6
3 2 2
9、实验室制备NaClO消毒液,有关实验装置和原理不能达到实验目的的是
( )
A.用甲装置制备Cl
2
B.用乙装置除去Cl 中混有的少量HCl
2
C.用丙装置吸收Cl
2
D.用丁装置蒸发浓缩NaClO消毒液
10、硫及其化合物的“价-类”二维图体现了化学变化之美。下列有关说
法正确的是( )A.硫在过量的氧气中燃烧直接生成Y
B.X通入BaCl 溶液中有白色沉淀生成
2
C.H S与X反应的氧化产物和还原产物的物质的量之比为2∶1
2
D.N可由其相应单质直接化合生成
11、定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的
是( )
A.传统陶瓷是典型的绝缘材料
B.陶瓷主要成分为SiO 和MgO
2
C.陶瓷烧制的过程为物理变化
D.白瓷的白色是因铁含量较高
12、下列关于硅及其化合物的描述中正确的是( )
A.SiO 硬度大,故可用于制造光导纤维
2
B . 在 给 定 条 件 下 , 下 列 物 质 间 转 化 可 实 现 :
CaCO ――→CaO――→CaSiO
3 3
C.硅太阳能电池工作时,光能转化成电能,该过程与氧化还原反应有关
D.在给定条件下,下列物质间转化可实现:SiO ――――→SiCl ――→Si
2 4
13、科学家研究发现,水蒸气冷凝成直径小于10 μm(1 μm=10-6 m)的水滴
后会自发形成H O ,揭示了世界上第一个O 分子可能来自H O 的分解。下列
2 2 2 2 2
有关说法不正确的是( )
A.太阳光直射过10 μm大小的水滴会产生丁达尔现象
B.“H O→H O ”中氧元素被氧化
2 2 2
C.每产生2.24 L O (标准状况下)需分解6.8 g H O
2 2 2
D.水蒸气冷凝生成H O 是一种简单经济的绿色杀菌剂生产工艺
2 2
14、分别取40 mL 0.50 mol·L-1盐酸与40 mL 0.55 mol·L-1氢氧化钠溶液进
行中和反应反应热的测定实验,实验装置如图。下列说法错误的是( )A.加入稍过量的氢氧化钠的目的是确保盐酸完全反应
B.仪器A的名称是玻璃搅拌器
C.在实验过程中,测量完盐酸的温度后,把温度计上的酸用水冲洗干净后
再测量NaOH溶液的温度
D.用稀醋酸代替稀盐酸,结果是一样的
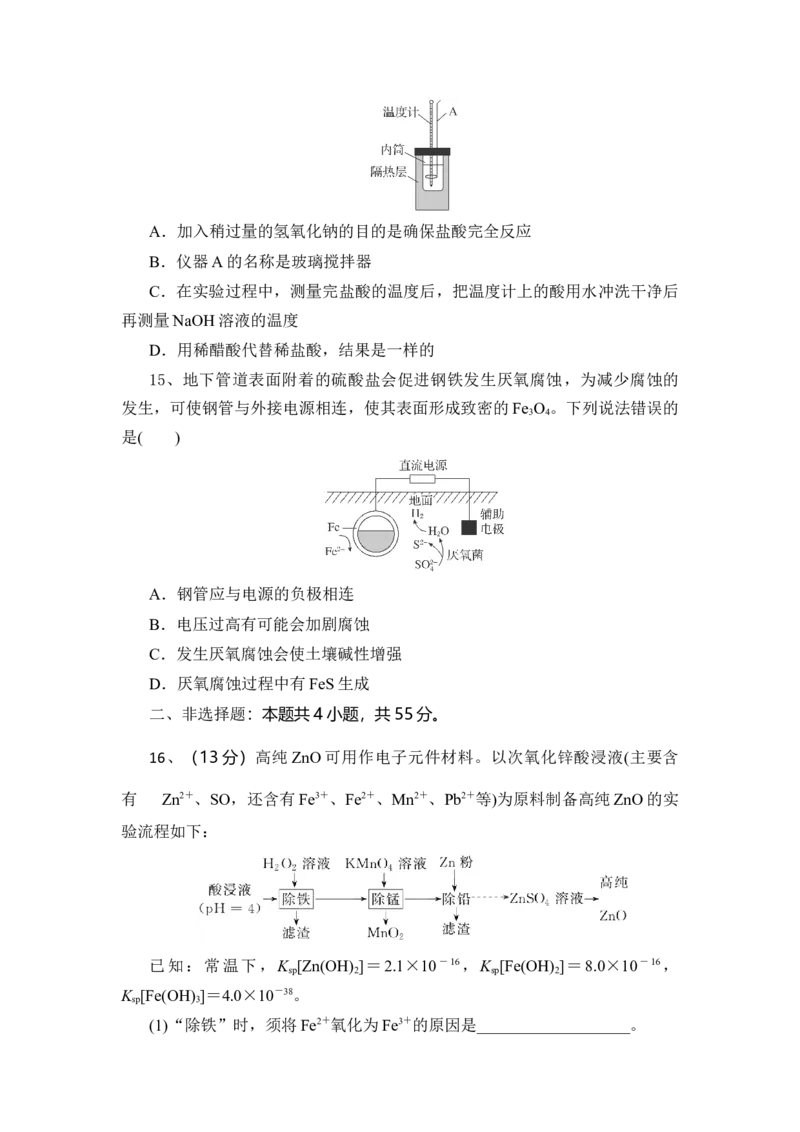
15、地下管道表面附着的硫酸盐会促进钢铁发生厌氧腐蚀,为减少腐蚀的
发生,可使钢管与外接电源相连,使其表面形成致密的Fe O 。下列说法错误的
3 4
是( )
A.钢管应与电源的负极相连
B.电压过高有可能会加剧腐蚀
C.发生厌氧腐蚀会使土壤碱性增强
D.厌氧腐蚀过程中有FeS生成
二、非选择题:本题共4小题,共55分。
16、(13分)高纯ZnO可用作电子元件材料。以次氧化锌酸浸液(主要含
有 Zn2+、SO,还含有Fe3+、Fe2+、Mn2+、Pb2+等)为原料制备高纯ZnO的实
验流程如下:
已知:常温下,K [Zn(OH) ]=2.1×10-16,K [Fe(OH) ]=8.0×10-16,
sp 2 sp 2
K [Fe(OH) ]=4.0×10-38。
sp 3
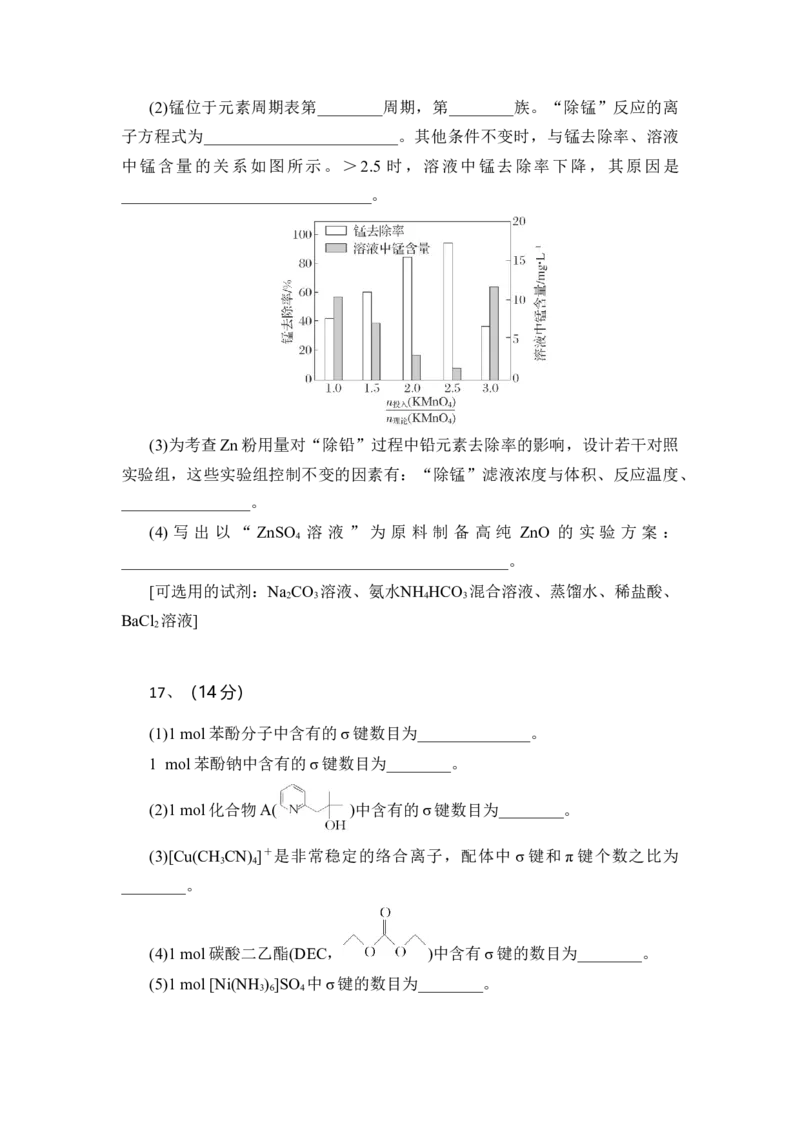
(1)“除铁”时,须将Fe2+氧化为Fe3+的原因是___________________。(2)锰位于元素周期表第________周期,第________族。“除锰”反应的离
子方程式为________________________。其他条件不变时,与锰去除率、溶液
中锰含量的关系如图所示。>2.5 时,溶液中锰去除率下降,其原因是
_______________________________。
(3)为考查Zn粉用量对“除铅”过程中铅元素去除率的影响,设计若干对照
实验组,这些实验组控制不变的因素有:“除锰”滤液浓度与体积、反应温度、
________________。
(4) 写 出 以 “ ZnSO 溶 液 ” 为 原 料 制 备 高 纯 ZnO 的 实 验 方 案 :
4
________________________________________________。
[可选用的试剂:Na CO 溶液、氨水NH HCO 混合溶液、蒸馏水、稀盐酸、
2 3 4 3
BaCl 溶液]
2
17、(14分)
(1)1 mol苯酚分子中含有的σ键数目为______________。
1 mol苯酚钠中含有的σ键数目为________。
(2)1 mol化合物A( )中含有的σ键数目为________。
(3)[Cu(CH CN) ]+是非常稳定的络合离子,配体中 σ 键和 π 键个数之比为
3 4
________。
(4)1 mol碳酸二乙酯(DEC, )中含有σ键的数目为________。
(5)1 mol [Ni(NH ) ]SO 中σ键的数目为________。
3 6 418、(14分)
如图为化学教学中所用的喷泉实验装置。某同学用烧瓶中盛不同成分的气
体进行喷泉实验,请帮助分析实验后烧瓶中所得溶液的浓度(假设是在标准状况
下完成实验,且溶质不扩散)。
(1)若用HCl气体,则c(HCl)=____________________________。
(2)若用NO 气体,则c(HNO )=___________________________。
2 3
(3)若用n(NO )∶n(O )=2∶1的混合气体,则c(HNO )=__________。
2 2 3
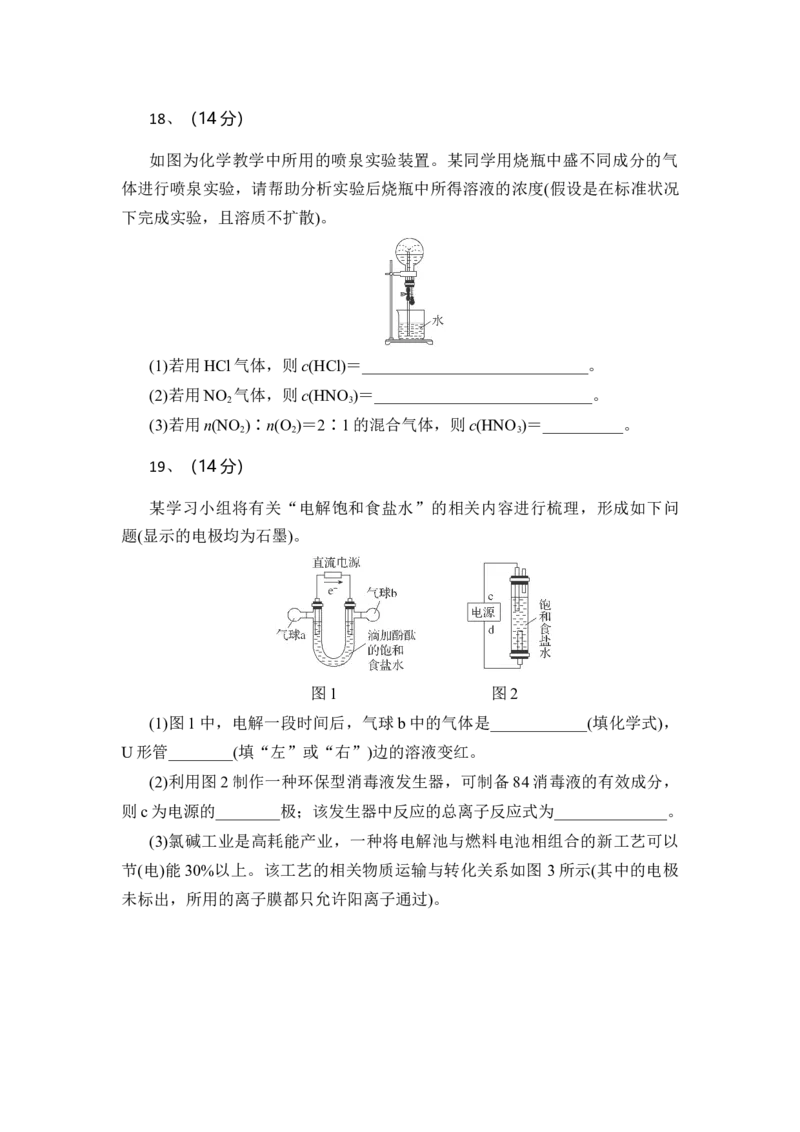
19、(14分)
某学习小组将有关“电解饱和食盐水”的相关内容进行梳理,形成如下问
题(显示的电极均为石墨)。
图1 图2
(1)图1中,电解一段时间后,气球b中的气体是____________(填化学式),
U形管________(填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,可制备84消毒液的有效成分,
则c为电源的________极;该发生器中反应的总离子反应式为______________。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以
节(电)能30%以上。该工艺的相关物质运输与转化关系如图 3所示(其中的电极
未标出,所用的离子膜都只允许阳离子通过)。图3
①燃料电池B中的电极反应式分别为
负极:______________________________________________________,
正极:_____________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序
为_____________________________________________________。高一化学试题答案
一、选择题:
1、解析:A A.Ca(OH) 与少量Ca(HCO ) 反应的离子方程式为Ca2++OH-+
2 3 2
HCO===CaCO ↓+H O,故A正确;B.Na O 不能拆为离子形式,离子方程式
3 2 2 2
为 2Na O +4H+===O ↑+2H O+4Na+,故 B 错误;C.向饱和食盐水中先通
2 2 2 2
NH ,再通足量 CO 会生成 NaHCO 晶体,离子方程式为 Na++NH +CO +
3 2 3 3 2
H O===NaHCO ↓+NH,故C错误;D.HClO为弱酸,不能拆开,离子方程式
2 3
为Cl +H O H++Cl-+HClO,故D错误。
2 2
2、解析:C
⥫ ⥬
A项,还原性:SO
2
>Fe2+,反应能发生;B项,还原性:SO
2
>I
-,反应能发生;C项,还原性:H O <SO ,反应不能发生;D项,还原性:
2 2 2
Fe2+>Cl-,反应能发生。
3、解析:B A.氯化钙和二氧化碳不反应,A错误;B.高锰酸钾具有强氧化
性,酸性介质中KMnO 氧化H O 生成氧气,同时高锰酸根离子被还原为锰离
4 2 2
子,B正确;C.向Ba(OH) 溶液中滴入少量NaHSO 溶液,氢氧根离子过量,反
2 4
应为H++SO+OH-+Ba2+===BaSO ↓+H O,C错误;D.氧化铁为三氧化二
4 2
铁,将稀盐酸滴在氧化铁上生成氯化铁和水:6H++Fe O ===2Fe3++3H O,D
2 3 2
错误;故选B。
4、解析:C 溶质的物质的量 n== mol,溶液体积 V=×10-3 L·mL-1=
L,Ca(NO ) 的物质的量浓度c=== mol·L-1,NO的物质的量浓度为 mol·L-
3 2
1×2= mol·L-1。
5、解析:B 先滴加氯水,再滴加KSCN溶液,溶液显红色,只能证明加氯水
后的溶液中含有Fe3+,无法确定加氯水前的溶液中是否含有 Fe2+、Fe3+,①不
正确;先滴加KSCN溶液,溶液不显红色,证明不含Fe3+,再滴加氯水,溶液
显红色,证明滴加氯水前的溶液中含有Fe2+,②正确;滴加NaOH溶液,先产
生白色絮状沉淀,后沉淀迅速变成灰绿色,最后变成红褐色,能证明原溶液中
含有Fe2+而不含有Fe3+,③正确;滴加KSCN溶液,溶液不显红色,只能证明
原溶液中不含有Fe3+,不能证明含有Fe2+,④不正确。
6、解析:D B装置的作用是吸收CO 中的水蒸气,即干燥CO ,故A正确;
2 2
在双球干燥管内CO 与Na O 反应,化学方程式为2Na O +2CO ===2Na CO +
2 2 2 2 2 2 2 3O ,故B正确;在双球干燥管中反应生成Na CO 使固体由淡黄色变为白色,反
2 2 3
应产生的O 有助燃性,能使点燃的蚊香燃烧更加剧烈,故C正确;若将Na O
2 2 2
换成Na O,Na O与CO 反应生成Na CO ,无O 生成,在CO 环境中蚊香逐渐
2 2 2 2 3 2 2
熄灭,故实验现象不相同,D项错误。
7、解析:B 经过反应①,Fe由二价升高为三价,需要空气作氧化剂,A正确;
硫酸过量,Al(OH) 会溶解,不能从混合体系中分离出来,B错误;Na CrO 加
3 2 4
入硫酸得到Na Cr O ,硫酸的作用是提高c(H+)促使Cr元素转化为Cr O,C正
2 2 7 2
确;④是Al和Cr O 在高温条件下发生的置换反应,属于铝热反应,D正确。
2 3
8、解析:C 石墨层间存在分子间作用力、层内存在金属键,层内具有金属晶
体的性质、层间具有分子晶体的性质,所以石墨晶体中层内导电性强于层间导
电性,故A正确;基态Cr3+的最高能层为M层,排布式为3s23p63d3,有8个成
对电子,3个未成对单电子,所以基态Cr3+的最高能层中成对电子与未成对电
子的数目比为8∶3,故B正确;ClO中中心氯原子的价层电子对数=3+=4,
氯原子含有 1 个孤电子对,ClO 的空间结构为三角锥形,故 C 错误;
(CH COO) Ni·4H O的空间构型为八面体,则CH COO-、H O都是Ni2+的配体,
3 2 2 3 2
所以其配位数是6,故D正确。
9、解析:D 蒸发浓缩消毒液需在蒸发皿中进行,D错误。
10、解析:C 根据图示可知,X为SO ,Y为SO ,Z为H SO ,M为CuSO ;
2 3 2 4 4
S在过量氧气中燃烧生成二氧化硫,SO 催化氧化生成SO ,故A错误;盐酸的
2 3
酸性大于亚硫酸的酸性,则SO 通入BaCl 溶液中,不发生反应,无现象,故B
2 2
错误;根据方程式2H S+SO ===3S+2H O,2 mol H S失去的电子与1 mol SO
2 2 2 2 2
得到的电子相等,则氧化产物和还原产物的物质的量之比为2∶1,故C正确;
由图中元素的化合价及物质类别可知,M 为硫酸铜,与 H S 反应生成 N 为
2
CuS,S具有弱氧化性,与Cu化合生成Cu S,故D错误。
2
11、解析:A 陶瓷是良好的绝缘体,传统陶瓷是典型的绝缘材料,A正确;陶
瓷的主要成分为硅酸盐,而不是SiO 和MgO,B错误;陶瓷烧制过程发生复杂
2
的化学反应,有新物质生成,属于化学变化,C错误;由于Fe2+、Fe3+和铁的
氧化物均有颜色,故陶瓷中含铁量越高,陶瓷的颜色越深,白瓷的白色是因为
铁含量较低甚至几乎不含,D错误。12、解析:B SiO 可用于制造光导纤维的原因是其导光性能好,与硬度无对应
2
关系,A 错误;CaCO 高温分解生成 CaO,CaO 与 SiO 在高温时反应生成
3 2
CaSiO ,B正确;硅太阳能电池工作时,利用半导体的光电效应,将光能转化
3
为电能,与氧化还原反应无关,C错误;SiO 不能与盐酸反应,D错误。
2
13、解析:A 只有胶体才有丁达尔效应,10 μm=10-5 m,此直径的水滴在空
气中形成的分散系不是胶体,故无丁达尔效应,故A错误;“H O→H O ”中
2 2 2
氧元素化合价升高,被氧化,故B正确;标准状况下2.24 L氧气的物质的量为
n==0.1 mol,而H O 的分解反应为2H O ===2H O+O ↑,故生成0.1 mol氧
2 2 2 2 2 2
气需要过氧化氢 0.2 mol,其质量m=0.2 mol×34 g·mol-1=6.8 g,故C正确;
过氧化氢有较强的氧化性,能杀菌消毒,水蒸气冷凝生成H O 是一种简单经济
2 2
的绿色杀菌剂生产工艺,故D正确。
14、解析:D 醋酸是弱酸,电离吸热,使测得的反应放出的热量偏小,D项错
误。
15、解析:A 钢管表面形成Fe O ,Fe失去电子,作为阳极,应与电源正极相
3 4
连,A错误;电压过高,Fe有可能转化为Fe2+或Fe3+,会加剧腐蚀,B正确;
发生厌氧腐蚀时,阴极会发生反应2H O+2e-===2OH-+H ↑,会使土壤碱性
2 2
增强,C正确;厌氧腐蚀过程中,阳极上有Fe2+生成,阴极附近有S2-生成,则
该过程中有FeS生成,D正确。
二、非选择题:
16、解析:(1)由 Zn(OH) 与 Fe(OH) 的 K 数据可知 Zn(OH) 与 Fe(OH) 沉淀时
2 2 sp 2 2
pH相近,不易通过调pH分离Fe2+和Zn2+;Zn(OH) 与Fe(OH) 沉淀时pH相差
2 3
较大,易于通过调 pH分离 Fe3+和Zn2+。(2)锰位于元素周期表第四周期,第
ⅦB族;“除锰”过程中,高锰酸钾溶液将Mn2+氧化为MnO ,离子方程式为:
2
3Mn2++2MnO+2H O===5MnO ↓+4H+;由图可知,当>2.5时,溶液中锰含
2 2
量增大,而锰去除率下降,其原因是:过量的KMnO 进入溶液。(3)为考查Zn
4
粉用量对“除铅”过程中铅元素去除率的影响,实验组控制不变的因素有:
“除锰”滤液浓度与体积、反应温度、反应时间、搅拌速率。(4)以“ZnSO 溶
4
液”为原料制备高纯ZnO的实验方案为:在搅拌下向ZnSO 溶液中缓慢滴加氨
4
水-NH HCO 混合溶液;当向上层清液中继续滴加氨水-NH HCO 溶液后不再产
4 3 4 3生沉淀时,过滤,所得滤渣用蒸馏水洗涤,直至最后一次洗涤滤液加入稀盐酸
和BaCl 溶液后不再产生浑浊;将所得沉淀烘干后灼烧至恒重。
2
答案:(1)Zn(OH) 与Fe(OH) 沉淀时 pH相近,不易通过调 pH分离 Fe2+和Zn2
2 2
+;Zn(OH) 与 Fe(OH) 沉淀时 pH 相差较大,易于通过调 pH 分离 Fe3+和
2 3
Zn2+
(2)四 ⅦB 3Mn2++2MnO+2H O===5MnO ↓+4H+ 过量的KMnO 进入溶
2 2 4
液 (3)反应时间、搅拌速率 (4)在搅拌下向 ZnSO 溶液中缓慢滴加氨水-
4
NH HCO 混合溶液;当向上层清液中继续滴加氨水-NH HCO 溶液后不再产生
4 3 4 3
沉淀时,过滤,所得滤渣用蒸馏水洗涤,直至最后一次洗涤滤液加入稀盐酸和
BaCl 溶液后不再产生浑浊;将所得沉淀烘干后灼烧至恒重
2
17、解析:(3)配体CH CN中含有 3个C—H、1个C—C和1个C≡N键,故1
3
mol CH CN中含有5N σ键、2N π键,σ键与π键个数之比为5∶2。
3 A A
答案:(1)13N 12N (2)24N (3)5∶2 (4)17N (5)28N
A A A A A
18、解析:设烧瓶的容积为V L,则气体(混合气体)的物质的量均为 mol。
(1)若用HCl气体,喷泉后,溶液充满烧瓶,则溶液的体积为V L,c(HCl)==
mol·L-1。
(2)若用NO ,喷泉后,溶质为HNO ,
2 3
3NO + H O=== 2HNO +NO
2 2 3
mol × mol
则喷泉后溶液的体积为V L,c(HNO )== mol·L-1。
3
(3)若为n(NO )∶n(O )=2∶1的混合气体,喷泉后,溶质为HNO ,
2 2 3
4NO + O + 2H O=== 4HNO
2 2 2 3
× ×× ×
则喷泉后溶液的体积为V L,c(HNO )== mol·L-1。
3
答案:(1) mol·L-1 (2) mol·L-1 (3) mol·L-1
19、解析:(1)图1中,根据电子流向知,左边电极是电解池阳极,右边电极是
电解池阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以
气球a中的气体是氯气,气球b中的气体是氢气,同时阴极附近有NaOH生成,溶液呈碱性,无色酚酞遇碱变红色,所以U形管右边溶液变红色。
(2)利用图2制作一种环保型消毒液发生器,阳极上氯离子放电生成氯气,阴极
上氢离子放电生成氢气,同时阴极有 NaOH生成,氯气和氢氧化钠反应生成
NaClO,次氯酸钠具有漂白性,为了使反应更充分,则下边电极生成氯气,上
边电极附近有NaOH生成,上边电极生成氢气,为阴极,则c为负极,d为正极,
总离子反应式为Cl-+H OClO-+H ↑。
2 2
(3)①B是燃料电池,电池右边中通入空气,左边通入气体Y,则Y是氢气,则
电解池中左边电极是阳极,右边电极是阴极,阳极上氯离子放电,阴极上氢离
子放电;燃料电池中通入空气的电极是正极,通入氢气的电极是负极,正极上
氧气得电子和水反应生成氢氧根离子,负极上氢气失电子和氢氧根离子反应生
成水,负极、正极反应式分别为 2H -4e-+4OH-===4H O、O +4e-+
2 2 2
2H O===4OH-。②图3电解池中加入NaOH溶液的目的是增大溶液导电性,通
2
入电解池后生成氢氧化钠,所以加入的NaOH溶液浓度小于出来的 NaOH溶液
浓度;燃料电池中,正极上生成氢氧化钠,所以出来的NaOH溶液浓度大于加
入的NaOH溶液浓度,所以NaOH溶液浓度大小顺序是b%>a%>c%。
答案:(1)H 右
2
(2)负 Cl-+H OClO-+H ↑
2 2
(3)①2H -4e-+4OH-===4H O O +4e-+2H O===4OH- ②b%>a%>c%
2 2 2 2