文档内容
【冲刺期末】高二化学期末单元复习测试
第三单元 水溶液中的离子反应与平衡
(时间:90分钟 满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.(2020河北唐山高二上期末)亚硫酸与氢硫酸都是二元弱酸,下列事实中,不能比较亚硫酸与氢硫酸的酸性
强弱的是
A. 亚硫酸的还原性比氢硫酸弱
B. 相同条件下,导电能力亚硫酸强于氢硫酸
C. 0.10 mol·L-1的亚硫酸和氢硫酸溶液的pH分别为2.1和4.5
D. 亚硫酸可以与碳酸氢钠溶液反应,而氢硫酸不能
【答案】A
【解析】氢硫酸的还原性强于亚硫酸,不能用于比较二者酸性的强弱,A错误;相同条件下,氢硫酸的导电能
力弱于亚硫酸,说明亚硫酸的电离程度大,则亚硫酸的酸性强于氢硫酸,B正确;0.10 mol·L-1的亚硫酸和氢硫
酸溶液的pH分别为2.1和4.5,说明亚硫酸的电离程度大,酸性较强,C正确;氢硫酸不能与碳酸氢钠溶液反应,
而亚硫酸可以,说明亚硫酸的酸性比氢硫酸的酸性强,D正确。
2.(2020陕西西安中学高二上期中)由表格中电离常数判断下列反应可以发生的是
弱酸 HClO HCO
2 3
电离平衡常数 K=4.3×10-7
1
K=3.2×10-8
(25 ℃) K=4.7×10-11
2
A. NaClO+NaHCO === HClO+Na CO
3 2 3
B. NaClO+CO +H O=== HClO+NaHCO
2 2 3
C. 2NaClO+CO +H O=== 2HClO+Na CO
2 2 2 3
D. 2HClO+Na CO=== 2NaClO+CO ↑+H O
2 3 2 2
【答案】B
【解析】由题表中数据可知,酸性:HCO>HClO> 。因酸性HClO> ,则反应NaClO+NaHCO ===
2 3 3
HClO+Na CO 不能发生,A项错误;
2 3
因酸性HCO>HClO> ,则反应NaClO+CO +H O=== HClO+NaHCO 能发生,B项正确;
2 3 2 2 3
因酸性HClO> ,则反应2NaClO+CO +H O=== 2HClO+Na CO 不能发生,C项错误;
2 2 2 3因酸性HCO>HClO,则反应2HClO+Na CO=== 2NaClO+CO ↑+H O不能发生,D项错误。
2 3 2 3 2 2
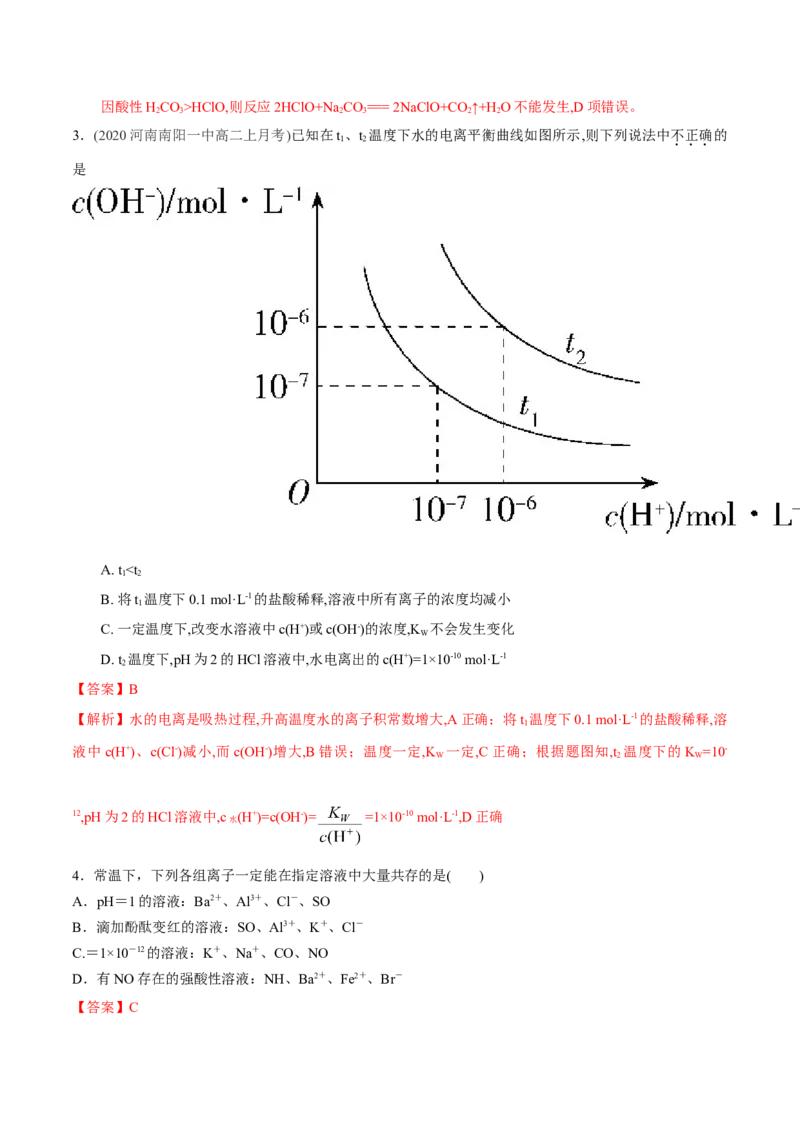
3.(2020河南南阳一中高二上月考)已知在t 、t 温度下水的电离平衡曲线如图所示,则下列说法中不正确的
1 2
是
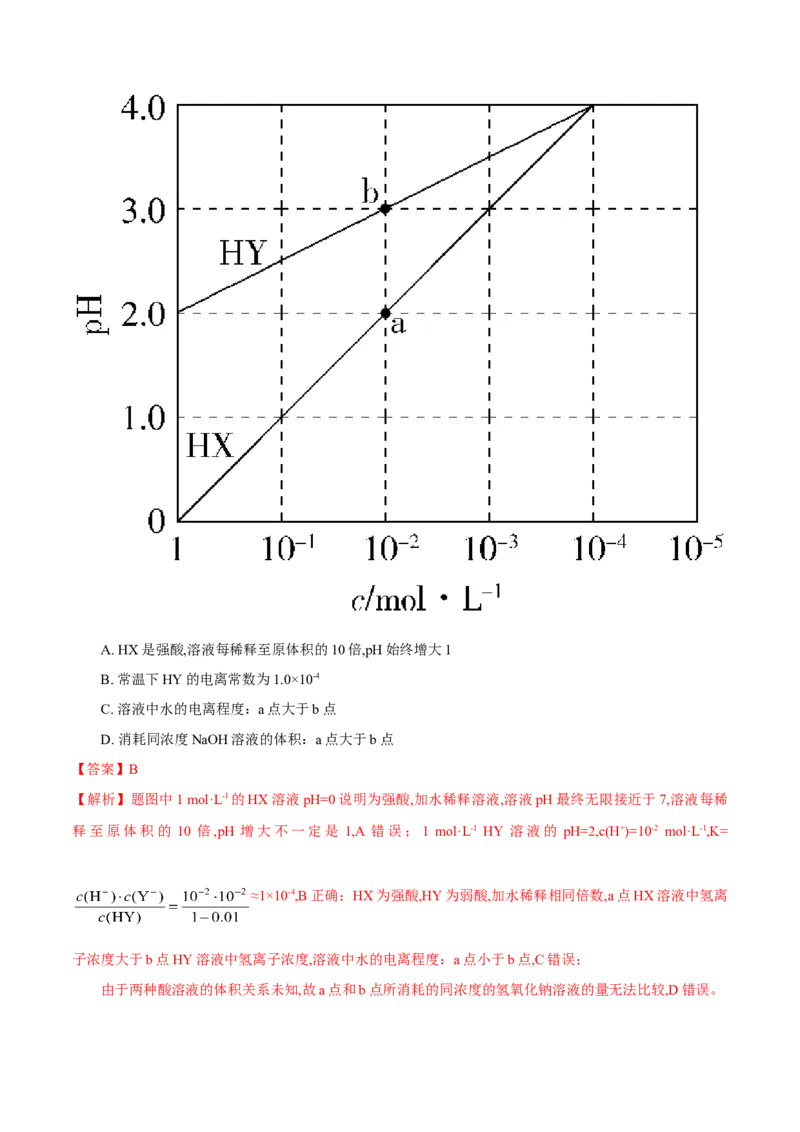
A. tc(K+)>c(OH-)
【答案】C
【解析】随着NaOH溶液的加入,混合溶液中离子浓度和种类发生变化,因此混合溶液的导电能力与离子浓
度和种类有关,A项正确;a点的混合溶液中能导电的离子主要为HA-和K+,b点为反应终点,因此b点的混合
溶液中能导电的离子主要为A2-、K+、Na+,故Na+与A2-的导电能力之和大于HA-的,B项正确;b点的混合溶
液中含有的 A2-能发生水解反应而使溶液呈碱性,C 项错误;b 点为反应终点,因此 b 点的混合溶液中
c(Na+)=c(K+)>c(OH-),继续加入氢氧化钠溶液后,c点的混合溶液中c(Na+)>c(K+)>c(OH-),D项正确。
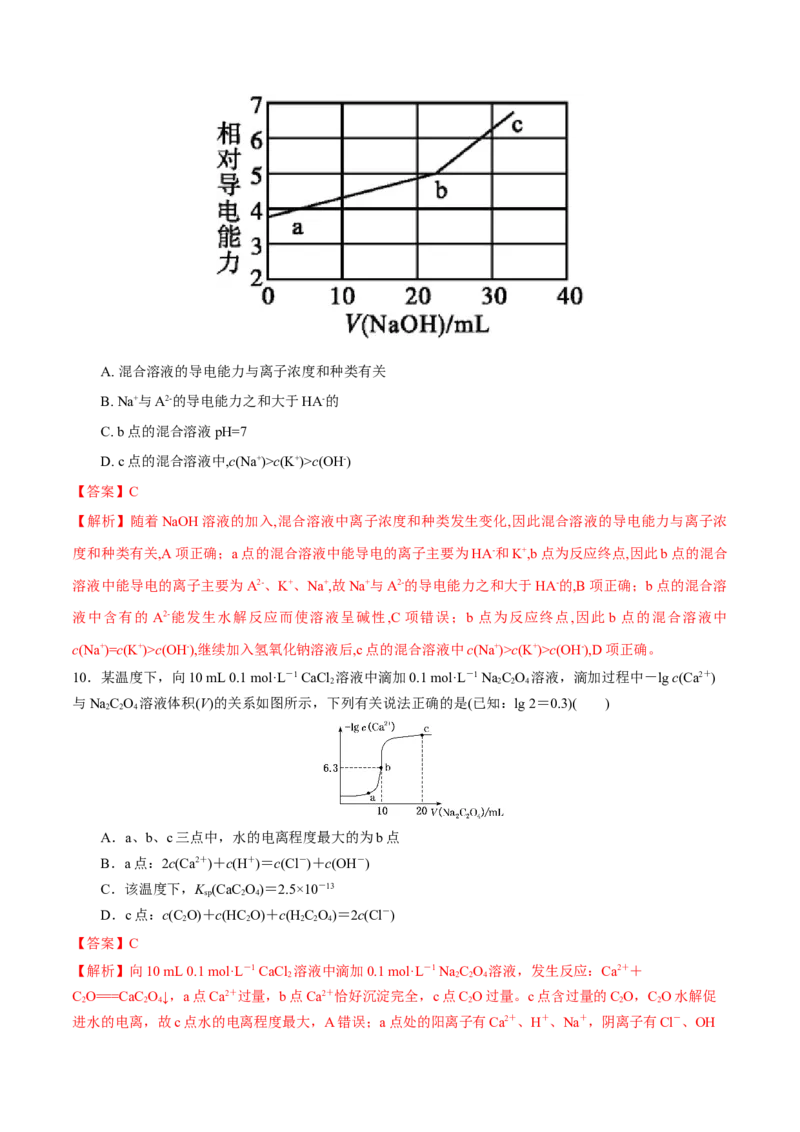
10.某温度下,向10 mL 0.1 mol·L-1 CaCl 溶液中滴加0.1 mol·L-1 Na C O 溶液,滴加过程中-lg c(Ca2+)
2 2 2 4
与NaC O 溶液体积(V)的关系如图所示,下列有关说法正确的是(已知:lg 2=0.3)( )
2 2 4
A.a、b、c三点中,水的电离程度最大的为b点
B.a点:2c(Ca2+)+c(H+)=c(Cl-)+c(OH-)
C.该温度下,K (CaC O)=2.5×10-13
sp 2 4
D.c点:c(C O)+c(HC O)+c(H C O)=2c(Cl-)
2 2 2 2 4
【答案】C
【解析】向10 mL 0.1 mol·L-1 CaCl 溶液中滴加0.1 mol·L-1 Na C O 溶液,发生反应:Ca2++
2 2 2 4
C O===CaC O↓,a点Ca2+过量,b点Ca2+恰好沉淀完全,c点C O过量。c点含过量的C O,C O水解促
2 2 4 2 2 2
进水的电离,故c点水的电离程度最大,A错误;a点处的阳离子有Ca2+、H+、Na+,阴离子有Cl-、OH-、C O、HC O,电荷守恒式为2(Ca2+)+(H+)+(Na+)=c(Cl-)+c(OH-)+2c(C O)+c(HC O),B错误;由
2 2 2 2
于lg 2=0.3,故100.3=2,所以10-0.6=。根据分析,b点Ca2+恰好沉淀完全,c(Ca2+)=c(C O)=10-6.3
2
mol·L-1,该温度下K (CaC O)=c(Ca2+)·c(C O)=10-6.3×10-6.3=10-12.6=10-12×10-0.6=10-12×=2.5×10-13,
sp 2 4 2
C正确;c点处n(Cl-)=2×0.01 L×0.1 mol·L-1=0.002 mol,过量n(Na C O)=0.01 L×0.1 mol·L-1=0.001
2 2 4
mol,由物料守恒可得2c(C O)+2c(HC O)+2c(H C O)=c(Cl-),D错误。
2 2 2 2 4
11.已知:25 ℃时,HC O 和HCO 的电离平衡常数如下:
2 2 4 2 3
分子式 HC O HCO
2 2 4 2 3
K =5.4×10-2, K =4.2×10-7,K =
a1 a1 a2
电离平衡常数
K =5.4×10-5 5.6×10-11
a2
以下操作均在25 ℃条件下进行,则下列说法不正确的是( )
A.KHC O 溶液呈酸性,KHCO 溶液呈碱性
2 4 3
B.在KHC O 溶液中通入足量CO 生成的盐只有KHCO
2 4 2 3
C.分别向20 mL 0.1 mol·L-1 H C O 和HCO 溶液中加入0.1 mol·L-1 NaOH溶液至中性,前者消耗
2 2 4 2 3
NaOH多
D.将等物质的量浓度的HC O 和NaOH溶液等体积混合,所得溶液中各微粒浓度大小顺序为c(Na+)
2 2 4
>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
【答案】B
【解析】HC O的水解平衡常数K ===×10-12<5.4×10-5,HC O的电离程度大于其水解程度,溶液显酸
2 h 2
性;HCO的水解常数K ===×10-7>5.6×10-11,HCO的水解程度大于其电离程度,溶液显碱性,A正确;
h
根据表中数据知, HC O 的K 大于HCO 的K ,可知在KHC O 溶液中通入足量CO 时,CO 与
2 2 4 a2 2 3 a1 2 4 2 2
KHC O 溶液不发生化学反应,B错误;草酸和碳酸均为二元弱酸,和NaOH反应生成的正盐均显碱性,草
2 4
酸氢根离子的电离常数大于碳酸氢根离子的电离常数,则相同条件下碳酸钠的碱性强于草酸钠,因此到达
中性时碳酸消耗的NaOH较少,C正确;两者等体积、等物质的量浓度混合,生成NaHC O,HC O的电
2 4 2
离程度大于水解,所得溶液中各微粒浓度大小顺序为c(Na+)>c(HC O)>c(C O)>c(H C O),D正确。
2 2 2 2 4
12.亚砷酸(H AsO )可以用于治疗白血病,在溶液中存在多种微粒形态。室温下,向25.00 mL 0.100 0
3 3
mol·L-1 H AsO 溶液中逐滴加入0.100 0 mol·L-1 KOH 溶液,各种微粒物质的量分数与溶液pH的关系如图
3 3
所示。下列说法不正确的是( )
A.HAsO 的电离平衡常数K =10-9.3
3 3 a1
B.M点对应的溶液中:c(H AsO )+2c(HAsO)+c(AsO)=0.100 0 mol·L-1
3 3
C.c(K+)=0.050 00 mol·L-1的溶液中:c(H+)+c(H AsO)+2c(H AsO )=0.050 00 mol·L-1+c(OH-)+
2 3 3
c(AsO)D.pH=12的溶液中:c(K+)>c(H AsO)>c(OH-)>c(H AsO )>c(H+)
2 3 3
【答案】B
【解析】c(H AsO)=c(H AsO )时,HAsO 的电离平衡常数K =c(H+)=10-pH=10-9.3,故A正确;M点对
2 3 3 3 3 a1
应的溶液中c(H AsO)=c(HAsO),该溶液中存在物料守恒n(H AsO )+n(HAsO)+n(AsO)+n(H AsO)=0.100
2 3 3 2
0 mol·L-1×0.025 L=0.002 5 mol,因为加入KOH溶液导致混合溶液体积增大,则c(H AsO )+2c(HAsO)+
3 3
c(AsO)<0.100 0 mol·L-1,故B错误;c(K+)=0.050 00 mol·L-1的溶液中,c(KOH)是原来的一半,说明混
合后溶液体积增大一倍,则酸碱的物质的量相等,溶液中存在电荷守恒:c(K+)+c(H+)=2c(HAsO)+
3c(AsO)+c(OH-)+c(H AsO),存在物料守恒:c(K+)=c(HAsO)+c(AsO)+c(H AsO )+c(H AsO)=0.050 00
2 3 3 2
mol·L-1,所以存在c(H AsO )+c(H+)=c(HAsO)+2c(AsO)+c(OH-),2c(H AsO )+c(H AsO)+c(H+)=
3 3 3 3 2
c(HAsO)+2c(AsO)+c(OH-)+c(H AsO )+c(H AsO)=0.050 00 mol·L-1+c(OH-)+c(AsO),故C正确;pH
3 3 2
=12的溶液呈碱性,则c(OH-)>c(H+),根据电荷守恒得c(K+)>c(H AsO),溶液呈碱性说明HAsO、
2 2
HAsO水解程度大于其电离程度且都水解生成OH-,则c(OH-)>c(H AsO ),溶液碱性较强,则溶液中c(H
3 3
+)很小,所以存在c(K+)>c(H AsO)>c(OH-)>c(H AsO )>c(H+),故D正确。
2 3 3
13.下列叙述正确的是( )
A.c(H+)等于1×10-7 mol·L-1的溶液一定是中性溶液
B.稀释醋酸钠溶液,CHCOO- 水解程度变大,故溶液的pH增大
3
C.0.2 mol·L-1 CH COOH溶液中的c(H+)是0.1 mol·L-1 CH COOH溶液中的c(H+)的2倍
3 3
D.相同条件下,弱酸HA比HB易电离,则同浓度的NaA溶液的pH比NaB溶液的pH小
【答案】D
【解析】常温时,c(H+)等于1×10-7 mol·L-1的溶液一定是中性溶液,但题目未给定温度,无法判断溶液是
否为中性,A错误;CHCOONa溶液存在水解平衡:CHCOO-+HOCH COOH+OH-,稀释溶液,平
3 3 2 3
衡正向移动,平衡状态下氢氧根离子浓度减小,溶液pH减小,B错误;0.2 mol·L-1 CH COOH溶液的体积
3
增大一倍,醋酸的电离平衡正向进行,溶液中的c(H+)大于0.1 mol·L-1,则0.2 mol·L-1 CH COOH溶液中
3
的c(H+)比0.1 mol·L-1 CH COOH溶液中的c(H+)的2倍小,C错误;相同条件下,弱酸HA比HB易电离,
3
则HA比HB的酸性强,同浓度的NaA溶液的水解程度比NaB溶液的小,NaA溶液产生的氢氧根离子少,
则NaA溶液的pH小,D正确。
14.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
A.向0.10 mol·L-1 CH COONa溶液中滴加0.10 mol·L-1 HCl溶液恰好使溶液呈中性:c(Na+)>c(CHCOO
3 3
-)>c(CHCOOH)>c(Cl-)
3
B.将NaCO 和NaHCO 的稀溶液混合恰好至溶液中c(CO)=c(HCO):2c(Na+)<3c(CO)+3c(HCO)+
2 3 3
3c(H CO)
2 3
C.向0.10 mol·L-1 NHHSO 溶液中滴加NaOH溶液恰好呈中性:c(Na+)=c(SO)+c(NH ·H O)
4 4 3 2
D.将等体积等物质的量浓度的CHCOONa和NaF溶液混合:c(CHCOOH)+c(HF)=c(OH-)+c(H+)
3 3
【答案】C
【解析】CHCOONa与盐酸反应生成CHCOOH和NaCl,溶液呈中性,推出溶质为CHCOONa、
3 3 3
CHCOOH和NaCl,根据电荷守恒,推出c(Na+)+c(H+)=c(CHCOO-)+c(OH-)+c(Cl-),因为溶液呈中
3 3性,推出c(Na+)=c(CHCOO-)+c(Cl-),根据物料守恒,推出c(Na+)=c(CHCOO-)+c(CHCOOH),推出
3 3 3
c(CHCOOH)=c(Cl-),故A错误;假设NaCO 和NaHCO 物质的量相等,根据物料守恒,有2c(Na+)=
3 2 3 3
3c(CO)+3c(HCO)+3c(H CO),CO的水解程度大于HCO的水解程度,为了达到c(CO)=c(HCO),需要多
2 3
加入些NaCO,因此有2c(Na+)>3c(CO)+3c(HCO)+3c(H CO),故B错误;加入NaOH溶液,使溶液呈
2 3 2 3
中性,即有c(H+)=c(OH-),溶液中含有的离子有Na+、NH、H+、OH-、SO,根据电荷守恒,有c(Na+)
+c(NH)=2c(SO),根据物料守恒,有c(SO)=c(NH)+c(NH ·H O),联立得到c(Na+)=c(SO)+
3 2
c(NH ·H O),故C正确;根据电荷守恒,有c(Na+)+c(H+)=c(OH-)+c(CHCOO-)+c(F-),根据物料守恒
3 2 3
有:c(Na+)=c(CHCOOH)+c(CHCOO-)+c(HF)+c(F-),代入上式,得出c(CHCOOH)+c(HF)=c(OH-)
3 3 3
-c(H+),故D错误。
15.常温下,用AgNO 溶液分别滴定浓度均为0.01 mol·L-1的KCl、KC O 溶液,所得的沉淀溶解平衡图
3 2 2 4
像如图所示(不考虑C O的水解)。下列叙述不正确的是( )
2
A.K (Ag C O)等于10-10
sp 2 2 4
B.n点表示Ag C O 的不饱和溶液
2 2 4
C.向c(Cl-)=c(C O)的混合液中滴入AgNO 溶液时,先生成Ag C O 沉淀
2 3 2 2 4
D.Ag C O(s)+2Cl-(aq)2AgCl(s)+C O(aq)的平衡常数为108
2 2 4 2
【答案】C
【解析】结合图示数据可知,K (Ag C O)=c2(Ag+)·c(C O)=(10-4)2×10-2=10-10,故A正确;n点时c(Ag+)
sp 2 2 4 2
比Ag C O 溶解平衡曲线上的c(Ag+)小,Ag C O 溶解平衡向形成Ag+的方向移动,所以n点表示Ag C O
2 2 4 2 2 4 2 2 4
的不饱和溶液,故B正确;由图像可知,当阴离子浓度c(Cl-)=c(C O)时,生成AgCl沉淀所需的c(Ag+)小,
2
则向c(Cl-)=c(C O)的混合液中滴入AgNO 溶液时,先析出氯化银沉淀,故C错误;Ag C O(s)+2Cl-
2 3 2 2 4
(aq)2AgCl(s)+C O(aq)的平衡常数K=,此时溶液中的c(Ag+)相同,故有:K===108,故D正确。
2
二、非选择题(本题共5小题,共55分)
16.(10分)在氨水中存在下列电离平衡:NH·H O +OH-。
3 2
(1)下列情况能引起电离平衡正向移动的有 (填字母,下同)。
①加NH Cl固体 ②加NaOH溶液 ③通入HCl ④加CHCOOH溶液 ⑤加水 ⑥加压
4 3
a. ①③⑤ b. ①④⑥
c. ③④⑤ d. ①②④
(2)在含有酚酞的0.1 mol·L-1氨水中加入少量的NH Cl晶体,则溶液颜色 。
4
a. 变蓝色 b. 变深
c. 变浅 d. 不变(3)在一定温度下,用水缓慢稀释1 mol·L-1氨水的过程中,溶液中随着水量的增加:
①n(OH-) (填“增大”“减小”或“不变”,下同);
② ;
③ 。
【答案】(1)c (2)c (3)①增大 ②增大 ③不变
【解析】(1)①加入NH Cl固体相当于加入 ,平衡左移;②加入OH-,平衡左移;③通入HCl,相当于
4
加入H+,中和OH-,平衡右移;④加CHCOOH溶液,相当于加H+,中和OH-,平衡右移;⑤加水稀释,越稀越电
3
离,平衡右移;⑥加压对NH ·H O的电离平衡无影响。
3 2
(2)氨水中加入NH Cl晶体,c( )增大,则NH ·H O电离平衡逆向移动,c(OH-)减小,溶液颜色变浅。
4 3 2
(3)加水稀释,NH·H O 电离平衡向电离方向移动,n(OH-)逐渐增大,n(NH ·H O)逐渐减小,所以
3 2 3 2
逐 渐 增 大 ; 电 离 平 衡 常 数 K = 与 温 度 有 关 , 所 以 加 水 稀 释 时 ,
b
不变。
17.(10分)我国国标推荐的食品、药品中Ca元素含量的测定方法之一为利用NaC O 使处理后的样品中的
2 2 4
Ca2+形成沉淀,过滤、洗涤,然后将所得CaC O 固体溶于过量的强酸,最后使用已知浓度的KMnO 溶液通过滴
2 4 4
定来测定溶液中Ca2+的含量。回答以下问题:
(1)KMnO 溶液应该用 (填“酸式”或“碱式”)滴定管盛装,除滴定管外,还需要的玻璃仪器有
4
__________________________(写出两种即可)。
(2)试写出滴定过程中发生反应的离子方程式: 。
(3)滴定终点的颜色变化为溶液由 色变为 色。
(4)以下操作会导致测定结果偏高的是 (填字母)。
a. 装入KMnO 溶液前未润洗滴定管
4b. 滴定结束后俯视读数
c. 滴定结束后,滴定管尖端悬有一滴溶液
d. 滴定过程中,振荡时将少量待测液洒出
(5)某同学对上述实验方案进行了改进并用于测定某品牌的钙片(主要成分为CaCO )中钙元素的含量,其
3
实验过程如下:取2.00 g样品放入锥形瓶中,用酸式滴定管向锥形瓶内加入20.00 mL浓度为0.10 mol·L-1的
盐酸(盐酸过量),充分反应一段时间,用酒精灯将锥形瓶内液体加热至沸腾,数分钟后,冷却至室温,加入2~3滴
酸碱指示剂,用浓度为0.10 mol·L-1的NaOH溶液滴定至终点,消耗NaOH溶液8.00 mL。[提示:Ca(OH) 微溶
2
于水,pH较低时不会产生沉淀]据此回答:
①为使现象明显、结果准确,滴定过程中的酸碱指示剂应选择 (填“石蕊”“甲基橙”或“酚
酞”)溶液。
②实验过程中将锥形瓶内液体煮沸的目的是 。
③则此2.00 g钙片中CaCO 的质量为 g。
3
【答案】 (1)酸式 烧杯、锥形瓶(答案合理即可)
(2)2 +5 +16H+=== 2Mn2++10CO ↑+8H O (3)无 浅紫 (4)ac
2 2
(5)①甲基橙 ②将溶解在溶液中的CO 气体赶出 ③0.06
2
【解析】(1)高锰酸钾具有强氧化性,会腐蚀橡胶,应放在酸式滴定管中,中和滴定前需进行赶气泡、调零
等操作,用烧杯盛液体,滴定中用锥形瓶盛待测液,用滴定管盛标准液,故所需玻璃仪器有:酸式滴定管、
碱式滴定管、锥形瓶、烧杯,故答案为:酸式;锥形瓶、烧杯;
(2)高锰酸钾具有强氧化性,在硫酸条件下将 氧化为CO,自身被还原为Mn2+,离子方程式为:2
2
+5 +16H+=== 2Mn2+ +10CO ↑+8H O
2 2
(3)高锰酸钾溶液本身有颜色,为紫色,在开始滴入C2O2−4中时被还原,颜色消失,当达到滴定终点时,
加入最后一滴高锰酸钾溶液颜色不褪去,溶液由无色变为浅紫色,且半分钟内不褪色,
故答案为:无;紫;
(4)
a. 滴定时,滴定管经水洗,蒸馏水洗后加入滴定剂高锰酸钾溶液,标准液体被稀释,浓度变稀,造成V(标准)
偏大,由此计算结果偏大;
b. 滴定前平视,滴定后俯视,则所用标准液读数偏小,由此计算结果偏小;
c. 滴定结束后,滴定管尖端悬有一滴溶液,造成V(标准)偏大,由此计算结果偏大;d. 滴定过程中,振荡时将待测液洒出,所用标准液偏小,由此计算结果偏小;
故答案为:ac;
(5)实验过程中将锥形瓶内液体煮沸的目的是将溶解的 CO 气体赶出;该滴定若用“酚酞”作指示剂,它
2
的变色范围为8.2~10.0,则Ca(OH) 可能会形成沉淀析出,造成较大误差。
2
CaCO +2HCl=== CaCl +H O+CO↑
3 2 2 2
HCl + NaOH=== NaCl+HO
2
8.00×10-3 L×0.10 mol·L-1 8.00×10-3 L×0.10 mol·L-1
CaCO 所 消 耗 的 HCl 的 物 质 的 量 为 20.00×10-3 L×0.10 mol·L-1-8.00×10-3 L×0.10 mol·L-1=1.2×10-3
3
mol,m(CaCO )= ×100 g·mol-1=0.06 g。
3
18.(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下,将0.2 mol·L-1某一元酸HA溶液和0.1 mol·L-1 NaOH溶液等体积混合后溶液pH大于7,若混
合液体积等于两溶液体积之和,则混合液中下列关系正确的是__________(填字母)。
A.c(HA)c(A
-),错误;B项,因等体积混合,则反应后c(HA)一定小于0.1 mol·L-1,错误;C项,反应后得到等量的
HA、NaA,则由物料守恒可知,2c(Na+)=c(HA)+c(A-),错误;D项,由电荷守恒可知,c(Na+)+c(H+)=
c(OH-)+c(A-),又知2c(Na+)=c(HA)+c(A-),则c(OH-)=c(H+)+[c(HA)-c(A-)],D正确。
(2)常温下在20 mL 0.1 mol·L-1 Na CO 溶液中逐滴加入0.1 mol·L-1 HCl溶液40 mL,先反应生成碳酸
2 3
氢钠,再与盐酸反应生成二氧化碳、水。①由反应及图像可知,在同一溶液中,HCO、HCO、CO不能大
2 3
量共存。②由图像可知,pH=7时,溶液中含碳元素的主要微粒为HCO、HCO,根据电荷守恒可知c(Na
2 3+)+c(H+)=c(Cl-)+c(HCO)+c(OH-)。③CO的水解常数K ==2×10-4,当溶液中c(HCO)∶c(CO)=2∶1时,
h
c(OH-)=10-4 mol·L-1,由K 可知,c(H+)=10-10 mol·L-1,所以pH=10。
w
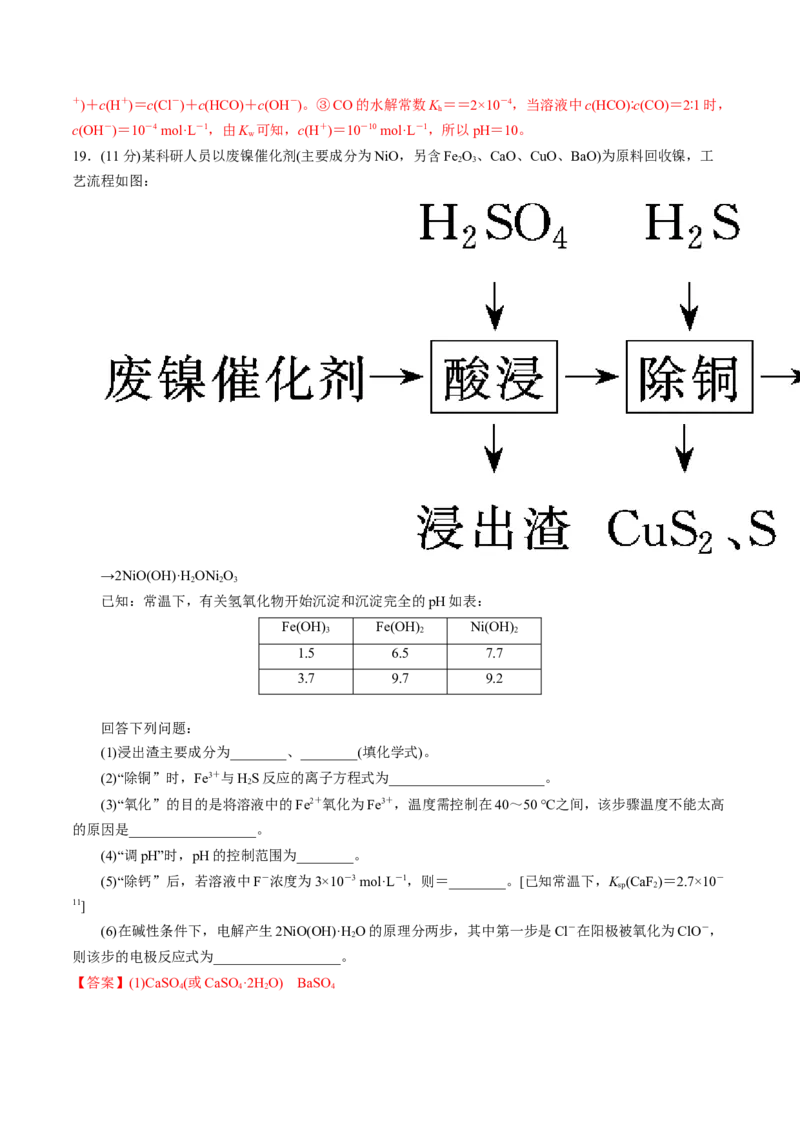
19.(11分)某科研人员以废镍催化剂(主要成分为NiO,另含Fe O、CaO、CuO、BaO)为原料回收镍,工
2 3
艺流程如图:
→2NiO(OH)·H ONi O
2 2 3
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如表:
Fe(OH) Fe(OH) Ni(OH)
3 2 2
1.5 6.5 7.7
3.7 9.7 9.2
回答下列问题:
(1)浸出渣主要成分为________、________(填化学式)。
(2)“除铜”时,Fe3+与HS反应的离子方程式为______________________。
2
(3)“氧化”的目的是将溶液中的Fe2+氧化为Fe3+,温度需控制在40~50 ℃之间,该步骤温度不能太高
的原因是__________________。
(4)“调pH”时,pH的控制范围为________。
(5)“除钙”后,若溶液中F-浓度为3×10-3 mol·L-1,则=________。[已知常温下,K (CaF )=2.7×10-
sp 2
11]
(6)在碱性条件下,电解产生2NiO(OH)·H O的原理分两步,其中第一步是Cl-在阳极被氧化为ClO-,
2
则该步的电极反应式为__________________。
【答案】(1)CaSO (或CaSO·2H O) BaSO
4 4 2 4(2)2Fe3++HS===2Fe2++S↓+2H+ (3)温度太高,HO 受热易分解 (4)3.7≤pH<7.7 (5)1.0×10-3
2 2 2
(6)Cl-+2OH--2e-===ClO-+HO
2
【解析】废镍催化剂(主要成分为NiO,另含Fe O、CaO、CuO、BaO等),用硫酸浸取,过滤得含有镍离
2 3
子、铁离子、钙离子、铜离子的溶液,再通入硫化氢除去铜离子,且使铁离子被还原成亚铁离子,得硫化
铜、硫固体,过滤的滤液中含有镍离子、亚铁离子、钙离子,加入过氧化氢氧化亚铁离子生成铁离子,调
节溶液pH生成氢氧化铁沉淀,加入氟化钠除去钙离子,再加入氯化钠后电解得2NiO(OH)·H O,灼烧得三
2
氧化二镍。
(1)用硫酸浸取,钙离子和钡离子与硫酸根离子结合得到CaSO、BaSO 沉淀,故浸出渣主要成分为
4 4
CaSO(或CaSO·2H O)、BaSO。
4 4 2 4
(2)“除铜”时,铁离子具有强氧化性,可与硫化氢反应生成亚铁离子和S,反应的离子方程式为2Fe3+
+HS===2Fe2++S↓+2H+。
2
(3)“氧化”时用过氧化氢将溶液中Fe2+氧化为Fe3+,过氧化氢受热易分解,故温度不能太高。
(4)“调pH”,要使铁离子完全沉淀,且避免生成Ni(OH) ,由表中数据可知,pH范围为3.7≤pH<7.7。
2
(5)已知常温下,K (CaF )=2.7×10-11,“除钙”后,若溶液中F-浓度为3×10-3 mol·L-1,则钙离子浓
sp 2
度为=3×10-6 mol·L-1,==1.0×10-3。
(6)阳极上氯离子失电子生成氯气,氯气和氢氧根离子反应生成次氯酸根离子和水,所以阳极反应式为
Cl-+2OH--2e-===ClO-+HO。
2
20.(14分)NaOH溶液可用于多种气体的处理。
(1)CO 是温室气体,可用NaOH溶液吸收得到NaCO 或NaHCO 。
2 2 3 3
①Na CO 俗称纯碱,因CO水解而使其水溶液呈碱性,写出CO第一步水解的离子方程式
2 3
______________________________。已知25 ℃时,CO第一步水解的平衡常数K =2×10-4,当溶液中
h
c(HCO)∶c(CO)=20∶1 时,溶液的pH=________。
②泡沫灭火器中通常装有NaHCO 溶液和Al (SO ) 溶液,请写出这两种溶液混合时反应的离子方程式
3 2 4 3
_______________________________________________________________
_______________________________________。
(2)金属与浓硝酸反应产生的NO 可用NaOH溶液吸收,反应的化学方程式为2NO +2NaOH===NaNO
2 2 3
+NaNO +HO。含0.2 mol NaOH的水溶液与0.2 mol NO 恰好完全反应得1 L溶液A,溶液B为0.1 mol·L
2 2 2
-1 CH COONa溶液,则两份溶液中c(NO)、c(NO)和c(CHCOO-)由大到小的顺序为________(已知HNO 的
3 3 2
电离常数K=5.6×10-4,CHCOOH的电离常数K=1.75×10-5)。可使溶液A和溶液B的 pH相等的方法是
a 3 a
________(填字母)。
A.向溶液A中加适量NaOH
B.向溶液A中加适量水
C.向溶液B中加适量NaOH
D.向溶液B中加适量水
(3)烟气中的SO 会引起酸雨,可利用氢氧化钠溶液吸收。吸收SO 的过程中,溶液中HSO 、HSO、
2 2 2 3
SO三者所占物质的量分数(α)随pH变化的关系如图所示:①图中pH=7时,溶液中离子浓度关系正确的是______(填字母)。
A.c(Na+)>2c(SO)>c(HSO)
B.c(Na+)=c(SO)+c(HSO)+c(H SO )
2 3
C.c(OH-)=c(H+)+c(H SO )+c(HSO)
2 3
D.c(Na+)>c(HSO)>c(SO)>c(H+)=c(OH-)
②利用上图中数据,求反应HSO H++HSO的平衡常数的数值________。
2 3
【答案】(1)①CO+HOHCO+OH- 9
2
②3HCO+Al3+===Al(OH) ↓+3CO↑
3 2
(2)c(NO)>c(NO)>c(CHCOO-) AD
3
(3)①A ②10-1.8
【解析】(1)①CO水解而使NaCO 溶液呈碱性,CO第一步水解的离子方程式为CO+HOHCO+OH
2 3 2
-,水解常数K =2×10-4,当溶液中c(HCO)∶c(CO)=20∶1时,c(OH-)=10-5 mol·L-1,由水的离子积K 可
h w
知,c(H+)=10-9 mol·L-1,所以pH=-lg 10-9=9;②Al (SO ) 溶液与NaHCO 溶液混合时能相互促进水
2 4 3 3
解生成氢氧化铝沉淀、二氧化碳气体,离子方程式为Al3++3HCO===Al(OH) ↓+3CO↑。
3 2
(2)0.2 mol NaOH的水溶液与0.2 mol NO 恰好完全反应得1 L溶液A,由2NO +2NaOH===NaNO +NaNO
2 2 3 2
+HO知,得到的溶液A中NaNO 的物质的量浓度为0.1 mol·L-1,NaNO 的物质的量浓度为0.1 mol·L-1,
2 3 2
溶液B为0.1 mol·L-1的CHCOONa溶液; 由HNO 的电离常数K=7.1×10-4,CHCOOH的电离常数K
3 2 a 3 a
=1.7×10-5,说明CHCOOH的酸性小于HNO 的酸性,溶液中醋酸根离子的水解程度大于亚硝酸根离子的
3 2
水解程度,则溶液B的碱性大于A溶液,两溶液中c(NO)、c(NO)和c(CHCOO-)由大到小的顺序为c(NO)
3
>c(NO)>c(CHCOO-);A.向溶液A中加适量NaOH,增大碱性,可以调节溶液pH与溶液B相等,故A
3
正确;B.溶液B的碱性大于A溶液,向溶液A中加适量水,稀释溶液,碱性减弱,不能调节溶液pH与溶
液B相等,故B错误;C.溶液B的碱性大于A溶液,向溶液B中加适量NaOH,溶液pH更大,故C错误;
D.向溶液B中加适量水,稀释溶液碱性减弱,可以调节溶液pH与溶液A相等,故D正确;故答案为A、
D;
(3)①由电荷守恒可知,c(H+)+c(Na+)=2c(SO)+c(HSO)+c(OH-),溶液的pH=7,则c(H+)=c(OH
-),则c(Na+)=2c(SO)+c(HSO),所以c(Na+)>2c(SO),而由图可知pH=7时,c(SO)=c(HSO),则c(Na
+)>2c(SO)>c(HSO),故A正确;由电荷守恒可知,c(H+)+c(Na+)=2c(SO)+c(HSO)+c(OH-),中性溶液
的c(H+)=c(OH-),则c(Na+)=2c(SO)+c(HSO),c(SO)≠c(H SO ),故B错误;pH=7时,c(H+)=c(OH
2 3
-),故C错误; 由图可知pH=7时,c(SO)=c(HSO),故D错误。②亚硫酸的第一步电离方程式为HSO H++HSO,根据图像可知,pH=1.8时,c(H SO )=c(HSO ),由K=可知,HSO 的第一级电离
2 3 2 3 a 2 3
平衡常数K =c(H+)=10-1.8。
a1