文档内容
第一章 第一节 第3课时 氧化还原反应规律应用 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共60分)
1. 中国传统文化对人类文明贡献巨大,我国古代文献《抱朴子》和《淮南万毕术》中均描述了大
量的化学反应,其中有:①“丹砂(HgS)烧之成水银,积变又还成丹砂”;②“曾青得铁则化
为铜”。下列有关叙述正确的是( )
A.①中“积变又还成丹砂”说明水银发生了还原反应
B.②中反应的离子方程式为2Fe+3Cu2+===2Fe3++3Cu
C.根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒
D.“曾青得铁则化为铜”说明该反应是氧化还原反应,铁发生还原反应
2. CuH不稳定,易跟盐酸反应:2CuH+2HCl===CuCl +2H ↑+Cu。下列说法正确的是( )
2 2
A.CuH中H的化合价为+1 B.CuH在反应中只被还原
C.在反应中HCl失去电子 D.Cu是反应的还原产物
3. 在一定条件下,KClO 与I 按下式反应:2KClO+I===2KIO+Cl,下列判断正确的是( A )
3 2 3 2 3 2
A.该反应属于置换反应
B.氧化性:I>KClO
2 3
C.还原性:KClO>I
3 2
D.还原剂为KIO ,氧化剂为I
3 2
4. 根据下列反应的化学方程式,判断有关物质的还原性强弱顺序是( )
①I+SO +2HO===H SO +2HI
2 2 2 2 4
②2FeCl +Cl===2FeCl
2 2 3
③2FeCl +2HI===2FeCl +2HCl+I
3 2 2
A.I->Fe2+>Cl->SO B.Cl->Fe2+>SO >I-
2 2
C.Fe2+>I->Cl->SO D.SO >I->Fe2+>Cl-
2 2
5. 已知:①2KCrO+H SO ===K Cr O+K SO +H O
2 4 2 4 2 2 7 2 4 2
②KCr O+6FeSO+7H SO ===3Fe (SO )+ Cr(SO ) +K SO +7H O
2 2 7 4 2 4 2 4 3 2 4 3 2 4 2
③Fe (SO )+2HI===2FeSO+I +H SO
2 4 3 4 2 2 4
下列结论正确的是( )
A.①②③均是氧化还原反应
B.氧化性强弱顺序是KCr O>Fe (SO )>I
2 2 7 2 4 3 2
C.反应②中氧化剂与还原剂的个数比为6∶1
D.反应③中1个还原剂失去电子数为2
6. MOx−离子和S2−在酸性溶液中发生反应:MOx−+3S2−+14H+===2M3++3S↓+7H O,则MOx−中
2 7 2 7 2 2 7
M的化合价是( )
1
学科网(北京)股份有限公司A.+2 B.+3 C.+4 D.+6
7. 多种氧化剂和还原剂相遇时,存在“争先恐后,强者优先”的现象。请预测,在含FeCl 、
2
MgCl 和HCl的溶液中加入适量Zn粉,首先置换出来的是( )
2
A.Fe B.H
2
C.Mg D.不能确定
8. 下列化学反应中溴元素仅被氧化的是( )
A.2NaBr+Cl===2NaCl+Br
2 2
B.Br +2NaI===2NaBr+I
2 2
C.3Br +6NaOH=====5NaBr+NaBrO +3HO
2 3 2
D.HBr+NaOH===NaBr+HO
2
9. 已知:①5Cl+I +6H O===2HIO+10HCl ②Cl O -+5Cl−+6H+===3Cl↑+3H O
2 2 2 3 3 2 2
下列按物质氧化性顺序由强到弱排列正确的是( )
A.Cl>Cl O ->IO - B.Cl O ->Cl>IO -
2 3 3 3 2 3
C.Cl O ->IO ->Cl D.Cl>Cl O ->IO -
3 3 2 2 3 3
10.已知某温度时发生如下三个反应:
①C+CO===2CO ②C+HO(g)===CO+H ③CO+HO(g)===CO +H
2 2 2 2 2 2
由此可以判断,在该温度下,C、CO、H 的还原性由强到弱的顺序为( )
2
A.CO>C>H B.CO>H>C
2 2
C.C>H >CO D.C>CO>H
2 2
11.已知氧化还原反应:
①Fe2++Zn===Fe+Zn2+ ②Cu2++Fe===Fe2++Cu ③2Fe3++Cu===2Fe2++Cu2+
下列说法不正确的是( )
A.氧化性:Fe3+>Cu2+>Fe2+>Zn2+
B.还原性:Zn>Fe>Cu>Fe2+
C.化学反应2Fe3++Zn===2Fe2++Zn2+能够发生
D.化学反应2Fe3++Fe===3Fe2+不能发生
12.常温下,在溶液中可以发生如下反应:①2Fe2++Br ==2Fe3++2Br-;②2Br-+Cl==Br +2Cl
2 2 2
-;③2Fe3++2I-==2Fe2++I。由此判断下列说法错误的是( )
2
A.铁元素在反应①和③中均被氧化
B.反应②中当有1个Cl 分子被还原时,有2个Br-被氧化
2
C.还原性强弱顺序为:I->Fe2+>Br->Cl-
D.氧化性强弱顺序为:Cl>Br >Fe3+>I
2 2 2
2
学科网(北京)股份有限公司13.下列反应中,氨的作用与反应4NH +5O 4NO+6HO中氨的作用相同的是( )
3 2 2
A.2Na+2NH ===2NaNH +H
3 2 2
B.NH +HNO===NHNO
3 3 4 3
C.4NH +6NO 5N+6HO
3 2 2
D.3SiH+4NH =====Si N+12H
4 3 3 4 2
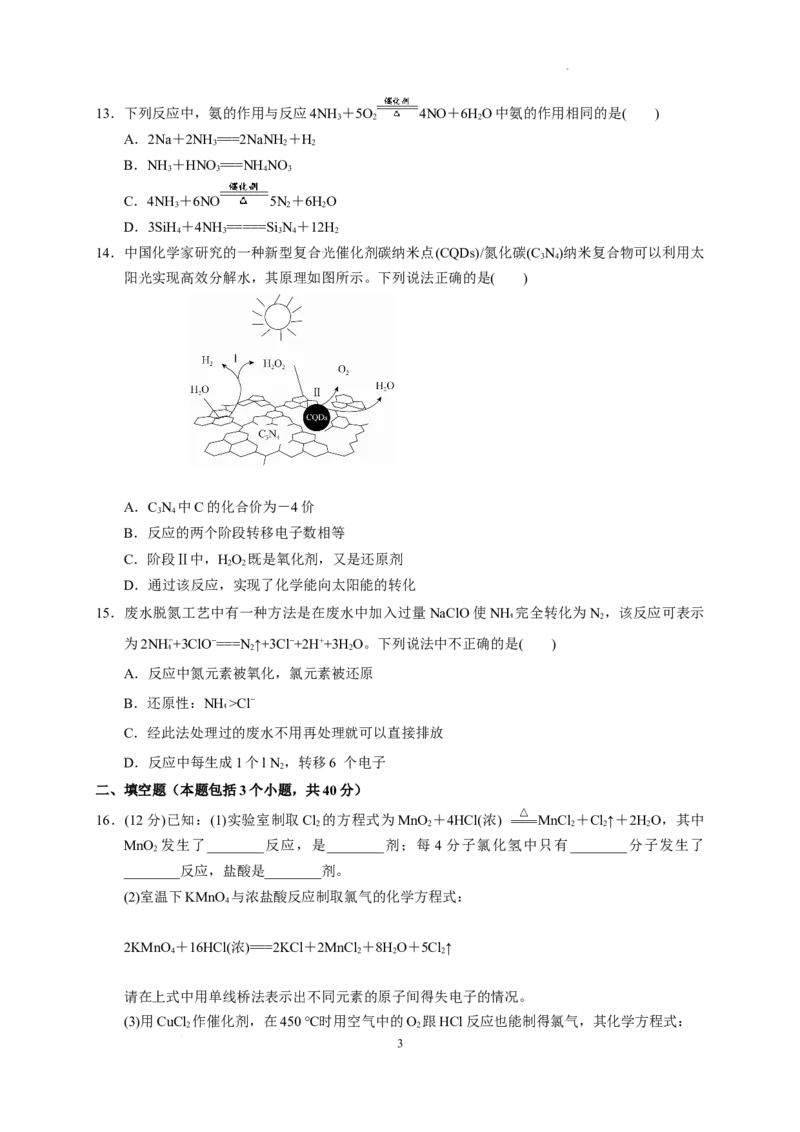
14.中国化学家研究的一种新型复合光催化剂碳纳米点(CQDs)/氮化碳(C N)纳米复合物可以利用太
3 4
阳光实现高效分解水,其原理如图所示。下列说法正确的是( )
A.C N 中C的化合价为-4价
3 4
B.反应的两个阶段转移电子数相等
C.阶段Ⅱ中,HO 既是氧化剂,又是还原剂
2 2
D.通过该反应,实现了化学能向太阳能的转化
15.废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH 完全转化为N ,该反应可表示
2
为2NH +3ClO−===N↑+3Cl−+2H++3H O。下列说法中不正确的是( )
2 2
A.反应中氮元素被氧化,氯元素被还原
B.还原性:NH >Cl−
C.经此法处理过的废水不用再处理就可以直接排放
D.反应中每生成1个l N ,转移6 个电子
2
二、填空题(本题包括3个小题,共40分)
16.(12分)已知:(1)实验室制取Cl 的方程式为MnO +4HCl(浓) MnCl +Cl↑+2HO,其中
2 2 2 2 2
MnO 发生了________反应,是________剂;每 4 分子氯化氢中只有________分子发生了
2
________反应,盐酸是________剂。
(2)室温下KMnO 与浓盐酸反应制取氯气的化学方程式:
4
2KMnO +16HCl(浓)===2KCl+2MnCl +8HO+5Cl↑
4 2 2 2
请在上式中用单线桥法表示出不同元素的原子间得失电子的情况。
(3)用CuCl 作催化剂,在450 ℃时用空气中的O 跟HCl反应也能制得氯气,其化学方程式:
2 2
3
学科网(北京)股份有限公司4HCl+O=====2HO+2Cl
2 2 2
从氯元素化合价的变化看,以上三种制氯气方法的共同点是_____________________________;
比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为______________________。
17.(14分)据题目要求完成下列各题:
(1)少量的NaHCO 与Ca(OH) 反应的离子反应方程式 。
3 2
(2)用双线桥标出方程式 2KMnO ===K MnO +MnO+O 中电子转移的方向和数目
4 2 4 2 2
。
(3)用双线桥标出方程式6HCl + KClO === KCl +3Cl +3H O 中电子转移的方向和数目_______,
3 2 2
并指出氧化产物与还原产物的质量的比___________。
(4)在MnO +4HCl===MnCl +Cl+2H O中氧化剂与还原剂的个数比为_______,当4个HCl被氧
2 2 2 2
化时,则生成Cl 的个数为________。
2
18.(14分)HIO 主要以HIO 形式存在,HIO 是白色晶体,易溶于水,具有很强的氧化性,在强酸
4 5 6 5 6
溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
_______Mn2++_______H IO ===__________MnO-+_______IO -+_______H++_______
5 6 4 3
(2)根据以上离子方程式判断HIO 是________电离物质(填“易”或“难”)。
5 6
(3)上述反应,被氧化的元素是________(填元素符号),当1个 Mn2+参加反应时,转移电子的
个为________。
1.答案:C
解析:A项,水银是汞的俗称,在Hg转化为HgS的过程中,汞元素化合价升高,水银发生了氧化
反应,错误;B项,“曾青得铁则化为铜”,说明铁与硫酸铜发生了置换反应,离子方程式为Fe+
Cu2+===Fe2++Cu,错误;C项,S和Hg反应可以生成HgS,因此用硫粉覆盖温度计打破后流出的
水银可以防止中毒,正确;D项,反应Fe+Cu2+===Fe2++Cu中,铁元素化合价升高,故铁发生氧
化反应,错误。
2.答案:D
解析:首先明确反应物、生成物中各元素的化合价:
CuH中H的化合价为−1,A项错;由反应方程式中元素价态变化知,CuH在反应中既被氧化又被
还原,B项错;HCl中氢元素价态降低,HCl得到电子,C项错。
3.答案:A
4
学科网(北京)股份有限公司解析:从反应中变价元素的化合价分析:KClO→Cl ,I―→KI O ,可知:氧化剂为KClO ,还原
3 2 2 3 3
剂为I ,氧化产物为KIO ,还原产物为Cl ,由此可得,氧化性:KClO>KIO ,还原性:I>Cl ,
2 3 2 3 3 2 2
可推知B、C、D错误;由反应方程式中反应物和生成物的类别和种类可知,A项正确。
4.答案:D
解析:在氧化还原反应中,还原剂的还原性强于还原产物的还原性。①在反应 I +SO +
2 2
2HO===H SO +2HI中,SO 是还原剂,HI是还原产物,还原性:SO >I-;②在反应2FeCl +
2 2 4 2 2 2
Cl===2FeCl 中,氯化亚铁是还原剂,氯化铁是还原产物,还原性:Fe2+>Cl-;③在反应2FeCl +
2 3 3
2HI===2FeCl +2HCl+I 中,HI是还原剂,氯化亚铁是还原产物,还原性:I->Fe2+。综上可得还
2 2
原性:SO >I->Fe2+>Cl-。
2
5.答案:B
解析:①2KCrO+H SO ===KCr O+K SO +H O,该反应中元素的化合价不变,不属于氧化还原反
2 4 2 4 2 2 7 2 4 2
应;②KCr O+6FeSO+7H SO ===3Fe (SO )+Cr (SO )+K SO +7H O,Cr元素的化合价降低,Fe
2 2 7 4 2 4 2 4 3 2 4 3 2 4 2
元素的化合价升高,为氧化还原反应;③Fe (SO )+2HI===2FeSO +I +H SO 中,Fe元素的化合价
2 4 3 4 2 2 4
降低,I元素的化合价升高,为氧化还原反应。②③属于氧化还原反应,而①不属于氧化还原反应,
故A错误;由②③中氧化剂的氧化性大于氧化产物的氧化性可知,氧化性强弱顺序是 KCr O >
2 2 7
Fe (SO ) >I ,故B正确;②中氧化剂为KCr O ,还原剂为FeSO ,氧化剂与还原剂的个数比为
2 4 3 2 2 2 7 4
1∶6,故C错误;③中还原剂为HI,1个 HI反应失去1个电子,故D错误;故选B。
6.答案:D
解析:MOx−+3S2−+14H+===2M3++3S↓+7H O中,S元素的化合价升高,M元素的化合价降低,设
2 7 2
MOx−中M元素的化合价为n,由电子守恒可知,2×(n−3)=3×[0−(−2)],解得n=+6,选D。
2 7
7.答案:B
解析:因为氧化性:H+>Fe2+>Zn2+>Mg2+,所以Zn粉首先与氧化性最强的H+发生置换反应,然后
再与Fe2+发生置换反应。
8.答案:A
解析:溴化钠中溴元素化合价升高被氧化作还原剂,选项A符合;溴单质中溴元素化合价降低被还
原作氧化剂,选项B不符合;溴单质既是氧化剂又是还原剂,被氧化生成溴酸钠,被还原生成溴化
钠,选项C不符合;反应属于中和反应,各元素化合价不变,不属于氧化还原反应,选项D不符合。
9.答案:B
解析:根据同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性。①中的氧化剂是氯气,氧
化产物是HIO ,所以氧化性Cl >IO -;②中的氧化剂是Cl O -,氧化产物是氯气,所以氧化性 Cl
3 2 3 3
O->Cl,所以综合起来是Cl O ->Cl>IO -,答案选B。
3 2 3 2 3
10.答案:D
解析:由氧化还原反应判断,还原性:①中,C>CO;②中,C>H ;③中,CO>H,整体排序为
2 2
C>CO>H 。
2
5
学科网(北京)股份有限公司11.答案:D
解析:反应①说明氧化性Fe2+>Zn2+,反应②说明氧化性Cu2+>Fe2+,反应③说明氧化性Fe3+>Cu2
+,则A正确;反应①说明还原性Zn>Fe,反应②说明还原性Fe>Cu,反应③说明还原性Cu>Fe2
+,则B正确;2Fe3++Cu===2Fe2++Cu2+能够发生,Zn、Fe的还原性均比Cu强,则2Fe3++
Zn===2Fe2++Zn2+和2Fe3++Fe===3Fe2+都能够发生,C正确、D不正确。
12.答案:A
解析:①中Fe2+作还原剂,在反应中被氧化,③中Fe3+作氧化剂,在反应中被还原,A错误;反应
②中Cl 作氧化剂,当有1个Cl 被还原时,有2个Br-被氧化,B正确;反应①可知,氧化性:
2 2
Br >Fe3+,还原性:Fe2+>Br-;由反应②可知,氧化性:Cl>Br ,还原性:Br->Cl-;由反应③可
2 2 2
知,氧化性:Fe3+>I ,还原性:I->Fe2+,整体再排序,故C、D正确。
2
13.答案:C
解析:在反应4NH +5O 4NO+6HO中,氨中的氮元素化合价升高,NH 作还原剂。A项,
3 2 2 3
NH 中的氢元素的化合价降低,NH 作氧化剂,与题中所给反应中氨的作用不相同,错误;B项,
3 3
氨中各元素的化合价都没有变化,与题中所给反应中氨的作用不相同,错误;C项,氨中的氮元素
化合价升高,NH 作还原剂,与题中所给反应中氨的作用相同,正确;D项,NH 中的氢元素得到
3 3
电子,被还原变为H,NH 作氧化剂,与题中所给反应中氨的作用不相同,错误。
2 3
14.答案:C
解析:化合物C N 中氮元素的化合价为-3价,碳元素的化合价为+4价,故A错误;由于两个过
3 4
程中,参与反应的量未知,因此无法比较转移电子数的大小,故B错误;阶段Ⅱ中发生反应的化学
方程式为2HO=====2HO+O↑,HO 中氧元素由-1价变为0价和-2价,因此HO 既是氧化剂,
2 2 2 2 2 2 2 2
又是还原剂,故C正确;该反应中,实现了太阳能转化为化学能,故D错误。
15.答案:C
解析:反应2NH ++3ClO−===N +3Cl−+2H++3H O中,Cl元素的化合价由+1价降低为−1价,N元素
4 2 2
的化合价由−3价升高为0价,以此来解答。Cl元素的化合价由+1价降低为−1价被还原,N元素的
化合价由−3价升高为0价被氧化,故A正确;2NH ++3ClO−===N +3Cl−+2H++3H O中,N元素的化
4 2 2
合价由−3价升高为0价,则NH +为还原剂,Cl元素的化合价由+1价降低为−1价,则生成Cl−为还
4
原产物,所以还原性 NH +>Cl−,故B正确;由2NH ++3ClO−===N +3Cl−+2H++3H O得出经此法处
4 4 2 2
理过的废水曾酸性,所以不能直接排放,故C错误;N元素的化合价由−3价升高为0价被氧化,
所以反应中每生成1个N,转移6 个电子,故D正确。故选C。
2
16.答案:(1)还原 氧化 2 氧化 还原
(2) ===2KCl+2MnCl +8HO+5Cl↑
2 2 2
(3)将氯元素从-1价氧化到0价的Cl KMnO >MnO >O。
2 4 2 2
6
学科网(北京)股份有限公司解析:(3)当不同氧化剂氧化同种还原剂时,如氧化产物价态相同,可根据反应的难易程度进行判断:
(1)需加热;(2)在室温即可发生;(3)需高温催化剂。故氧化性强弱顺序:KMnO >MnO >O。
4 2 2
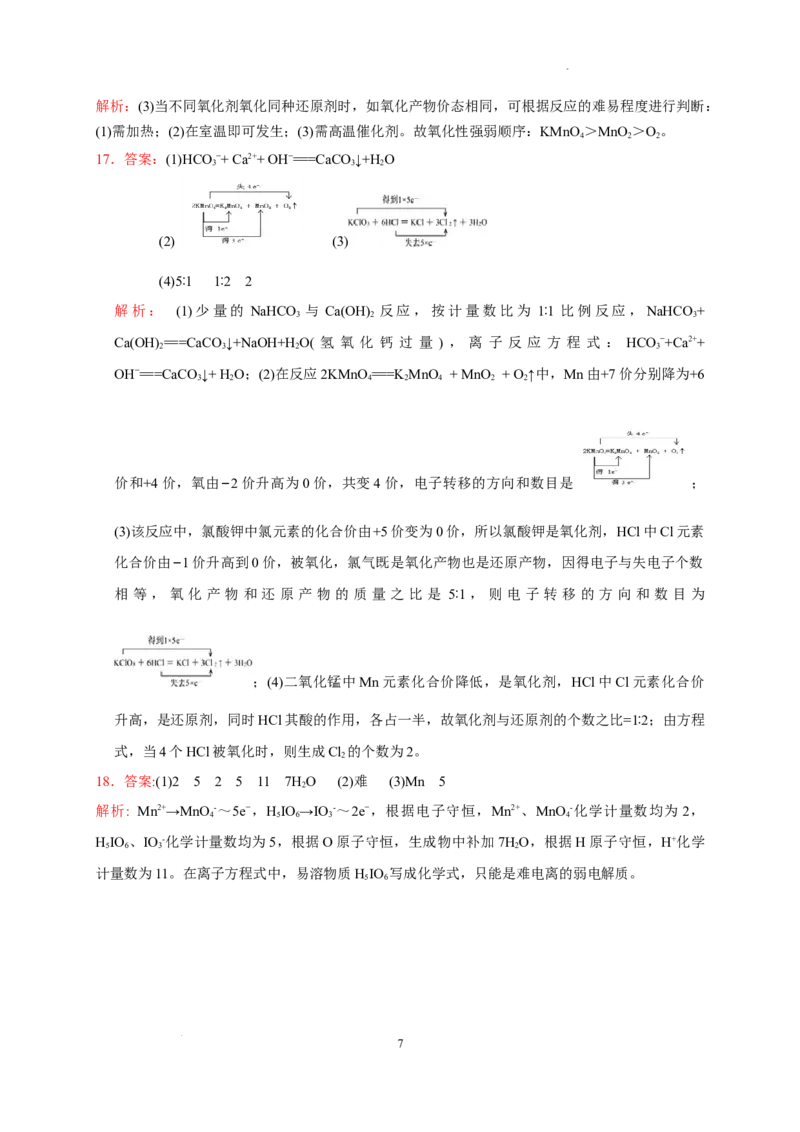
17.答案:(1)HCO −+ Ca2++ OH−===CaCO ↓+H O
3 3 2
(2) (3)
(4)5∶1 1∶2 2
解析: (1)少量的 NaHCO 与 Ca(OH) 反应,按计量数比为 1∶1 比例反应,NaHCO +
3 2 3
Ca(OH) ===CaCO ↓+NaOH+HO( 氢 氧 化 钙 过 量 ) , 离 子 反 应 方 程 式 : HCO −+Ca2++
2 3 2 3
OH−===CaCO ↓+ H O;(2)在反应2KMnO ===KMnO + MnO + O ↑中,Mn由+7价分别降为+6
3 2 4 2 4 2 2
价和+4价,氧由−2价升高为0价,共变4价,电子转移的方向和数目是 ;
(3)该反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂,HCl中Cl元素
化合价由−1价升高到0价,被氧化,氯气既是氧化产物也是还原产物,因得电子与失电子个数
相 等 , 氧 化 产 物 和 还 原 产 物 的 质 量 之 比 是 5∶1 , 则 电 子 转 移 的 方 向 和 数 目 为
;(4)二氧化锰中Mn元素化合价降低,是氧化剂,HCl中Cl元素化合价
升高,是还原剂,同时HCl其酸的作用,各占一半,故氧化剂与还原剂的个数之比=1∶2;由方程
式,当4个HCl被氧化时,则生成Cl 的个数为2。
2
18.答案:(1)2 5 2 5 11 7HO (2)难 (3)Mn 5
2
解析: Mn2+→MnO-~5e−,HIO →IO -~2e−,根据电子守恒,Mn2+、MnO-化学计量数均为 2,
4 5 6 3 4
HIO 、IO -化学计量数均为5,根据O原子守恒,生成物中补加7HO,根据H原子守恒,H+化学
5 6 3 2
计量数为11。在离子方程式中,易溶物质HIO 写成化学式,只能是难电离的弱电解质。
5 6
7
学科网(北京)股份有限公司8
学科网(北京)股份有限公司