文档内容
第 04 讲 氧化还原反应的基本概念
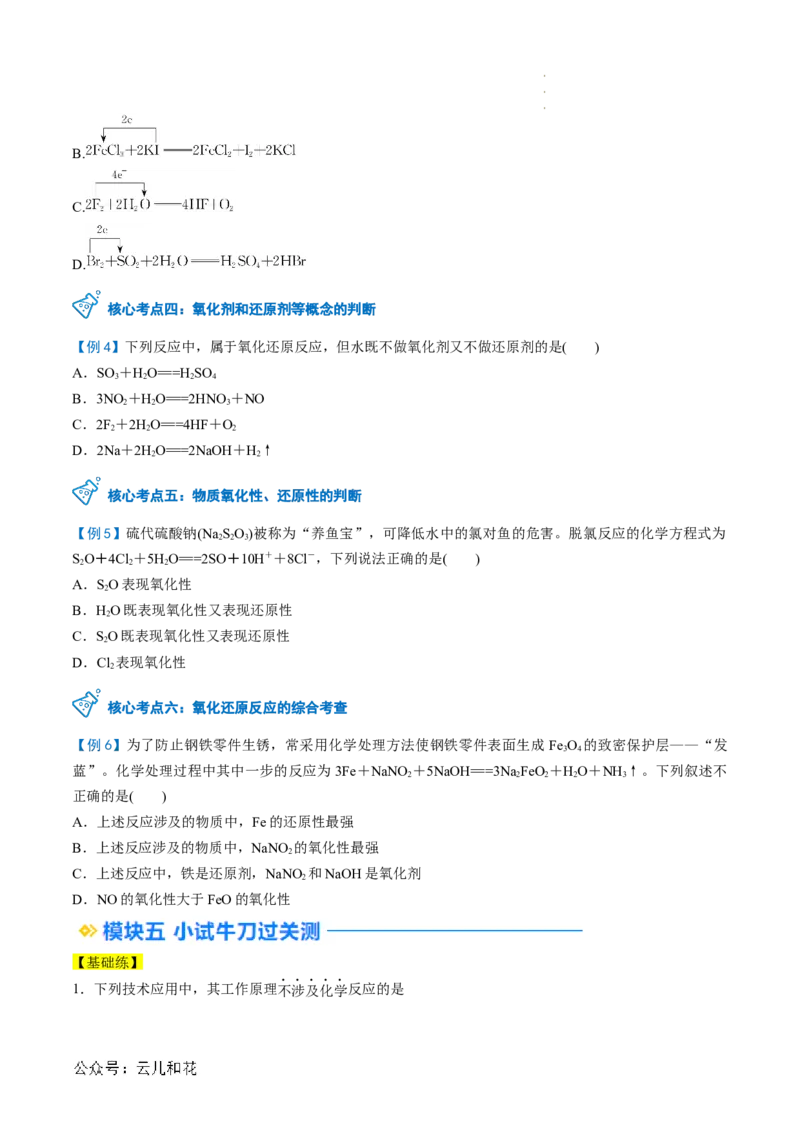
模块一 思维导图串知识 1.从化合价变化和电子转移的角度认识并判断氧化还
模块二 基础知识全梳理(吃透教材) 原反应。
模块三 教材习题学解题 2.理解氧化还原反应与四种基本反应类型的关系。
模块四 核心考点精准练(7大考点) 3.能从化学反应中元素化合价的变化认识氧化剂和还
模块五 小试牛刀过关测 原剂、氧化产物和还原产物等概念。
(基础练10题) 4.认识物质的氧化性、还原性,学会分析预测物质具
(提升练6题) 有的氧化性或还原性。
学科网(北京)股份有限公司一、氧化还原反应的特征和本质
1.多角度认识氧化还原反应
(1)从得失氧的角度
对于反应2CuO+C=====2Cu+CO↑
2
(1)氧化铜失去氧,发生 反应,被碳还原。
(2)碳得到氧,发生 反应,被氧化铜氧化。
(3)结论:在化学反应中,一种物质得到氧发生 反应,必然有一种物质失去氧发生 反应。氧
化反应和还原反应是在一个反应中同时发生的,这样的反应称为氧化还原反应。
(2)从元素化合价变化的角度
(1)对于有氧得失的反应2CuO+C=====2Cu+CO↑
2
①铜元素化合价降低,发生 反应。
②碳元素化合价升高,发生 反应。
(2)对于无氧得失的反应Fe+CuSO ===FeSO+Cu
4 4
①铜元素化合价降低,发生 反应。
②铁元素化合价升高,发生 反应。
(3)结论:①反应前后有元素化合价变化(升降)的反应称为氧化还原反应。
②物质所含元素化合价升高的反应是 反应,物质所含元素化合价降低的反应是 反应。
③氧化还原反应的特征:反应前后有元素化合价的 。
(3)从电子转移的角度
(1)从电子得失的角度分析反应:2Na+Cl=====2NaCl
2
在有些氧化还原反应中,物质所含元素的原子失去电子,该物质发生 反应;得到电子,该物质
发生 反应。
(2)从共用电子对偏移的角度分析反应:H+Cl=====2HCl
2 2
在有些氧化还原反应中,元素的原子间有共用电子对的偏移(偏离和偏向)。
共用电子对偏离的物质发生 反应,共用电子对偏向的物质发生 反应。
(3)结论:①有电子转移(电子得失或共用电子对偏移)的反应是氧化还原反应。
②元素的原子失去电子(或电子对偏离),则元素的化合价升高,物质被氧化,发生 反应;元素的原子
得到电子(或电子对偏向),则元素的化合价降低,物质被还原,发生 反应。
③氧化还原反应的本质是电子转移。
2.氧化还原反应的特征
一种或几种元素的 发生变化。
3.氧化还原反应的实质
氧化还原反应的实质是 。
4.氧化还原反应与四种基本反应类型之间的关系
学科网(北京)股份有限公司(1)置换反应 氧化还原反应。
(2)复分解反应 氧化还原反应。
(3)有单质参加的化合反应 氧化还原反应。
(4)有单质生成的分解反应 氧化还原反应。
二、氧化还原反应中电子转移的表示方法
1.双线桥法
表明同一种元素反应前后的电子得失(或偏移)情况。
①双线桥法表示电子转移的基本步骤
【易错警示】
a.箭尾、箭头必须指向反应物、生成物中相应的同种元素。
b.采用a×be-形式表示得失电子数,a为得失电子的原子总数,b为每个原子得失电子数,a、b是“1”时
省略。得到与失去的电子总数相等。
2.单线桥法
表明反应中化合价变化的元素原子间的电子转移情况。
①单线桥法表示电子转移的基本步骤
学科网(北京)股份有限公司【易错警示】
a.单线桥法从反应物中失电子的元素指向反应物中得电子的元素,表示反应物中变价元素原子间电子的
转移情况;
b.箭头已标明电子转移的方向,因此不需再标明“得”或“失”,只标明电子转移数目。
三、氧化还原反应中的相关概念
1.氧化还原反应中的六大概念
(1)氧化剂与还原剂
氧化剂:在氧化还原反应中,所含元素的化合价 ,即得到电子(或电子对偏向)的物质。
还原剂:在氧化还原反应中,所含元素的化合价 ,即失去电子(或电子对偏离)的物质。
(2)氧化产物与还原产物
氧化产物:还原剂失去电子被 的产物。
还原产物:氧化剂得到电子被 的产物。
(3)氧化性与还原性
氧化性:物质 的性质或能力。
还原性:物质 的性质或能力。
【归纳提升】氧化还原反应概念间的关系
记忆口诀:
升→失→氧→氧→氧
降→得→还→还→还
2.常见的氧化剂、还原剂
(1)常见的氧化剂
①活泼的 单质:如Cl、O 等。
2 2
②变价元素的 化合物
a.某些酸:如浓HSO 、HNO、HClO等;
2 4 3
学科网(北京)股份有限公司b.某些氧化物、过氧化物:如MnO 、HO、NaO 等;
2 2 2 2 2
c.某些盐:如KMnO 、FeCl 、NaClO等。
4 3
(2)常见的还原剂
①活泼的 单质:如Al、Fe、Zn等。
②某些 单质:如H、S、C等。
2
③变价元素的低价态化合物
a.某些氧化物:如CO、SO 等;
2
b.某些氢化物:如HCl、HS等;
2
c.某些盐:如KI、NaS、FeCl 等。
2 2
【易错警示】
(1)在一个具体的化学反应中氧化剂和还原剂可能是同一物质,被氧化和被还原的也可能是同种元素,
氧化产物和还原产物也可能是同一物质。
(2)氧化还原反应中的反应物可能既不是氧化剂也不是还原剂,生成物也可能既不是氧化产物也不是还
原产物。
四、氧化性、还原性强弱比较
1.氧化性、还原性的强弱与得失电子的关系
(1)氧化性:物质越易得电子,氧化性 。
(2)还原性:物质越易失电子,还原性 。
【易错警示】
物质氧化性、还原性的强弱与得失电子的难易有关,与得失电子的多少无关。
2.物质的氧化性及还原性与元素化合价的关系
核心元素化合价 实例 性质
最高价 KMnO、浓HNO、浓HSO 只有
4 3 2 4
中间价 SO、NaSO、FeSO 、S 既有 又有
2 2 3 4
最低价 Fe、Na、KI 只有
3.氧化性、还原性强弱比较的方法
(1)根据元素的活动性顺序比较
如:Fe+CuSO ===FeSO+Cu
4 4
金属还原性:Fe>Cu
在反应中Fe是 剂,Cu是 产物。
学科网(北京)股份有限公司(2)根据氧化还原反应的化学方程式比较
氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
(3)根据氧化产物的价态高低判断
同一物质在相同条件下,被不同氧化剂氧化的程度越大,氧化剂的氧化性越强。
例如:2Fe+3Cl=====2FeCl 、Fe+S=====FeS
2 3
Fe被Cl 氧化成+3价,而S只能把其氧化成+2价,故氧化性:Cl>S;判断还原剂还原性的原理类似。
2 2
(4)根据反应条件来判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还原剂)的
氧化性(或还原性)越强,反之越弱。如:
①MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
②2KMnO+16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
后者比前者更容易发生,故氧化性:KMnO >MnO。
4 2
教材习题01 解题思路
下列诗词中不涉及氧化还原反应的是( )
A.爆竹声中一岁除
B.吹尽狂沙始到金
C.野火烧不尽
D.蜡炬成灰泪始干
教材习题02 解题思路
二氧化氯(ClO )是一种在水处理等方面有广泛应用的
2
高效安全消毒剂,它可以根据反应:2NaClO+
3
4HCl=2ClO ↑+Cl↑+NaCl+2HO制备,对于该
2 2 2
反应,下列说法正确的是( )
A.该反应属于置换反应 B.HCl是氧化剂
C.NaClO 是还原剂 D.ClO 是还原产物 D
3 2
是还原产物
学科网(北京)股份有限公司核心考点一:氧化还原反应的概念及判断
【例1】下列铜及其化合物的性质实验中,涉及到的反应不属于氧化还原反应的是( )
A.铜丝在空气中加热
B.用氢气还原氧化铜
C.将铁丝插入CuSO 溶液中
4
D.向CuSO 溶液中滴加NaOH溶液
4
核心考点二:氧化还原反应与四种基本反应类型的关系
【例2】氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于阴影区域的是( )
A.2HClO=====2HCl+O↑
2
B.NH HCO =====NH ↑+HO+CO↑
4 3 3 2 2
C.4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
D.Fe O+3CO=====2Fe+3CO
2 3 2
核心考点三:氧化还原反应中的电子转移
【例3】下列氧化还原反应中电子转移数目及方向都正确的是( )
A.
学科网(北京)股份有限公司B.
C.
D.
核心考点四:氧化剂和还原剂等概念的判断
【例4】下列反应中,属于氧化还原反应,但水既不做氧化剂又不做还原剂的是( )
A.SO +HO===HSO
3 2 2 4
B.3NO +HO===2HNO+NO
2 2 3
C.2F+2HO===4HF+O
2 2 2
D.2Na+2HO===2NaOH+H↑
2 2
核心考点五:物质氧化性、还原性的判断
【例5】硫代硫酸钠(Na SO)被称为“养鱼宝”,可降低水中的氯对鱼的危害。脱氯反应的化学方程式为
2 2 3
SO+4Cl+5HO===2SO+10H++8Cl-,下列说法正确的是( )
2 2 2
A.SO表现氧化性
2
B.HO既表现氧化性又表现还原性
2
C.SO既表现氧化性又表现还原性
2
D.Cl 表现氧化性
2
核心考点六:氧化还原反应的综合考查
【例6】为了防止钢铁零件生锈,常采用化学处理方法使钢铁零件表面生成 Fe O 的致密保护层——“发
3 4
蓝”。化学处理过程中其中一步的反应为 3Fe+NaNO +5NaOH===3NaFeO +HO+NH ↑。下列叙述不
2 2 2 2 3
正确的是( )
A.上述反应涉及的物质中,Fe的还原性最强
B.上述反应涉及的物质中,NaNO 的氧化性最强
2
C.上述反应中,铁是还原剂,NaNO 和NaOH是氧化剂
2
D.NO的氧化性大于FeO的氧化性
【基础练】
1.下列技术应用中,其工作原理不涉及化学反应的是
学科网(北京)股份有限公司A.火药使用 B.用 和 合成 C.转轮排字 D.用氧化铁冶炼铁
2.下列化学反应基本类型中一定是氧化还原反应的是
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
3.下列关于氧化还原反应的说法中正确的是
A.得到电子的一定是还原剂
B.氧化还原反应前后可以没有元素化合价发生变化
C.元素化合价升高的反应是氧化反应
D.氧化剂和还原剂一定是不同的物质
4.下列化学反应中,属于化合反应但不属于氧化还原反应的是
A. B.
C. D.
5.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于区域3的是
A. B.
C. D.
6.下列反应中, 只作为氧化剂的是
A. B.
C. D.
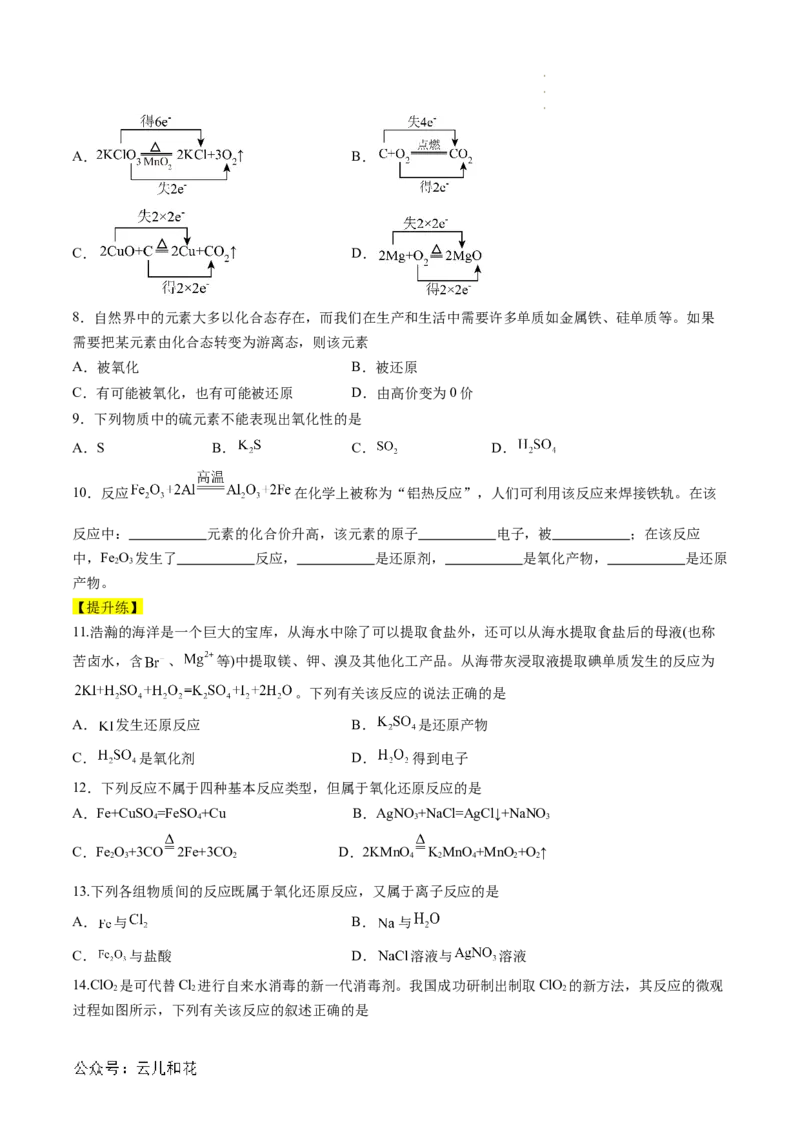
7.下列氧化还原反应中,电子转移的方向和数目均正确的是
学科网(北京)股份有限公司A. B.
C. D.
8.自然界中的元素大多以化合态存在,而我们在生产和生活中需要许多单质如金属铁、硅单质等。如果
需要把某元素由化合态转变为游离态,则该元素
A.被氧化 B.被还原
C.有可能被氧化,也有可能被还原 D.由高价变为0价
9.下列物质中的硫元素不能表现出氧化性的是
A.S B. C. D.
10.反应 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该
反应中: 元素的化合价升高,该元素的原子 电子,被 ;在该反应
中,Fe O 发生了 反应, 是还原剂, 是氧化产物, 是还原
2 3
产物。
【提升练】
11.浩瀚的海洋是一个巨大的宝库,从海水中除了可以提取食盐外,还可以从海水提取食盐后的母液(也称
苦卤水,含 、 等)中提取镁、钾、溴及其他化工产品。从海带灰浸取液提取碘单质发生的反应为
。下列有关该反应的说法正确的是
A. 发生还原反应 B. 是还原产物
C. 是氧化剂 D. 得到电子
12.下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Fe+CuSO=FeSO+Cu B.AgNO+NaCl=AgCl↓+NaNO
4 4 3 3
C.Fe O+3CO 2Fe+3CO D.2KMnO KMnO +МnO+O ↑
2 3 2 4 2 4 2 2
13.下列各组物质间的反应既属于氧化还原反应,又属于离子反应的是
A. 与 B. 与
C. 与盐酸 D. 溶液与 溶液
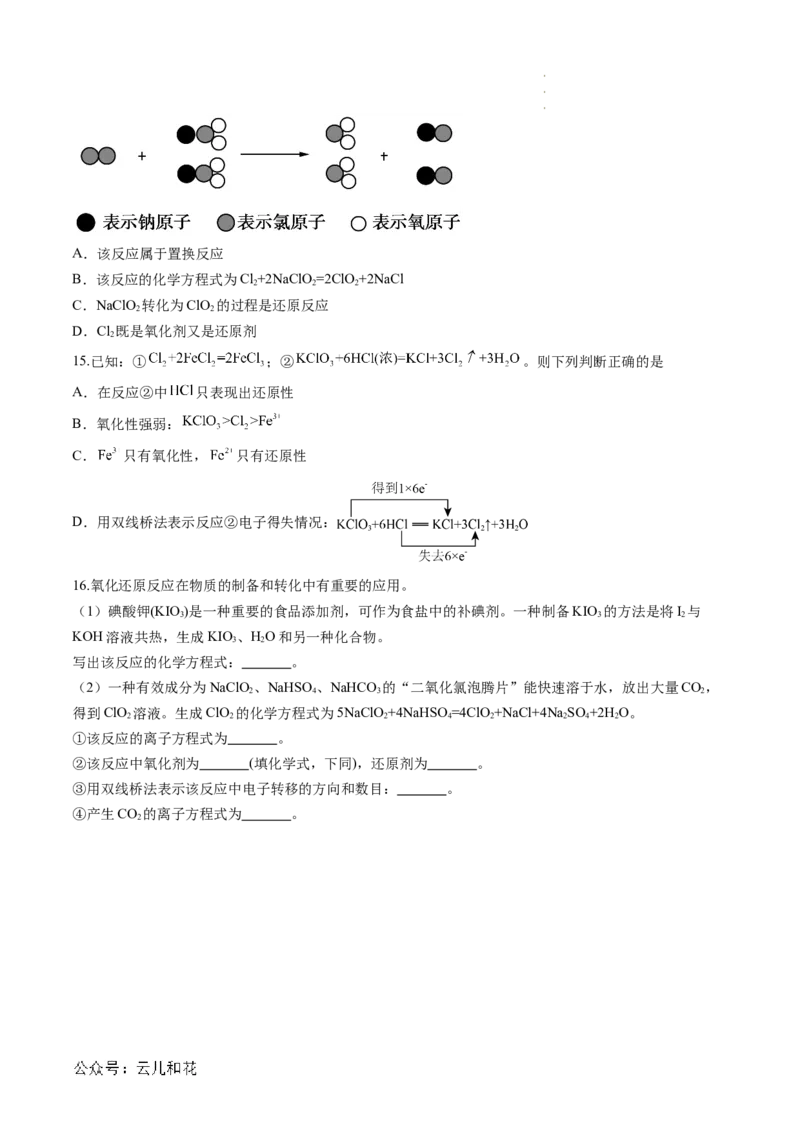
14.ClO 是可代替Cl 进行自来水消毒的新一代消毒剂。我国成功研制出制取ClO 的新方法,其反应的微观
2 2 2
过程如图所示,下列有关该反应的叙述正确的是
学科网(北京)股份有限公司A.该反应属于置换反应
B.该反应的化学方程式为Cl+2NaClO =2ClO +2NaCl
2 2 2
C.NaClO 转化为ClO 的过程是还原反应
2 2
D.Cl 既是氧化剂又是还原剂
2
15.已知:① ;② 。则下列判断正确的是
A.在反应②中 只表现出还原性
B.氧化性强弱:
C. 只有氧化性, 只有还原性
D.用双线桥法表示反应②电子得失情况:
16.氧化还原反应在物质的制备和转化中有重要的应用。
(1)碘酸钾(KIO )是一种重要的食品添加剂,可作为食盐中的补碘剂。一种制备KIO 的方法是将I 与
3 3 2
KOH溶液共热,生成KIO 、HO和另一种化合物。
3 2
写出该反应的化学方程式: 。
(2)一种有效成分为NaClO、NaHSO、NaHCO 的“二氧化氯泡腾片”能快速溶于水,放出大量CO,
2 4 3 2
得到ClO 溶液。生成ClO 的化学方程式为5NaClO+4NaHSO =4ClO +NaCl+4Na SO +2H O。
2 2 2 4 2 2 4 2
①该反应的离子方程式为 。
②该反应中氧化剂为 (填化学式,下同),还原剂为 。
③用双线桥法表示该反应中电子转移的方向和数目: 。
④产生CO 的离子方程式为 。
2
学科网(北京)股份有限公司