文档内容
巴蜀中学 2023 届高考适应性月考卷(七)
化学
注意事项:
1.答题前,考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号在答题卡上
填写清楚。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。在试题卷上作答无效。
3.考试结束后,请将本试卷和答题卡一并交回。满分100分,考试用时75分钟。
以下数据可供解题时参考。
可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5 Ba—137
一、选择题:本题共14小题,每小题3分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
1.化学与生产、生活密切相关。下列说法不正确的是( )
A.国产大飞机C919机壳一般不会使用高密度不锈钢
B.“天宫课堂”实验乙酸钠过饱和溶液结晶形成温热“冰球”,该过程发生吸热反应
C.“闽鹭”是我国制造的第四艘LNG船,船底镶嵌锌块,锌作负极,以防船体被腐蚀
D.核酸采样时,利用植绒技术将聚酯和尼龙纤维制成“拭子”,有利于吸附病原体
2.已知 ,下列化学用语正确的是
( )
A.HOOC—COOH属于羧酸,不能使酸性高锰酸钾溶液褪色
B. 是极性分子
C.NaClO的电子式为
D. 分子中键角为107°
3.若 表示阿伏加德罗常数,下列说法正确的是( )
A.熔融状态下,1 mol 中含 的数目为
B.密闭容器中,0.2 mol NO与0.1 mol 完全反应后,容器中气体分子数为
C.甲醇催化氧化生成1 mol HCHO的过程中,断裂的C—H键的数目为
D.浓度均为1 mol/L的KCl和 两种溶液中所含 的数目之比为1∶2
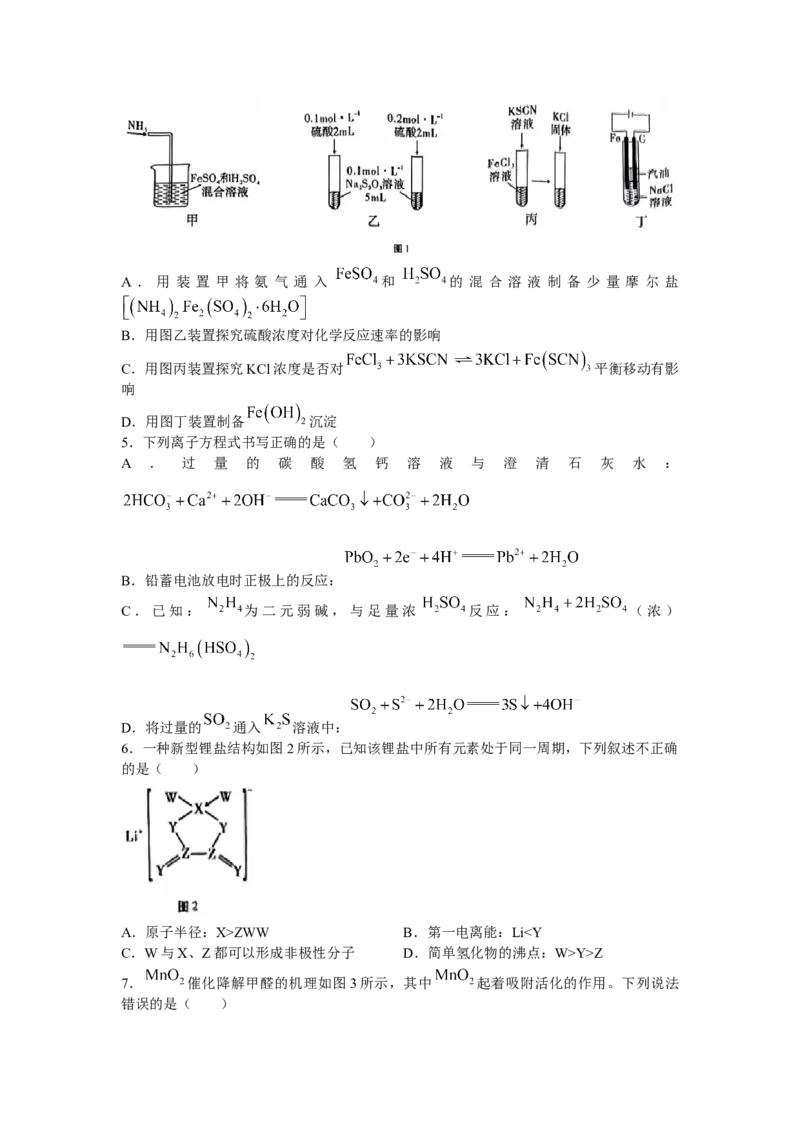
4.图1所示实验操作不能达到实验目的的是( )A . 用 装 置 甲 将 氨 气 通 入 和 的 混 合 溶 液 制 备 少 量 摩 尔 盐
B.用图乙装置探究硫酸浓度对化学反应速率的影响
C.用图丙装置探究KCl浓度是否对 平衡移动有影
响
D.用图丁装置制备 沉淀
5.下列离子方程式书写正确的是( )
A . 过 量 的 碳 酸 氢 钙 溶 液 与 澄 清 石 灰 水 :
B.铅蓄电池放电时正极上的反应:
C.已知: 为二元弱碱,与足量浓 反应: (浓)
D.将过量的 通入 溶液中:
6.一种新型锂盐结构如图2所示,已知该锂盐中所有元素处于同一周期,下列叙述不正确
的是( )
A.原子半径:X>ZWW B.第一电离能:LiY>Z
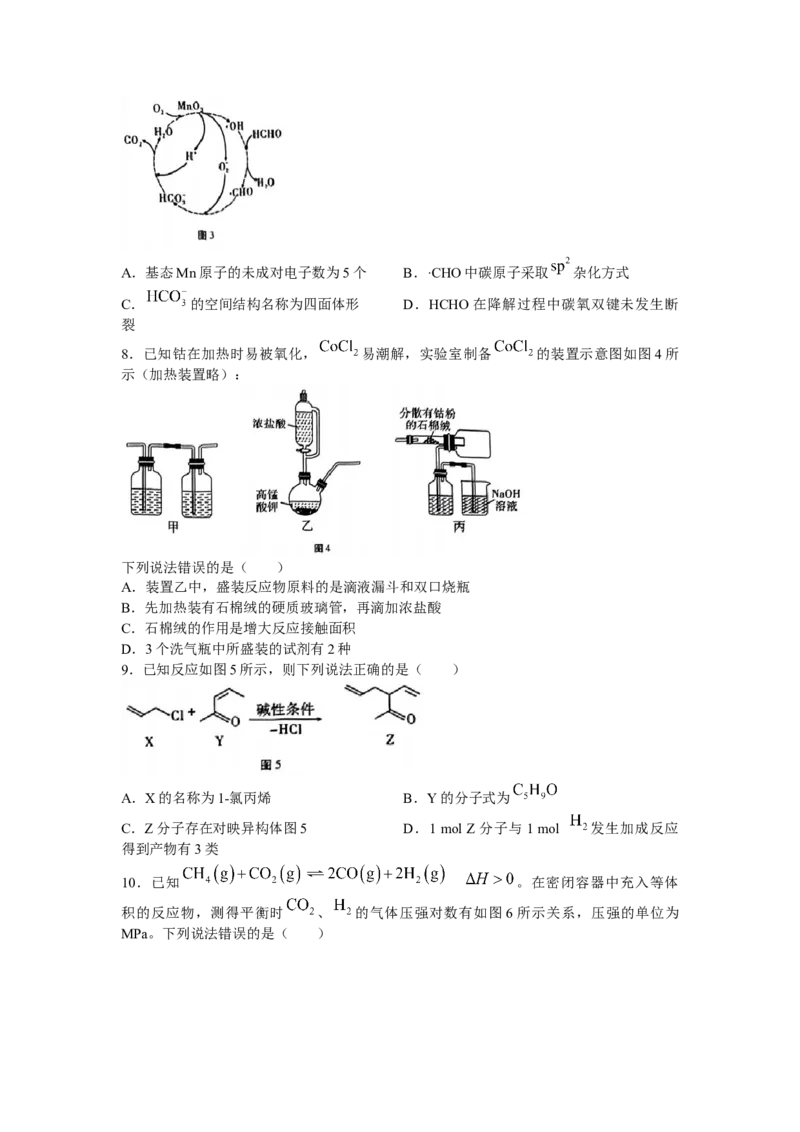
7. 催化降解甲醛的机理如图3所示,其中 起着吸附活化的作用。下列说法
错误的是( )A.基态Mn原子的未成对电子数为5个 B.·CHO中碳原子采取 杂化方式
C. 的空间结构名称为四面体形 D.HCHO在降解过程中碳氧双键未发生断
裂
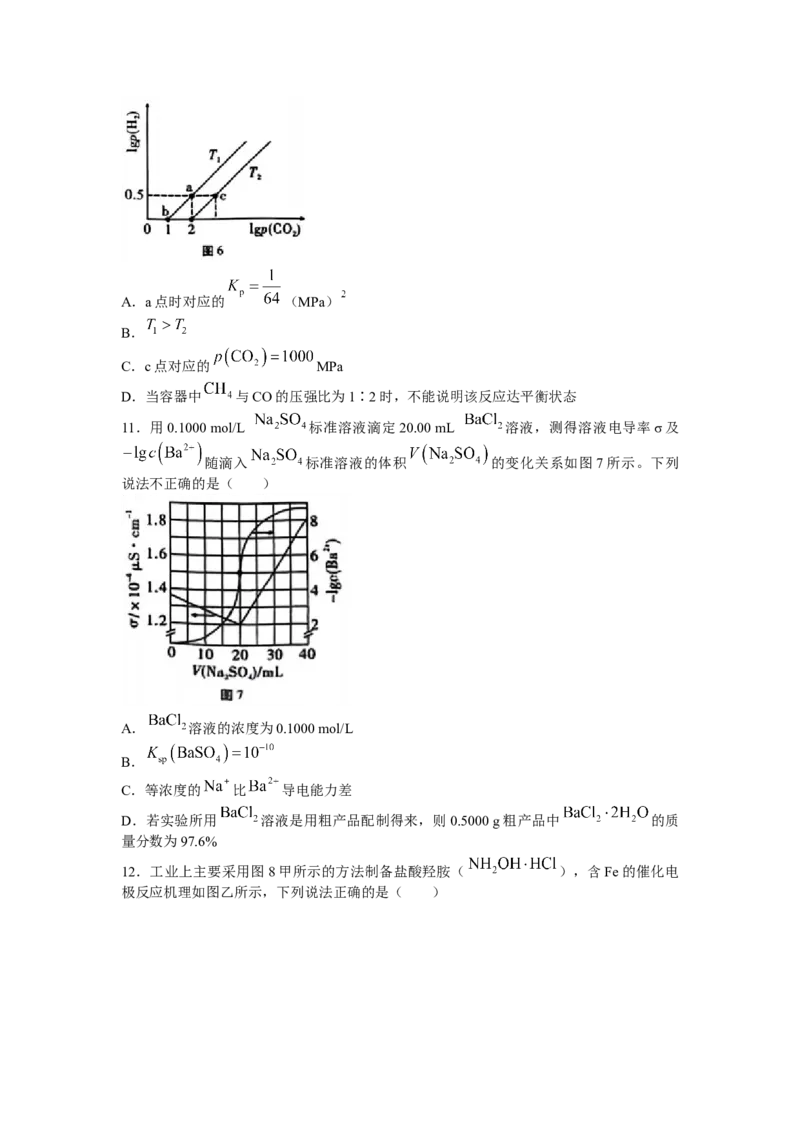
8.已知钴在加热时易被氧化, 易潮解,实验室制备 的装置示意图如图4所
示(加热装置略):
下列说法错误的是( )
A.装置乙中,盛装反应物原料的是滴液漏斗和双口烧瓶
B.先加热装有石棉绒的硬质玻璃管,再滴加浓盐酸
C.石棉绒的作用是增大反应接触面积
D.3个洗气瓶中所盛装的试剂有2种
9.已知反应如图5所示,则下列说法正确的是( )
A.X的名称为1-氯丙烯 B.Y的分子式为
C.Z分子存在对映异构体图5 D.1 mol Z分子与1 mol 发生加成反应
得到产物有3类
10.已知 。在密闭容器中充入等体
积的反应物,测得平衡时 、 的气体压强对数有如图6所示关系,压强的单位为
MPa。下列说法错误的是( )A.a点时对应的 (MPa)
B.
C.c点对应的 MPa
D.当容器中 与CO的压强比为1∶2时,不能说明该反应达平衡状态
11.用0.1000 mol/L 标准溶液滴定20.00 mL 溶液,测得溶液电导率σ及
随滴入 标准溶液的体积 的变化关系如图7所示。下列
说法不正确的是( )
A. 溶液的浓度为0.1000 mol/L
B.
C.等浓度的 比 导电能力差
D.若实验所用 溶液是用粗产品配制得来,则0.5000 g粗产品中 的质
量分数为97.6%
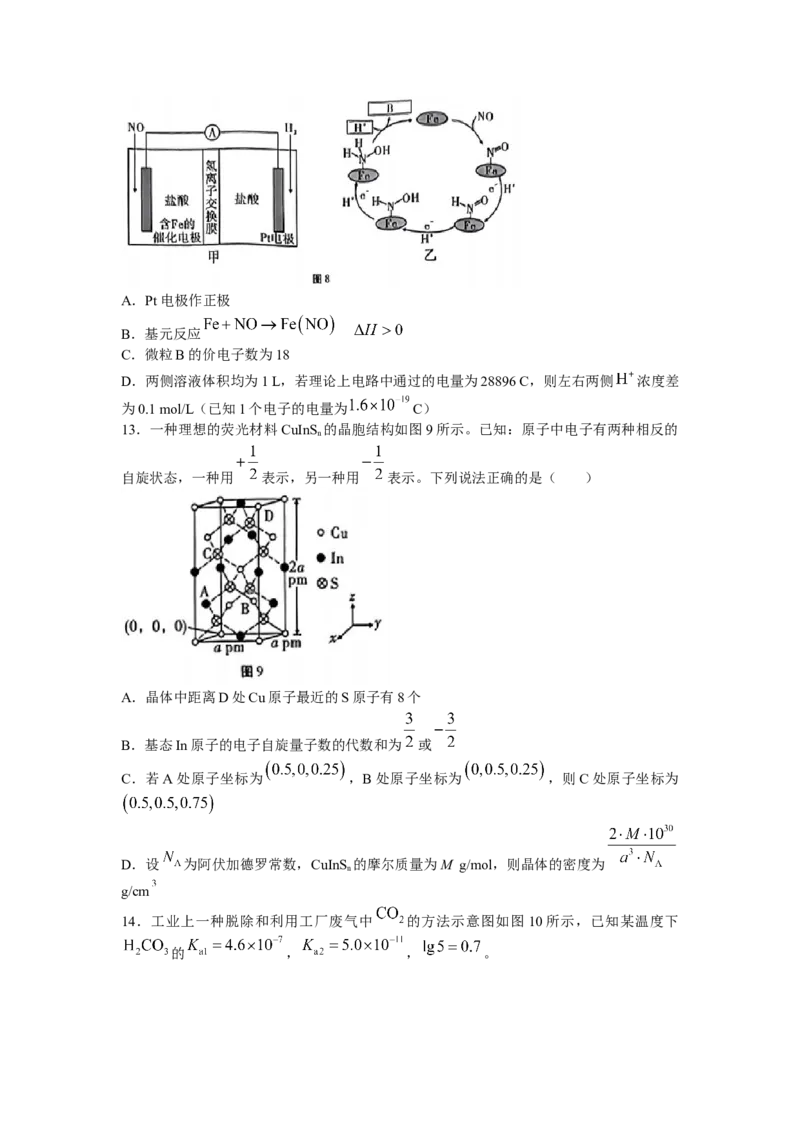
12.工业上主要采用图8甲所示的方法制备盐酸羟胺( ),含Fe的催化电
极反应机理如图乙所示,下列说法正确的是( )A.Pt电极作正极
B.基元反应
C.微粒B的价电子数为18
D.两侧溶液体积均为1 L,若理论上电路中通过的电量为28896 C,则左右两侧 浓度差
为0.1 mol/L(已知1个电子的电量为 C)
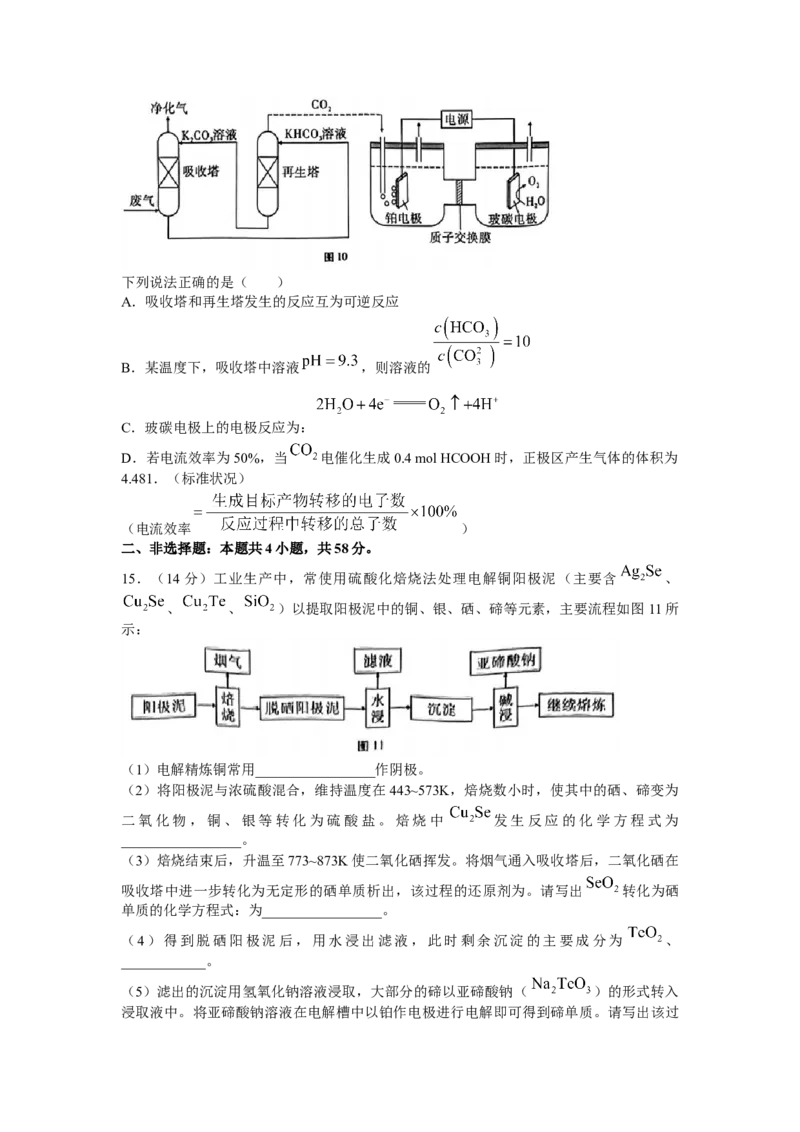
13.一种理想的荧光材料CuInS 的晶胞结构如图9所示。已知:原子中电子有两种相反的
n
自旋状态,一种用 表示,另一种用 表示。下列说法正确的是( )
A.晶体中距离D处Cu原子最近的S原子有8个
B.基态In原子的电子自旋量子数的代数和为 或
C.若A处原子坐标为 ,B处原子坐标为 ,则C处原子坐标为
D.设 为阿伏加德罗常数,CuInS 的摩尔质量为M g/mol,则晶体的密度为
n
g/cm
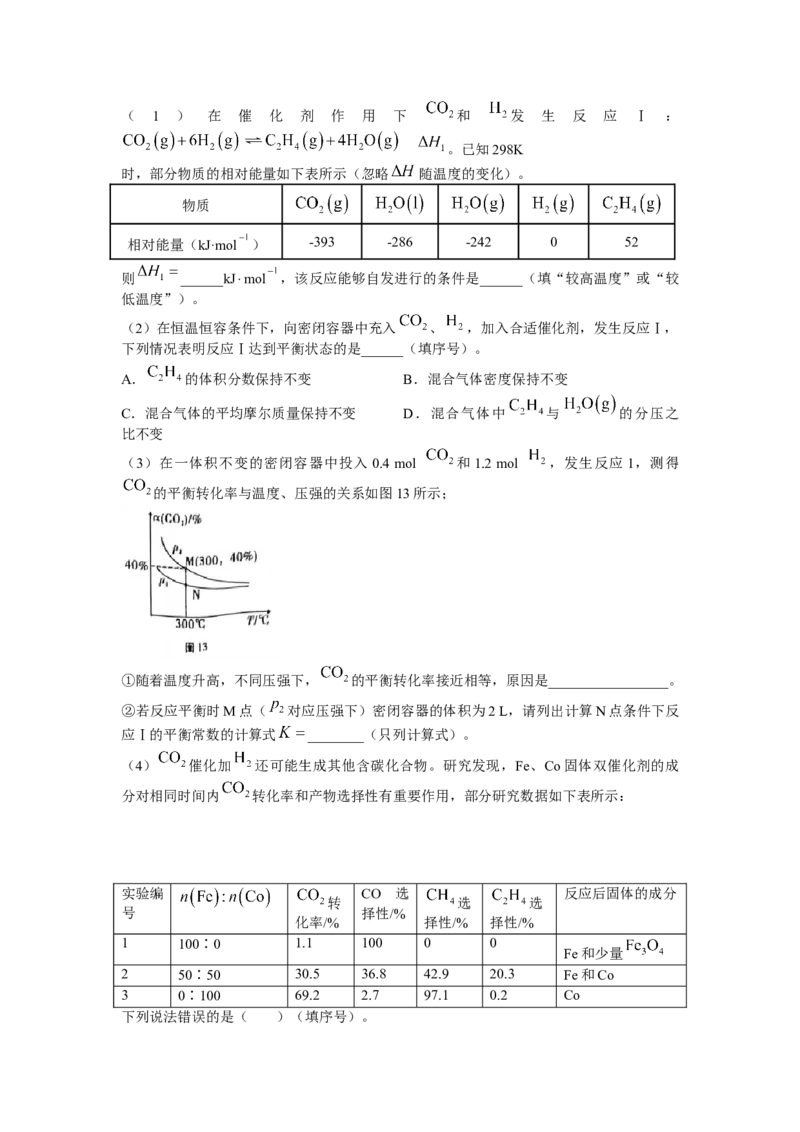
14.工业上一种脱除和利用工厂废气中 的方法示意图如图10所示,已知某温度下
的 , , 。下列说法正确的是( )
A.吸收塔和再生塔发生的反应互为可逆反应
B.某温度下,吸收塔中溶液 ,则溶液的
C.玻碳电极上的电极反应为:
D.若电流效率为50%,当 电催化生成0.4 mol HCOOH时,正极区产生气体的体积为
4.481.(标准状况)
(电流效率 )
二、非选择题:本题共4小题,共58分。
15.(14分)工业生产中,常使用硫酸化焙烧法处理电解铜阳极泥(主要含 、
、 、 )以提取阳极泥中的铜、银、硒、碲等元素,主要流程如图 11所
示:
(1)电解精炼铜常用_________________作阴极。
(2)将阳极泥与浓硫酸混合,维持温度在443~573K,焙烧数小时,使其中的硒、碲变为
二氧化物,铜、银等转化为硫酸盐。焙烧中 发生反应的化学方程式为
_________________。
(3)焙烧结束后,升温至773~873K使二氧化硒挥发。将烟气通入吸收塔后,二氧化硒在
吸收塔中进一步转化为无定形的硒单质析出,该过程的还原剂为。请写出 转化为硒
单质的化学方程式:为_________________。
(4)得到脱硒阳极泥后,用水浸出滤液,此时剩余沉淀的主要成分为 、
____________。
(5)滤出的沉淀用氢氧化钠溶液浸取,大部分的碲以亚碲酸钠( )的形式转入
浸取液中。将亚碲酸钠溶液在电解槽中以铂作电极进行电解即可得到碲单质。请写出该过程 的 电 极 反 应 方 程 式 : 阳 极 ______________________________ ; 阴 极
______________________。
(6)在磷酸和硫酸的混合溶液中,高锰酸钾可将碲(Ⅳ)氧化为碲(Ⅵ)。用此性质可以
测定样品中碲
(Ⅳ)的含量,过程如下:在亚碲酸钠样品中加入0.1000 mol/L高锰酸钾30.00 mL充分
反应,反应后的溶液用0.1000 mol/L 标准溶液滴定至紫色恰好褪去;
重复实验3次,平均消耗 标准溶液10.00 mL,则样品中亚碲酸钠的含量
为________g。( 的相对分子质量为222)
16.(15分)三聚氯氰是重要的精细化工产品,具有广泛的用途,其生产通常是由氯化氰
制备和氯化氰聚合两个过程组成。
Ⅰ.氯化氰制备
已知:氯化氰为无色液体,熔点-6.5℃,沸点12.5℃。可溶于水、乙醇、乙醚等,遇水缓慢
水解为氰酸和盐酸。现用氰化钠和氯气在四氯化碳中反应制备氯化氰,反应式:
。反应装置如图12所示,在三口烧瓶上装有温度计、搅
拌器、进气管、出气管,据图回答下列问题:
(1)CNCl的结构式为____________;其中C原子的杂化类型为__________________。
(2)在氯化氰的制备装置中,装置3、装置9中的试剂为____________。在反应前需要先
向装置内通入约3分钟干燥氮气,目的是______。
(3)该制备分为两个阶段。
阶段一:将40 g氰化钠粉末及140 mL四氯化碳装入烧瓶中,缓慢送入氯气并搅拌使得氯
气与NaCN充分反应。此阶段装置7、装置10、装置11作用相同,为____________;当D
中出现__________________现象时,说明阶段一结束。
阶段二:将______(填“装置7”“装置10”或“装置11”)的温度调整至60℃,将
____________(填“装置7”“装置10”或“装置11”)的温度调整至-40℃并缓慢通入氮
气直至阶段二结束。阶段二结束之后产品将被集中在______中(填字母)。
Ⅱ.氯化氰聚合
(4)氯化氰干燥后,在聚合塔中加热至400℃后便能得到氯化氰三聚物,请画出氯化氰三
聚物的结构式:______________________________。
17.(14分)2020年中国向世界宣布2030年前实现碳达峰,2060年前实现碳中和。转化
和吸收 的研究成为更加迫切的任务。( 1 ) 在 催 化 剂 作 用 下 和 发 生 反 应 Ⅰ :
。已知298K
时,部分物质的相对能量如下表所示(忽略 随温度的变化)。
物质
相对能量(kJ·mol ) -393 -286 -242 0 52
则 ______kJ⋅mol ,该反应能够自发进行的条件是______(填“较高温度”或“较
低温度”)。
(2)在恒温恒容条件下,向密闭容器中充入 、 ,加入合适催化剂,发生反应Ⅰ,
下列情况表明反应Ⅰ达到平衡状态的是______(填序号)。
A. 的体积分数保持不变 B.混合气体密度保持不变
C.混合气体的平均摩尔质量保持不变 D.混合气体中 与 的分压之
比不变
(3)在一体积不变的密闭容器中投入 0.4 mol 和1.2 mol ,发生反应1,测得
的平衡转化率与温度、压强的关系如图13所示;
①随着温度升高,不同压强下, 的平衡转化率接近相等,原因是_________________。
②若反应平衡时M点( 对应压强下)密闭容器的体积为2 L,请列出计算N点条件下反
应Ⅰ的平衡常数的计算式 ________(只列计算式)。
(4) 催化加 还可能生成其他含碳化合物。研究发现,Fe、Co固体双催化剂的成
分对相同时间内 转化率和产物选择性有重要作用,部分研究数据如下表所示:
实验编 CO 选 反应后固体的成分
转 选 选
号 择性/%
化率/% 择性/% 择性/%
1 100∶0 1.1 100 0 0
Fe和少量
2 50∶50 30.5 36.8 42.9 20.3 Fe和Co
3 0∶100 69.2 2.7 97.1 0.2 Co
下列说法错误的是( )(填序号)。A.实验1中生成 的化学方程式为
B.用该方法制备 时,最好选用金属Co作催化剂
C. 对该制备过程影响很大
D.若生成等物质的量的 和 ,转移的电子数比值为2∶1
(5)在一定条件下,选择合适的催化剂使 只发生转化为CO的反应
。调整 和 初始投料比,测得在
一定投料比和一定
温度下,该反应 的平衡转化率如图14所示:
已 知 : 是 以 物 质 的 量 分 数 表 示 的 化 学 平 衡 常 数 ; 反 应 速 率
, 、 分别为正、逆向反应
速率常数,x为物质的量分数。B、E、F三点反应温度最高的是______点,
计算E点所示的投料比在从起始到平衡的过程中,当 转化率达到 40%时,
______。
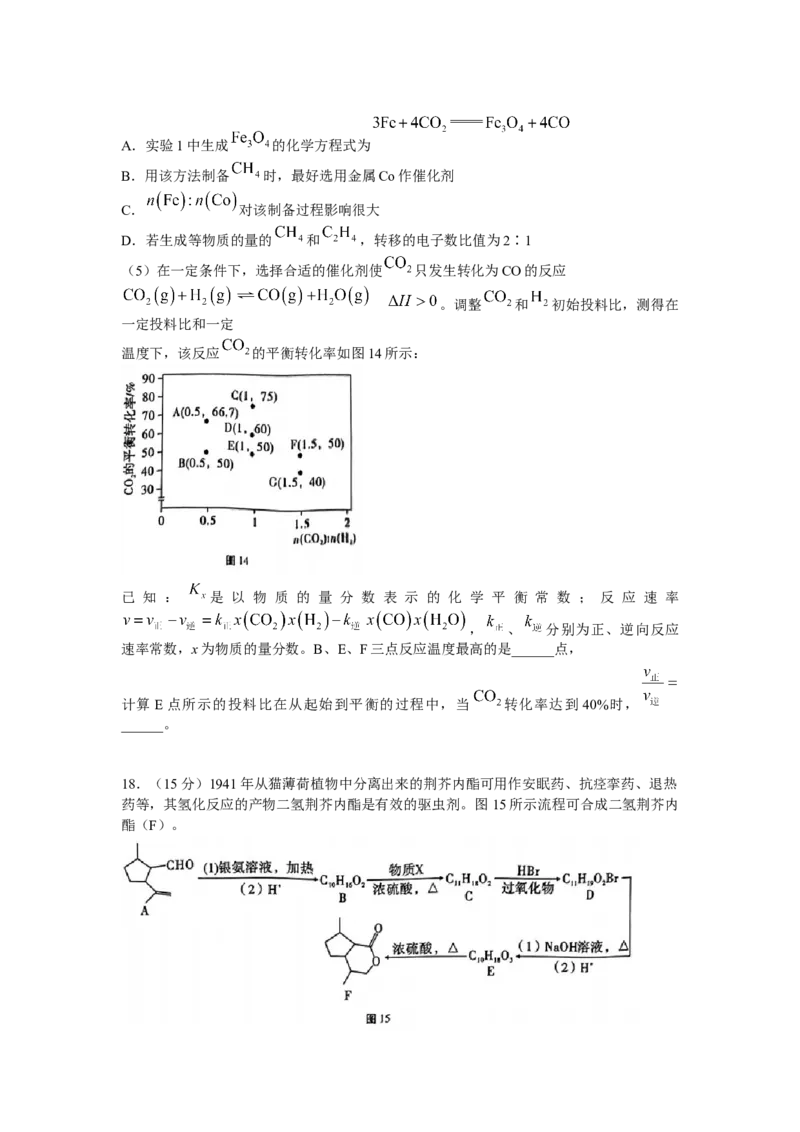
18.(15分)1941年从猫薄荷植物中分离出来的荆芥内酯可用作安眠药、抗痉挛药、退热
药等,其氢化反应的产物二氢荆芥内酯是有效的驱虫剂。图 15所示流程可合成二氢荆芥内
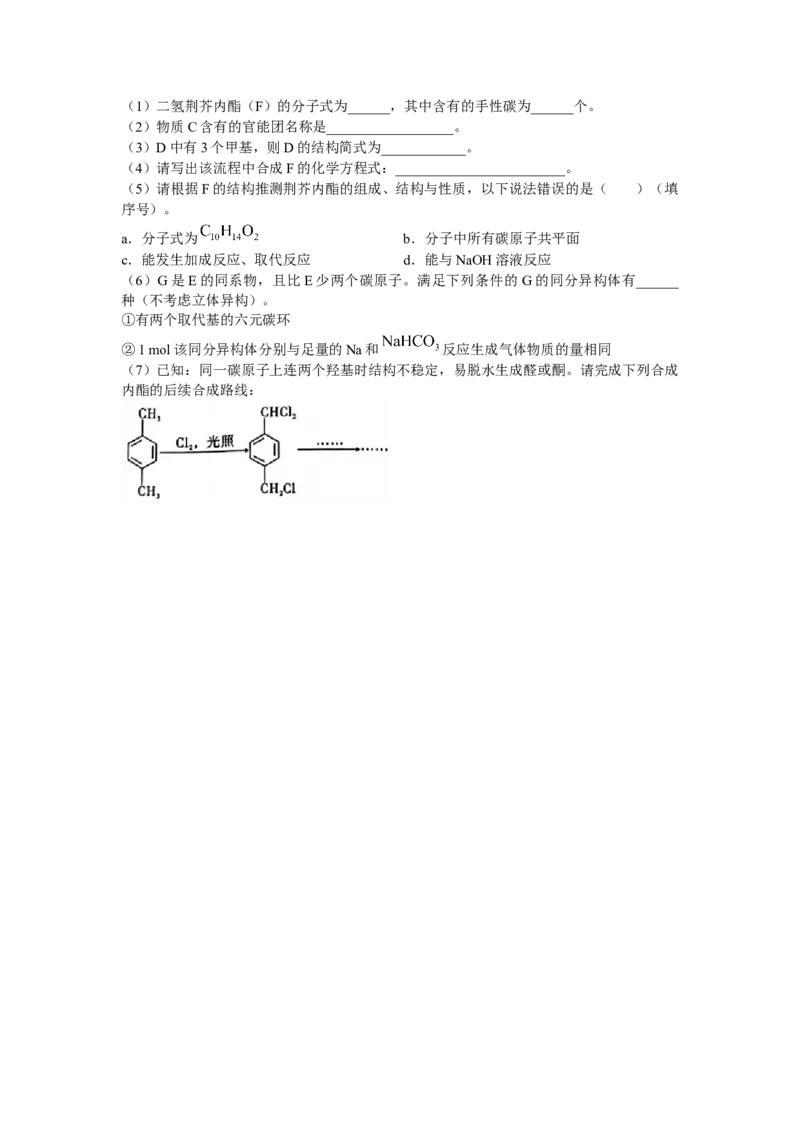
酯(F)。(1)二氢荆芥内酯(F)的分子式为______,其中含有的手性碳为______个。
(2)物质C含有的官能团名称是__________________。
(3)D中有3个甲基,则D的结构简式为____________。
(4)请写出该流程中合成F的化学方程式:________________________。
(5)请根据F的结构推测荆芥内酯的组成、结构与性质,以下说法错误的是( )(填
序号)。
a.分子式为 b.分子中所有碳原子共平面
c.能发生加成反应、取代反应 d.能与NaOH溶液反应
(6)G是E的同系物,且比E少两个碳原子。满足下列条件的G的同分异构体有______
种(不考虑立体异构)。
①有两个取代基的六元碳环
②1 mol该同分异构体分别与足量的Na和 反应生成气体物质的量相同
(7)已知:同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮。请完成下列合成
内酯的后续合成路线: