文档内容
第五章 化工生产中的重要非金属元素(单元测试)
(时间:60分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分。)
1.《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无砂粘土而为之”,“凡坯既成,干燥之后,
则堆积窖中燃薪举火”,“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是( )
A.沙子和粘土主要成分为硅酸盐
B.“燃薪举火”使粘土发生复杂的物理化学变化
C.烧制后自然冷却成红瓦,浇水冷却成青瓦
D.粘土是制作砖瓦和陶瓷的主要原料
【答案】A
【解析】沙子的主要成分是SiO ,粘土的主要成分是硅酸盐,A错误;“燃薪举火”烧制粘土,发生一系
2
列复杂的物理化学变化,制得砖、瓦等硅酸盐产品,B正确;据“浇水转釉(主要为青色),与造砖同法”
可知,烧制后浇水冷却成青瓦,C正确;粘土是制作砖瓦和陶瓷的主要原料,D正确。
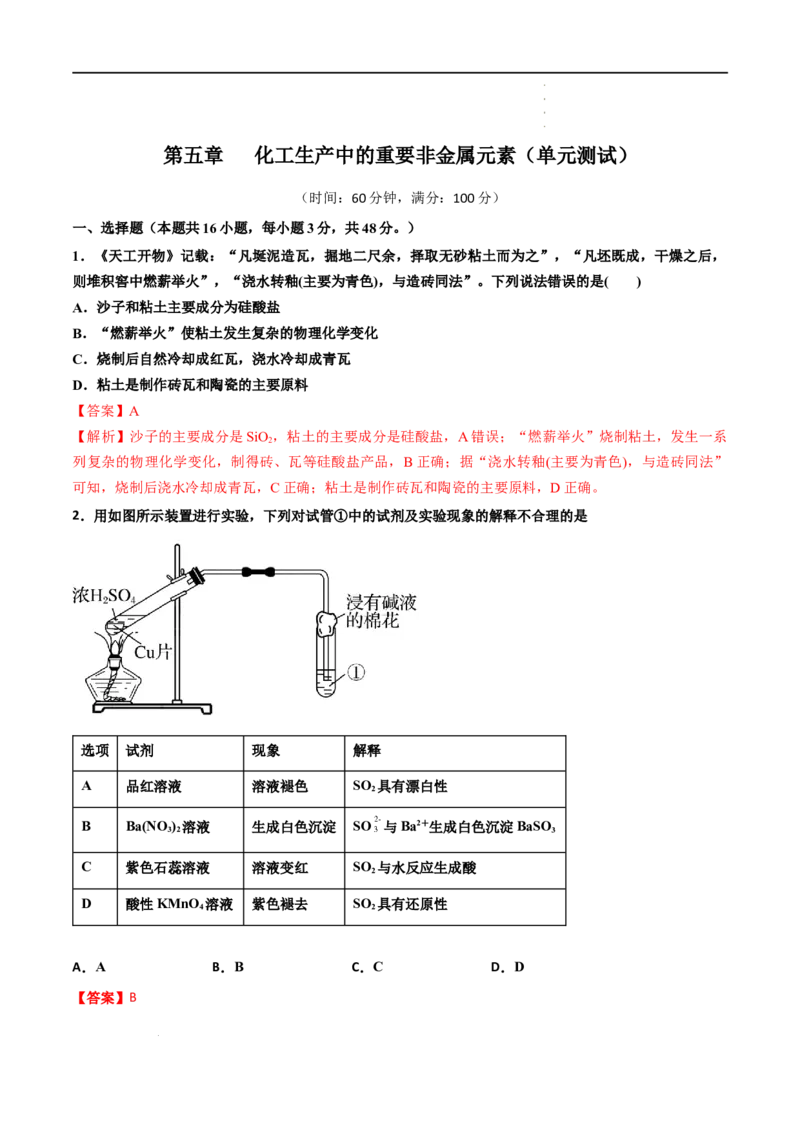
2.用如图所示装置进行实验,下列对试管①中的试剂及实验现象的解释不合理的是
选项 试剂 现象 解释
A 品红溶液 溶液褪色 SO 具有漂白性
2
B Ba(NO ) 溶液 生成白色沉淀 SO 与Ba2+生成白色沉淀BaSO
3 2 3
C 紫色石蕊溶液 溶液变红 SO 与水反应生成酸
2
D 酸性KMnO 溶液 紫色褪去 SO 具有还原性
4 2
A.A B.B C.C D.D
【答案】B
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【详解】
Cu和浓HSO 在加热条件下反应生成SO 。
2 4 2
A.SO 具有漂白性,能使品红溶液褪色,A项正确;
2
B.SO 通入Ba(NO ) 溶液中,酸性条件下,NO 将SO 氧化为SO ,得到BaSO 沉淀,B项错误;
2 3 2 2 4
C.SO 与水反应生成HSO ,使紫色石蕊溶液变红,C项正确;
2 2 3
D.SO 具有还原性,能与酸性KMnO 溶液反应而使溶液褪色,D项正确;
2 4
答案选B。
3.(2022·上海浦东新·一模)浓硫酸与潮湿的蔗糖反应时,没有体现出的性质是
A.吸水性 B.脱水性 C.酸性 D.氧化性
【答案】C
【详解】
浓硫酸吸收潮湿的蔗糖中的水时表现吸水性,使蔗糖脱水碳化时表现脱水性,脱水得到的碳与浓硫酸共热
反应生成二氧化碳和二氧化硫时表现强氧化性,则反应过程中没有体现出的性质是酸性,故选C。
4.2021年,我国研制的九章二号量子计算机,在求解高斯玻色取样数学问题上,比目前世界上最快的计
算机“超算”要快亿亿亿倍。计算机芯片的主要材料是
A.硅 B.碳 C.铁 D.锰
【答案】A
【详解】
硅是半导体,计算机芯片的主要材料是硅,故选A。
5.下列说法中正确的是
A.根据化合价可知,S在化学反应中只能作还原剂
B.试管内壁上的硫黄可用CS 清洗
2
C.S+O SO ,S被氧化,作氧化剂
2 2
D.硫只以化合态存在于自然界中
【答案】B
【详解】
A.0价是S的中间价态,所以S既可作氧化剂,又可作还原剂,A错误;
B.S易溶于CS,所以可以用CS 清洗试管内壁的硫粉,B正确;
2 2
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司C.S被氧化,化合价升高,作还原剂,C错误;
D.硫在自然界中既有游离态又有化合态,D错误;
故选:B。
6.下列试剂的保存方法正确的是
A.少量的金属钠保存在石蜡油或煤油中
B.氢氟酸(HF)保存在带磨口玻璃塞的细口瓶中
C.漂白粉可放置在空气中保存
D.新制的氯水保存在无色带橡胶塞的玻璃试剂瓶中
【答案】A
【详解】
A. 钠的密度比煤油大,且不反应,少量的金属钠保存在石蜡油或煤油中,以隔绝空气,故A正确;
B. 氢氟酸(HF)能与玻璃成分中的二氧化硅反应,保存在塑料瓶中,故B错误;
C. 漂白粉能与空气中的水和二氧化碳反应生成次氯酸,次氯酸不稳定发生分解而失效,所以不可放置在
空气中保存,故C错误;
D. 新制的氯水具有不稳定性、强氧化性,应保存在棕色带磨口玻璃塞的细口瓶中,故D错误;
故选A。
7.(2021·上海杨浦·高三阶段练习)将 分别通入下列溶液中,对现象的分析正确的是
选项 溶液 现象 分析
A 含酚酞的 溶液 红色消失 是酸性氧化物
B 溴水 橙色消失 具有漂白性
C 溶液 变为浅绿色溶液
D 溶液 产生淡黄色浑浊
A.A B.B C.C D.D
【答案】A
【详解】
A.将SO 气体通入含有酚酞的氢氧化钠溶液中,二氧化硫是酸性氧化物,和氢氧化钠发生反应形成
2
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司NaSO 和水,所以溶液褪色,故A正确;
2 3
B.将SO 气体通入溴水中,二氧化硫和溴发生氧化还原反应生成硫酸和溴化氢使溴水褪色,而不是因为
2
具有漂白性,故B错误;
C.将SO 气体通入氯化铁溶液中, 二氧化硫和氯化铁发生氧化还原反应,离子方程式为:
2
,溶液变为浅绿色溶液,故C错误;
D.将SO 气体通入 溶液中,SO 和 反应生成黄色沉淀硫单质,其离子方程式为
2 2
,故D错误;
答案选A。
8.下列物质之间的转化都能一步实现的是( )
A.HS→S→SO →HSO B.Si→SiO →HSiO →Na SiO
2 3 2 4 2 2 3 2 3
C.FeS →SO →Na SO →Na SO D.N→NH →NO →HNO →NO
2 2 2 3 2 4 2 3 2 3 2
【答案】C
【解析】
A.硫与氧气反应只能生成二氧化硫,不能一步反应生成三氧化硫,故A错误;
B.二氧化硅不能一步生成硅酸,可由可溶性的硅酸盐与酸反应生成硅酸,故B错误;
C.FeS 在高温条件下与氧气反应生成SO ,SO 与氢氧化钠溶液反应生成NaSO ,NaSO 被氧气氧化为
2 2 2 2 3 2 3
NaSO ,各物质之间的转化均能一步完成,故C正确;
2 4
D.氨气催化氧化得到一氧化氮,不能一步生成二氧化氮,故D错误。
故选C。
9.下列说法正确的是
A.硅酸不溶于水,因此不与NaOH溶液反应
B.据SiO +CaCO CaSiO +CO↑的反应,可推知硅酸酸性比碳酸酸性强
2 3 3 2
C.硅太阳能电池、石英光导纤维和计算机芯片所用的材料都是Si
D.普通玻璃是以纯碱、石灰石和石英为原料经高温烧结而制成的
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司【答案】D
【详解】
A.硅酸不溶于水,但是二氧化硅可以与氢氧化钠反应生成硅酸钠和水,故A错误;
B.反应高温下进行,生成的二氧化碳是气体,SiO+CaCO CaSiO +CO ↑的反应,是高沸点的物质制
2 3 3 2
取低沸点的物质,不能说明硅酸的酸性比碳酸强,故B错误;
C.石英光导纤维所用的材料是SiO,故C错误;
2
D.普通玻璃是以纯碱、石灰石、石英为原料高温烧结而成,故D正确;
故选D。
10.(2022·安徽芜湖·高一期末)下列是对“某溶液”进行离子检测的方法和结论,其中说法正确的是
A.加入稀HCl产生能使澄清石灰水变浑浊的无色气体,则溶液中一定含有
B.先加入氯水,再加入KSCN溶液显红色,则溶液中一定含有Fe3+
C.依次加入BaCl 溶液、HNO 溶液,有白色沉淀产生,则溶液中一定含有
2 3
D.加入HNO 酸化的AgNO 液,有白色沉淀产生,则溶液中一定含有Cl-
3 3
【答案】D
【详解】
A.加入稀HCl产生能使澄清石灰水变浑浊的无色气体,该气体可能是CO,也可能是SO ,则溶液中可能
2 2
含有 ,也可能含有 或 、 ,不一定含有 ,A错误;
B.向溶液中先加入氯水,再加入KSCN溶液显红色,说明加入氯水后的溶液中含有Fe3+,该Fe3+可能是原
溶液中含有的,也可能是Fe2+被氯水氧化产生的,因此不能确定原溶液中是否含有Fe3+,B错误;
C.由于HNO 具有强氧化性,可能会将 氧化为 ,所以向某溶液中依次加入BaCl 溶液、HNO 溶
3 2 3
液,有白色沉淀产生,则溶液中可能含有 ,加入BaCl 溶液时产生BaSO 白色沉淀,再加入稀
2 3
HNO,HNO 将BaSO 氧化为BaSO 白色沉淀,因此原溶液中不一定含有 ,C错误;
3 3 3 4
D.由于AgCl是白色既不溶于水、也不溶于稀硝酸的物质,所以向某溶液中加入HNO 酸化的AgNO 液,
3 3
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司有白色沉淀产生,则溶液中一定含有Cl-,D正确;
故合理选项是D。
11.(2022·上海市杨浦高级中学高一期末)将一定量的 通入 溶液中,再加入适量 溶液,一
定会大量增加的是
A. B. C. D.
【答案】A
【详解】
二氧化硫是酸性氧化物、对应的亚硫酸是中强酸,SO 不与氯化钡溶液反应,过氧化氢具有强氧化性,能
2
够氧化二氧化硫生成硫酸,则硫酸根离子遇钡离子生成硫酸钡沉淀;
A.加入过氧化氢溶液后,发生SO +H O=HSO ,氢离子一定是增加的,A符合;
2 2 2 2 4
B.据分析,硫酸根离子被沉淀、浓度减小,B不符合;
C.据分析,钡离子被沉淀、浓度减小,C不符合;
D.氯离子不参加反应,加入双氧水溶液后,溶液体积增大,氯离子浓度减小,D不符合;
故答案选A。
12. 可溶于浓硫酸生成 ,继续与水反应转化为 ,下列有关硫酸的说法正确的是
A.浓硫酸具有吸水性,可用于干燥氨气
B.浓硫酸与铁不反应,可用铁罐储运浓硫酸
C.常温下,可用浓硫酸与 反应制备
D.将 全部转化为 需消耗
【答案】D
【详解】
A.浓硫酸具有很强的吸水性,但能与氨气反应生成硫酸铵,不可用于干燥氨气,选项A错误;
B.常温下金属Fe与浓硫酸发生钝化反应,会在金属表面形成致密的氧化膜,阻止反应进一步发生,可用
铁罐来进行贮存、运输冷的浓硫酸,不是不反应,选项B错误;
C.常温下,铜和浓硫酸不反应,加热条件下可用浓硫酸与 反应制备 ,选项C错误;
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司D.将 全部转化为 需消耗 得到2mol ,选项D正确;
答案选D。
13.根据下列实验操作和现象所得出的结论正确的是
选项 实验操作和现象 实验结论
A 用铂丝蘸取待测液置于酒精灯火焰上灼烧,火焰呈黄色 该溶液中一定不含
B 向某白色粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体 该粉末一定是碳酸盐
向某溶液中加入 溶液,将湿润的红色石蕊试纸靠近试管口,试纸不
C 溶液中一定不含
变蓝
将除去表面氧化膜的相同大小的镁片和铝片分别投入 的盐酸
D 金属性:
中,镁片反应更剧烈
A.A B.B C.C D.D
【答案】D
【详解】
A.钠的焰色反应为黄色,待测液置于酒精灯外焰灼烧时,焰色反应为黄色,一定含有钠元素,说明溶液
中含有Na+,但钾离子要经过蓝色的钴玻璃来看,否则无法判断,故A错误;
B.二氧化碳、二氧化硫均使石灰水变浑浊,由操作和现象可知粉末可能为碳酸盐或碳酸氢盐,或亚硫酸
盐等,故B错误;
C.铵根离子和稀的NaOH溶液反应生成一水合氨,不加热得不到氨气,所以往某溶液中加入NaOH溶液,
将湿润的红色石蕊试纸靠近试管口,试纸颜色不变蓝,该溶液中也可能含铵根离子,故C错误;
D.金属性越强,反应越剧烈,镁片表面产生气泡速率大于铝片,可说明镁较活泼,则金属性: ,
故D正确;
故选:D。
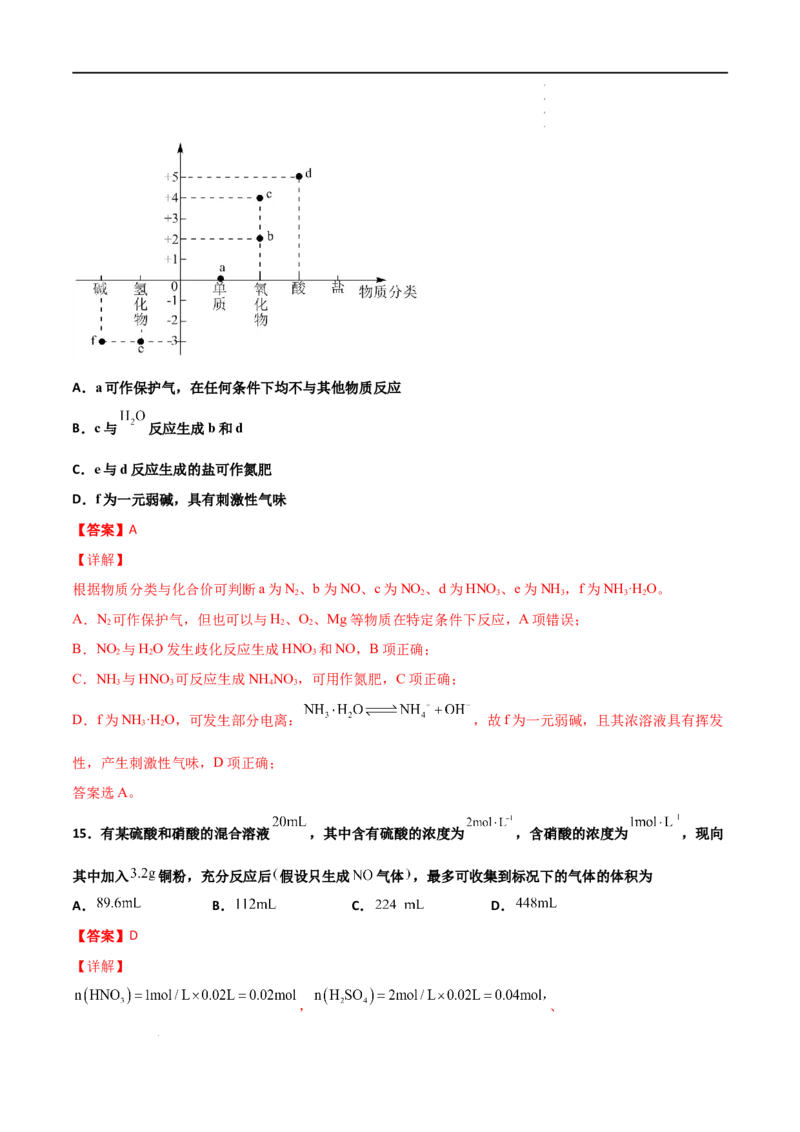
14.(2021·广东·高三阶段练习)价类二维图可以帮助我们梳理物质间的转化关系,下图为氮及其化合物
的价类二维图,有关说法不正确的是
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司A.a可作保护气,在任何条件下均不与其他物质反应
B.c与 反应生成b和d
C.e与d反应生成的盐可作氮肥
D.f为一元弱碱,具有刺激性气味
【答案】A
【详解】
根据物质分类与化合价可判断a为N、b为NO、c为NO 、d为HNO、e为NH ,f为NH ·H O。
2 2 3 3 3 2
A.N 可作保护气,但也可以与H、O、Mg等物质在特定条件下反应,A项错误;
2 2 2
B.NO 与HO发生歧化反应生成HNO 和NO,B项正确;
2 2 3
C.NH 与HNO 可反应生成NH NO ,可用作氮肥,C项正确;
3 3 4 3
D.f为NH ·H O,可发生部分电离: ,故f为一元弱碱,且其浓溶液具有挥发
3 2
性,产生刺激性气味,D项正确;
答案选A。
15.有某硫酸和硝酸的混合溶液 ,其中含有硫酸的浓度为 ,含硝酸的浓度为 ,现向
其中加入 铜粉,充分反应后 假设只生成 气体 ,最多可收集到标况下的气体的体积为
A. B. C. D.
【答案】D
【详解】
, 、
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司,发生反应为
,根据方程式知,硝酸根离子完全反应需要 为
、 为 ,所以硝酸根离子不足量,所以硝酸根离子完全被还原生成
,根据 原子守恒得 ,则 ,
故选D。
二、非选择题(本题共4小题,共52分。)
16.归纳、演绎和模型等是化学学习的重要方法,回答下列问题。
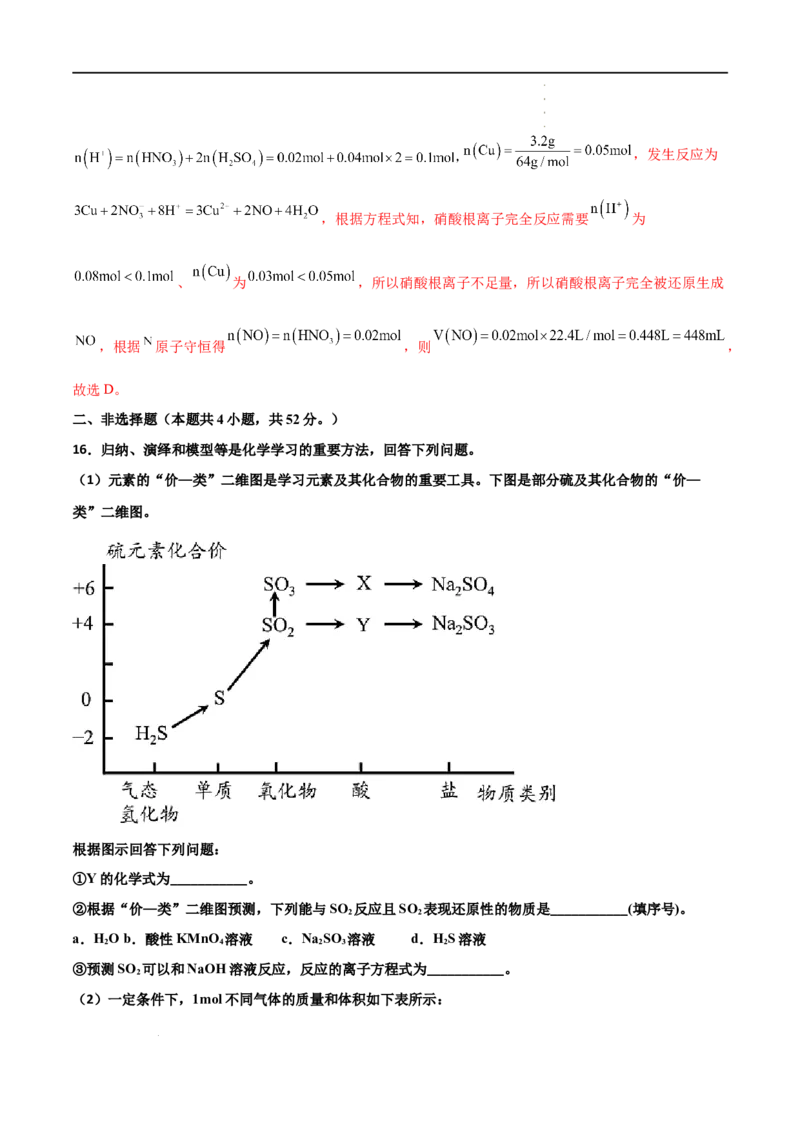
(1)元素的“价—类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价—
类”二维图。
根据图示回答下列问题:
①Y的化学式为___________。
②根据“价—类”二维图预测,下列能与SO 反应且SO 表现还原性的物质是___________(填序号)。
2 2
a.HO b.酸性KMnO 溶液 c.Na SO 溶液 d.HS溶液
2 4 2 3 2
③预测SO 可以和NaOH溶液反应,反应的离子方程式为___________。
2
(2)一定条件下,1mol不同气体的质量和体积如下表所示:
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司化学式 质量 0℃、101kPa 20℃、101kPa 0℃、202kPa
H 2g 22.4L 24.0L 11.2L
2
O 32g 22.4L 24.0L 11.2L
2
CO 44g 22.3L 24.0L 11.2L
2
分析表中数据,可得出温度、压强与气体体积关系的结论是___________(写出两点即可)。
【答案】(共8分,每空2分)
(1) HSO b SO +2OH−=H O+SO 或SO +OH−=HSO
2 3 2 2 2
(2)相同温度和压强下,1mol(或物质的量相同)气体的体积相等;温度相同时,压强越大,1mol气体的
体积越小;压强相同时,温度越高,1mol气体体积越大(其它答案合理)
【解析】
(1)①根据图像,Y中硫元素的化合价为+4价,属于酸,推知其为亚硫酸,化学式为HSO 。
2 3
②能与SO 反应且SO 表现还原性的物质应该具有氧化性,符合条件的是酸性高锰酸钾溶液,答案选b。
2 2
③SO 为酸性氧化物,可以和NaOH溶液反应,若氢氧化钠过量则反应的离子方程式为
2
SO +2OH−=H O+SO ;若二氧化硫过量则反应的离子方程式为SO +OH−=HSO 。
2 2 2
(2)根据表格数据可知,相同温度和压强下,1mol(或物质的量相同)气体的体积相等;温度相同时,压强
越大,1mol气体的体积越小;压强相同时,温度越高,1mol气体体积越大(其它答案合理)。
17.(2020·宁夏·吴忠中学)实验室里研究不同价态硫元素之间的转化
(1)A中发生反应的化学方程式为________________。
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(2)B中的现象是__________________。
(3)C中出现淡黄色沉淀,反应中Na S做____________(填“氧化剂”或“还原剂”)。
2
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为________________价。
(5)E的作用是_____________,离子方程式为_________________________。
(6)上述实验D体现SO 的性质是_________________。
2
【答案】(共15分,除标注外,每空2分)
(1)Cu+2H SO (浓) CuSO +SO↑+2H O (3分)
2 4 4 2 2
(2) 品红褪色
(3)还原剂
(4) +6
(5)吸收SO 尾气,防止污染环境 SO +2OH−= +H O
2 2 2
(6)还原性
【详解】
装置A中浓硫酸与Cu在加热条件反应生成SO ,B中品红溶液可以检验二氧化硫的漂白性,C中硫化钠可
2
以和二氧化硫发生归中反应生成S单质,从而验证二氧化硫的还原性,D中溴水具有较强氧化性,可以将
二氧化硫氧化成硫酸根,溴被还原从而溴水褪色,E中NaOH溶液可以吸收未反应的二氧化硫。
(1)浓硫酸具有强氧化性,加热条件可以将Cu氧化,自身被还原生成二氧化硫,结合电子守恒和元素守恒
可得化学方程式为Cu+2H SO (浓) CuSO +SO↑+2H O;
2 4 4 2 2
(2)二氧化硫具有漂白性可以使品红溶液褪色,所以现象为品红褪色;
(3)C中出现淡黄色沉淀说明生成S单质,硫化钠和二氧化硫发生归中反应,硫化钠中硫元素化合价升高,
所以硫化钠作还原剂;
(4)溴水具有氧化性可以将+4价的硫氧化,根据硫的价态变化规律可知被氧化成+6价;
(5)二氧化硫会污染空气不能直接排放,可用NaOH溶液吸收,离子方程式为SO +2OH−= +H O;
2 2
(6)D中二氧化硫被氧化,体现了二氧化硫的还原性。
18.(2022·四川成都·高一期末)氯气有毒,管道工人用浓氨水靠近氯气管道检查管道是否泄漏,其反应
为 。
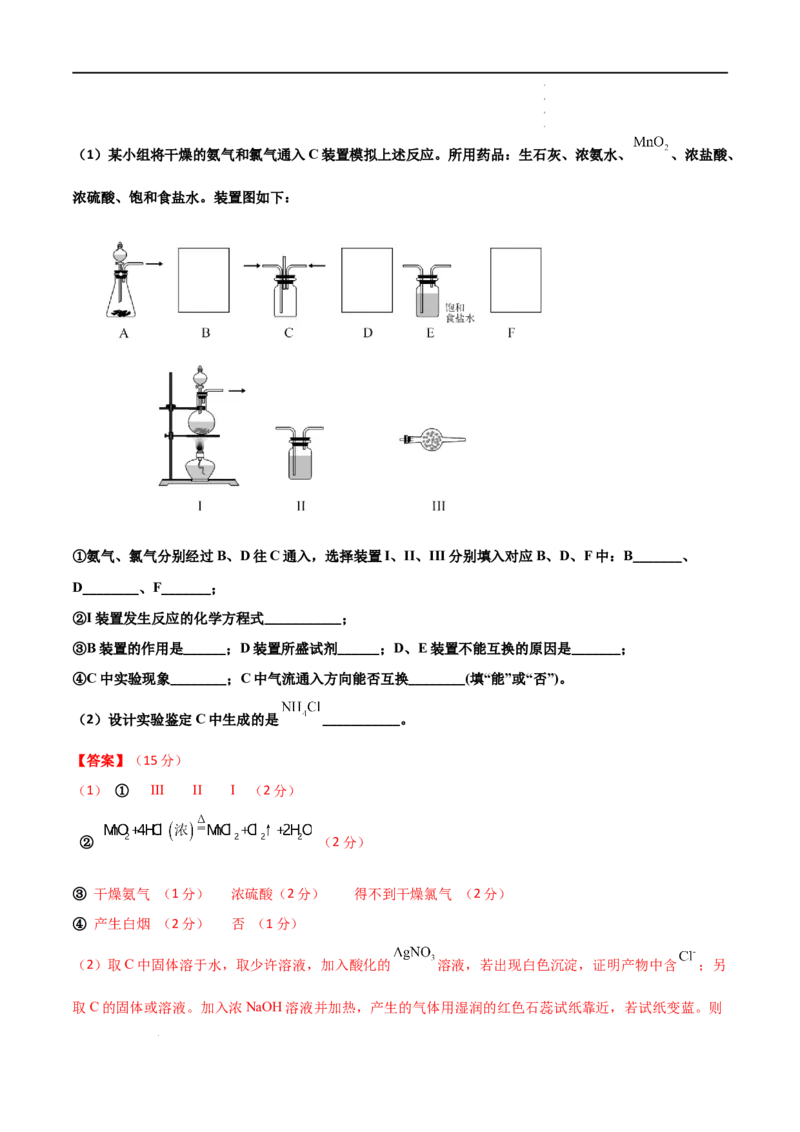
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(1)某小组将干燥的氨气和氯气通入C装置模拟上述反应。所用药品:生石灰、浓氨水、 、浓盐酸、
浓硫酸、饱和食盐水。装置图如下:
①氨气、氯气分别经过B、D往C通入,选择装置I、II、III分别填入对应B、D、F中:B_______、
D________、F_______;
②I装置发生反应的化学方程式___________;
③B装置的作用是______;D装置所盛试剂______;D、E装置不能互换的原因是_______;
④C中实验现象________;C中气流通入方向能否互换________(填“能”或“否”)。
(2)设计实验鉴定C中生成的是 ___________。
【答案】(15分)
(1) ① III II I (2分)
② (2分)
③ 干燥氨气 (1分) 浓硫酸(2分) 得不到干燥氯气 (2分)
④ 产生白烟 (2分) 否 (1分)
(2)取C中固体溶于水,取少许溶液,加入酸化的 溶液,若出现白色沉淀,证明产物中含 ;另
取C的固体或溶液。加入浓NaOH溶液并加热,产生的气体用湿润的红色石蕊试纸靠近,若试纸变蓝。则
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司证明产物中含 (3分)
【解析】
(1)①利用浓氨水与生石灰在装置A中制备氨气,制得氨气通过III中装有碱石灰的干燥管,再进入C;
利用二氧化锰和浓盐酸共热在I中制氯气,制得氯气通过E中的饱和食盐水除去氯化氢,再通过D中浓硫
酸干燥,故D选II,对应B、D、F中:B:III、D:II、F:I;
②I装置利用二氧化锰和浓盐酸共热生成氯化锰、氯气和水, 发生反应的化学方程式为
;
③B装置的作用是干燥氨气;D装置用来干燥氯气,所盛试剂浓硫酸;D、E装置不能互换,否则得不到干
燥氯气;
④C中氨气和氯气混合生成氯化铵和氮气,实验现象产生白烟;C中气流通入方向不能互换,因为氯气的
密度大于空气而氨气的密度小于空气,互换则无法充分反应;
(2)取C中固体溶于水,取少许溶液,加入酸化的 溶液,若出现白色沉淀,证明产物中含 ;另
取C的固体或溶液。加入浓NaOH溶液并加热,产生的气体用湿润的红色石蕊试纸靠近,若试纸变蓝。则
证明产物中含 ,则C中生成的是 。
19.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地亮质量的90%以上。
(1)下列物质不属于硅酸盐材料的是___________。
A.陶瓷 B.玻璃 C.水泥 D.生石灰
(2) 是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程式为___________,工艺师常用
___________(填物质名称)来雕刻玻璃。
(3)用 水溶液浸泡过的棉花不易燃烧,说明 可用作___________。 可通过
与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是___________。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司(4)工业上常利用反应 制备硅单质,该反应中氧化剂是___________。
(5)根据如图所示装置回答以下问题。
若要用此装置证明酸性: ,从以下所给物质中选出甲同学设计的实验所用到的物质:
①稀 ②稀盐酸 ③碳酸钙 ④ 溶液 ⑤ 。试剂A与C分别为___________(填序号);
试管中发生反应的离子方程式为___________。有同学认为此实验不能说明酸性强弱,你认为原因是
___________。
【答案】(14分,除标注外,每空2分)
(1)D (1分)
(2) 氢氟酸 (1分)
(3)防火剂(1分) D (1分)
(4)
(5) ①④ 有挥发性,也会和硅酸钠反应生成硅酸
【解析】
(1)陶瓷、玻璃、水泥都是硅酸盐材料,生石灰是氧化钙,不属于硅酸盐,答案选D。
(2)二氧化硅是酸性氧化物,与碱反应生成盐和水,与氢氧化钠溶液反应的化学方程式为:
。
(3)硅酸钠是矿物胶,不燃烧,而将硅酸钠浸泡棉花就阻隔了棉花与空气中氧气的直接接触,可用作防
火剂的原料;普通玻璃坩埚、石英玻璃坩埚都含有二氧化硅,能够与纯碱反应,氧化铝与纯碱能够发生反
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司应(生成偏铝酸钠和二氧化碳),铁和碳酸钠在高温下不会反应,所以高温熔融纯碱时可选用的是铁坩埚。
(4)氧化剂具有氧化性,化合价降低,反应中硅元素化合价降低,因此氧化剂是二氧化硅。
(5)证明酸性:HNO>H CO>H SiO,试剂A、B、C分别为稀硝酸、碳酸钠和硅酸钠溶液;试管中发生
3 2 3 2 3
反应的离子方程式为: ;有同学认为此实验不能说明酸性强弱,原因是硝酸
具有挥发性,也会和硅酸钠反应生成硅酸。
学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司学学学学 科科科科 网网网网 (((( 北北北北 京京京京 )))) 股股股股 份份份份 有有有有 限限限限 公公公公 司司司司