文档内容
下学期期末测试卷 02
高二化学 B. 属于醛类,官能团为—CHO
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考
证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动, C. 的名称为2,3,4-三甲基-2-乙基戊烷
用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:人教2019选择性必修三全册。
5.考试结束后,将本试卷和答题卡一并交回。
第Ⅰ卷
D.β -月桂烯的结构简式为 ,该物质与等物质的量的溴发生加成反应的产物(不考虑
一、选择题:本题共16小题,1至10题,每小题2分,共20分;11至16题,每小题4分,共24分。选择
题总分共44分。在每小题给出的四个选项中,均只有一项符合题目要求。 立体异构)理论上最多有4种
1、新冠肺炎疫情出现以来,一系列举措体现了中国力量。在各种防护防控措施中,化学知识起了重要作用, 5、氧化2.12g有机物X的蒸汽,生成了7.04g二氧化碳和1.80g水,通过仪器分析得知X的相对分子质量为
下列有关说法正确的是 106,用核磁共振氢谱仪测出X的核磁共振氢谱中有2组峰,其峰面积之比为2:3,用红外光谱仪测得X分
A.过氧化氢、乙醇、过氧乙酸等消毒液均可以将病毒氧化而达到消毒目的 子的红外光谱如图所示,下列说法错误的是
B.“84”消毒液是以NaClO为有效成分的消毒液,与医用酒精混合可以提升消毒效果
C.用药皂洗手能有效防止病毒传染,药皂中的苯酚能杀菌消毒。
D.医用防护服的核心材料是微孔聚四氟乙烯薄膜,其单体四氟乙烯属于烯烃
2、下列有关化学用语表示正确的是
A.乙炔的结构简式:(CH) B.2−甲基−2−丁醇的分子式:C H O
2 5 12
C.对硝基甲苯的结构简式 D.甲醛的电子式:
A、上述测X的相对分子质量的方法称为质谱法
B、X的结构简式为
C、X的红外光谱测定含有苯环,属于苯的同系物
D、Y是X的同分异构体,符合①属于芳香烃②苯环上的一氯代物有三种这两个条件的Y的结构简式有三种
6、下列各反应中属于氧化反应的是
3、“碧玉妆成一树高,万条垂下绿丝绦。不知细叶谁裁出,二月春风似剪刀。”《咏柳》名句赋物入妙。
下列有关说法中错误的是
A.玉石是珍贵的无机矿物材料 B.柳叶的主要成分可表示为(C H O)
6 10 5 n
① +15O 12CO+6H O
2 2 2
C.制造剪刀的材料钢铁是使用最广泛的金属材料 D.柳树皮加工处理后的纤维产品是合成纤维
4、下列叙述正确的是
A. 与 含有相同的官能团,互为同系物
② CH-CH-OH
3 2验证乙醇分子中的氢与水分 金属钠与乙醇和水分别反应,观察钠浮在液面,还是沉在
D
子中的氢的活性 底部
③2CH=CH +O
2 2 2
10、法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是
④CHCH+Cl CHCHCl+HCl
3 3 2 3 2
A.①② B.①③ C.②③ D.②④
A.该分子中N、O、F的第一电离能大小顺序为F>N>O
7、新冠肺炎病毒疫情爆发以来,我国科学家、医务工作者一直奋战在第一线,攻坚克难,成功研制出多种
B.该分子中C—N键的键能大于C—F键的键能
抑制新冠病毒药物,应用于临床,为战胜疫情立下赫赫战功。我们从化学的角度分析药物的结构,探究其
C.该分子中σ键与π键数目之比为7:2
性质,以此向战疫英雄致敬。2020年2月4日,中国工程院院士李兰娟团队发布最新研究成果:盐酸阿比
D.该分子中存在手性碳原子
多尔在体外细胞实验中能有效抑制冠状病毒。盐酸阿比多尔的结构简式如图所示,下列有关该有机物的说
11、下列实验能达到实验目的且操作正确的是
法不正确的是
A B C D
蒸发浓缩氯
用乙醇萃取碘水中 检验淀粉水解生成了葡 测定锌与稀硫酸反应速
化铵溶液析
的I 萄糖 率(计时器未画出)
出晶体 2
A.该有机物能与FeCl 溶液发生显色反应
3
B.能够使酸性高锰酸钾溶液褪色
C.能与NaOH溶液发生水解反应
D.1mol该有机物最多与8molH 发生加成反应
2
8、2020年3月24日,中国工程院院士、天津中医药大学校长张伯礼表示,中成药连花清瘟胶囊对于治疗
轻型和普通型的新冠肺炎有确切的疗效。其有效成分绿原酸的结构简式如图,下列有关绿原酸说法正确的
是
12、55.某DNA分子的片段如图所示。下列关于该片段的说法错误的是
A.最多有7个碳原子共面 B.1mol绿原酸可消耗7mol NaOH
C.不能与NaHCO 反应产生CO D.能发生加成、取代、加聚、缩聚反应
3 2
9、下列操作可以达到实验目的是
选项 实验目的 实验操作
验证乙炔能被酸性高锰酸钾 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶
A
溶液氧化 液,观察溶液是否褪色
B 除去苯中少量的苯酚 加入过量溴水,振荡、静置、分液
除去乙酸乙酯中混有的少量 加入足量饱和NaCO 溶液,振荡,静置,分液,取出上
C 2 3
乙酸 层液体A.氢键的强度:①>②
B.该片段中所有参与形成氢键的原子都共平面
C.该片段在一定条件下可发生水解反应
D.胞嘧啶与鸟嘌呤分子中酰胺基的化学活性并不完全相同
13、N 为阿伏加德罗常数的值,下列说法正确的是
A
A.60g NaHSO 固体中含有H+的数目为0.5N
4 A
B.12g金刚石中含有碳碳单键的数目为2N
A
C.1.0mol Cl 与1.0mol CH 在光照下反应,生成CHCl的分子数为N
2 4 3 A
D.0.1mol环氧乙烷( )中含有σ键的数目为0.3N
A
14、Ni可活化C H 放出CH,其反应历程如图所示:
2 6 4
下列关于活化历程的说法错误的是( )
A.决速步骤:中间体2→中间体3
B.总反应为Ni+C H→NiCH+CH
2 6 2 4
C.Ni—H键的形成有利于氢原子的迁移
D.涉及非极性键的断裂和生成
15、新冠肺炎病毒疫情爆发以来,我国科学家、医务工作者一直奋战在第一线,攻坚克难,成功研制出多
种抑制新冠病毒药物,应用于临床,为战胜疫情立下赫赫战功。我们从化学的角度分析药物的结构,探究
其性质,以此向战疫英雄致敬。钟南山院士指出,实验证明中药连花清瘟胶囊对治疗新冠肺炎有明显疗效,
G是其有效药理成分之一,存在如图转化关系:
下列有关说法正确的是
A.若在反应中,G与水按1:1发生反应,则G的分子式为C H O
16 20 10
B.化合物Ⅰ分子中碳原子均采取sp3杂化
C.化合物Ⅱ中所有碳原子可能都共面
D.化合物G、Ⅰ、Ⅱ均能发生氧化反应、取代反应、消去反应
16、有一种有机物的键线式酷似牛,故称为牛式二烯炔醇(cowenynenynol)。下列有关说法不正确的是A.牛式二烯炔醇含有3种官能团,可以属于不饱和醇类
B.牛式二烯炔醇含有3个手性碳原子,与氢气完全加成反应后仍含有5个手性碳原子
C.1mol牛式二烯炔醇最多可与6molH 发生加成反应
2
D.牛式二烯炔醇既能发生消去反应,又能发生催化氧化反应
第Ⅱ卷
二、非选择题,共4题,每题14分,共56分。
17、实验室制备苯乙酮的化学方程式为: +(CH CO) O +CH COOH。制备过
3 2 3
程中还有CHCOOH+AlCl →CHCOOAlCl +HCl↑ 等副反应。主要实验装置和步骤如图:
3 3 3 2
(I)合成:
在三颈烧瓶中加入20g无水AlCl 和30mL无水苯。边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,
3
使反应液缓缓回流。滴加完毕后加热回流1小时,形成黑黄色液体。
(Ⅱ)分离与提纯:
将冷却后的反应瓶置于冰水浴中,加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙
醚萃取,与有机相合并,有机相用10%NaOH溶液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,
弃去无机层,有机层用MgSO 干燥,得到苯乙酮粗产品。
4
回答下列问题:
(1)仪器a的名称:___;使用恒压滴定漏斗的优点是:___。
(2)球形干燥管的作用是___。
(3)若将乙酸酐和苯的混合液一次性倒入三颈烧瓶,可能导致__。
A.反应太剧烈 B.液体太多搅不动 C.反应变缓慢 D.副产物增多
(4)分离和提纯操作中是否可改用乙醇萃取?___(填“是”或“否”),原因是___。
(5)分液漏斗使用前须___并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振荡并__后,将分液漏斗置
于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先___,然后打开活塞放出下层液体,上层液体
从上口倒出。
(6)已知常压下:
熔点/℃ 沸点/℃
苯 5.5 80.1
乙醚 -116.3 34.6
苯乙酮 19.6 202
则从粗产品中提纯苯乙酮使用的操作是___;为了收集纯净的苯乙酮馏分,分离苯乙酮应使用下面的图___
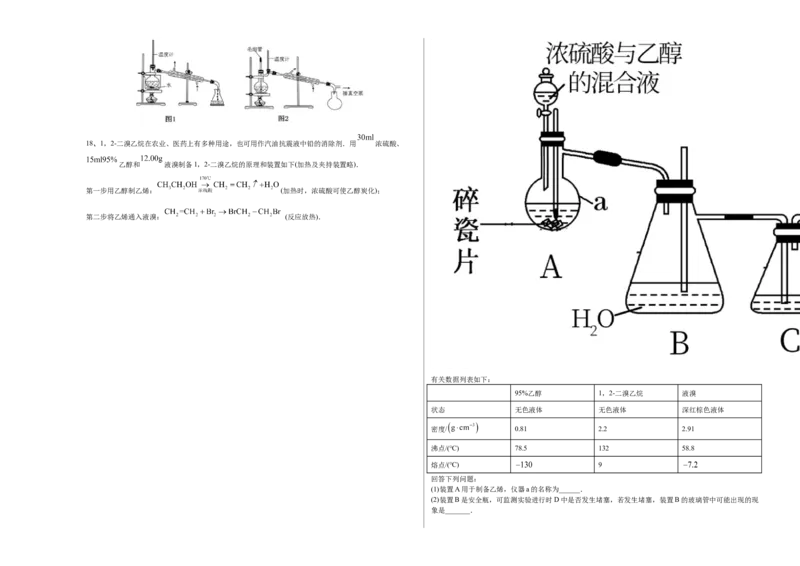
装置。18、1,2-二溴乙烷在农业、医药上有多种用途,也可用作汽油抗震液中铅的消除剂.用 浓硫酸、
乙醇和 液溴制备1,2-二溴乙烷的原理和装置如下(加热及夹持装置略).
第一步用乙醇制乙烯: (加热时,浓硫酸可使乙醇炭化);
第二步将乙烯通入液溴: (反应放热).
有关数据列表如下:
95%乙醇 1,2-二溴乙烷 液溴
状态 无色液体 无色液体 深红棕色液体
密度/ 0.81 2.2 2.91
沸点/(℃) 78.5 132 58.8
熔点/(℃) 9
回答下列问题:
(1)装置A用于制备乙烯,仪器a的名称为______.
(2)装置B是安全瓶,可监测实验进行时D中是否发生堵塞,若发生堵塞,装置B的玻璃管中可能出现的现
象是_______.(3)装置C中盛装的是 溶液,若没有装置C,装置D中还可能发生反应的化学方程式为____;装置C
与D之间可增加一个盛装品红溶液的试剂瓶,目的是_________.
(4)装置D中试管和烧杯内水的作用分别是______、_________.
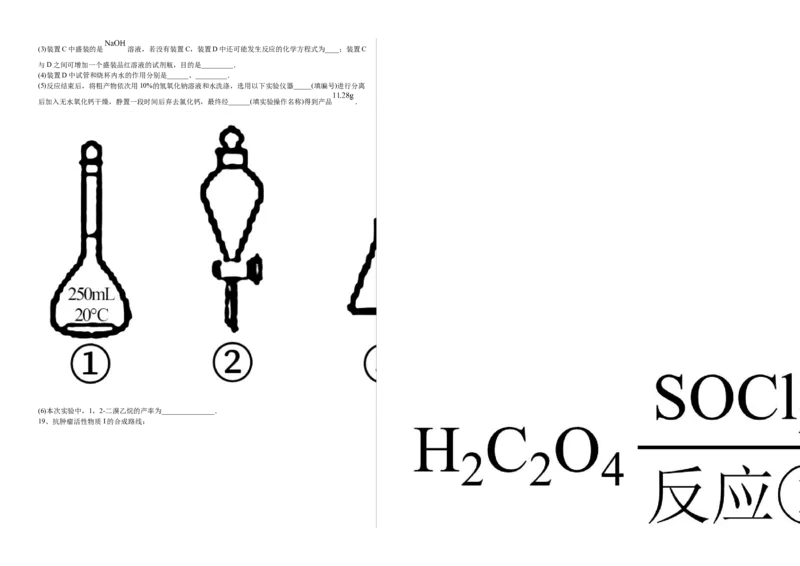
(5)反应结束后,将粗产物依次用10%的氢氧化钠溶液和水洗涤,选用以下实验仪器_____(填编号)进行分离
后加入无水氧化钙干燥,静置一段时间后弃去氯化钙,最终经______(填实验操作名称)得到产品 .
(6)本次实验中,1,2-二溴乙烷的产率为_______________.
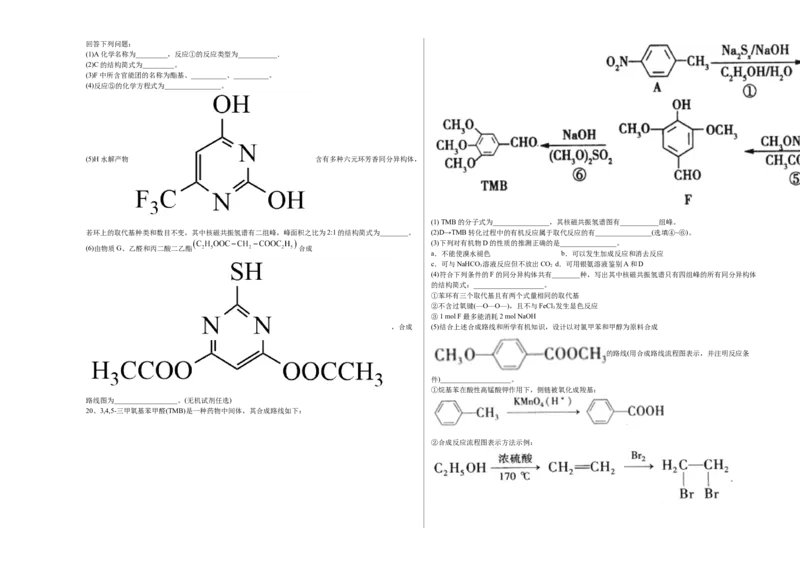
19、抗肿瘤活性物质I的合成路线:回答下列问题:
(1)A化学名称为_________,反应①的反应类型为___________.
(2)C的结构简式为_________。
(3)F中所含官能团的名称为酯基、__________、__________。
(4)反应⑤的化学方程式为________________。
(5)H水解产物 含有多种六元环芳香同分异构体,
(1) TMB的分子式为________________,其核磁共振氢谱图有___________组峰。
若环上的取代基种类和数目不变,其中核磁共振氢谱有二组峰,峰面积之比为2:1的结构简式为________。 (2)D→TMB转化过程中的有机反应属于取代反应的有________________(选填④~⑥)。
(3)下列对有机物D的性质的推测正确的是________________。
(6)由物质G、乙醛和丙二酸二乙酯 合成
a.不能使溴水褪色 b.可以发生加成反应和消去反应
c.可与NaHCO 溶液反应但不放出CO d.可用银氨溶液鉴别A和D
3 2
(4)符合下列条件的F的同分异构体共有________种,写出其中核磁共振氢谱只有四组峰的所有同分异构体
的结构简式:____________________。
①苯环有三个取代基且有两个式量相同的取代基
②不含过氧键(—O—O—),且不与FeCl 发生显色反应
3
③1 mol F最多能消耗2 mol NaOH
,合成 (5)结合上述合成路线和所学有机知识,设计以对氯甲苯和甲醇为原料合成
的路线(用合成路线流程图表示,并注明反应条
件)____________________。
①烷基苯在酸性高锰酸钾作用下,侧链被氧化成羧基:
路线图为__________________。(无机试剂任选)
20、3,4,5-三甲氧基苯甲醛(TMB)是一种药物中间体,其合成路线如下:
②合成反应流程图表示方法示例:
。