文档内容
2025—2026 学年第一学期期末考试
高二年级化学试卷
考试时间:75 分钟 试卷满分:100 分
一、选择题:(本题共 14 小题,每小题 3 分,满分 42 分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1. 中华文化博大精深,源远流长。下列诗句或成语不涉及放热反应的是
A. 烈火焚烧若等闲 B. 爆竹声中一岁除 C. 蜡炬成灰泪始干 D. 铁杵磨成针
2. 已知:① ;
② 。
转化为 的热量变化为
A. 放出 B. 吸收 C. 放出 D. 吸收
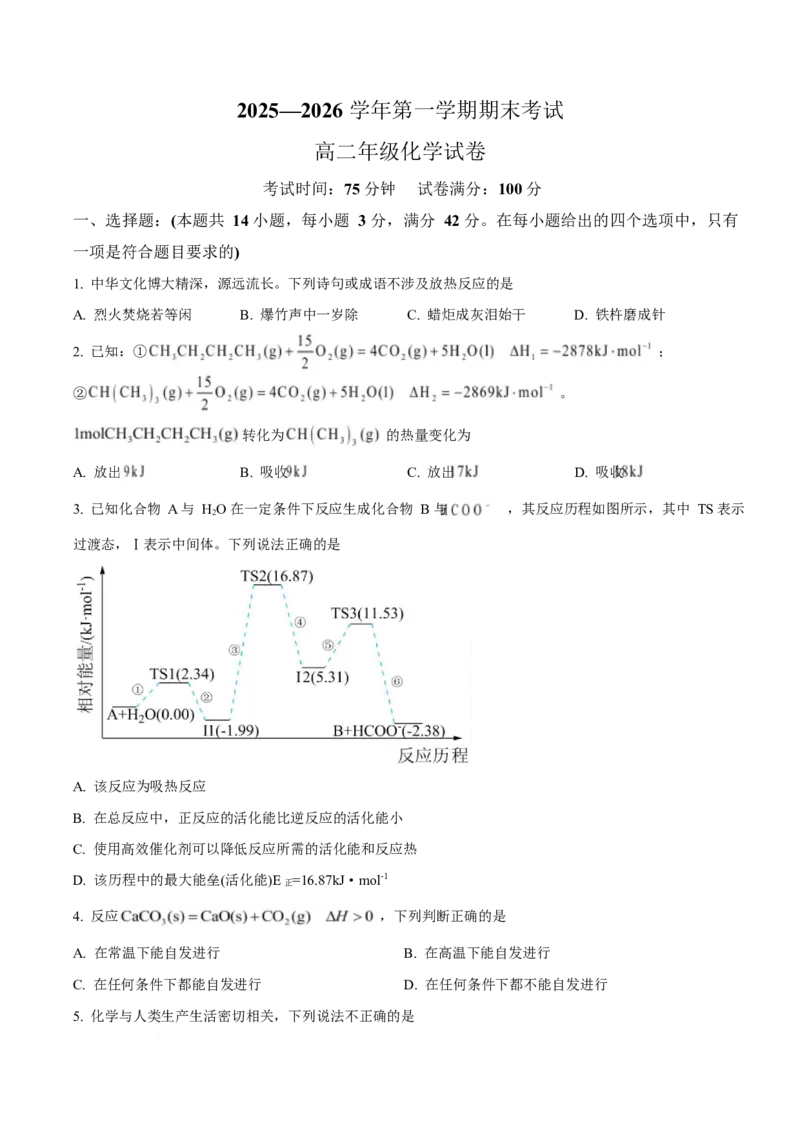
3. 已知化合物 A 与 HO 在一定条件下反应生成化合物 B 与 ,其反应历程如图所示,其中 TS 表示
2
过渡态,Ⅰ表示中间体。下列说法正确的是
A. 该反应为吸热反应
B. 在总反应中,正反应的活化能比逆反应的活化能小
C. 使用高效催化剂可以降低反应所需的活化能和反应热
D. 该历程中的最大能垒(活化能)E =16.87kJ·mol-1
正
4. 反应 ,下列判断正确的是
A. 在常温下能自发进行 B. 在高温下能自发进行
C. 在任何条件下都能自发进行 D. 在任何条件下都不能自发进行
5. 化学与人类生产生活密切相关,下列说法不正确的是A. 神舟十八号的主电源储能电池由镉镍电池更改为锂离子电池,锂离子电池属于二次电池,具有质量小、
体积小、储存和输出能量大等特点
B. 神舟十八号采用的燃料之一为液态的偏二甲肼(造),完全燃烧放出大量的热,只生成二氧化碳、氮气和
水,具有产物清洁无污染等优点
C. 使用干冰进行人工降雨,固态干冰升华为 是吸热反应
D. 升温,能增大单位体积活化分子百分数,所以反应速率增大
6. 下列用于解释事实的化学用语书写不正确的是
A. 电解精炼铜的阴极反应:
B. 用 溶液清洗油污的原因:
C. 用饱和 溶液处理锅炉水垢中的 :
D. 将纯水加热至较高温度,水的 :
7. 《自然》发表的关于乳酸的研究认为,乳酸是经血液循环转换能量的基本成员。常温下,乳酸(用 表
示)的 ,碳酸的 。下列说法正确的是
A. 乳酸酸性比碳酸弱 B. 乳酸溶液的
C. 乳酸溶液中: D. 稀释乳酸溶液,乳酸电离程度减小
8. 下列物质能促进水电离,且水溶液显碱性的是
A. B. C. D.
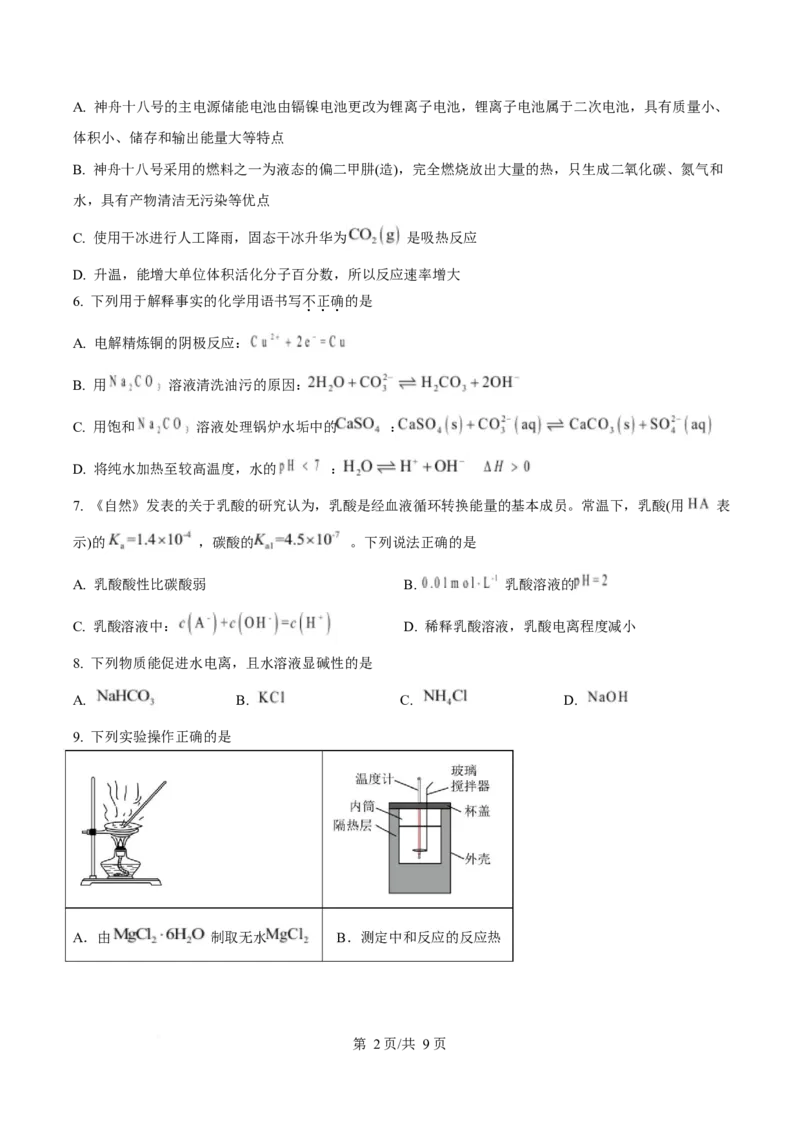
9. 下列实验操作正确的是
A.由 制取无水 B.测定中和反应的反应热
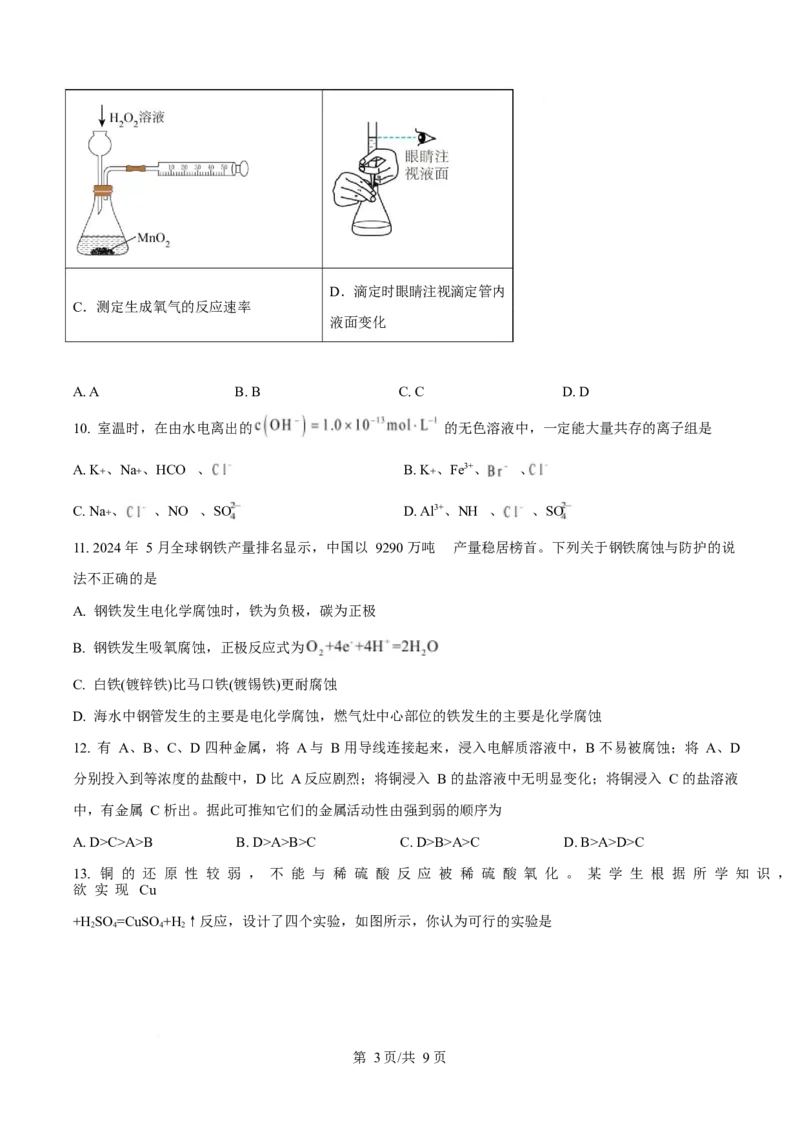
第 2页/共 9页D.滴定时眼睛注视滴定管内
C.测定生成氧气的反应速率
液面变化
A. A B. B C. C D. D
10. 室温时,在由水电离出的 的无色溶液中,一定能大量共存的离子组是
A. K+ 、Na+ 、HCO 、 B. K+ 、Fe3+、 、
C. Na+ 、 、NO 、SO D. Al3+、NH 、 、SO
11. 2024 年 5 月全球钢铁产量排名显示,中国以 9290 万吨 产量稳居榜首。下列关于钢铁腐蚀与防护的说
法不正确的是
A. 钢铁发生电化学腐蚀时,铁为负极,碳为正极
B. 钢铁发生吸氧腐蚀,正极反应式为
C. 白铁(镀锌铁)比马口铁(镀锡铁)更耐腐蚀
D. 海水中钢管发生的主要是电化学腐蚀,燃气灶中心部位的铁发生的主要是化学腐蚀
12. 有 A、B、C、D 四种金属,将 A 与 B 用导线连接起来,浸入电解质溶液中,B 不易被腐蚀;将 A、D
分别投入到等浓度的盐酸中,D 比 A 反应剧烈;将铜浸入 B 的盐溶液中无明显变化;将铜浸入 C 的盐溶液
中,有金属 C 析出。据此可推知它们的金属活动性由强到弱的顺序为
A. D>C>A>B B. D>A>B>C C. D>B>A>C D. B>A>D>C
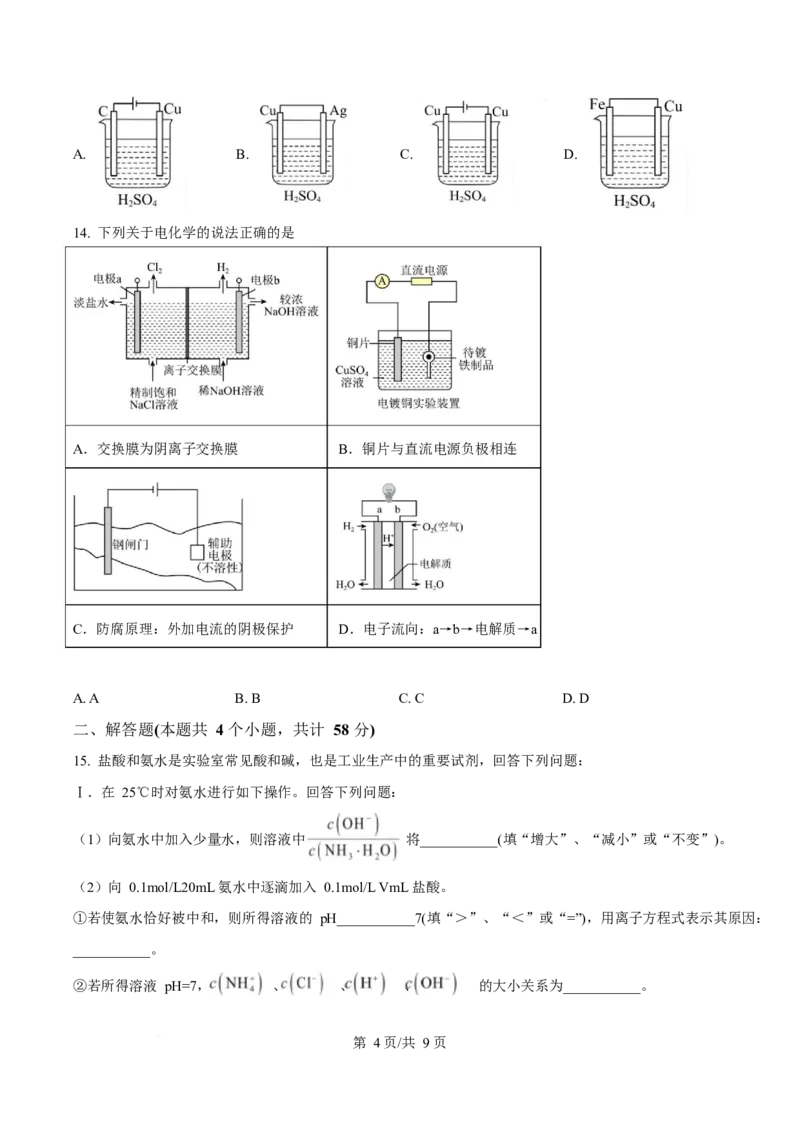
13. 铜 的 还 原 性 较 弱 , 不 能 与 稀 硫 酸 反 应 被 稀 硫 酸 氧 化 。 某 学 生 根 据 所 学 知 识 ,
欲 实 现 Cu
+H SO =CuSO+H ↑反应,设计了四个实验,如图所示,你认为可行的实验是
2 4 4 2
第 3页/共 9页A. B. C. D.
14. 下列关于电化学的说法正确的是
A.交换膜为阴离子交换膜 B.铜片与直流电源负极相连
C.防腐原理:外加电流的阴极保护 D.电子流向:a→b→电解质→a
A. A B. B C. C D. D
二、解答题(本题共 4 个小题,共计 58 分)
15. 盐酸和氨水是实验室常见酸和碱,也是工业生产中的重要试剂,回答下列问题:
Ⅰ.在 25℃时对氨水进行如下操作。回答下列问题:
(1)向氨水中加入少量水,则溶液中 将___________(填“增大”、“减小”或“不变”)。
(2)向 0.1mol/L20mL 氨水中逐滴加入 0.1mol/L VmL 盐酸。
①若使氨水恰好被中和,则所得溶液的 pH___________7(填“>”、“<”或“=”),用离子方程式表示其原因:
___________。
②若所得溶液 pH=7, 、 、 、 的大小关系为___________。
第 4页/共 9页(3)向 CuSO 溶液中滴加氨水产生蓝色沉淀,若所得溶液 pH=10,已知 ,
4
则溶液中 c(Cu2+)=___________mol/L。
Ⅱ.某课外兴趣小组用 0.1000mol/L 的 NaOH 标准溶液滴定未知浓度的盐酸溶液,请完成以下问题。
(4)该小组同学选用酚酞做指示剂,滴定终点的现象为___________。
(5)该小组学生某 3 次实验的有关数据分别记录如下表:
0.1000mol/LNaOH 的体积(mL)
待测 HCl 溶液的体
积 滴定次数
/mL
滴定前刻度 滴定后刻度
第一次 25.00 2.00 26.90
第二次 25 00 0.50 30.50
第三次 25.00 0.20 25.30
依据上表数据列式计算该 HCl 溶液的物质的量浓度为___________mol/L。
(6)下列操作中可能使测定结果偏低的是___________(填字母)。
a.酸式滴定管未润洗就直接注入待测液 HCl 溶液
b.滴定前盛放 HCl 溶液的锥形瓶用蒸馏水洗净后没有干燥
c.碱式滴定管尖嘴部分在滴定前有气泡,滴定后气泡消失
d.读取 NaOH 标准液时,开始仰视读数,滴定结束时俯视读数
16. 孔雀石的主要成分为 ,还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验
室以孔雀石为原料制备 晶体的流程图:
(1)试剂 A 的化学式是___________;操作Ⅰ的名称是___________。
(2)加快浸泡速率的方法有(任写一条):___________。
(3)使用试剂 B 的目的是将溶液中的 Fe2+转化为 Fe3+,试剂 B 最好选用___________。
(4)已知:
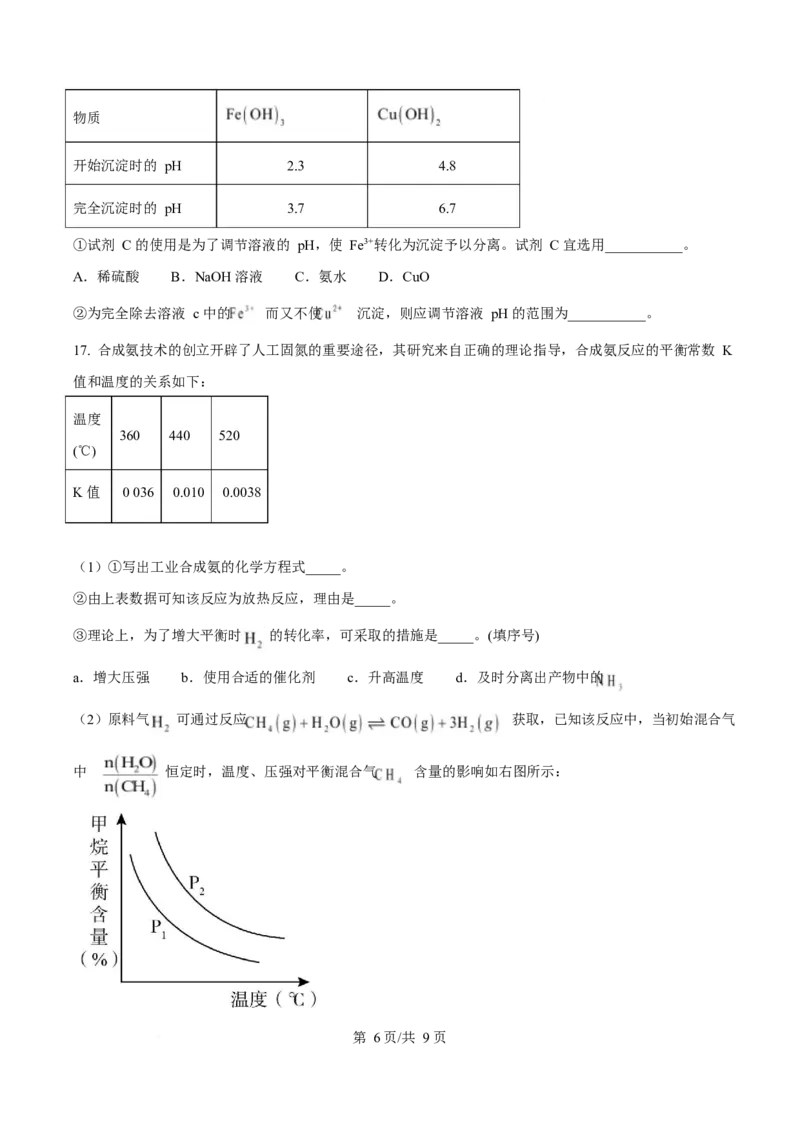
第 5页/共 9页物质
开始沉淀时的 pH 2.3 4.8
完全沉淀时的 pH 3.7 6.7
①试剂 C 的使用是为了调节溶液的 pH,使 Fe3+转化为沉淀予以分离。试剂 C 宜选用___________。
A.稀硫酸 B.NaOH 溶液 C.氨水 D.CuO
②为完全除去溶液 c 中的 而又不使 沉淀,则应调节溶液 pH 的范围为___________。
17. 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数 K
值和温度的关系如下:
温度
360 440 520
(℃)
K 值 0 036 0.010 0.0038
(1)①写出工业合成氨的化学方程式_____。
②由上表数据可知该反应为放热反应,理由是_____。
③理论上,为了增大平衡时 的转化率,可采取的措施是_____。(填序号)
a.增大压强 b.使用合适的催化剂 c.升高温度 d.及时分离出产物中的
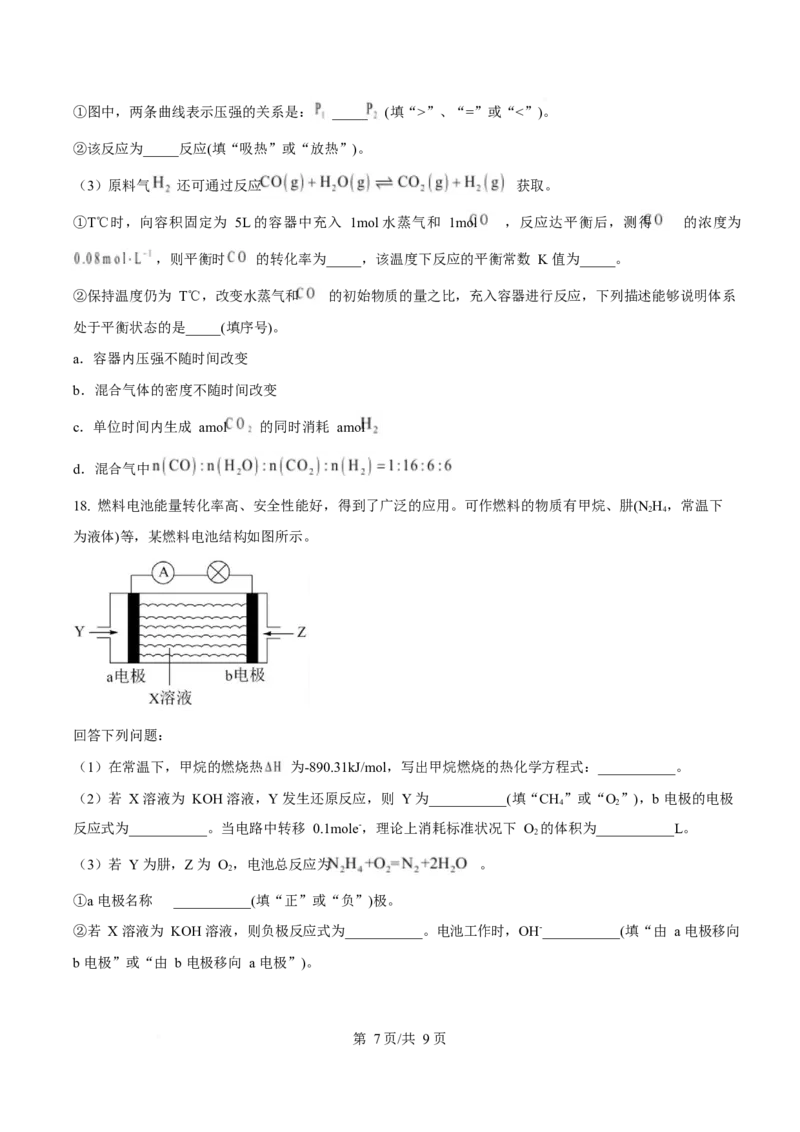
(2)原料气 可通过反应 获取,已知该反应中,当初始混合气
中 恒定时,温度、压强对平衡混合气 含量的影响如右图所示:
第 6页/共 9页①图中,两条曲线表示压强的关系是: _____ (填“>”、“=”或“<”)。
②该反应为_____反应(填“吸热”或“放热”)。
(3)原料气 还可通过反应 获取。
①T℃时,向容积固定为 5L 的容器中充入 1mol 水蒸气和 1mol ,反应达平衡后,测得 的浓度为
,则平衡时 的转化率为_____,该温度下反应的平衡常数 K 值为_____。
②保持温度仍为 T℃,改变水蒸气和 的初始物质的量之比,充入容器进行反应,下列描述能够说明体系
处于平衡状态的是_____(填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成 amol 的同时消耗 amol
d.混合气中
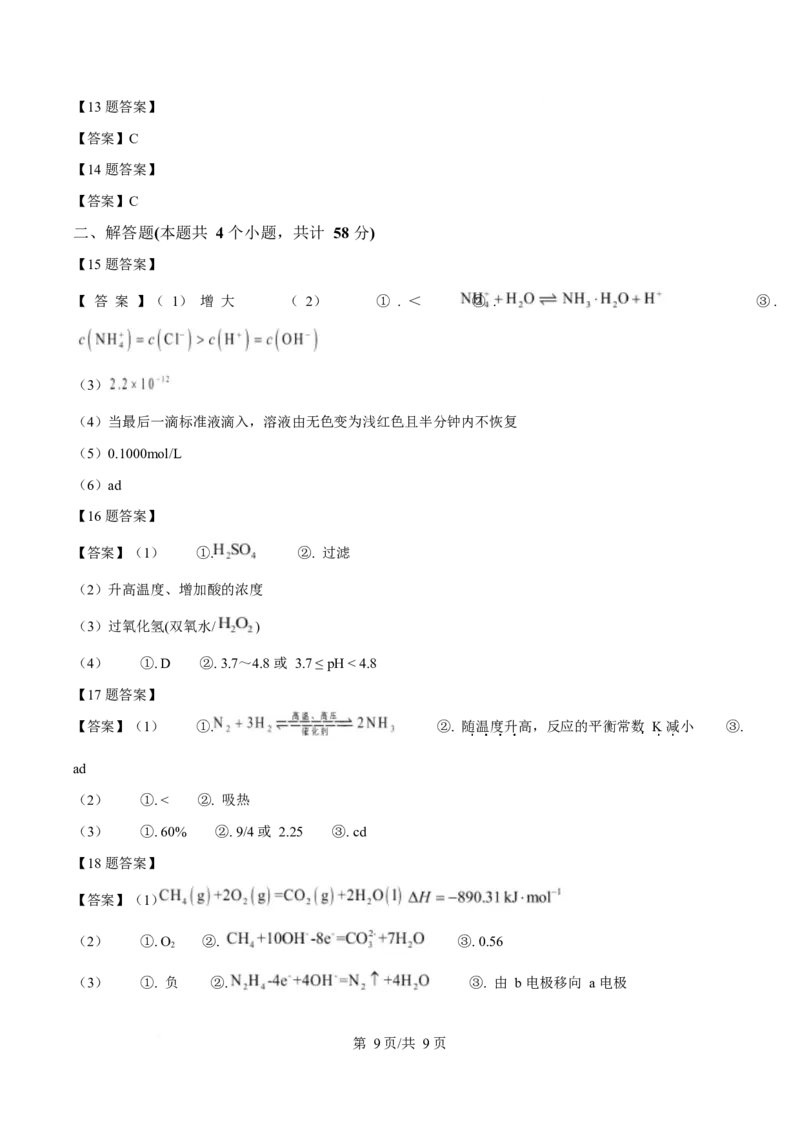
18. 燃料电池能量转化率高、安全性能好,得到了广泛的应用。可作燃料的物质有甲烷、肼(N H,常温下
2 4
为液体)等,某燃料电池结构如图所示。
回答下列问题:
(1)在常温下,甲烷的燃烧热 为-890.31kJ/mol,写出甲烷燃烧的热化学方程式:___________。
(2)若 X 溶液为 KOH 溶液,Y 发生还原反应,则 Y 为___________(填“CH”或“O”),b 电极的电极
4 2
反应式为___________。当电路中转移 0.1mole-,理论上消耗标准状况下 O 的体积为___________L。
2
(3)若 Y 为肼,Z 为 O,电池总反应为 。
2
①a 电极名称 ___________(填“正”或“负”)极。
②若 X 溶液为 KOH 溶液,则负极反应式为___________。电池工作时,OH-___________(填“由 a 电极移向
b 电极”或“由 b 电极移向 a 电极”)。
第 7页/共 9页2025—2026 学年第一学期期末考试
高二年级化学试卷
考试时间:75 分钟 试卷满分:100 分
一、选择题:(本题共 14 小题,每小题 3 分,满分 42 分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
【1 题答案】
【答案】D
【2 题答案】
【答案】A
【3 题答案】
【答案】B
【4 题答案】
【答案】B
【5 题答案】
【答案】C
【6 题答案】
【答案】B
【7 题答案】
【答案】C
【8 题答案】
【答案】A
【9 题答案】
【答案】B
【10 题答案】
【答案】C
【11 题答案】
【答案】B
【12 题答案】
【答案】B
第 8页/共 9页【13 题答案】
【答案】C
【14 题答案】
【答案】C
二、解答题(本题共 4 个小题,共计 58 分)
【15 题答案】
【 答 案 】( 1) 增 大 ( 2) ① . < ② . ③ .
(3)
(4)当最后一滴标准液滴入,溶液由无色变为浅红色且半分钟内不恢复
(5)0.1000mol/L
(6)ad
【16 题答案】
【答案】(1) ①. ②. 过滤
(2)升高温度、增加酸的浓度
(3)过氧化氢(双氧水/ )
(4) ①. D ②. 3.7~4.8 或 3.7 ≤ pH < 4.8
【17 题答案】
【答案】(1) ①. ②. 随温度升高,反应的平衡常数 K 减小 ③.
ad
(2) ①. < ②. 吸热
(3) ①. 60% ②. 9/4 或 2.25 ③. cd
【18 题答案】
【答案】(1)
(2) ①. O ②. ③. 0.56
2
(3) ①. 负 ②. ③. 由 b 电极移向 a 电极
第 9页/共 9页