文档内容
机密★启用前
2025年4月山东师大附中高二阶段性检测试题
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对分子质量:H 1 C 12 O 16 Ti 48
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
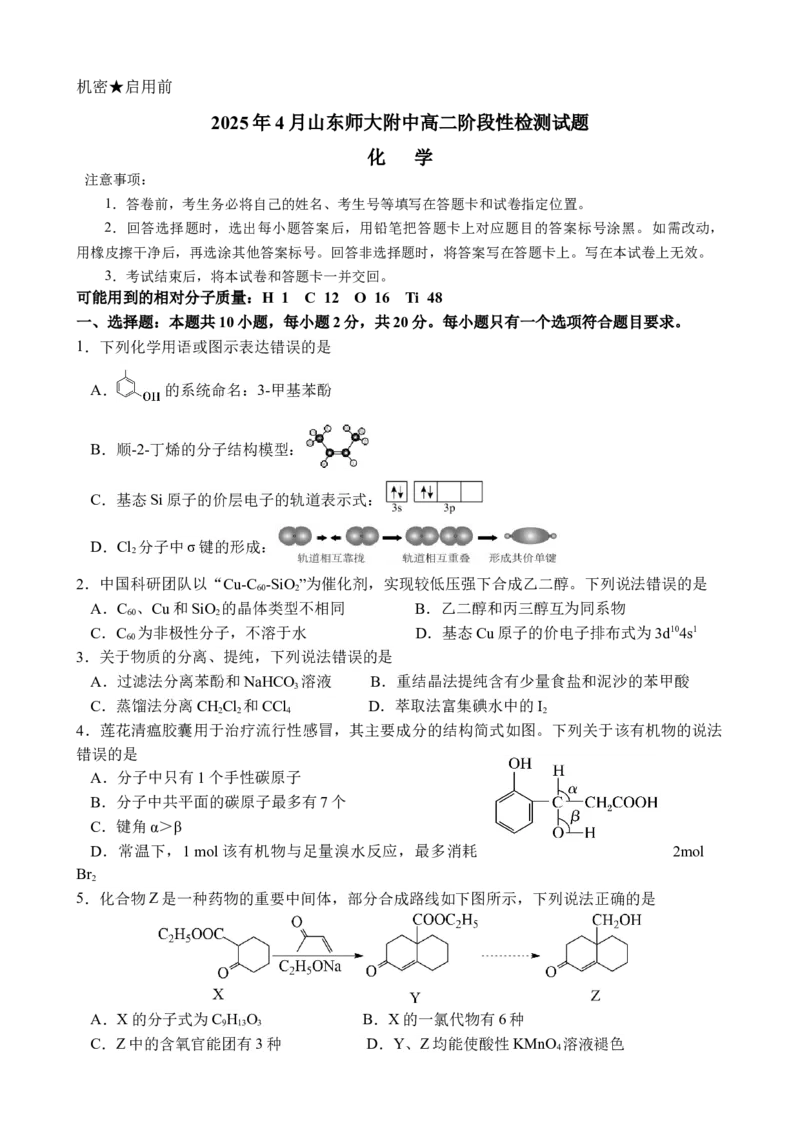
1.下列化学用语或图示表达错误的是
A. 的系统命名:3-甲基苯酚
B.顺-2-丁烯的分子结构模型:
C.基态Si原子的价层电子的轨道表示式:
D.Cl 分子中σ键的形成:
2
2.中国科研团队以“Cu-C -SiO ”为催化剂,实现较低压强下合成乙二醇。下列说法错误的是
60 2
A.C 、Cu和SiO 的晶体类型不相同 B.乙二醇和丙三醇互为同系物
60 2
C.C 为非极性分子,不溶于水 D.基态Cu原子的价电子排布式为3d104s1
60
3.关于物质的分离、提纯,下列说法错误的是
A.过滤法分离苯酚和NaHCO 溶液 B.重结晶法提纯含有少量食盐和泥沙的苯甲酸
3
C.蒸馏法分离CH Cl 和CCl D.萃取法富集碘水中的I
2 2 4 2
4.莲花清瘟胶囊用于治疗流行性感冒,其主要成分的结构简式如图。下列关于该有机物的说法
错误的是
A.分子中只有1个手性碳原子
B.分子中共平面的碳原子最多有7个
C.键角α>β
D.常温下,1 mol该有机物与足量溴水反应,最多消耗 2mol
Br
2
5.化合物Z是一种药物的重要中间体,部分合成路线如下图所示,下列说法正确的是
A.X的分子式为C H O B.X的一氯代物有6种
9 13 3
C.Z中的含氧官能团有3种 D.Y、Z均能使酸性KMnO 溶液褪色
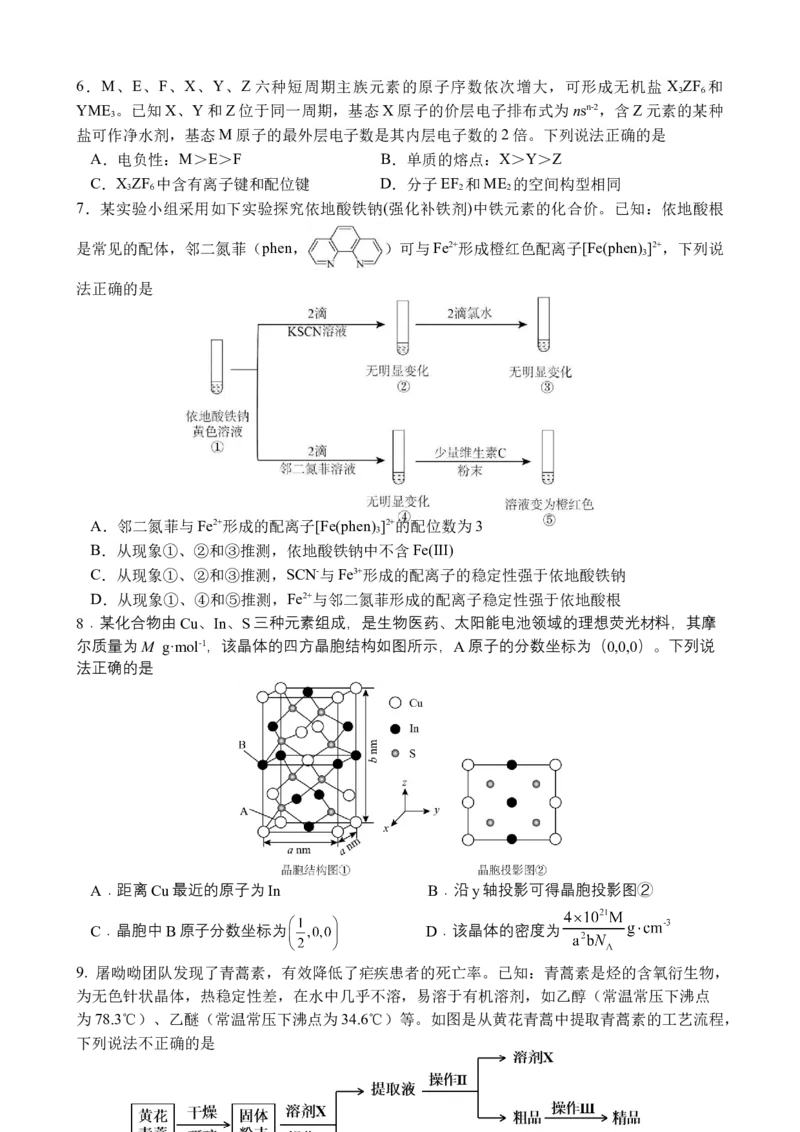
46.M、E、F、X、Y、Z六种短周期主族元素的原子序数依次增大,可形成无机盐 X ZF 和
3 6
YME 。已知X、Y和Z位于同一周期,基态X原子的价层电子排布式为nsn-2,含Z元素的某种
3
盐可作净水剂,基态M原子的最外层电子数是其内层电子数的2倍。下列说法正确的是
A.电负性:M>E>F B.单质的熔点:X>Y>Z
C.X ZF 中含有离子键和配位键 D.分子EF 和ME 的空间构型相同
3 6 2 2
7.某实验小组采用如下实验探究依地酸铁钠(强化补铁剂)中铁元素的化合价。已知:依地酸根
是常见的配体,邻二氮菲(phen, )可与Fe2+形成橙红色配离子[Fe(phen) ]2+,下列说
3
法正确的是
A.邻二氮菲与Fe2+形成的配离子[Fe(phen) ]2+的配位数为3
3
B.从现象①、②和③推测,依地酸铁钠中不含Fe(Ⅲ)
C.从现象①、②和③推测,SCN-与Fe3+形成的配离子的稳定性强于依地酸铁钠
D.从现象①、④和⑤推测,Fe2+与邻二氮菲形成的配离子稳定性强于依地酸根
8.某化合物由Cu、In、S三种元素组成,是生物医药、太阳能电池领域的理想荧光材料,其摩
尔质量为M g·mol-1,该晶体的四方晶胞结构如图所示,A原子的分数坐标为(0,0,0)。下列说
法正确的是
A.距离Cu最近的原子为In B.沿y轴投影可得晶胞投影图②
C.晶胞中B原子分数坐标为 D.该晶体的密度为
9. 屠呦呦团队发现了青蒿素,有效降低了疟疾患者的死亡率。已知:青蒿素是烃的含氧衍生物,
为无色针状晶体,热稳定性差,在水中几乎不溶,易溶于有机溶剂,如乙醇(常温常压下沸点
为78.3℃)、乙醚(常温常压下沸点为34.6℃)等。如图是从黄花青蒿中提取青蒿素的工艺流程,
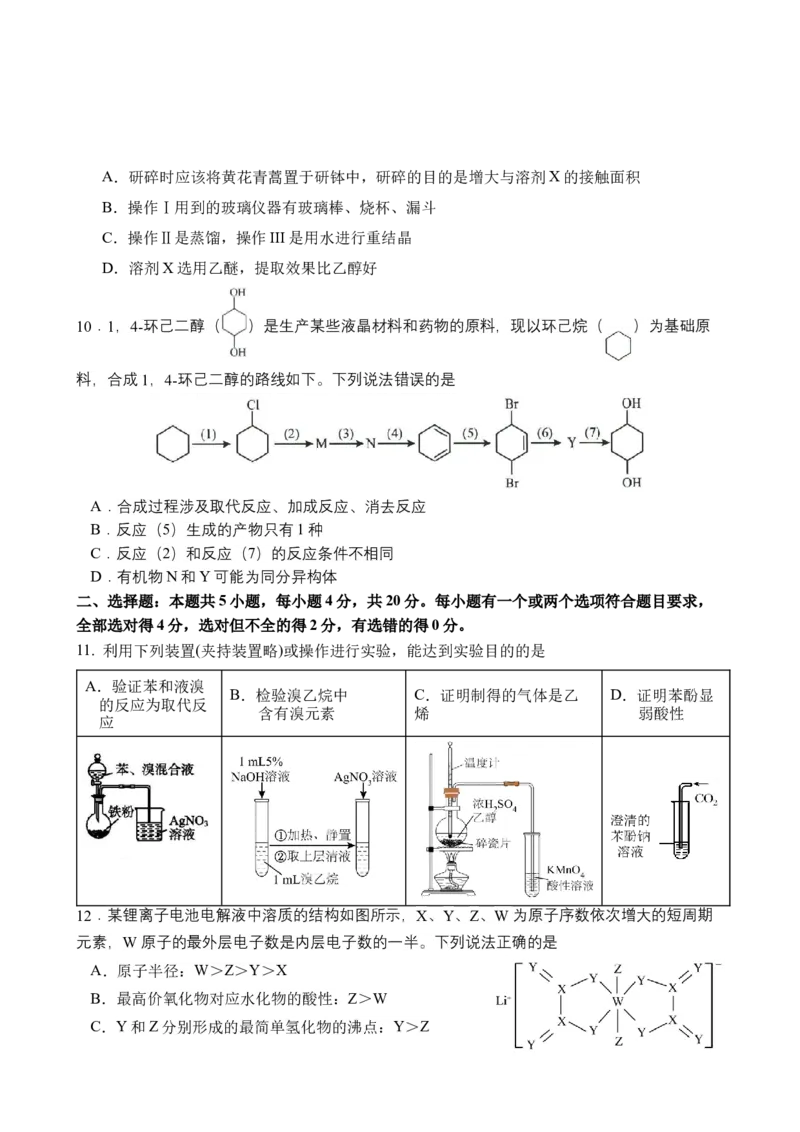
下列说法不正确的是A.研碎时应该将黄花青蒿置于研钵中,研碎的目的是增大与溶剂X的接触面积
B.操作Ⅰ用到的玻璃仪器有玻璃棒、烧杯、漏斗
C.操作Ⅱ是蒸馏,操作III是用水进行重结晶
D.溶剂X选用乙醚,提取效果比乙醇好
10.1,4-环己二醇( )是生产某些液晶材料和药物的原料,现以环己烷( )为基础原
料,合成1,4-环己二醇的路线如下。下列说法错误的是
A.合成过程涉及取代反应、加成反应、消去反应
B.反应(5)生成的产物只有1种
C.反应(2)和反应(7)的反应条件不相同
D.有机物N和Y可能为同分异构体
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,
全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 利用下列装置(夹持装置略)或操作进行实验,能达到实验目的的是
A.验证苯和液溴
B.检验溴乙烷中 C.证明制得的气体是乙 D.证明苯酚显
的反应为取代反
含有溴元素 烯 弱酸性
应
12.某锂离子电池电解液中溶质的结构如图所示,X、Y、Z、W为原子序数依次增大的短周期
元素,W原子的最外层电子数是内层电子数的一半。下列说法正确的是
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W
C.Y和Z分别形成的最简单氢化物的沸点:Y>ZD.基态W原子核外电子的空间运动状态有9种
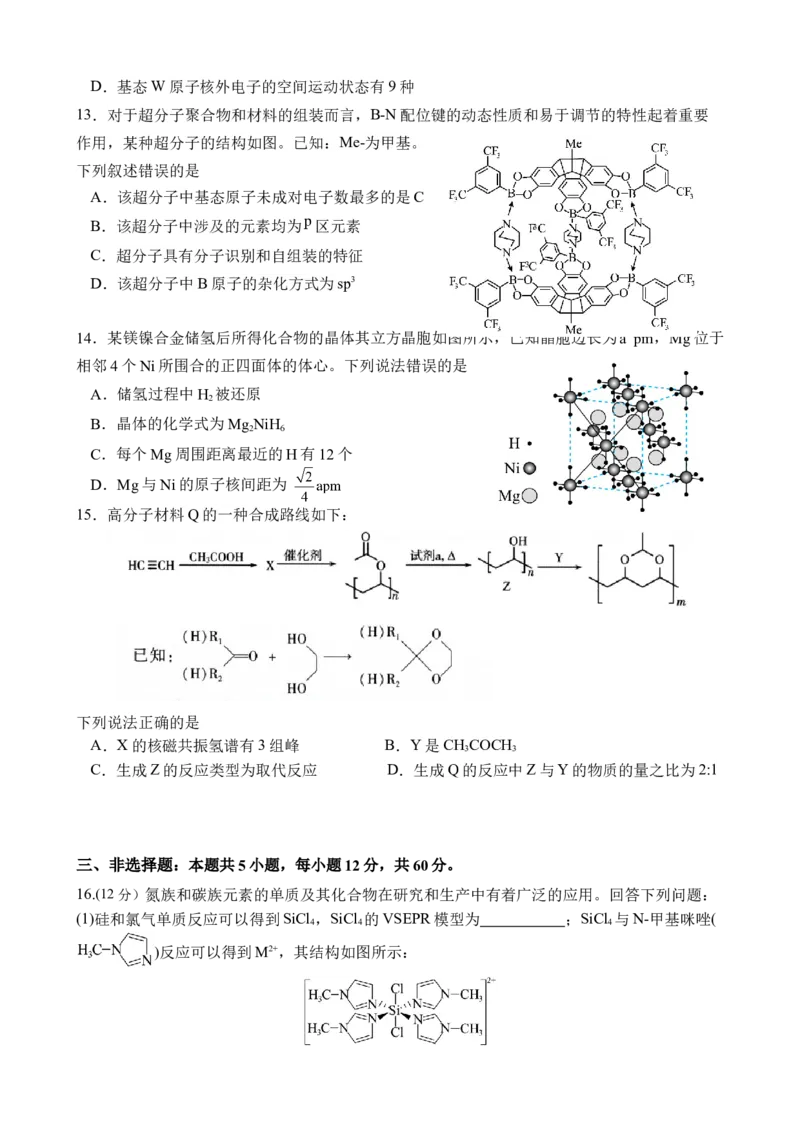
13.对于超分子聚合物和材料的组装而言,B-N配位键的动态性质和易于调节的特性起着重要
作用,某种超分子的结构如图。已知:Me-为甲基。
下列叙述错误的是
A.该超分子中基态原子未成对电子数最多的是C
B.该超分子中涉及的元素均为 区元素
3
C.超分子具有分子识别和自组装的特征
3
D.该超分子中B原子的杂化方式为sp3
14.某镁镍合金储氢后所得化合物的晶体其立方晶胞如图所示,已知晶胞边长为a pm,Mg位于
相邻4个Ni所围合的正四面体的体心。下列说法错误的是
A.储氢过程中H 被还原
2
B.晶体的化学式为Mg NiH
2 6
C.每个Mg周围距离最近的H有12个
D.Mg与Ni的原子核间距为
15.高分子材料Q的一种合成路线如下:
Z
Q
下列说法正确的是
A.X的核磁共振氢谱有3组峰 B.Y是CH COCH
3 3
C.生成Z的反应类型为取代反应 D.生成Q的反应中Z与Y的物质的量之比为2:1
三、非选择题:本题共5小题,每小题12分,共60分。
16.(12分)氮族和碳族元素的单质及其化合物在研究和生产中有着广泛的应用。回答下列问题:
(1)硅和氯气单质反应可以得到SiCl ,SiCl 的VSEPR模型为 ;SiCl 与N-甲基咪唑(
4 4 4
)反应可以得到M2+,其结构如图所示:1个M2+ 中含有 个 键,下列对M2+ 中心原子Si的杂化方式推断合理的是 (填标号)。
A.sp2 B. sp3 C.sp3d D.sp3d2
(2)锗及其化合物广泛应用于光电材料领域,基态锗原子核外电子占据的最高能级符号为 。
(3)纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是 。
(4)已知偏二甲肼[(CH ) NNH ]、肼(N H )均可做运载火箭的主体燃料, 前
3 2 2 2 4
者沸点为63.9℃,后者沸点为113.5℃。请分析二者沸点存在差异的主 要
原因 。
(5)N H 2+ 中所有原子共面,结构如右图所示,其中的大π键可表示为 。
4 6
(分子中的大 键可用符号 表示,其中m代表参与形成大 键的原 子
数,n代表参与形成大 键的电子数,如苯分子中的大 键可表示为 )
17.(12分)光电材料(KBe BO F 、CaTiO 等)是目前科学家特别关注的材料,在光、电、热等领
2 3 2 3
域有着独特的性质特征。回答下列问题:
(1)基态Ti原子的核外电子排布式为 。
(2)KBe BO F 的组成元素中,非金属元素的电负性由强到弱的顺序为 (填元素符号)。
2 3 2
(3) CaTiO 的晶胞结构如图(a)所示,与Ti4+最邻近的氧离子构成的几何图形为 。
3
(4)一种立方钙钛矿型结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH NH +,其晶
3 3
胞如图(b)所示,其中Pb2+与图(a)中 (填元素符号)的空间位置相同。CH NH +中,
3 3
存在的化学键有 (填标号)。 A.共价键 B.离子键 C.金属键 D.配位键 E. 氢键
(5)反型钙钛矿电池无需使用具有光催化活性的TiO ,通过氮掺杂生成TiO N ,以及掺杂的空穴
2 2-a b
传输层,光照下的输出稳定性更好,更具发展潜力,反应如图(c)所示。
图(c)
已知在图(c)所示的TiO 的四方晶胞中,氧原子位于棱上、面上和体内,原子1、2的原子坐标为
2
(0,0, )和(1,0,0),则原子3的坐标为 ,设阿伏加德罗常数的值为N ,TiO 的密度
A 2
为 g·cm-3,TiO N 晶体中a= 。
2-a b18. (12分)有机物M(只含C、H、O三种元素中的两种或三种)具有令人愉悦的牛奶香气,主
要用于配制奶油、乳品和草莓型香精等。某化学兴趣小组从粗品中分离提纯有机物M,然后借
助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体过程如下:
步骤一:将粗品纯化后确定M的实验式和分子式。
按图1实验装置(部分装置省略)对有机化合物M进行C、H元素分析。
图1
回答下列问题:
(1)进行实验时,依次点燃煤气灯 。(填“a、b” 或者“b、a”)
(2)c和d中的试剂分别是 、 (填标号)。c和d中的试剂不可调换,理由是 。
A.无水CaCl B.NaCl C.碱石灰(固体CaO和NaOH的混合物) D.Na SO
2 2 3
(3)经上述燃烧分析实验测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1% ,则M
的实验式为 。
(4)已知M的密度是同温同压下氢气密度的44倍,则M的相对分子质量为 ,分子式为
。
步骤二:确定M的结构简式。
(5)用核磁共振仪测出M的核磁共振氢谱如图2,图中峰面积之比为1:3:1:3;利用红外光谱仪测
得M的红外光谱如图3。
M中官能团的名称为 ,M的结构简式为 。
19. (12分)苯胺( )的沸点为184℃,有碱性,易被氧化,微溶于水,易溶于乙醚等有
机物,广泛应用于医药和染料行业。实验室以苯为原料制取苯胺,具体过程如下:
I.制取硝基苯
(1)写出以苯为原料制取硝基苯的化学方程式___________________________________。
(2)制取的粗硝基苯用5% NaOH溶液洗涤的目的是_______________________________。
II.制取苯胺
硝基苯与氢气制取苯胺的反应原理为 + 3H + 2H O,实验装置如下
2 2
图所示(部分夹持装置省略)。已知: +HCl → (苯胺盐酸盐,易溶于水)。
回答下列问题:
(3)盛有硝基苯的仪器名称为_________________,采用的加热方式为________________。
(4)实验时,须先打开K,通一段时间H 的原因是________________________________。
2
III.苯胺的提纯
(5)实验制得的苯胺粗产品中含有少量硝基苯,某同学设计如下流程提纯苯胺、回收硝基苯。
① “步骤Ⅰ”中“分液”需要用到下列仪器中的______________(填仪器名称)。
② “步骤Ⅱ”中,加入NaOH溶液发生的主要反应的化学方程式为_____________________。20.(12分)有机化合物F是一种重要的有机合成中间体,其合成路线如图所示:
已知:① R-CH=CH R-CH CH OH
2 2 2
②通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A→B的反应条件为 ,B的名称为 (系统命名法)。
(2)C→D的化学方程式为 。
(3)X→Y的化学方程式为 ,反应类型为 。
(4)Z的结构简式为 。
(5)化合物W的相对分子质量比X大14,其同分异构体中满足以下条件的共有 种。
①结构中含有苯环 ②遇FeCl 溶液不发生显色反应 ③能与钠反应放出氢气
3机密★启用前
2025年4月山东师大附中高二阶段性检测试题化学(答案)
1-5 CBABD 6-10CDDCB 11.D 12.CD 13.AB 14.D 15.AC
除标记外,每空2分
16.(1)(正)四面体形(1分) 54 D
(2)4p(1分)
(3)温度升高,磷酸分子间氢键被破坏;
(4) N H 分子间氢键数目多于偏二甲肼[(CH ) NNH ]
2 4 3 2 2
(5)Π
17. (1) 或 [Ar]3d24s2(1分) (2) F>O>B (1分)
(3)正八面体 (1分) (4) Ti (1分) AD(选对一个得1分)
(5) (1,1, )
18.(1)b、a (1分) (2) A(1分)C(1分) 碱石灰会同时吸收水和CO
2
(3 ) C H O(1分) (4) 88(1分)C H O (1分)
2 4 4 8 2
(5) 羟基、(酮)羰基(写对一个得1分);
19.(1) +HNO +H O(条件写加热也可以)
3 2
(2)除去粗硝基苯中混有的硫酸、硝酸等
(3)恒压滴液漏斗(或恒压分液漏斗) (1分)油浴加热(1分)(恒温加热也得分)
(4)排尽装置中的空气,防止苯胺被氧化
(5)① 烧杯、分液漏斗 (写对一个得1分)
② (主要)
NaOH+HCl NaCl+H O(不写不扣分)
2
20.(1) 浓硫酸、加热 (1分) 甲基丙烯 (或者 甲基-1-丙烯)
(2)2(CH ) CHCH OH+O 2(CH ) CHCHO+2H O
3 2 2 2 3 2 2
(3) +2Cl 2HCl+ 取代反应(1分)
2
(4)
(5)5