文档内容
湖南师大附中2025届高三月考试卷(六)
化学
得分:,
本试题卷分选择题和非选择题两部分,共8页。时址75分钟,满分100分。
可能用到的相对原子质ihH~】C〜12 0—16 Na〜23 S~32
CI-'-35. 5 Fe〜56 Cu〜64
一、选择题:本题共14小题,每小题3分,共42分。诲小题只有一个选项符合题
目要求。
1.《厉害了,我的国》展示了中国五年来探索太空,开发深海,建设世界一流的离
展
铁、桥梁、码头,5G技术联通世界等取得的举世瞩目的成就.它们与化学有膂
密切联系。下列说法正确的是
迦
A.为打造生态文明建设,我国近年来大力发展的核电、光电、风电、水电等电能
瞅 属于一次能源
B.大飞机C919采用了大量先进复合材料、铝锂合金等,其中相锂合金属于金
篡 K- 属材料
C.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是
■S 晶体硅
D. “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶镒的主要成分是硅
酸盐
2,下列说法正确的是
盘 a. sOz和0,、p。丁和cio7互为等电子体
B甲烷分子失去一个H+,形成CH7,其碳原子的杂化类型发生了改变
C CH八BCQ、Sa都是含有极性键的非极性分子
D.元素的基态原子核外电子排布都遵循构造原理
3 .下列尚子方程式书写正确的是
A. Na2520a溶液与稀硫酸反应的离子方程式:507十6H+-2SC +3HQ
R向饱和NajCOh溶液中通人过斌COaiCOr+COj+HjO-2HCOf
C AgN03与过黄浓氨水反应的璐子方程式:Ag++NK • HQ -
AgOH1+NH^
D. Fe 与稀硝酸以 n(Fe) : n(HN03) = l : 2 反应:3Fe+2NOT +8H+---
科
3FeZ+ + 2NO}+4HQ
4 . C102广泛用于纸浆漂白、杀菌消毒等领域,因C15消毒效果好、不产生致癌物
或诱变剂,已被广泛应用于污水处理工程.其一种制备方法为5NaC10z +
4HC1-5NaCl+4C】d 1+2%0。下列说法错误的是
A. QQ具有强氧化性
B. HC1在反应中只起到提供酸性环境的作用
C.反应生成1 mol CICX时,转移5 moi电子
n当还原产物均为C厂时.等质坦的ClOz的氧化能力是02的2.63倍
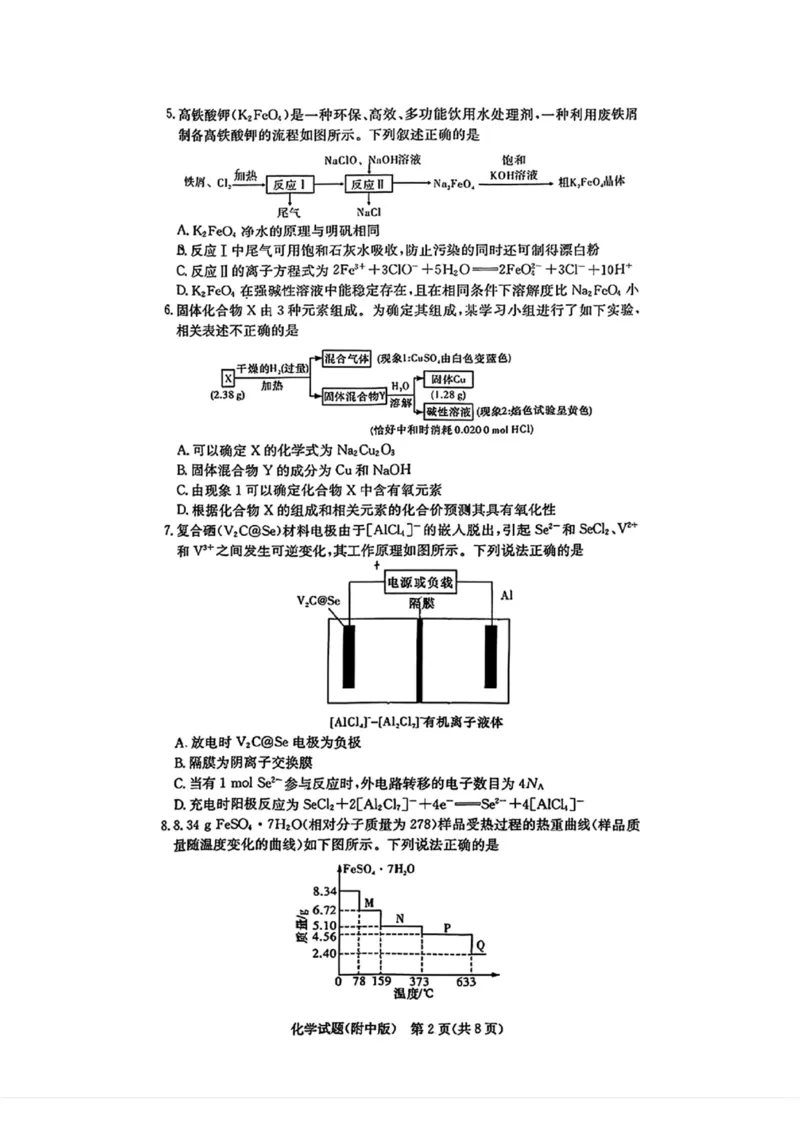
化学试题(附中版)第1页(共8页)5.高铁酸翅(KzFeO,)是一种环保、高效、多功能饮用水处理剂,一种利用废铁屑
制备高铁酸钾的流程如图所示。下列叙述正确的是
NaClO. pnOH济滋 饱和
铁阐、以邂L辰面——反应口 |-------•Nn/cO, K°喻液•粗灯皿品体
I I
尾气 NuCI
A. K2FeO4净水的原理与明矶相同
B.反应I中尾气可用饱和石灰水吸收,防止污染的同时还可制得漂白粉
C 反应 U 的编子方程式为 2Fe"+3cICT +5HzO==2FeOr +3Cr+10H+
D.KzFea在强鼓性溶液中能稳定存在,且在相同条件下溶解度比N%FeO,小
6 .固体化合物X由3种元素组成,为确定其组成,某学习小组进行了如下实验,
相关表述不正确的是
国混合气体| (现煞l:Cu6O.由白也变蓝色)
干燥的电(过员)I . :
国
H肉体a |
(2.38 b) 加热 T因体混合物丫|^^[g8 g)
U球性溶液| (现象2:熔色试验呈黄色)
(恰好中和时捎耗0.0200 mol HC1)
A.可以确定X的化学式为NaiCuzOs
B固体混合物Y的成分为Cu和NaOH
C.由现象1可以确定化合物X中含有僦元素
D.根据化合物X的组成和相关元素的化合价预泅其具有氧化性
7 .复合硒(VzC@Se)材料电极由于[AlCUl一的嵌入脱出,引起$才一和SeCLV2+
和V3+之间发生可逆变化,其工作原理如图所示.下列说法正确的是
电源或负栽
[AIOJTAIKU市机离子液体
A.放电时V2C@Se电极为负极
B .隔膜为阴离子交换膜
C.当有1 mol Se2-参与反应时,外电路转移的电子数目为4N“
D.充电时阳极反应为 SeCI2+2LAUCld- +4e-=Se3- +4[A1CL,
8.8.34 g FeSO, , 7%0(相对分子质盘为278)样品受热过程的热重曲线(样品质
员随温度变化的曲线)如下图所示.下列说法正确的是
化学试题(附中版)第2页(共8页)A. FcSO, • 7HzO受热过程中发生的四次反应均为非氧化还原反应
B.温度为200 9时固体N的化学式为FeSCX • 2HQ
C.取适垃380 C时所得的固体P,隔绝空气加热至633。,得到一种黑色固体
物质Q
D.在隔绝空气条件下,由固体N得到固体P的化学方程式为FeSO, , HSO
-FeSO, + H2O
9.类推法是化学学习和研究常用的重要思维方法,但所得结论要经过实践的检验
才能确定其正确与否。根据你所掌握的知识,判断下列类推结论正确的是
A. Mg燃烧时不能用CO?灭火,故Na燃烧时也不能用CQ灭火
民AI在5中燃烧生成AlzOj,故Fe在Q中燃烧生成FaOw
C. COz与Na,02反应生成Na?8〉和Oz,故SO?与N电Q反应生成Na?SQ
和
D. A1与NaOH溶液反应生成Hz,故Mg与NaOH溶液反应也生成H2
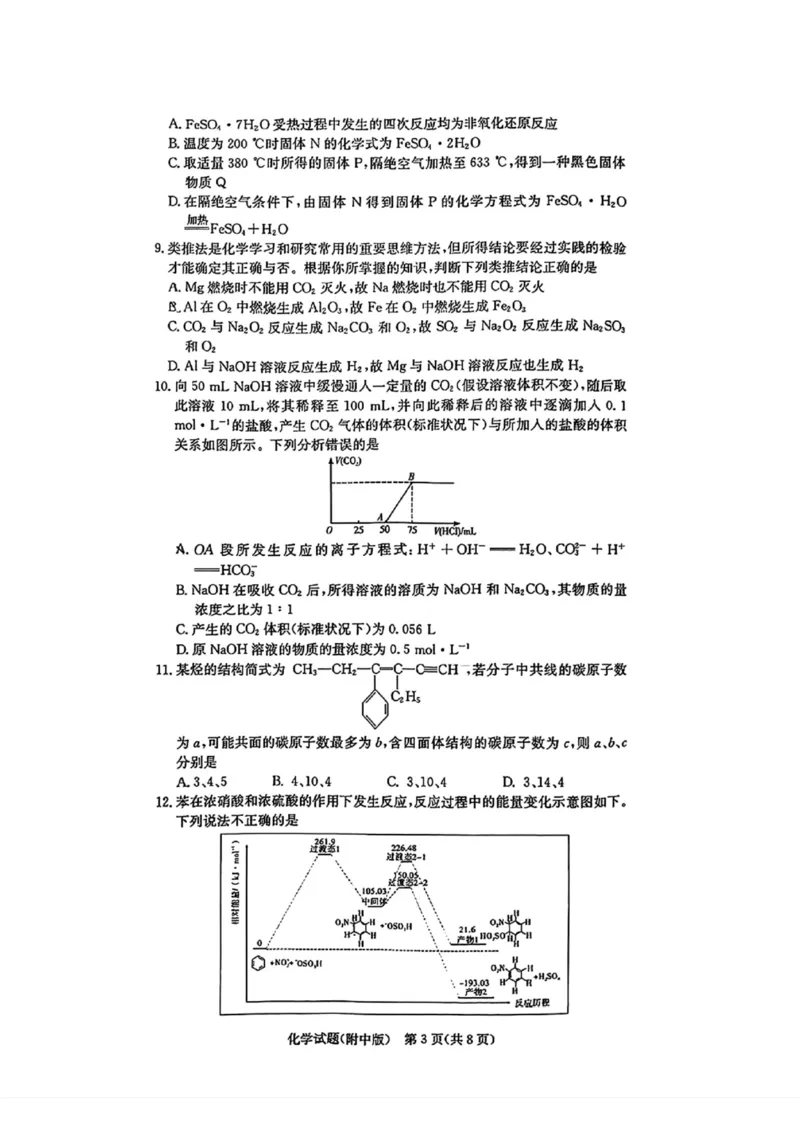
10.向50 mL NaOH溶液中缓慢通人一定量的CO?(假设溶液体积不变),随后取
此溶液10 mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0. 1
mol • LT的盐酸,产生COz气体的体积(标准状况下)与所加入的盐酸的体积
关系如图所示.下列分析错误的是
,KCOJ
B
0 25 50 75 V(HC!)/mL
A. OA段所发生反应的离子方程式:H+ +OH- -HQ、C0r + H+
=Hcor
B. NaOH在吸收CQ后,所得溶液的溶质为NaOH和Naz。%,其物质的班
浓度之比为1 = 1
C.产生的CO;体积(标准状况下)为0. 056 L
D.原NaOH溶液的物质的:浓度为0.5 mol • L-1
11 .某煌的结构简式为CM-CHz—[f-gCH;若分子中共线的碳原子数
入8国
0
为a,可能共面的碳原子数最多为6,含四面体结构的碳原子数为c,则a、b、c
分别是
A3、4、5 B. 4、10、4 C. 3、10、4 D. 3」4、4
12 .米在浓硝酸和浓硫酸的作用下发生反应,反应过程中的能就变化示意图如下.
下列说法不正确的悬
化学试题(附中版)第3页(共8页)A.从中间体到产物,无论从产物毯定性还是反应速率的角度均有利于生成产
物2
R产物1为落的加成产物,产物2为苯的取代产物
C.生成中间体时碳的杂化方式未发生改变
D.该反应历程中的决速步骤的活化能(能垒)为261. 9 U • mor1.
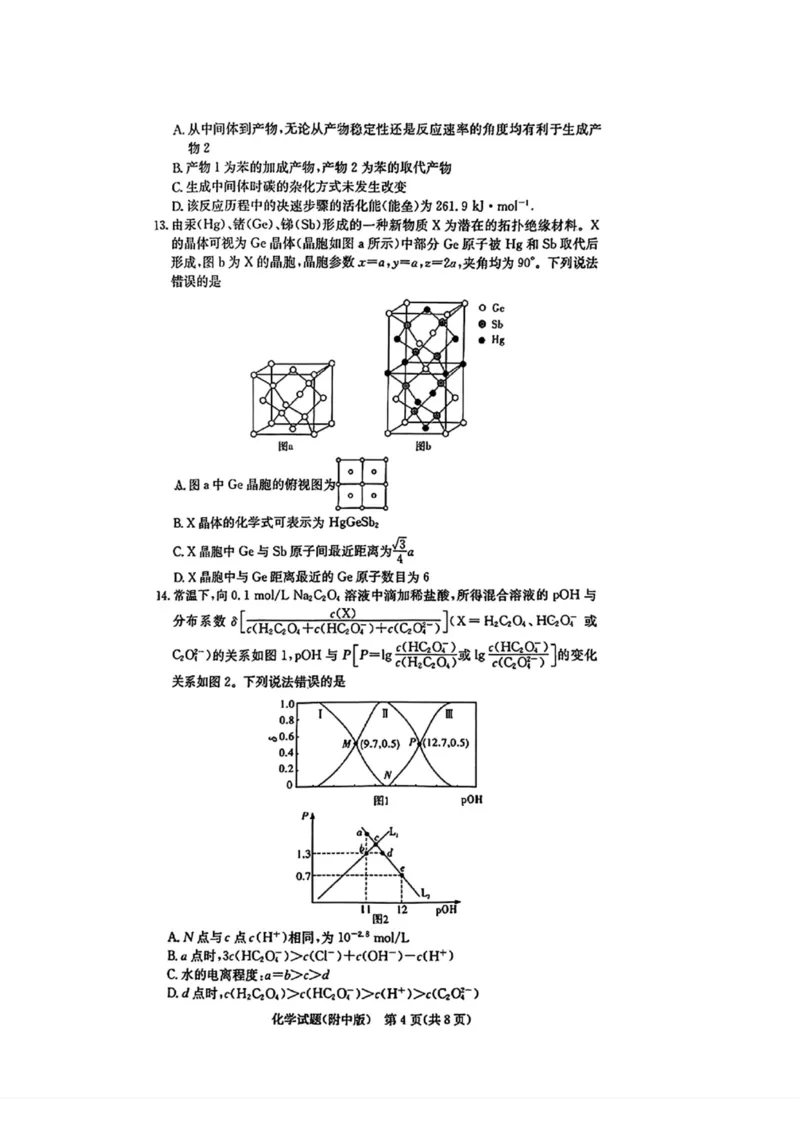
13 .由汞(Hg)、错(Ge)、镖(Sb)形成的一种新物质X为潜在的拓扑绝缘材料。X
的晶体可视为Ge晶体(晶胞如图a所那)中部分Ge原子被Hg和Sb取代后
形成.图b为X的晶胞.晶胞参数了=。d=。避=外,夹角均为90°.下列说法
错误的是
RX晶体的化学式可表示为HgGeSbj
C. X晶胞中Ge与Sb原子间最近距窗为
D. X晶胞中与Ge距离最近的Ge原子数目为6
14.常温下,向0.1 mol/L Na2G0,溶液中滴加稀地酸,所得混合溶液的pOH与
分布系数 3[«H2Gd+c(鉴3 + “淑-〉](* = HzGO,、HGO'或
&戢一)的关系如图1,P°H与尸伊=39^^或电^^?]的变化
关系如图2.下列说法错误的是
图】 pOH
P+
II 12 pOB
图2 「
A.N点与c点c(H+)相同,为 lOTSmol/L
B.0 点时,3c(HCiO?)>c(Cr ) +c(.OH-)-c(H+)
C,水的电离程度:a=K>c>d
D.d 点时,c(HzGOi)>c(HaO「)>HH+)>c(Ga-)
化学试题(附中版)第4页(共8页)选择题答题卡
15. (14分)某同学在实验室进行铁盐与亚铁盐相互转化的实验。
实验I:将Fe,+转化为F*
3SS0.1 mol - L ' KSCN临催
FfSOJ萨法
(DFe3+与铜粉发生反应的离子方程式为
(2)某学生用对比实验法探究白色沉淀产生的原因,靖填写实验方案:
实脸方案 现象 结论
步骤 1:取 4 mUD_______ mol • L CuSO,溶 产生
液,向其中满加3滴0.1 mol • LT KSCN溶液 白色沉淀 CuSO(与 KSCN
在溶液中反应
产生了白色
步骤 2:取 4 mL②_______mol • L"1 FeSOt 溶 无明显 沉淀
液响其中滴加3滴。.1 mol • V KSCN溶液 现氽
推阅资料:
①SCN-的化学性质与「相似;
② 2Cij2++4==~"2Cul ] +Iz»
Cu计与SCN-反应的离子方程式为③
实验D:将F*转化为Fe,+
实骐方案 现象
向 3 mL 0. 1 mol ♦ L FeSO,溶液中加入 3 tnL 蓄液变为棕色,放置一段时间
0. 5 mol,IT1 稀硝酸 后,棕色消失,溶液变为黄色
探究上述现象出现的原因:
查阅资料1 F¥+ +NO LFe(NO)z+ (棕色)
(3)用离子方程式解稀NO产生的原因:—
(4)从化学反应速率与限度的角度对体系中存在的反应进行分析:
反应I :F*与HNO,反曲反应口 :Fe"与NO反应
①反应I是一个不可逆反应,设计实验方案加以证明:
②请用化学平衡移动原理解释溶液由粽色变为黄色的原因:
化学试题(附中版)第5页(共8页)16. (15分)以钛铁矿(主要成分为FeTiO「含有少fit Fs。、55)为主要原料制
取Ti和绿矶,同时联合氯碱工业生产甲醉的工艺流程如图所示。
辘取侬 铁制 愫职 过璇曲发
.帙旷胆哼1函]一低:①卜就谓M丽]一叵画一画}画劭-ti
电知口长水一^^一气体A,体C
济£气体8一医囤一甲酢
已知:①“酸浸”时,FeTiCb转化为TiO",钛.铁元素的价态不改变,
②“加热”过程中发生反应:TiOSO<+2HzO = HECU +m$。・。
(DTi在元素周期表中的位性为*
(2)“酸浸”时发生的主要反应的化学方程式为 ..
(3)“还原①”后溶液仍显强酸性,分析加入适fit铁粉的目的是______ _________,
_____________________________ (用离子方程式解释).
(4)由“工序①”的滤液得到绿砒的系列模作为,_____________________________ ,
过渡,再对所得到的绿矶晶体用75%的乙醇溶液洗涤,用乙醐溶液洗涤的
优点是.
(5)下列有关“工序②”和“还原②”步骤的说法正确的是(填标号)。
A. “工序②”发生反应TiQ+ZClz+C=TiCU+COa(反应条件略)
B.:'还原②"可以用氮气做保护气
C.铝热反应制镂与“还原②”冶炼制钛方法相似
(6)当嘿=2附,为了提高气体B和气体C制落甲静的平衡产率,工业生产
中通常采取的措施是___________________________________________________
(写出两点兀
(7)钛与卤索形成的化合物TiX,的熔点如表所示。
TiX4 TiCU TiBq TiL
熔点/( 377 -24 38.3 153
解释笛凡熔点差异的原因:.
17. (14分)有机物PAS - Na是一种治疗肺结核药物的有效成分,有机物G是一
种食用香料,以甲苯为原料合成这两种物质的路线如困所示。
—生案…燃
G
COONu
8r/FeBr,i 试剂£ 7~工用0乩地;加即
B
浓硝物浓破敏,△
PAS-N©
21里 O-CH。.
化学试题(附中版)第6页(共8页)回答下列问题;
(D由 生成A的反应类型是 0
(2)F中含辄官能团的名称是,试剂a的结构荷式为
(3)写出由A生成B的化学方程式:.
(4)质谱图显示试剂b的相对分子质斑为58,分子中不含甲基,且为链状结构,
写出肉桂酸与试剂b反应生成G的化学方程式:
(5)当试剂d过贵时.可以选用的试剂d是(填标号)0
a. NaHCOj b, NaOH c. N&CO,
(6)肉桂酸有多种同分异构体,符合下列条件的有 种.
a.茉环上有三个取代基;
b.能发生根镜反应,且消耗1 moi该有机物最多生成4 mol Agt
上述符合条件的同分异构体中,米环上有两种不同化学环境瓠原子的有机
物的结构简式为(任写一种即可).
18.(15分)“雾?g”成为人们越来越关心的环境问题。雾霾中含有二辄化硫、氮辄
化物和可吸入颗粒物等污染性物质。请回答下列问题:
(1)汽车尾气是雾籁形成的原因之一.可在催化剂作用下用由汽油挥发出的
烧类物质(GH,还原尾筋中的NO气体进行尾气治理,该过程的化学方
程式为.
(2)冬季燃煤供暧产生的废气也是雾霸形成的主要原因之一.经研究发现将
媒碳在OJCO的气氛下燃烧,能够降低燃燥时NO的排放,主要反应为
2NO(g)+2CO(g) 一 N式 g)+2CO2(g)AH.
已知:①N式g)+Oz(g)一2NO(g) AH, =+180. 5 kJ ・ mol-1
®2CO(g);=i2C(s)+Ot(g) aH2=4-221 kJ , mo I-'
③C(s)+5 (gB^COz (g) A% ——393.5 kJ • mo L
则 AH=°
(3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,并将得到的NazSO?溶
液进行电解,其中阴、阳膜组合电解装置如图1所示,电极材料为石墨,
a b
Wl
化学试题(附中法)第7页(共8页)①a表示(填“阴”或“阳”)离子交换膜.A〜E分别代表生产中的
原料或产品,其中C为航酸,则A表示 正表示
②阳极的电极反应式为________________________________________________•
(4)20,经过净化后与空气混合进行催化氯化可制取硫酸,其中SOz发生健化
氧化的反应为SSC^CgJ+O:(g).若在料七条件下,往一恒
容密闭容器中通入SO:和Oz[其中”(SOz)! ”(0口=2 : 11,测得容器内
起始压强为0.1 MPa,总压强与反应时间的关系如图2所示.
•p/MPa
、
X(:.0.085) 430.0.078)
*-------------T,
5 10 15 20 25 30 35 4045 50,/rain
图
2
①图中A点时,沁的转化率为.
②在其他条件不变的情况下,冥七时C点的正反应速率的(C)与A点的
逆反应速率隈(A)的大小关系为年(C)《填或
“="M(A)。
③用中B点的压强平衡常数Kp=(用平衡分压代表平衡浓
度计算,分压=总压X物质的温分数).
化学试题(附中版)第8页(共8页)