文档内容
大联考雅礼中学 2025 届高三月考试卷(一)
化学
命题人:于雯 审题人:吴建新
得分:______
本试题卷分选择题和非选择题两部分,共 8页。时量 75分钟,满分100分。
可能用到的相对原子质量:H~1 C~12 N~14 O~16 Na~23 Al~27 Si~28 P~31
第Ⅰ卷(选择题 共 42分)
一、选择题(本题共 14 小题,每小题 3分,共 42分,每小题只有一个选项符合题意。)
1.下列有关叙述错误的是( )
A.放电影时,放映机到银幕间光柱的形成是因为丁达尔效应
B.工业上一般可以采用电解饱和食盐水的方法制取NaOH
C.FeO在空气中受热,能迅速被氧化成Fe O
2 3
D.硬铝是一种铝合金,密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料
2.设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.40gSiC晶体中含有的Si−C的数目为2N
A
B.100g质量分数为46%的C H OH的水溶液中含有的氧原子数目为4N
2 5 A
C.标准状况下,11.2LNH 与11.2LHF均含有5N 个质子
3 A
D.1molC H 中含有的σ键的数目为20N
6 14 A
3.下列关于Na CO 和NaHCO 的说法中,错误的是( )
2 3 3
A.两种物质的溶液中,所含微粒的种类相同
B.可用NaOH溶液使NaHCO 转化为Na CO
3 2 3
C.利用二者热稳定性差异,可从它们的固体混合物中除去NaHCO
3
D.室温下,二者饱和溶液的pH差约为4,主要是因为它们的溶解度差异
4.在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A.制备HCl:NaCl溶液电解→H 和Cl 点燃→HCl
2 2
B.制备金属Mg:Mg ( OH ) 盐酸→MgCl 溶液电解→Mg
2 2
C.纯碱工业:NaCl溶液CO 2→NaHCO △→Na CO
3 2 3
D.硫酸工业:FeS O 2→SO H2 O→H SO
2 高温 2 2 4
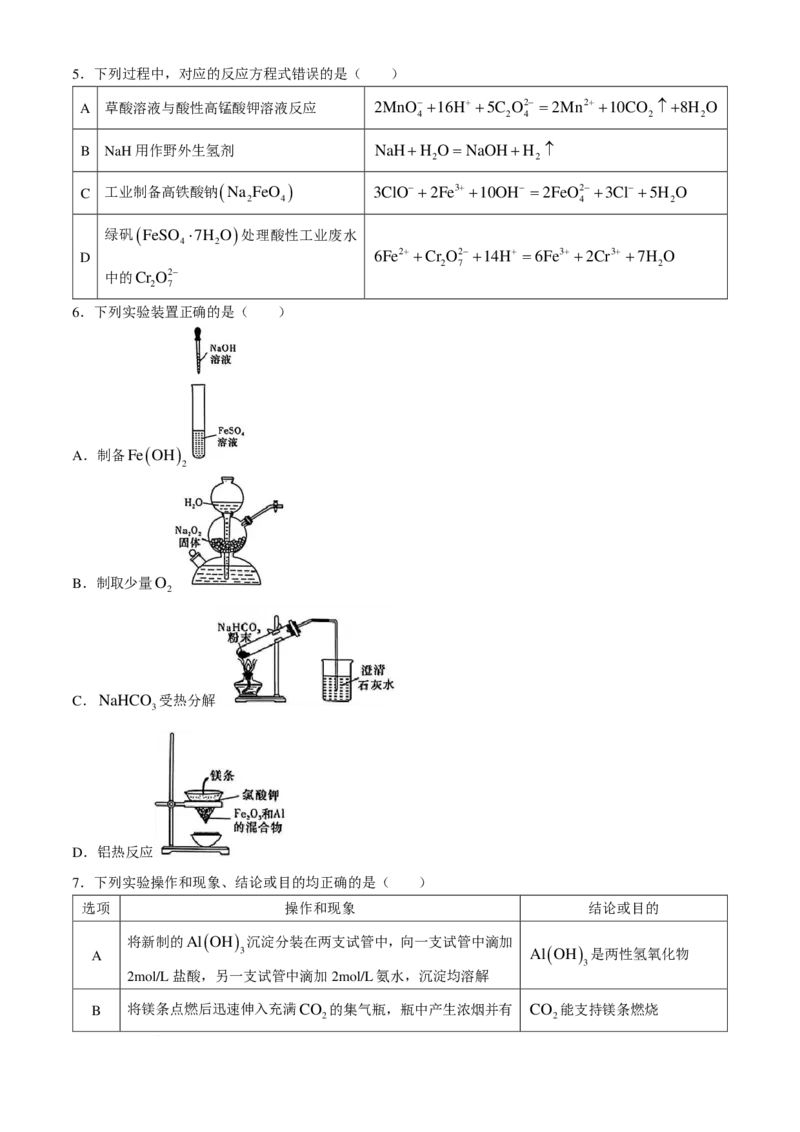
学科网(北京)股份有限公司5.下列过程中,对应的反应方程式错误的是( )
A 草酸溶液与酸性高锰酸钾溶液反应 2MnO− +16H+ +5C O2− =2Mn2+ +10CO ↑+8H O
4 2 4 2 2
B NaH用作野外生氢剂 NaH+H O= NaOH+H ↑
2 2
C 工业制备高铁酸钠( Na FeO ) 3ClO− +2Fe3+ +10OH− =2FeO2− +3Cl− +5H O
2 4 4 2
绿矾( FeSO ⋅7H O )处理酸性工业废水
4 2
D 6Fe2+ +Cr O2− +14H+ =6Fe3+ +2Cr3+ +7H O
2 7 2
中的Cr O2−
2 7
6.下列实验装置正确的是( )
A.制备Fe ( OH )
2
B.制取少量O
2
C.NaHCO 受热分解
3
D.铝热反应
7.下列实验操作和现象、结论或目的均正确的是( )
选项 操作和现象 结论或目的
将新制的Al ( OH ) 沉淀分装在两支试管中,向一支试管中滴加
A 3 Al ( OH ) 是两性氢氧化物
3
2mol/L盐酸,另一支试管中滴加2mol/L氨水,沉淀均溶解
B 将镁条点燃后迅速伸入充满CO 的集气瓶,瓶中产生浓烟并有 CO 能支持镁条燃烧
2 2
学科网(北京)股份有限公司黑色颗粒生成
取FeCl 溶液置于试管中,加入几滴酸性高锰酸钾溶液,酸性高
C 2 Fe2+具有还原性
锰酸钾溶液的紫色褪去
各取Na CO 溶液与NaHCO 溶液少许于试管中,加入澄清石
2 3 3 鉴别Na CO 溶液与NaHCO
2 3 3
D
灰水,仅Na CO 溶液中出现白色沉淀 溶液
2 3
( )
8.已知电对的标准电极电势 E0 越高,其电对中氧化剂的氧化性越强。现有4组电对的标准电极电势:
①E0( PbO PbSO )=+1.69V;②E0 ( MnO− Mn2+) =+1.51V;③E0 ( Fe3+ Fe2+) =+0.77V;④
2 4 4
E0
(
Cl
Cl−)
=+1.36V。下列有关说法正确的是( )
2
A.溶液中浓度均为1mol/L的Fe3+和Cl−可发生反应:2Fe3+ +2Cl− =2Fe2+ +Cl ↑
2
B.酸化高锰酸钾时既可以用硫酸也可以用盐酸
C.向含2molFeCl 的溶液中加1molPbO 可观察到黄绿色气体产生
2 2
D.PbO 与酸性MnSO 溶液反应的离子方程式:
2 4
5PbO +2Mn2+ +4H+ +5SO2− =5PbSO +2MnO− +2H O
2 4 4 4 2
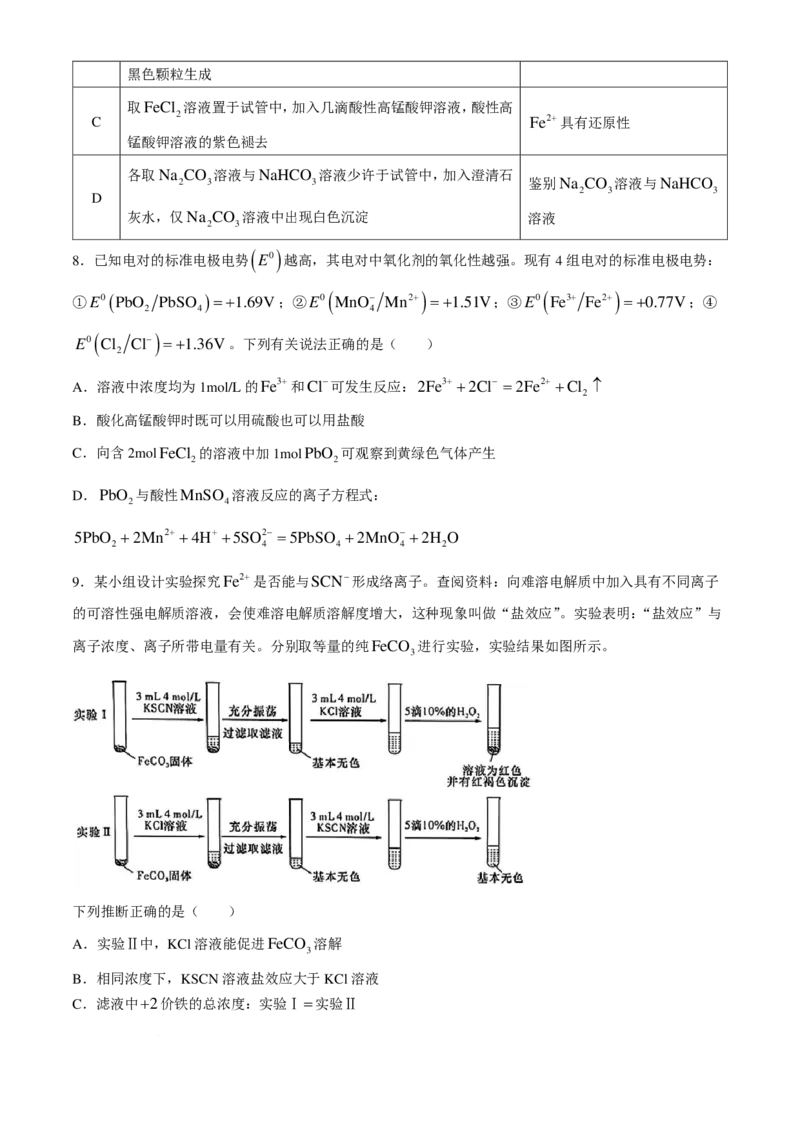
9.某小组设计实验探究Fe2+是否能与SCN−形成络离子。查阅资料:向难溶电解质中加入具有不同离子
的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与
离子浓度、离子所带电量有关。分别取等量的纯FeCO 进行实验,实验结果如图所示。
3
下列推断正确的是( )
A.实验Ⅱ中,KCl溶液能促进FeCO 溶解
3
B.相同浓度下,KSCN溶液盐效应大于KCl溶液
C.滤液中+2价铁的总浓度:实验Ⅰ=实验Ⅱ
学科网(北京)股份有限公司D.实验表明,Fe2+和SCN−不能形成络离子
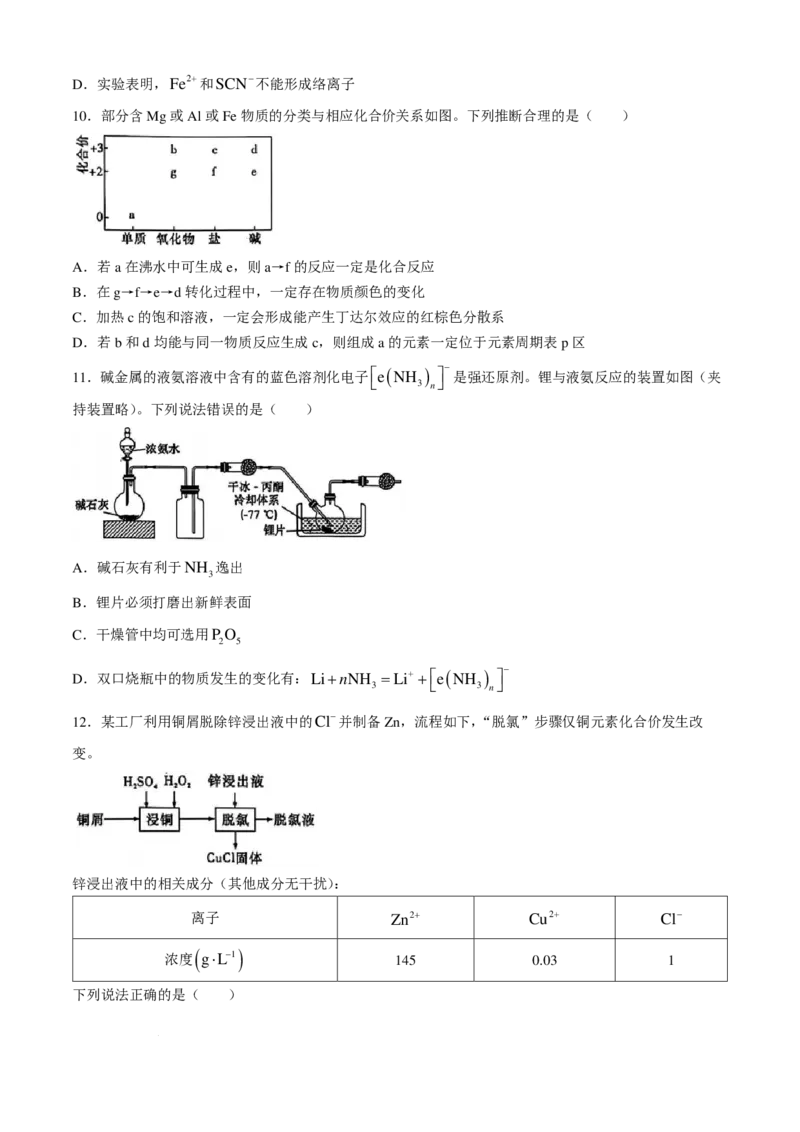
10.部分含Mg或Al或Fe物质的分类与相应化合价关系如图。下列推断合理的是( )
A.若a在沸水中可生成e,则a→f的反应一定是化合反应
B.在g→f→e→d转化过程中,一定存在物质颜色的变化
C.加热c的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系
D.若b和d均能与同一物质反应生成c,则组成a的元素一定位于元素周期表p区
11.碱金属的液氨溶液中含有的蓝色溶剂化电子
e ( NH
3
)
n
− 是强还原剂。锂与液氨反应的装置如图(夹
持装置略)。下列说法错误的是( )
A.碱石灰有利于NH 逸出
3
B.锂片必须打磨出新鲜表面
C.干燥管中均可选用PO
2 5
D.双口烧瓶中的物质发生的变化有:Li+nNH
3
=Li+ +
e ( NH
3
)
n
−
12.某工厂利用铜屑脱除锌浸出液中的Cl−并制备Zn,流程如下,“脱氯”步骤仅铜元素化合价发生改
变。
锌浸出液中的相关成分(其他成分无干扰):
离子 Zn2+ Cu2+ Cl−
浓度 ( g⋅L−1 ) 145 0.03 1
下列说法正确的是( )
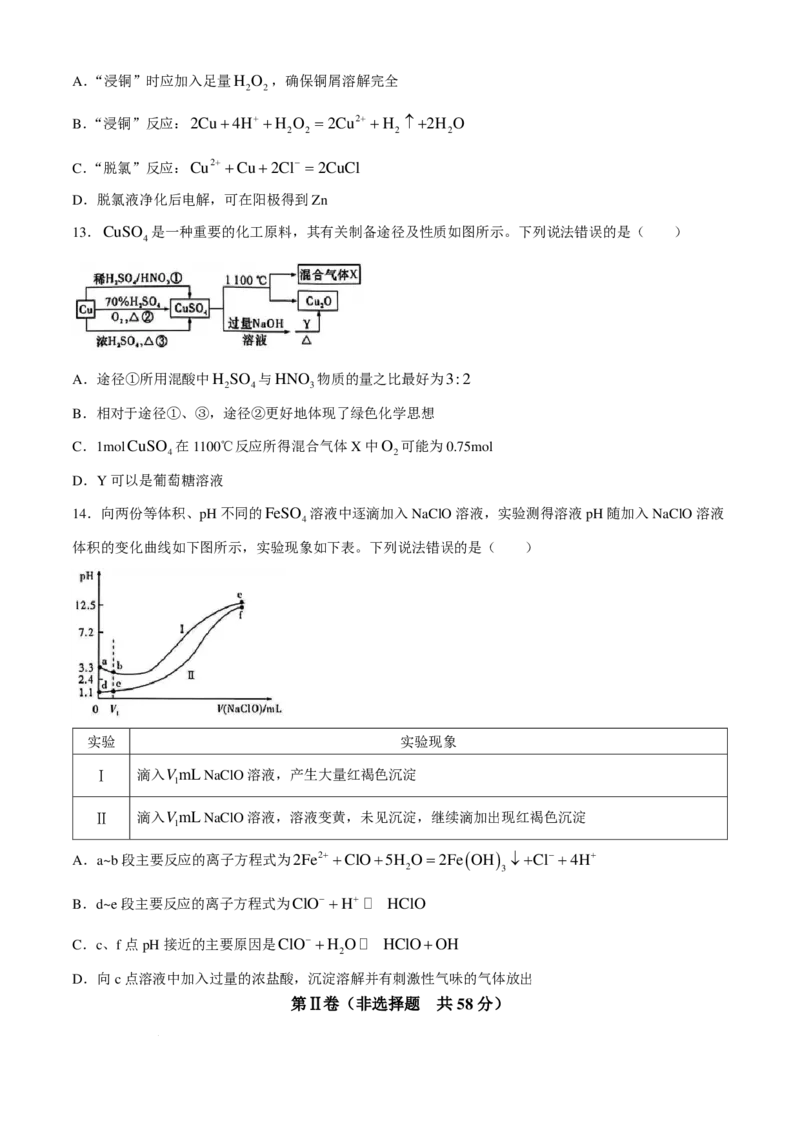
学科网(北京)股份有限公司A.“浸铜”时应加入足量H O ,确保铜屑溶解完全
2 2
B.“浸铜”反应:2Cu+4H+ +H O =2Cu2+ +H ↑+2H O
2 2 2 2
C.“脱氯”反应:Cu2+ +Cu+2Cl− =2CuCl
D.脱氯液净化后电解,可在阳极得到Zn
13.CuSO 是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法错误的是( )
4
A.途径①所用混酸中H SO 与HNO 物质的量之比最好为3:2
2 4 3
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1molCuSO 在1100℃反应所得混合气体X中O 可能为0.75mol
4 2
D.Y可以是葡萄糖溶液
14.向两份等体积、pH不同的FeSO 溶液中逐滴加入NaClO溶液,实验测得溶液pH随加入NaClO溶液
4
体积的变化曲线如下图所示,实验现象如下表。下列说法错误的是( )
实验 实验现象
Ⅰ 滴入VmLNaClO溶液,产生大量红褐色沉淀
1
Ⅱ 滴入VmLNaClO溶液,溶液变黄,未见沉淀,继续滴加出现红褐色沉淀
1
A.a~b段主要反应的离子方程式为2Fe2+ +ClO+5H O=2Fe ( OH ) ↓+Cl− +4H+
2 3
B.d~e段主要反应的离子方程式为ClO− +H+ HClO
C.c、f点pH接近的主要原因是ClO− +H O HClO+OH
2
D.向c点溶液中加入过量的浓盐酸,沉淀溶解并有刺激性气味的气体放出
第Ⅱ卷(非选择题 共 58分)
学科网(北京)股份有限公司二、非选择题(本题共 4小题,共 58分。)
15.(16分)钠及其化合物在人类生产、生活中起着重要的作用。请回答下列问题:
(1)工业上,将Na CO 和Na S以1:2的物质的量之比配成溶液,再通入SO 可制取Na S O ,同时
2 3 2 2 2 2 3
放出CO ,写出该反应的化学方程式:______。Na S溶液在空气中久置,会生成浅黄色物质,经测定该
2 2
物质具有与过氧化钠相似的结构,该物质的电子式为______。
(2)我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如
图所示(部分物质已略去)。
①写出反应①的化学方程式:______。
②下列关于该流程的说法正确的是______(填标号)。
A.可循环使用的物质只有CO
2
B.副产物NH Cl可用作氮肥
4
C.优先通入CO 气体至饱和,后通入NH ,就会产生NaHCO 沉淀
2 3 3
(3)向50mL的氢氧化钠溶液中通入一定量的二氧化碳,充分反应后再向溶液中逐滴滴入0.1mol/L的稀
盐酸,产生气体的体积(标准状况)如图所示。
①通入二氧化碳后形成溶液的溶质成分是______(填化学式)。
②滴入25mL稀盐酸过程中,溶液导电性______(填“增强”“减弱”或“不变”),试解释其原因:
______。
③原50mL氢氧化钠溶液的浓度为______。
16.(14分)以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag的工艺流程如下:
2
学科网(北京)股份有限公司回答下列问题:
(1)“热浸”时,难溶的PbS和Ag S转化为[ PbCl ]2− 和[ AgCl ]− 及单质硫。溶解等物质的量的PbS和
2 4 2
Ag S时,消耗Fe3+物质的量之比为______;溶液中盐酸浓度不宜过大,除防止“热浸”时HCl挥发外,
2
另一目的是防止产生______(填化学式)。
(2)将“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水“热溶”,电解所得溶液可制备金属Pb,“电解
2
Ⅰ”阳极产物用尾液吸收后在该流程中可循环使用,利用该吸收液的操作步骤为______。
(3)“还原”中加入铅精矿的目的是______。
(4)“置换”中适宜选用的试剂X为______(填标号)。“置换”反应的离子方程式为______。
A.Al B.Zn C.Pb D.Ag
(5)“电解Ⅱ”中将富银铅泥制成电极板,可电解精炼铅,其中富银铅泥用作______(填“阴极”或“阳
极”)。
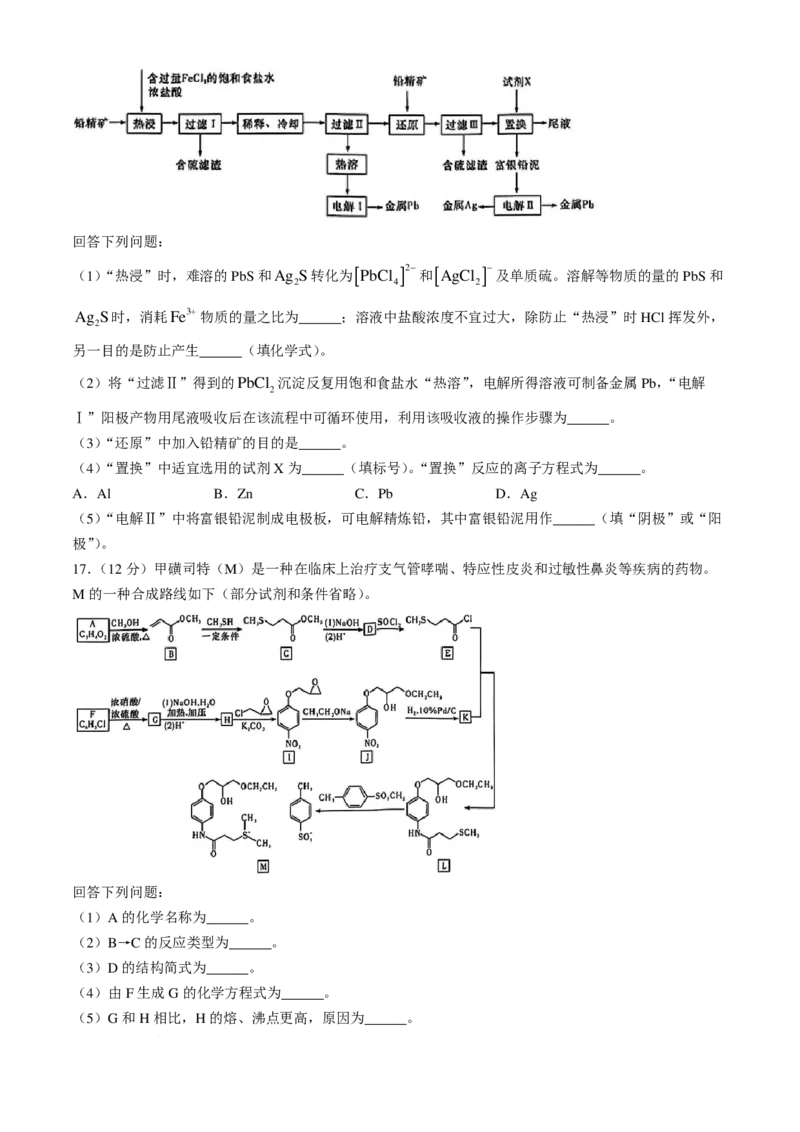
17.(12分)甲磺司特(M)是一种在临床上治疗支气管哮喘、特应性皮炎和过敏性鼻炎等疾病的药物。
M的一种合成路线如下(部分试剂和条件省略)。
回答下列问题:
(1)A的化学名称为______。
(2)B→C的反应类型为______。
(3)D的结构简式为______。
(4)由F生成G的化学方程式为______。
(5)G和H相比,H的熔、沸点更高,原因为______。
学科网(北京)股份有限公司(6)同时满足下列条件的Ⅰ的同分异构体共有______种。
(a)核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:2;
(b)红外光谱中存在C=O和对硝基苯基( )的吸收峰。
其中一种结构可以通过水解反应得到化合物H,符合该要求的结构简式为______。
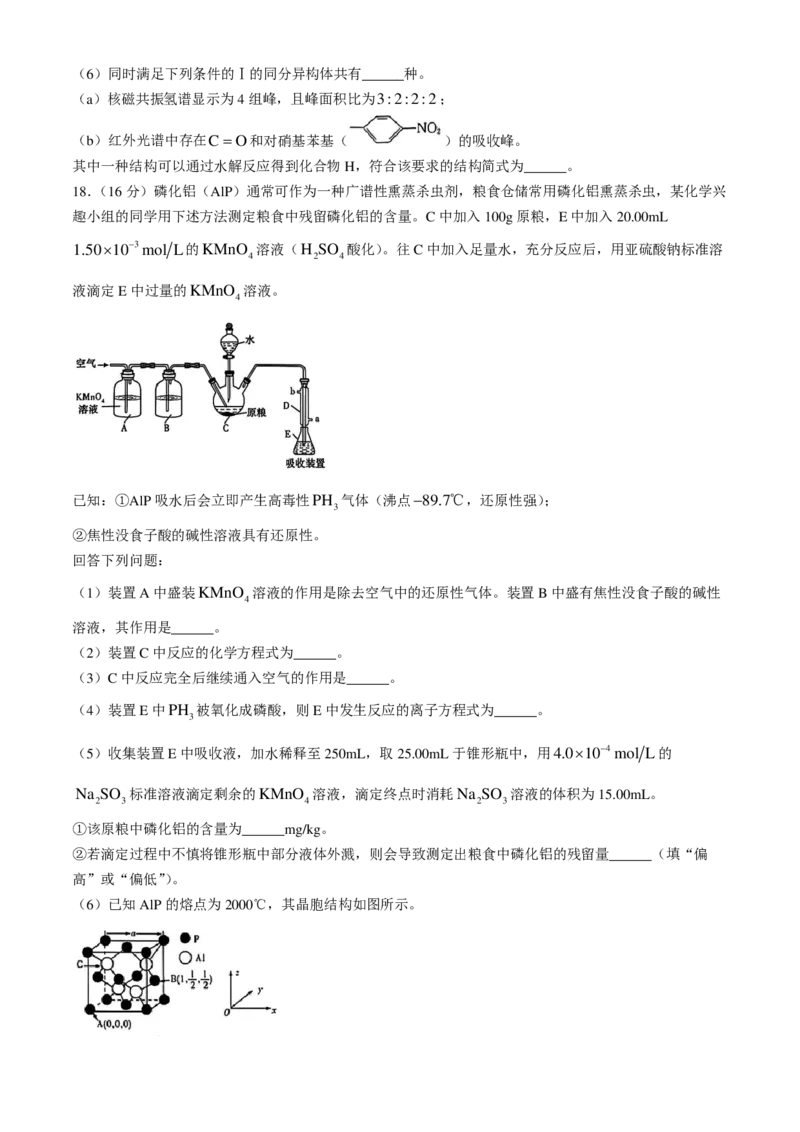
18.(16分)磷化铝(AlP)通常可作为一种广谱性熏蒸杀虫剂,粮食仓储常用磷化铝熏蒸杀虫,某化学兴
趣小组的同学用下述方法测定粮食中残留磷化铝的含量。C中加入100g原粮,E中加入20.00mL
1.50×10−3mol L的KMnO 溶液(H SO 酸化)。往C中加入足量水,充分反应后,用亚硫酸钠标准溶
4 2 4
液滴定E中过量的KMnO 溶液。
4
已知:①AlP吸水后会立即产生高毒性PH 气体(沸点−89.7℃,还原性强);
3
②焦性没食子酸的碱性溶液具有还原性。
回答下列问题:
(1)装置A中盛装KMnO 溶液的作用是除去空气中的还原性气体。装置B中盛有焦性没食子酸的碱性
4
溶液,其作用是______。
(2)装置C中反应的化学方程式为______。
(3)C中反应完全后继续通入空气的作用是______。
(4)装置E中PH 被氧化成磷酸,则E中发生反应的离子方程式为______。
3
(5)收集装置E中吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10−4mol L的
Na SO 标准溶液滴定剩余的KMnO 溶液,滴定终点时消耗Na SO 溶液的体积为15.00mL。
2 3 4 2 3
①该原粮中磷化铝的含量为______mg/kg。
②若滴定过程中不慎将锥形瓶中部分液体外溅,则会导致测定出粮食中磷化铝的残留量______(填“偏
高”或“偏低”)。
(6)已知AlP的熔点为2000℃,其晶胞结构如图所示。
学科网(北京)股份有限公司①A、B点的原子坐标如图所示,则C点的原子坐标为______。
②AlP晶体中配位键与普通共价键数目之比为______。
炎德·英才大联考雅礼中学 2025 届高三月考试卷(一)
化学参考答案
一、选择题(本题共 14 小题,每小题 3分,共 42分,每小题只有一个选项符合题意。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C B D A A D B D A B C C C B
1.C 【解析】FeO在空气中受热,迅速被氧化成Fe O ,C错误。
3 4
2.B 【解析】40gSiC晶体中含有的Si−C的数目为4N ,A错误;标准状况下HF不是气体,无法计
A
算质子数,C错误;1molC H 中含有的σ键的数目为19N ,D错误。
6 14 A
3.D 【解析】Na CO 和NaHCO 的溶液中均存在H O、H CO 、H+、OH−、Na+、CO2−、
2 3 3 2 2 3 3
HCO−,A正确;NaHCO 中加入NaOH溶液会发生反应:NaOH+NaHCO = Na CO +H O,B
3 3 3 2 3 2
正确;NaHCO 受热易分解,可转化为Na CO ,而Na CO 热稳定性较强,利用二者热稳定性差异,
3 2 3 2 3
可从它们的固体混合物中除去NaHCO ,C正确;室温下,Na CO 和NaHCO 饱和溶液的pH相差较
3 2 3 3
大的主要原因是CO2−的水解程度远大于HCO−,D错误。
3 3
4.A 【解析】电解熔融氯化镁获得金属镁,B错误;饱和氯化钠溶液中通入氨气和二氧化碳制备碳酸氢
钠,C错误;硫酸工业中,二氧化硫与氧气反应得到三氧化硫,然后用98.3%的浓硫酸吸收,D错误。
5.A 【解析】草酸为弱酸,不拆为离子形式,草酸与酸性高锰酸钾溶液反应的离子方程式为
2MnO− +6H+ +5H C O =2Mn2+ +10CO ↑+8H O,A错误。
4 2 2 4 2 2
6.D 【解析】氢氧化亚铁容易被氧气氧化,制备时应注意隔绝空气,故A错误;过氧化钠和水反应过
于剧烈,过氧化钠也不能保持固体的状态,会溶于水中,该反应不适宜使用启普发生器,故B错误;给固
体加热时,试管的管口应稍向下倾斜,以防水回流到试管底部使试管炸裂,故C错误;铝热法是一种利用
铝的还原性获得高熔点金属单质的方法,铝可以将铁单质还原出来,装置中的氯酸钾作为引燃剂,其作用
是分解提供氧气,使镁条快速充分燃烧,为铝热反应提供高温条件,铝热反应产物的承接器是装有沙子的
蒸发皿,故D正确。
7.B 【解析】氢氧化铝沉淀不溶于氨水,A错误;氯离子也可以被酸性高锰酸钾溶液氧化,导致酸性高
锰酸钾溶液的紫色褪去,无法证明Fe2+的还原性,C错误;NaHCO 溶液中加入澄清石灰水也会产生
3
CaCO 白色沉淀,无法鉴别,D错误。
3
8.D 【解析】由电对的标准电极电势越高,其中氧化剂的氧化性越强可知,氧化剂的氧化性由强到弱的
学科网(北京)股份有限公司顺序为PbO >MnO− >Cl >Fe3+。Cl 的氧化性强于Fe3+,Fe3+不能与Cl−反应生成Cl ,A错误;
2 4 2 2 2
MnO−的氧化性强于Cl ,MnO−能与盐酸发生氧化还原反应生成Cl ,则酸化高锰酸钾时不能用盐酸,
4 2 4 2
B错误;还原性:Fe2+ >Cl−,FeCl 溶液与少量PbO 混合时,还原性强的Fe2+先与PbO 反应,根据
2 2 2
FeCl 与PbO 的量可知不会有黄绿色气体生成,C错误;PbO 的氧化性强于MnO−,PbO 能将Mn2+
2 2 2 4 2
氧化成MnO−,自身转化为PbSO 沉淀,反应的离子方程式为
4 4
5PbO +2Mn2+ +5SO2− +4H+ =5PbSO +2MnO− +2H O,D正确。
2 4 4 4 2
9.A 【解析】两个为对比实验,通过实验现象的不同可知,实验Ⅰ中Fe(Ⅱ)浓度较大,Fe2+和
SCN−能形成无色络离子,会促进FeCO 沉淀的溶解,使FeCO 在KSCN溶液中的溶解度大于FeCO 在
3 3 3
KCl溶液中的溶解度,据此分析。盐效应的实质是阴、阳离子之间的静电吸引力,促进平衡向溶解方向移
动,A正确;根据盐效应的影响因素可知,KSCN和KCl的阳离子相同、阴离子所带电荷数相等,在浓度
相同条件下,它们的盐效应相近,B错误;实验Ⅰ最终产生红褐色沉淀,说明对应的滤液中含有Fe(Ⅱ)
总浓度较大,实验Ⅱ中Fe(Ⅱ)总浓度较小,C错误;通过实验说明,Fe2+和SCN−能形成无色络离子,
D错误。
10.B 【解析】若a在沸水中可生成e,此时a为Mg,e为Mg ( OH ) ,即f为镁盐,a→f的反应有多
2
△
种,可能为Mg+2HCl=MgCl +H ↑,该反应属于置换反应,可能为Mg+Cl MgCl ,该反
2 2 2 2
应属于化合反应,综上,a→f的反应不一定是化合反应,故A错误;e能转化为d,此时e为白色沉淀
Fe ( OH ) ,d为红褐色沉淀Fe ( OH ) ,说明在g→f→e→d转化过程中,一定存在物质颜色的变化,故B
2 3
正确;由题意知,此时能产生丁达尔效应的红棕色分散系为Fe ( OH ) 胶体,c应为铁盐,加热铁盐的饱和
3
溶液,也有可能直接得到Fe ( OH ) 沉淀,故C错误;假设b为Al O ,即d为Al ( OH ) ,c为铝盐,
3 2 3 3
Al O 、Al ( OH ) 与稀盐酸反应均生成铝盐,此时组成a的元素为Al,位于周期表p区;假设b为
2 3 3
Fe O ,即d为Fe ( OH ) ,c为铁盐,Fe O 、Fe ( OH ) 与稀盐酸反应均生成铁盐,此时组成a的元素
2 3 3 2 3 3
为Fe,位于周期表d区,故D错误。
11.C 【解析】本题利用Li和液氨反应:Li+nNH
3
=Li+ +
e ( NH
3
)
n
− 制备
e ( NH
3
)
n
− ;碱石灰
可以吸收浓氨水中的水分,同时吸水过程大量放热,使浓氨水受热分解产生氨气;利用集气瓶收集氨气;
过量的氨气进入双口烧瓶中在冷却体系中发生反应生成e ( NH ) − ;最后的球形干燥管中可装PO ,
3 n 2 5
除掉过量的氨气,同时防止空气中的水进入引起副反应。碱石灰为生石灰和氢氧化钠的混合物,可以吸收
学科网(北京)股份有限公司浓氨水中的水分,同时吸水过程大量放热,有利于NH 逸出,A正确;锂片表面有Li O,Li O会阻碍
3 2 2
Li和液氨的接触,所以必须打磨出新鲜表面,B正确;第一个干燥管的作用是干燥氨气,PO 为酸性干
2 5
燥剂,能与氨气反应,所以不能用PO ,而装置末端的干燥管的作用为吸收过量的氨气,可用PO ,C
2 5 2 5
错误。
12.C 【解析】“浸铜”时,铜屑不能溶解完全,Cu在“脱氯”步骤还需要充当还原剂,故A错误;“浸
铜”时,铜屑中加入H SO 和H O 得到Cu2+,反应的离子方程式为
2 4 2 2
Cu+2H+ +H O =Cu2+ +2H O,故B错误;“脱氯”步骤中仅铜元素的化合价发生改变,得到CuCl
2 2 2
固体,即Cu的化合价升高,Cu2+的化合价降低,发生归中反应,离子方程式为
Cu2+ +Cu+2Cl− =2CuCl,故C正确;脱氯液净化后电解,Zn2+应在阴极得到电子变为Zn,故D错
误。
13.C 【解析】根据极限思想,1molCuSO 分解产生的氧气应小于0.75mol,C错误。
4
14.B 【解析】a~b段生成红褐色沉淀,即生成了氢氧化铁沉淀,反应的离子方程式为
2Fe2+ +ClO− +5H O=2Fe ( OH ) ↓+Cl− +4H+,故A正确;d~e段溶液变黄,说明生成了铁离子,反
2 3
应的离子方程式为2Fe2+ +ClO− +2H+ =2Fe3+ +Cl− +H O,故B错误;c、f点NaClO过量,NaClO
2
水解使溶液显碱性,水解的离子方程式为ClO− +H O HClO+OH−,故C正确;盐酸与氢氧化铁反
2
应生成氯化铁,盐酸与次氯酸钠反应生成氯气,所以加入过量的盐酸,沉淀溶解并有刺激性气味的气体放
出,故D正确。
二、非选择题(本题共 4小题,共 58分。)
15.(16分,每空2分)
(1)Na CO +2Na S+4SO =3Na S O +CO
2 3 2 2 2 2 3 2
(2)①CO +NH +NaCl+H O= NaHCO ↓+NH Cl ②B
2 3 2 3 4
(3)①NaOH、Na CO ②减弱 发生中和反应,溶液中的离子总数不变,溶液体积增大,导致溶液的
2 3
导电性减弱 ③0.15mol/L
16.(14分,每空2分)
(1)1:1 H S
2
(2)热浸
(3)将过量的Fe3+还原为Fe2+
学科网(北京)股份有限公司(4)C Pb+2 [ AgCl ]− =2Ag+[ PbCl ]2−
2 4
(5)阳极
【解析】本题以铅精矿(含PbS、Ag S等)为主要原料提取金属Pb和Ag,“热浸”时,难溶的PbS和
2
Ag S转化为[ PbCl ]2− 和[ AgCl ]− 及单质硫,Fe3+被还原为Fe2+,“过滤Ⅰ”除掉单质硫滤渣,滤液中
2 4 2
[ PbCl ]2− 在“稀释、冷却”的过程中转化为PbCl 沉淀,然后用饱和食盐水“热溶”,增大氯离子浓度,
4 2
使PbCl 又转化为[ PbCl ]2− ,电解得到Pb;“过滤Ⅱ”后的滤液成分主要为[ AgCl ]− 、FeCl 、
2 4 2 2
FeCl ,故加入铅精矿将FeCl 还原为FeCl ,试剂X将[ AgCl ]置换为Ag,得到富银铅泥,试剂X为
3 3 2 2
铅,尾液主要成分为FeCl 。
2
(1)“热浸”时,Fe3+将PbS和Ag S中−2价的硫氧化为单质硫,Fe3+被还原为Fe2+,在这个过程中
2
Pb和Ag的化合价保持不变,所以溶解等物质的量的PbS和Ag S时,S2−物质的量相等,消耗Fe3+的物
2
质的量相等,比值为1:1;溶液中盐酸浓度过大,这里主要考虑氢离子浓度过大,会生成H S气体。
2
(2)“过滤Ⅱ”得到的PbCl 沉淀反复用饱和食盐水“热溶”,会溶解为[ PbCl ]2− ,电解[ PbCl ]2− 溶液
2 4 4
制备金属Pb,Pb在阴极产生,阳极Cl−放电产生Cl ,尾液成分为FeCl ,FeCl 吸收Cl 后转化为
2 2 2 2
FeCl ,可以在“热浸”步骤中循环使用。
3
(3)“过滤Ⅱ”所得的滤液中有过量的未反应的Fe3+,根据“还原”之后可以得到含硫滤渣,“还原”中
加入铅精矿的目的是将过量的Fe3+还原为Fe2+。
(4)“置换”中加入试剂X可以得到富银铅泥,为了防止引入其他杂质,则试剂X应为Pb,发生的反应
为Pb+2 [ AgCl ]− =2Ag+[ PbCl ]2− 。
2 4
学科网(北京)股份有限公司