文档内容
白城一中2025-2026学年度高二上学期第一次月考
化学试卷
一、选择题(本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,
只有一项符合题目要求)
1.将零散的化学知识整理归纳,得出一般的规律,是学好化学的方法之一,以下归纳中全部正确
的是( )
A. 物质的组成、结构和性质关系归纳:①原子的核内质子数决定了元素的种类;②元素的化学性
质与原子最外层电子数目关系密切;③原子是化学变化中的最小粒子,因此在化学反应中原子不
可再分;④物质是由分子、原子、离子等粒子构成的
B. 物质的属类归纳:①蔗糖、酒精、甲烷等这类含碳化合物称为有机化合物;②由金属离子和酸
根离子组成的化合物称为盐;③由同种元素组成的物质称为单质;④含氧元素的化合物称为氧化
物
C. 实验方法归纳:①玻璃容器都可用作反应容器;②制取气体时,应先检查装置的气密性;③加
热试管里的固体或液体,先要预热;④点燃可燃性气体前必须检验气体纯度
D. 物质俗称归纳:①干冰是固态二氧化碳;②纯碱是碳酸钠;③石灰水是氢氧化钙;④天然气的
主要成分是甲烷
2.下列反应中,不属于氧化还原反应的是( )
A. 2NO +2NaOH===NaNO +NaNO +HO B. SO +HO===HSO
2 2 3 2 2 2 2 2 4
C. 3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO D. CaCO CaO+CO↑
3 3 2 2 3 2
3.不同的金属在冶炼方法上也有所不同,下列说法不正确的是( )
A. 锰、铁等难熔金属通常采用铝热法炼制 B. 电解熔融态氯化铝可以冶炼铝单质
C. 银采用热分解法冶炼 D. 沙里淘金是物理变化
4.SCR法是工业上消除氮氧化物的常用方法,反应原理为 4NH (g)+4NO(g)+O(g) 4N(g)
3 2 2
+6HO(g) ΔH<0。该法可能发生副反应4NH (g)+5O(g) 4NO(g)+6HO(g)。投料比一定
2 3 2 2
时,下列说法中不正确的是( )
A. 提高NO平衡转化率的条件是高温高压
B. 提高NO平衡转化率的条件是低温低压
C. 减少副反应的措施是选择合适的催化剂
D. 减少副反应的措施是控制O 的用量
2
5.下列反应的离子方程式中,书写正确的是( )
A. 将绿豆大的钠加入FeCl 溶液中:6Na+2Fe3+=6Na++2Fe
3B. NH HCO 溶于过量的NaOH溶液中:HCO-+OH-=CO2-+H O
4 3 3 3 2
C. 硝酸银溶液与铜反应:Cu+Ag+=Cu2++Ag
D. 用小苏打治疗胃酸过多:HCO-+H+=CO ↑+H O
3 2 2
6.宏观辨识和微观探析是化学学科的核心素养之一,下列相关描述中正确的是( )
A. P
4
(白磷,s)=4P(红磷,s) ΔH=-29.2kJ⋅mol-1,则白磷比红磷稳定
B. 表示C
2
H
4
燃烧热的热化学方程式C
2
H
4
(g)+3O
2
(g)=2CO
2
(g)+2H
2
O(g) ΔH=-1411.0 kJ⋅
mol-1
C. 已知稀溶液中H+ (aq)+OH- (aq)=H O(1) ΔH=-57.3 kJ⋅mol-1,则稀硫酸与稀氢氧化钡溶液
2
反应生成1 mol水时放出57.3 kJ的热量
D. 已知500℃、30 MPa下,N (g)+3H (g)⇌2NH (g) ΔH=-92.4 kJ⋅mol-1,则相同条件下
2 2 3
1 mol N 和3 moI H 充分反应,放出热量小于92.4 kJ
2 2
7.下列物质用途不正确的是( )
A. NaHCO -制玻璃 B. Cl-制消毒液
3 2
C. Fe O-油漆 D. Al O-耐高温材料
2 3 2 3
8.人体中因缺少或过多会患甲状腺疾病的元素是( )
A. I B. Na C. Fe D. Cl
9.用N 表示阿伏加德罗常数的数值,下列说法正确的是( )
A
A. 7 g乙烯在空气中完全燃烧生成水和二氧化碳时转移的电子数为3N
A
B. 在标准状况下,11.2 L丙烷含有的极性键数目为5N
A
C. 1 mol葡萄糖(C H O)分子含有的羟基数目为6N
6 12 6 A
D. 常温下,22.4 L苯中含有的碳原子数等于0.6N
A
10.下列无机非金属材料的主要成分是二氧化硅的是( )
A. 华为手机的麒麟芯片 B. 通讯使用的光导纤维
C. 汽车上使用的钢化玻璃 D. 白鹤滩水电站使用的水泥
11.化学与社会、科学、技术、生活等密切相关,下列说法错误的是( )
A. N95型口罩的核心材料聚丙烯能使酸性高锰酸钾溶液褪色
B. “天街小雨润如酥,草色遥看近却无”,pH<5.6的雨水为酸雨,会对植物造成巨大危害
C. 在三星堆“祭祀坑”提取到丝绸制品的残留物,其中丝绸主要成分为蛋白质
D. “天和”核心舱腔体使用的氮化硼陶瓷基复合材料,氮化硼陶瓷属于新型无机非金属材料
12.下列关于催化剂的说法正确的是( )A. 任何化学反应都需要催化剂 B. 化学反应中的催化剂一般并不唯一
C. 催化剂对化学反应历程无影响 D. 催化剂的化学性质在反应前后会发生改变
13.砷为第四周期第VA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是(
)
A. 砷在通常情况下是固体 B. 可以存在-3、+3、+5等多种化合价
C. 砷的最高价氧化物对应水化物的酸性比HPO 弱 D. 砷的气态氢化物比磷的气态
3 4
氢化物稳定
14.已知2HO(l)===2HO(l)+O(g) ΔH=-98 kJ·mol-1。在含少量I-的溶液中,HO 的分解
2 2 2 2 2 2
反应过程为ⅰ.HO(l)+I-(aq)===HO(l)+IO-(aq) ΔH
2 2 2 1
ⅱ.HO(l)+IO-(aq)===HO(l)+O(g)+I-(aq) ΔH
2 2 2 2 2
下列说法不正确的是( )
A. ΔH+ΔH=ΔHB. I-是HO 分解反应的催化剂
1 2 2 2
C. 欲分解2 mol HO(l),至少需要提供98 kJ的热量 D. 若生成1 mol O ,则反应ⅱ
2 2 2
转移电子的物质的量为2 mol
15.工业上制备相关物质,涉及的反应原理及部分流程较为合理的是( )
Cl 2Br 热空气吹出SO 2 吸收溴蒸汽HBr溶液Cl 2Br
A. 制溴:浓缩海水 2 2
石灰乳 盐酸 电解
MgOH MgCl 溶液Mg
B. 制镁:海水 2 2
先通CO 2NaHCO ΔNa CO
C. 制纯碱:饱和食盐水 再通NH 3 2 3
3
H2 O/浸泡浸泡液H2 SO4 /H2 O 2碘水萃取I
D. 制碘:干海带 2,其中萃取剂可以选取乙醇
二、非选择题(本大题共4小题,共55分)
16.纳米磁性Fe O 在生物靶向材料、微波吸收材料及静电复印显影剂等方面都有极其广泛的用途。
3 4
一种利用废旧镀锌铁皮制备纳米磁性Fe O 的工艺流程如下:
3 4
已知:镀锌铁皮就是铁皮表面镀上一层锌;Zn溶于强碱时生成[Zn(OH) ]
2-
。
4
(1)“碱洗”废旧镀锌铁皮的目的是_______(填字母)。A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化铁皮
(2)“酸溶”后的溶液中阳离子主要有 。
(3)“氧化”时发生的总反应离子方程式为 。在酸性条件下,FeSO 很容易
4
发生反应:4FeSO +O +6H O=4FeOOH+4H SO 。为避免生成FeOOH影响产品纯度,则“氧
4 2 2 2 4
化”时应选择的加料方式为 。
(4)“氧化”后溶液中Fe2+ 、Fe3+的物质的量之比是1∶2,检验其中Fe3+可选用的试剂是_______。
A.HSO 溶液 B.KSCN溶液 C.酸性KMnO 溶液 D.Cu
2 4 4
(5)“分离”时Fe O 纳米粒子不能采用过滤法实现固液分离,理由是 。
3 4
(6)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe O 中的二价铁含量。若需配制浓度为
3 4
0.01000 mol·L-1的K Cr O 标准溶液240mL,应准确称取 g K Cr O (保留4位有效数
2 2 7 2 2 7
字,已知M(K Cr O )=294.0 g·mol-1 )。
2 2 7
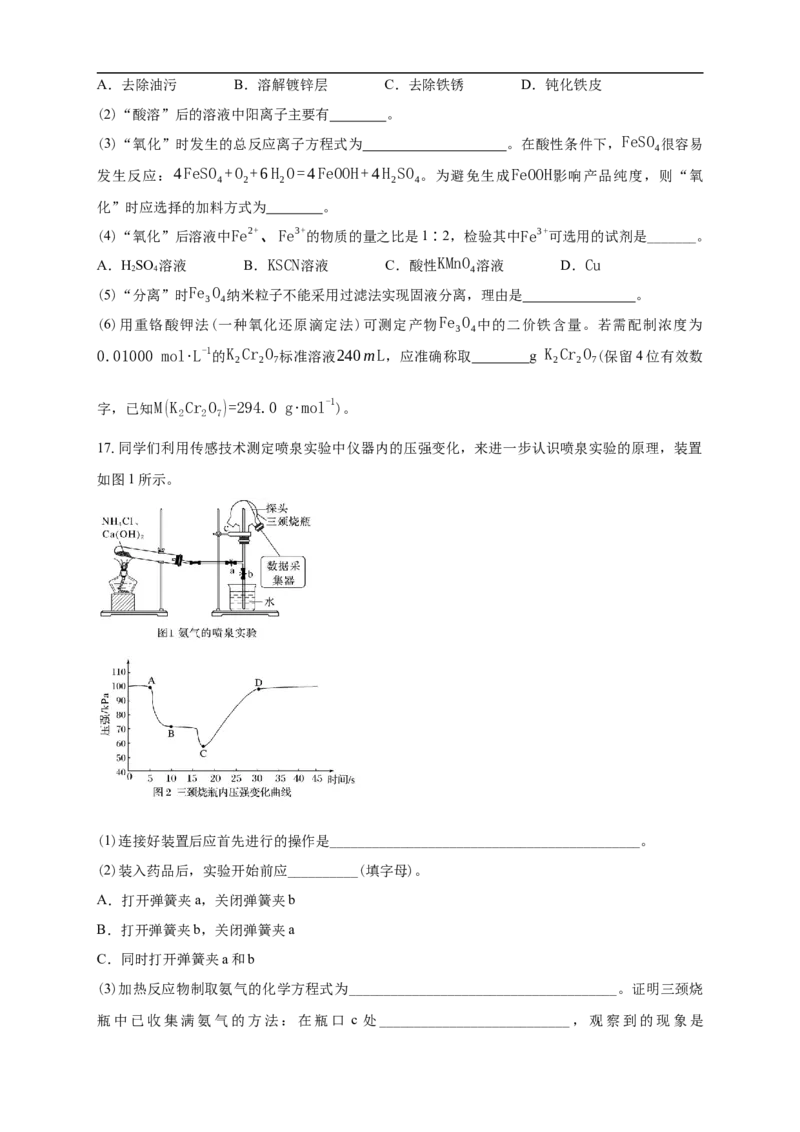
17.同学们利用传感技术测定喷泉实验中仪器内的压强变化,来进一步认识喷泉实验的原理,装置
如图1所示。
(1)连接好装置后应首先进行的操作是____________________________________________。
(2)装入药品后,实验开始前应__________(填字母)。
A.打开弹簧夹a,关闭弹簧夹b
B.打开弹簧夹b,关闭弹簧夹a
C.同时打开弹簧夹a和b
(3)加热反应物制取氨气的化学方程式为______________________________________。证明三颈烧
瓶中已收集满氨气的方法:在瓶口 c 处___________________________,观察到的现象是___________________________________________________。
(4)停止加热后,引发喷泉的操作是:关闭弹簧夹______(填“a”或“b”),用带有胶头滴管(预先
吸入水)的橡胶塞塞紧瓶口c,打开弹簧夹________(填“a”或“b”),挤压胶头滴管,使水进入
烧瓶,形成喷泉,此实验利用了氨气具有________的性质。由数据采集器和电脑绘制的三颈烧瓶
内压强变化曲线如图2,其中________(填字母)点所对应的是喷泉最剧烈的时刻。
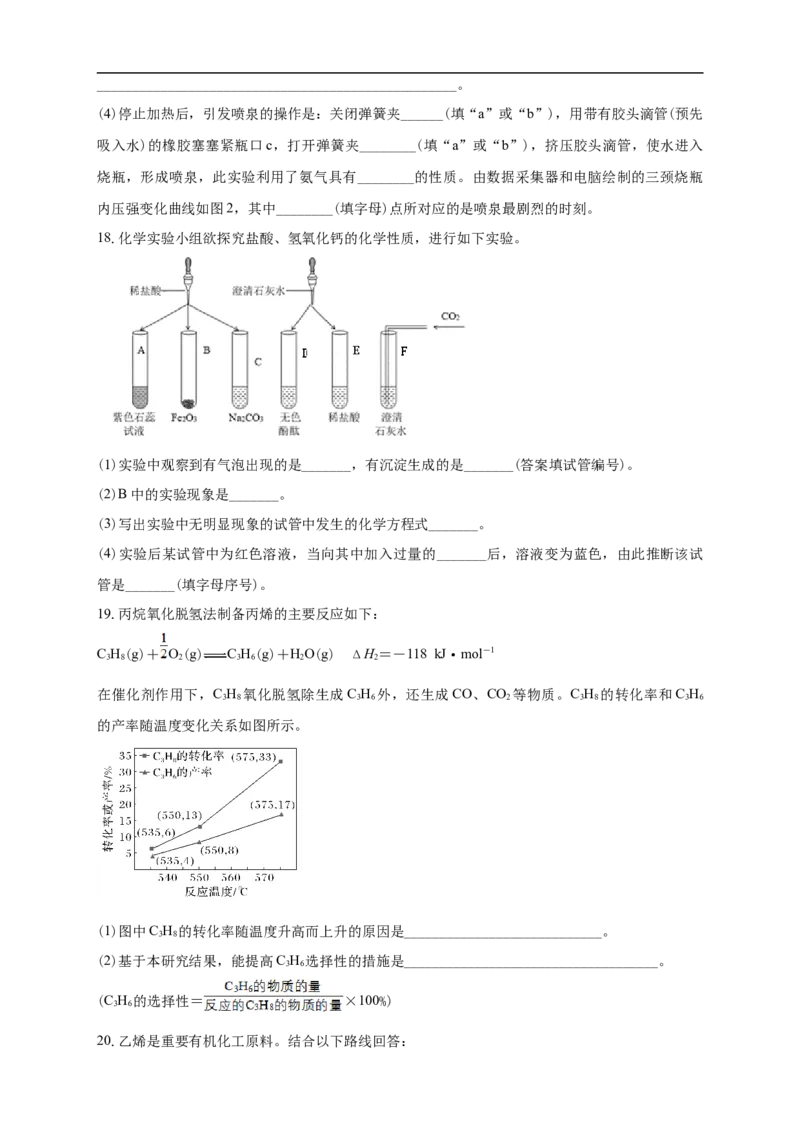
18.化学实验小组欲探究盐酸、氢氧化钙的化学性质,进行如下实验。
(1)实验中观察到有气泡出现的是_______,有沉淀生成的是_______(答案填试管编号)。
(2)B中的实验现象是_______。
(3)写出实验中无明显现象的试管中发生的化学方程式_______。
(4)实验后某试管中为红色溶液,当向其中加入过量的_______后,溶液变为蓝色,由此推断该试
管是_______(填字母序号)。
19.丙烷氧化脱氢法制备丙烯的主要反应如下:
C H(g)+ O(g) C H(g)+HO(g) ΔH=-118 kJ·mol-1
3 8 2 3 6 2 2
在催化剂作用下,C H 氧化脱氢除生成C H 外,还生成CO、CO 等物质。C H 的转化率和C H
3 8 3 6 2 3 8 3 6
的产率随温度变化关系如图所示。
(1)图中C H 的转化率随温度升高而上升的原因是____________________________。
3 8
(2)基于本研究结果,能提高C H 选择性的措施是____________________________________。
3 6
(C H 的选择性= ×100%)
3 6
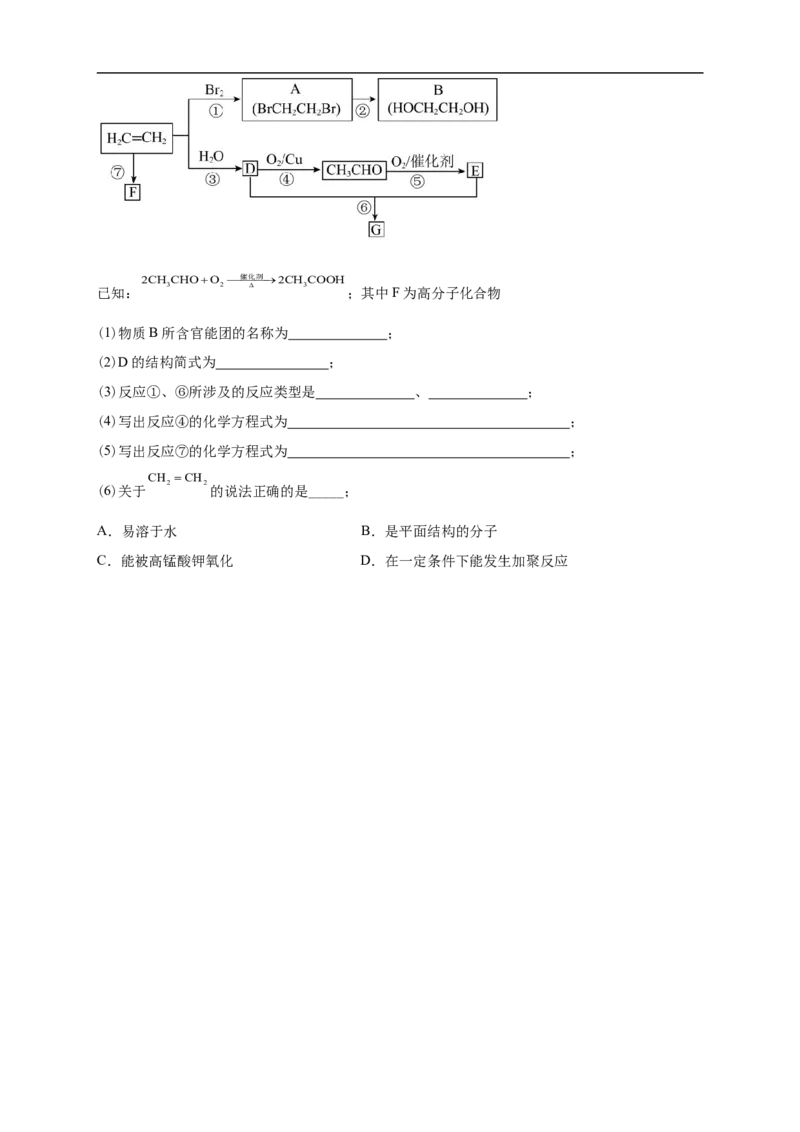
20.乙烯是重要有机化工原料。结合以下路线回答:2CH CHOO 催化剂2CH COOH
已知: 3 2 3 ;其中F为高分子化合物
(1)物质B所含官能团的名称为 ;
(2)D的结构简式为 ;
(3)反应①、⑥所涉及的反应类型是 、 ;
(4)写出反应④的化学方程式为 ;
(5)写出反应⑦的化学方程式为 ;
CH CH
2 2
(6)关于 的说法正确的是_____;
A.易溶于水 B.是平面结构的分子
C.能被高锰酸钾氧化 D.在一定条件下能发生加聚反应