文档内容
2021年枣庄市初中学业水平考试
65
化学
(满分:50分 考试时间:与物理共用120分钟)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Ca 40
第Ⅰ卷 选择题(共16分)
一、选择题
13 14 15 16 17 18 19 20
13.(2021山东枣庄,13,2分)2021年3月29日是第26个全国中小学生安全教育日。下列标识与安全无关的是
( )
13.D 腐蚀品、禁止火种、爆炸品标识都与安全有关,图D是节约用水标识,与安全无关。
14.(2021山东枣庄,14,2分)“冠世榴园”是枣庄打造全域旅游城市的一张名片。石榴营养丰富,含有维生素C、蛋
白质、糖类、脂肪,以及钙、磷、钾等矿物质。下列说法错误的是( )
A.石榴中钙、磷、钾是指单质
B.人体缺乏维生素C,会引起坏血病
C.蛋白质遇到重金属盐会失去生理活性
D.糖类与脂肪的组成元素相同,但分子结构不同
14.A 石榴中钙、磷、钾指的是元素,故A错误;人体缺乏维生素C,会引起坏血病,故B正确;重金属盐能使蛋白质
失去活性,故C正确;糖类和脂肪都是由C、H、O元素组成的,但分子结构不同,故D正确。
15.(2021山东枣庄,15,2分)下列为四种食物的近似pH,其中酸性最强的是 ( )
食物 牛奶 豆浆 苹果汁 鸡蛋清
pH 6.3~6.6 7.4~7.9 2.9~3.3 7.6~8.0
A.牛奶 B.豆浆
C.苹果汁 D鸡蛋清
15.C pH越大碱性越强,pH越小酸性越强,故选C。
16.(2021山东枣庄,16,2分)3月22日是“世界水日”,2021年的主题为“珍惜水、爱护水”。下列有关水的说法错
误的是 ( )
A.硬水软化常用肥皂水
B.海水淡化可用蒸馏法
C.河水净化中活性炭起吸附作用
D.水汽化过程中分子间隔变大
16.A 肥皂水只能检验硬水和软水,不能将硬水软化,故A错误;蒸馏可以将海水变为蒸馏水,使海水淡化,故B正确;
活性炭在河水的净化中起吸附作用,故C正确;水汽化是由液态变为气态,分子间隔变大,故D正确。
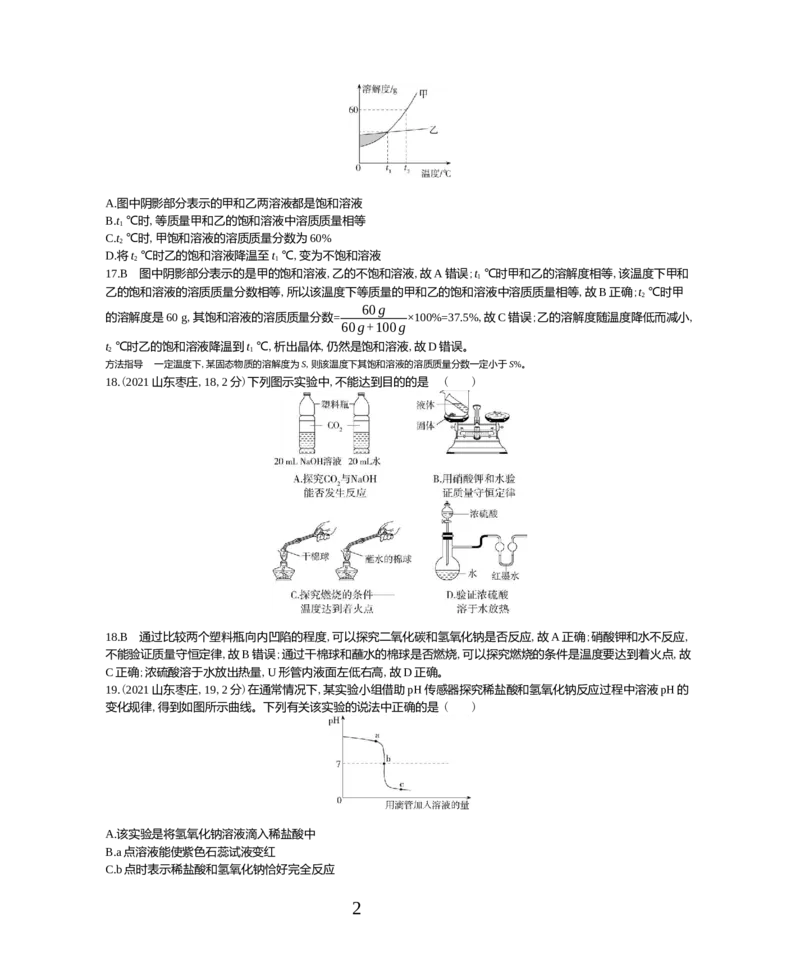
17.(2021山东枣庄,17,2分)如图是甲和乙两种物质(不含结晶水)的溶解度曲线。下列说法正确的是( )
1A.图中阴影部分表示的甲和乙两溶液都是饱和溶液
B.t ℃时,等质量甲和乙的饱和溶液中溶质质量相等
1
C.t ℃时,甲饱和溶液的溶质质量分数为60%
2
D.将t ℃时乙的饱和溶液降温至t ℃,变为不饱和溶液
2 1
17.B 图中阴影部分表示的是甲的饱和溶液,乙的不饱和溶液,故A错误;t ℃时甲和乙的溶解度相等,该温度下甲和
1
乙的饱和溶液的溶质质量分数相等,所以该温度下等质量的甲和乙的饱和溶液中溶质质量相等,故B正确;t ℃时甲
2
60g
的溶解度是60 g,其饱和溶液的溶质质量分数= ×100%=37.5%,故C错误;乙的溶解度随温度降低而减小,
60g+100g
t ℃时乙的饱和溶液降温到t ℃,析出晶体,仍然是饱和溶液,故D错误。
2 1
方法指导 一定温度下,某固态物质的溶解度为S,则该温度下其饱和溶液的溶质质量分数一定小于S%。
18.(2021山东枣庄,18,2分)下列图示实验中,不能达到目的的是 ( )
18.B 通过比较两个塑料瓶向内凹陷的程度,可以探究二氧化碳和氢氧化钠是否反应,故A正确;硝酸钾和水不反应,
不能验证质量守恒定律,故B错误;通过干棉球和蘸水的棉球是否燃烧,可以探究燃烧的条件是温度要达到着火点,故
C正确;浓硫酸溶于水放出热量,U形管内液面左低右高,故D正确。
19.(2021山东枣庄,19,2分)在通常情况下,某实验小组借助pH传感器探究稀盐酸和氢氧化钠反应过程中溶液pH的
变化规律,得到如图所示曲线。下列有关该实验的说法中正确的是( )
A.该实验是将氢氧化钠溶液滴入稀盐酸中
B.a点溶液能使紫色石蕊试液变红
C.b点时表示稀盐酸和氢氧化钠恰好完全反应
2D.c点时,溶液中的溶质只有氯化钠
19.C pH逐渐变小,说明是将稀盐酸滴入氢氧化钠溶液中,故A错误;a点的pH大于7,溶液显碱性,能使紫色石蕊试
液变蓝,故B错误;b点的pH等于7,说明稀盐酸和氢氧化钠恰好完全反应,故C正确;c点的pH小于7,说明稀盐酸过
量,溶液中的溶质是NaCl和HCl,故D错误。
方法指导 中和反应时,pH逐渐减小,是把酸溶液滴入碱溶液中;pH逐渐变大,是把碱溶液滴入酸溶液中。
20.(2021山东枣庄,20,2分)向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤渣和滤液,
滤液呈蓝色。下列说法正确的是 ( )
A.滤渣中一定有Ag、Cu
B.滤液中一定有Cu2+、Zn2+
C.向滤渣中滴加稀盐酸一定有气泡产生
D.向滤液中加入稀盐酸一定有沉淀生成
20.B 向硝酸银和硝酸铜的混合溶液中加入一定量的锌,锌先和硝酸银反应,硝酸银反应完后,再和硝酸铜反应。滤
液呈蓝色,说明滤液中有硝酸铜,不能证明硝酸铜是否反应,所以滤渣中一定有Ag,可能含有Cu,故A错误;结合A项
分析可知,滤液中一定有反应生成的Zn2+和未反应的Cu2+,故B正确;反应后有硝酸铜剩余,则滤渣中一定没有Zn,加
入稀盐酸一定没有气泡产生,故C错误;由分析知不能确定硝酸银是否反应完全,加入稀盐酸不一定有沉淀生成,故D
错误。
第Ⅱ卷 非选择题(共34分)
一、填空与简答题(本题包括5个小题,共30分)
33.(2021山东枣庄,33,4分)(4分)初中化学常见的四种物质:①浓盐酸 ②纯碱 ③烧碱 ④生石灰,选择适当的物
质填空(填序号)。
(1)化学式为NaOH的是 。
(2)主要成分属于盐的是 。
(3)能与水发生化合反应的是 。
(4)可用作除锈剂的是 。
33.答案 (1)③ (2)② (3)④ (4)①
解析 (1)氢氧化钠的俗称为烧碱、火碱、苛性钠。
(2)纯碱是碳酸钠的俗称,属于盐。
(3)生石灰是氧化钙的俗称,能和水发生化合反应生成氢氧化钙。
(4)盐酸可和铁锈反应生成可溶性的铁盐和水,可以用来除锈。
34.(2021山东枣庄,34,5分)(5分)2021年5月15日,中国“天问一号”探测器成功着陆火星,它应用的新型镁锂合金
材料是由西安四方超轻材料有限公司自主研发。
回答下列问题:
(1)镁锂合金硬度比其纯金属的硬度 (填“大”或“小”)。
(2)
图1
3图2
图1为镁在元素周期表中的部分信息,则镁的相对原子质量为 。
图2为几种粒子的结构示意图,其中属于同种元素的是 (填序号),与镁元素化学性质相似的是 (填序
号)。
(3)锂原子(Li)在反应中易失去1个电子形成锂离子,写出锂离子的符号: 。
34.答案 (1)大 (2)24.31 ①④ ③ (3)Li+
解析 (1)合金的硬度和耐腐蚀性比纯金属大。
(2)从图1信息可知,镁的相对原子质量是24.31。①和④的质子数相同,属于同种元素,③和镁原子的最外层电子数
相同,化学性质相似。
(3)锂原子失去一个电子形成锂离子,符号为Li+。
35.(2021山东枣庄,35,7分)(7分)2020年9月22日,国家主席习近平在第75届联合国大会上宣布:中国二氧化碳排
放力争2030年前达到峰值,2060年前实现“碳中和”。为达成这一目标,一方面要减少碳排放,另一方面要尽量吸收
不可避免的碳排放。
(1)生活中我们要树立“低碳”理念,下列符合这一理念的是 (填字母)。
A.露天焚烧秸秆
B.使用节能电器
C.大力发展火力发电
D.减少使用一次性筷子等用品
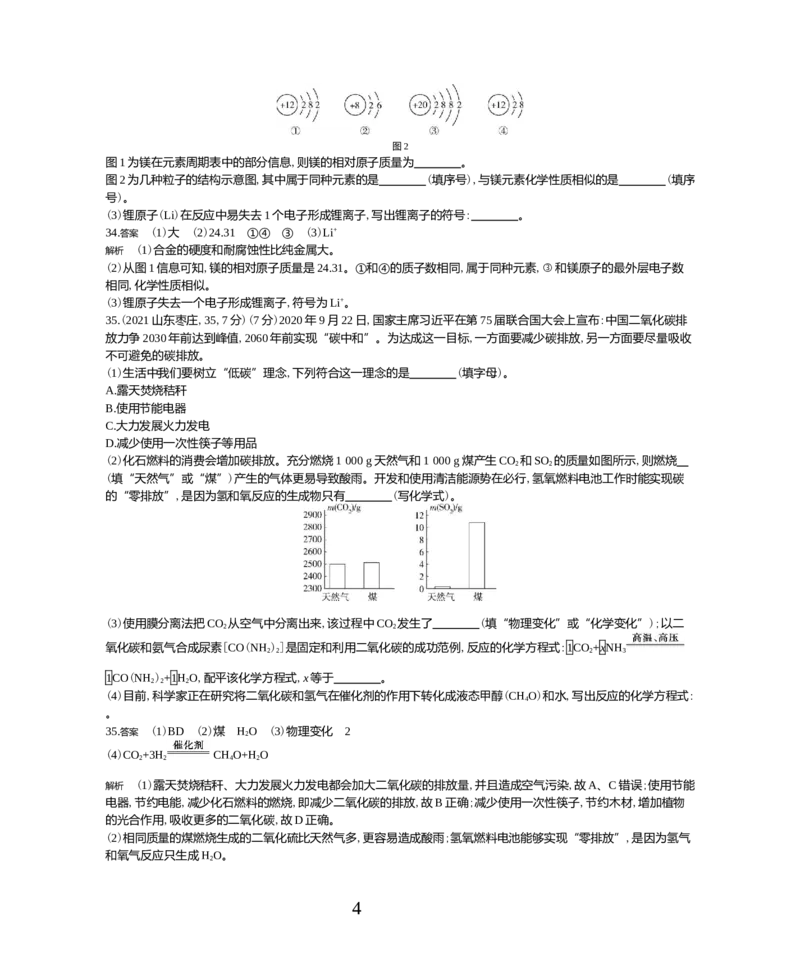
(2)化石燃料的消费会增加碳排放。充分燃烧1 000 g天然气和1 000 g煤产生CO 和SO 的质量如图所示,则燃烧
2 2
(填“天然气”或“煤”)产生的气体更易导致酸雨。开发和使用清洁能源势在必行,氢氧燃料电池工作时能实现碳
的“零排放”,是因为氢和氧反应的生成物只有 (写化学式)。
(3)使用膜分离法把CO 从空气中分离出来,该过程中CO 发生了 (填“物理变化”或“化学变化”);以二
2 2
氧化碳和氨气合成尿素[CO(NH)]是固定和利用二氧化碳的成功范例,反应的化学方程式:1CO+xNH
2 2 2 3
1CO(NH)+1HO,配平该化学方程式,x等于 。
2 2 2
(4)目前,科学家正在研究将二氧化碳和氢气在催化剂的作用下转化成液态甲醇(CHO)和水,写出反应的化学方程式:
4
。
35.答案 (1)BD (2)煤 H
2
O (3)物理变化 2
(4)CO+3H CHO+HO
2 2 4 2
解析 (1)露天焚烧秸秆、大力发展火力发电都会加大二氧化碳的排放量,并且造成空气污染,故A、C错误;使用节能
电器,节约电能,减少化石燃料的燃烧,即减少二氧化碳的排放,故B正确;减少使用一次性筷子,节约木材,增加植物
的光合作用,吸收更多的二氧化碳,故D正确。
(2)相同质量的煤燃烧生成的二氧化硫比天然气多,更容易造成酸雨;氢氧燃料电池能够实现“零排放”,是因为氢气
和氧气反应只生成HO。
2
4(3)使用膜分离法把二氧化碳从空气中分离出来,没有新物质生成,属于物理变化;根据反应前后原子的种类和数目不
变可知,x=2。
(4)二氧化碳和氢气在催化剂的作用下反应生成甲醇和水,化学方程式为CO+3H CHO+HO。
2 2 4 2
知识拓展 实现碳中和的战略基于以下几点:改善能源结构,减少碳排放;改变农业耕作方式,将更多碳固存在地下;在供应链中减少森林采伐,抵
消剩余的碳排放量。
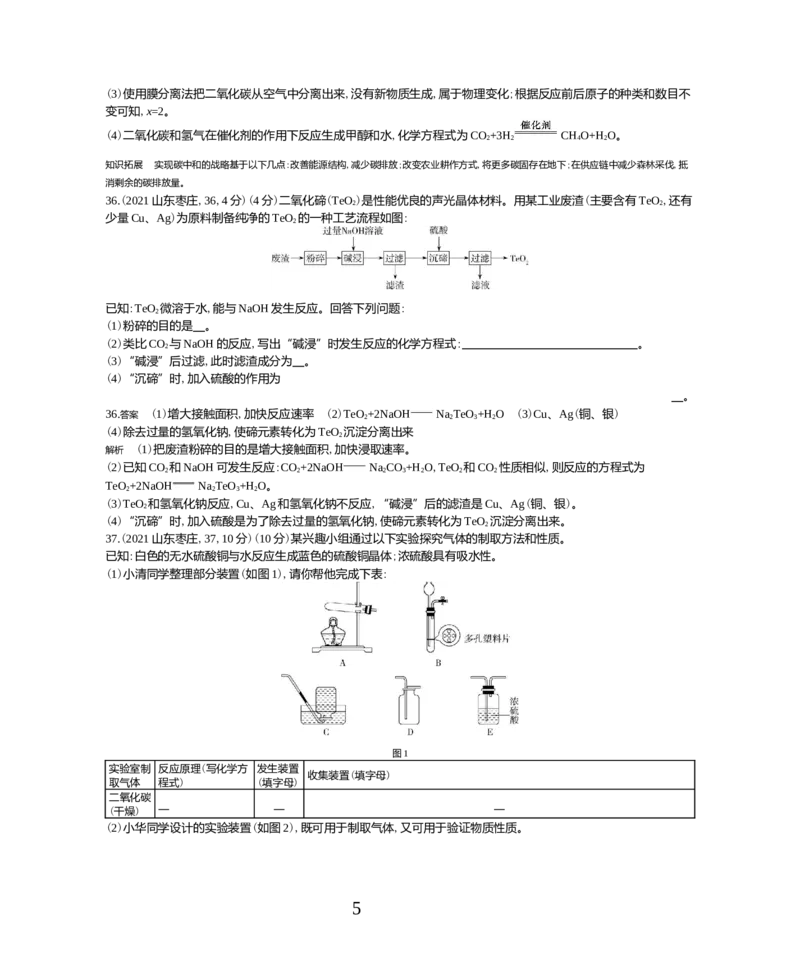
36.(2021山东枣庄,36,4分)(4分)二氧化碲(TeO)是性能优良的声光晶体材料。用某工业废渣(主要含有TeO,还有
2 2
少量Cu、Ag)为原料制备纯净的TeO 的一种工艺流程如图:
2
已知:TeO 微溶于水,能与NaOH发生反应。回答下列问题:
2
(1)粉碎的目的是 。
(2)类比CO 与NaOH的反应,写出“碱浸”时发生反应的化学方程式: 。
2
(3)“碱浸”后过滤,此时滤渣成分为 。
(4)“沉碲”时,加入硫酸的作用为
。
36.答案 (1)增大接触面积,加快反应速率 (2)TeO
2
+2NaOH Na
2
TeO
3
+H
2
O (3)Cu、Ag(铜、银)
(4)除去过量的氢氧化钠,使碲元素转化为TeO 沉淀分离出来
2
解析 (1)把废渣粉碎的目的是增大接触面积,加快浸取速率。
(2)已知CO 和NaOH可发生反应:CO+2NaOH NaCO+HO,TeO 和CO 性质相似,则反应的方程式为
2 2 2 3 2 2 2
TeO+2NaOH NaTeO+HO。
2 2 3 2
(3)TeO 和氢氧化钠反应,Cu、Ag和氢氧化钠不反应,“碱浸”后的滤渣是Cu、Ag(铜、银)。
2
(4)“沉碲”时,加入硫酸是为了除去过量的氢氧化钠,使碲元素转化为TeO 沉淀分离出来。
2
37.(2021山东枣庄,37,10分)(10分)某兴趣小组通过以下实验探究气体的制取方法和性质。
已知:白色的无水硫酸铜与水反应生成蓝色的硫酸铜晶体;浓硫酸具有吸水性。
(1)小清同学整理部分装置(如图1),请你帮他完成下表:
图1
实验室制 反应原理(写化学方 发生装置
收集装置(填字母)
取气体 程式) (填字母)
二氧化碳
(干燥)
(2)小华同学设计的实验装置(如图2),既可用于制取气体,又可用于验证物质性质。
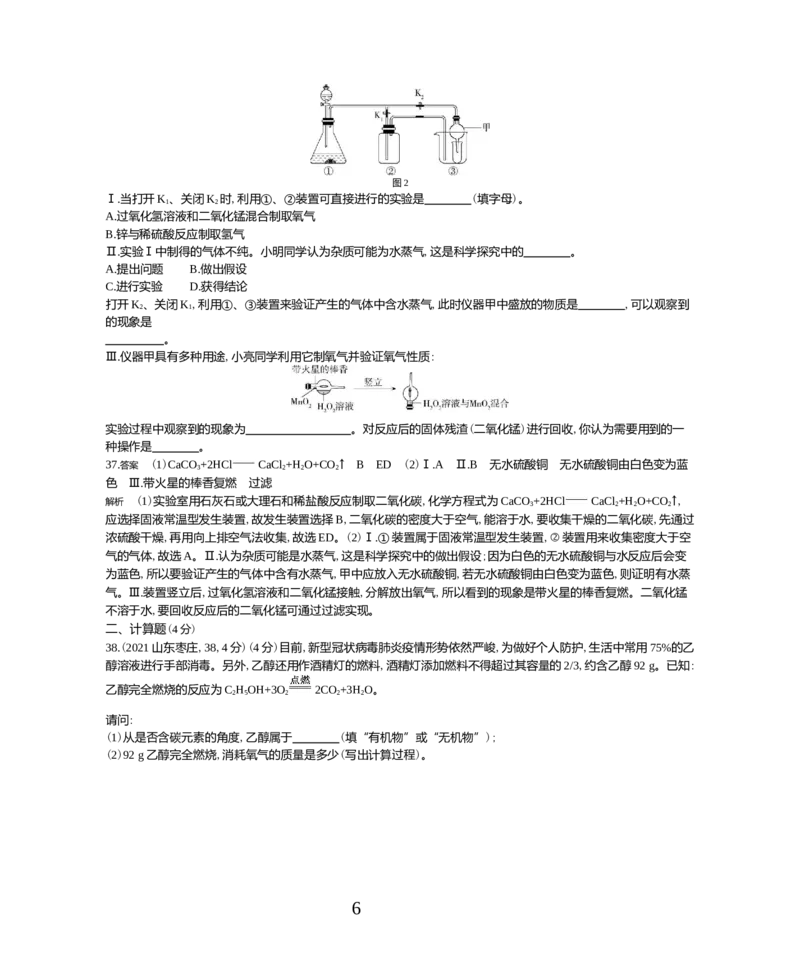
5图2
Ⅰ.当打开K、关闭K 时,利用①、②装置可直接进行的实验是 (填字母)。
1 2
A.过氧化氢溶液和二氧化锰混合制取氧气
B.锌与稀硫酸反应制取氢气
Ⅱ.实验Ⅰ中制得的气体不纯。小明同学认为杂质可能为水蒸气,这是科学探究中的 。
A.提出问题 B.做出假设
C.进行实验 D.获得结论
打开K、关闭K,利用①、③装置来验证产生的气体中含水蒸气,此时仪器甲中盛放的物质是 ,可以观察到
2 1
的现象是
。
Ⅲ.仪器甲具有多种用途,小亮同学利用它制氧气并验证氧气性质:
实验过程中观察到的现象为 。对反应后的固体残渣(二氧化锰)进行回收,你认为需要用到的一
种操作是 。
37.答案 (1)CaCO
3
+2HCl CaCl
2
+H
2
O+CO
2
↑ B ED (2)Ⅰ.A Ⅱ.B 无水硫酸铜 无水硫酸铜由白色变为蓝
色 Ⅲ.带火星的棒香复燃 过滤
解析 (1)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳,化学方程式为CaCO 3 +2HCl CaCl 2 +H 2 O+CO 2 ↑,
应选择固液常温型发生装置,故发生装置选择B,二氧化碳的密度大于空气,能溶于水,要收集干燥的二氧化碳,先通过
浓硫酸干燥,再用向上排空气法收集,故选ED。(2)Ⅰ.①装置属于固液常温型发生装置,②装置用来收集密度大于空
气的气体,故选A。Ⅱ.认为杂质可能是水蒸气,这是科学探究中的做出假设;因为白色的无水硫酸铜与水反应后会变
为蓝色,所以要验证产生的气体中含有水蒸气,甲中应放入无水硫酸铜,若无水硫酸铜由白色变为蓝色,则证明有水蒸
气。Ⅲ.装置竖立后,过氧化氢溶液和二氧化锰接触,分解放出氧气,所以看到的现象是带火星的棒香复燃。二氧化锰
不溶于水,要回收反应后的二氧化锰可通过过滤实现。
二、计算题(4分)
38.(2021山东枣庄,38,4分)(4分)目前,新型冠状病毒肺炎疫情形势依然严峻,为做好个人防护,生活中常用75%的乙
醇溶液进行手部消毒。另外,乙醇还用作酒精灯的燃料,酒精灯添加燃料不得超过其容量的2/3,约含乙醇92 g。已知:
乙醇完全燃烧的反应为CHOH+3O 2CO+3HO。
2 5 2 2 2
请问:
(1)从是否含碳元素的角度,乙醇属于 (填“有机物”或“无机物”);
(2)92 g乙醇完全燃烧,消耗氧气的质量是多少(写出计算过程)。
638.答案 (1)有机物
(2)解:设消耗氧气的质量为x。
CHOH+3O 3HO+2CO
2 5 2 2 2
46 96
92 g x
46 92g
=
96 x
x=192 g
答:消耗氧气的质量为192 g。
解析 (1)乙醇中含有碳元素,属于有机物。
78