文档内容
2024~2025 学年高三年级第一次质量检测
化学试题
(完卷时间75分钟;满分100分)
可能用到的相对原子质量:H−1 C−12 O−16 Zn−65
一、选择题:本题共 10 小题,每小题 4分,共 40分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.福建舰拥有世界上最先进的雷达系统,其雷达射频微波器件所用的碳化硅材料能实现电信号的可控改
变。下列关于碳化硅的说法错误的是( )。
A.C原子的杂化类型为sp3 B.属于高分子化合物
C.熔点高、硬度大 D.属于半导体材料
2.“扑热息痛”是重要的解热镇痛药,其结构如下。下列有关该物质的说法正确的是( )。
A.分子式为C H NO B.含有2种官能团
8 7 2
C.所有原子可能处于同一平面 D.能与溴水发生加成反应
3.寿山石的主要成分为Z
4
W
4
Y
10
( YX )
8
,X、Y、Z、W为四种原子序数递增的短周期不同族元素,X
是周期表中半径最小的原子,基态Y原子有2个未成对电子,W的L层电子数是M层的2倍。下列说法
正确的是( )。
A.原子半径Z<W B.简单氢化物的稳定性Y<W
C.电负性Z>X D.Z最高价氧化物的水化物呈两性
4.乙烯在Ag的催化作用下可发生反应:2CH =CH +O Ag→2 ,下列说法错误的是( )。
2 2 2
A.11.2L CH =CH 所含的原子数目为3N
2 2 A
B.1.4g CH =CH 中所含的电子数目为0.8N
2 2 A
C.1mol环氧乙烷中含有σ键的数目为7N
A
学科网(北京)股份有限公司D.常温常压下,16g O 发生反应时,转移电子的数目为2N
2 A
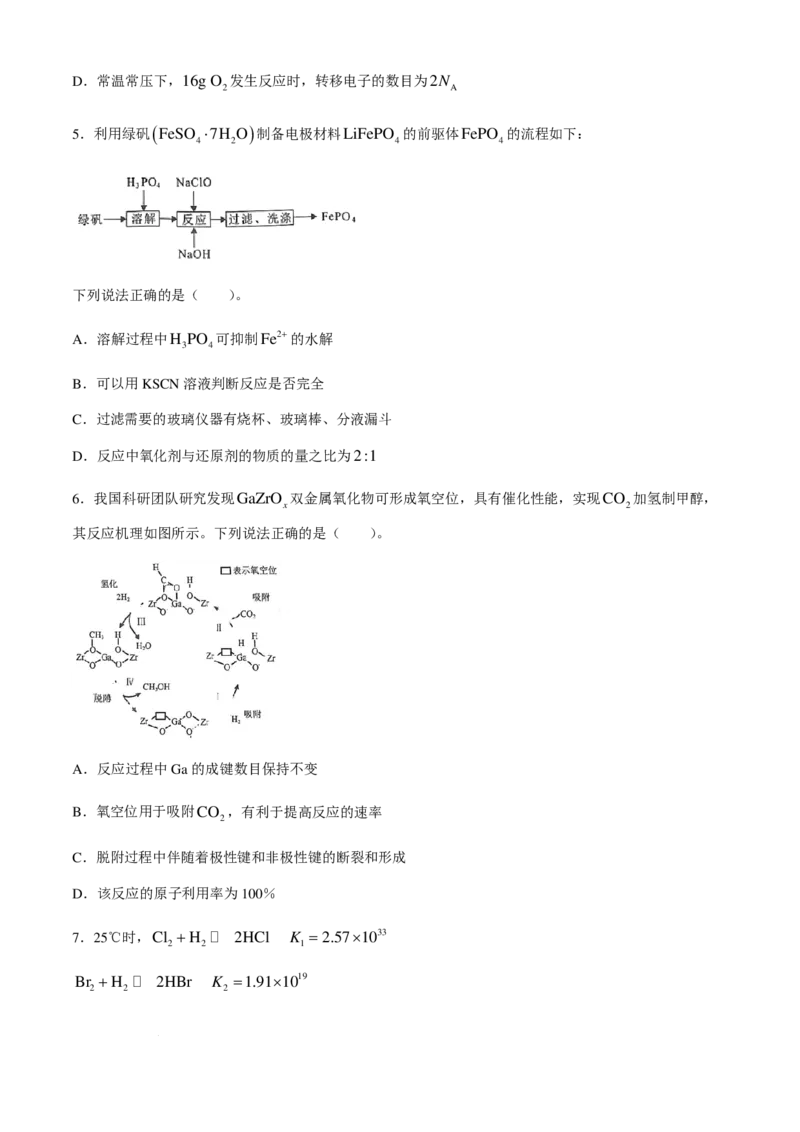
5.利用绿矾( FeSO ⋅7H O )制备电极材料LiFePO 的前驱体FePO 的流程如下:
4 2 4 4
下列说法正确的是( )。
A.溶解过程中H PO 可抑制Fe2+的水解
3 4
B.可以用KSCN溶液判断反应是否完全
C.过滤需要的玻璃仪器有烧杯、玻璃棒、分液漏斗
D.反应中氧化剂与还原剂的物质的量之比为2:1
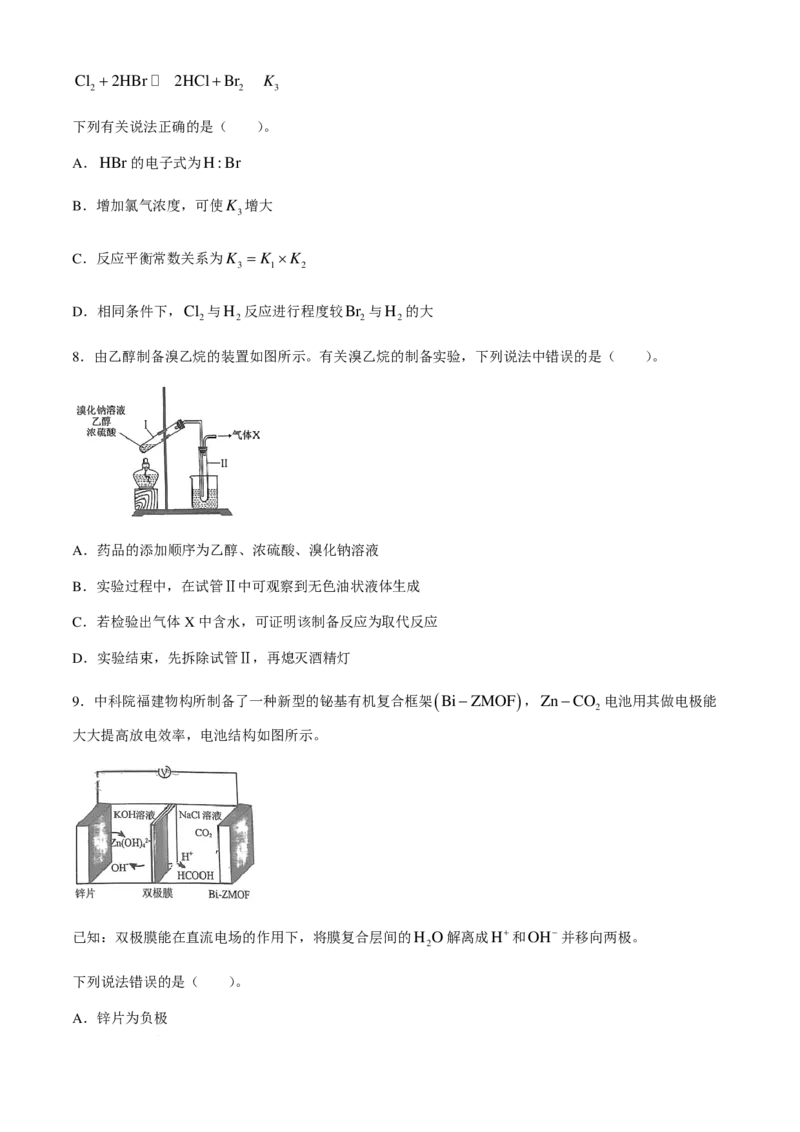
6.我国科研团队研究发现GaZrO 双金属氧化物可形成氧空位,具有催化性能,实现CO 加氢制甲醇,
x 2
其反应机理如图所示。下列说法正确的是( )。
A.反应过程中Ga的成键数目保持不变
B.氧空位用于吸附CO ,有利于提高反应的速率
2
C.脱附过程中伴随着极性键和非极性键的断裂和形成
D.该反应的原子利用率为100%
7.25℃时,Cl +H 2HCl K =2.57×1033
2 2 1
Br +H 2HBr K =1.91×1019
2 2 2
学科网(北京)股份有限公司Cl +2HBr 2HCl+Br K
2 2 3
下列有关说法正确的是( )。
A.HBr的电子式为H:Br
B.增加氯气浓度,可使K 增大
3
C.反应平衡常数关系为K = K ×K
3 1 2
D.相同条件下,Cl 与H 反应进行程度较Br 与H 的大
2 2 2 2
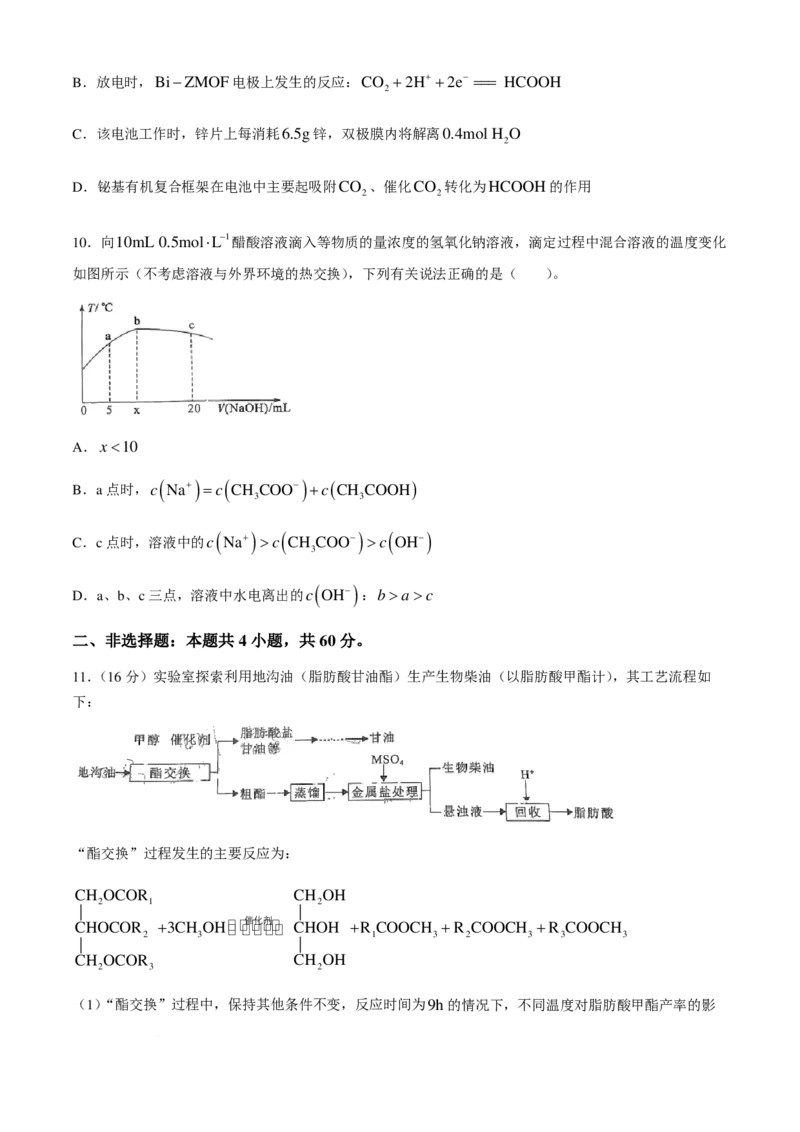
8.由乙醇制备溴乙烷的装置如图所示。有关溴乙烷的制备实验,下列说法中错误的是( )。
A.药品的添加顺序为乙醇、浓硫酸、溴化钠溶液
B.实验过程中,在试管Ⅱ中可观察到无色油状液体生成
C.若检验出气体X中含水,可证明该制备反应为取代反应
D.实验结束,先拆除试管Ⅱ,再熄灭酒精灯
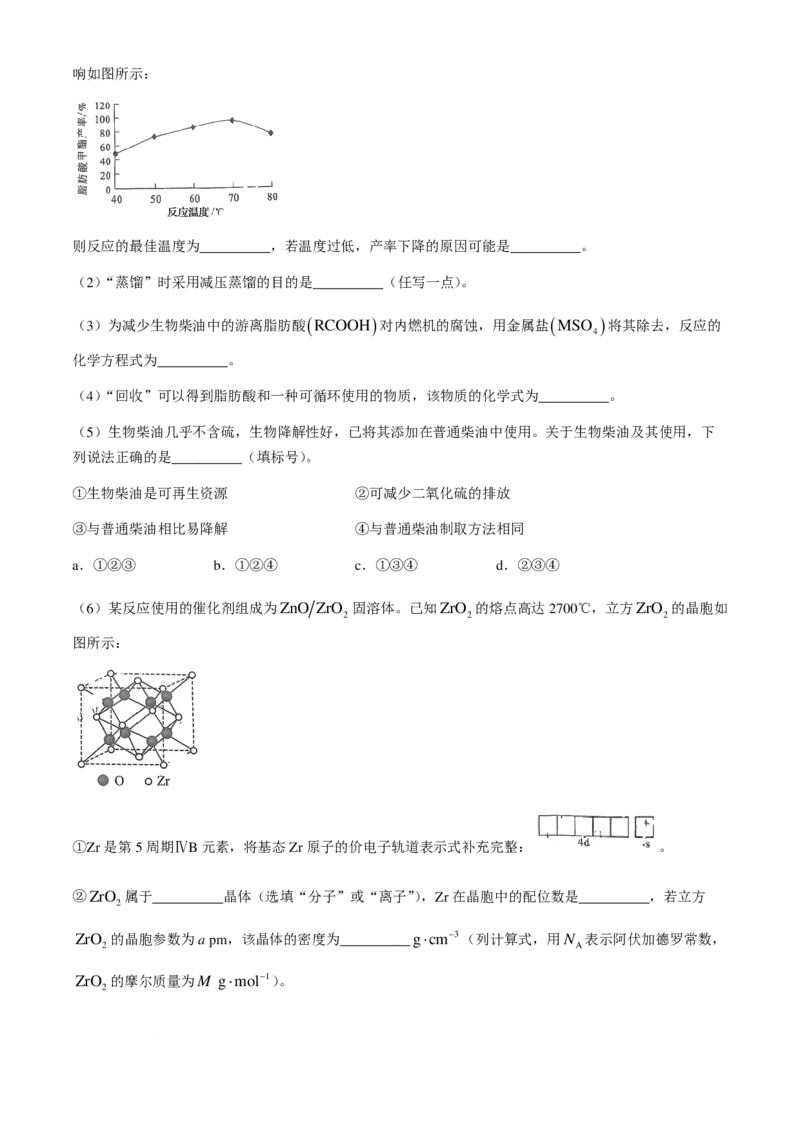
9.中科院福建物构所制备了一种新型的铋基有机复合框架( Bi−ZMOF ),Zn−CO 电池用其做电极能
2
大大提高放电效率,电池结构如图所示。
已知:双极膜能在直流电场的作用下,将膜复合层间的H O解离成H+和OH−并移向两极。
2
下列说法错误的是( )。
A.锌片为负极
学科网(北京)股份有限公司B.放电时,Bi−ZMOF电极上发生的反应:CO +2H+ +2e− === HCOOH
2
C.该电池工作时,锌片上每消耗6.5g锌,双极膜内将解离0.4mol H O
2
D.铋基有机复合框架在电池中主要起吸附CO 、催化CO 转化为HCOOH的作用
2 2
10.向10mL 0.5mol⋅L−1醋酸溶液滴入等物质的量浓度的氢氧化钠溶液,滴定过程中混合溶液的温度变化
如图所示(不考虑溶液与外界环境的热交换),下列有关说法正确的是( )。
A.x<10
B.a点时,c ( Na+) =c ( CH COO−) +c ( CH COOH )
3 3
C.c点时,溶液中的c
( Na+)
>c
(
CH
COO−)
>c
( OH−)
3
D.a、b、c三点,溶液中水电离出的c
( OH−)
:b>a>c
二、非选择题:本题共 4小题,共 60分。
11.(16分)实验室探索利用地沟油(脂肪酸甘油酯)生产生物柴油(以脂肪酸甲酯计),其工艺流程如
下:
“酯交换”过程发生的主要反应为:
CH OCOR CH OH
2 1 2
| |
CHOCOR +3CH OH 催化 剂 CHOH +R COOCH +R COOCH +R COOCH
2 3 1 3 2 3 3 3
| |
CH OCOR CH OH
2 3 2
(1)“酯交换”过程中,保持其他条件不变,反应时间为9h的情况下,不同温度对脂肪酸甲酯产率的影
学科网(北京)股份有限公司响如图所示:
则反应的最佳温度为__________,若温度过低,产率下降的原因可能是__________。
(2)“蒸馏”时采用减压蒸馏的目的是__________(任写一点)。
(3)为减少生物柴油中的游离脂肪酸(
RCOOH
)对内燃机的腐蚀,用金属盐(
MSO
)将其除去,反应的
4
化学方程式为__________。
(4)“回收”可以得到脂肪酸和一种可循环使用的物质,该物质的化学式为__________。
(5)生物柴油几乎不含硫,生物降解性好,已将其添加在普通柴油中使用。关于生物柴油及其使用,下
列说法正确的是__________(填标号)。
①生物柴油是可再生资源 ②可减少二氧化硫的排放
③与普通柴油相比易降解 ④与普通柴油制取方法相同
a.①②③ b.①②④ c.①③④ d.②③④
(6)某反应使用的催化剂组成为ZnO ZrO 固溶体。已知ZrO 的熔点高达2700℃,立方ZrO 的晶胞如
2 2 2
图所示:
①Zr是第5周期ⅣB元素,将基态Zr原子的价电子轨道表示式补充完整: 。
②ZrO 属于__________晶体(选填“分子”或“离子”),Zr在晶胞中的配位数是__________,若立方
2
ZrO 的晶胞参数为a pm,该晶体的密度为__________g⋅cm−3(列计算式,用N 表示阿伏加德罗常数,
2 A
ZrO 的摩尔质量为M g⋅mol−1)。
2
学科网(北京)股份有限公司12.(15分)碘酸钙可用作防臭剂、药物和食品添加剂等。实验室制备六水合碘酸钙
Ca ( IO ) ⋅6H O
3 2 2
并测定碘酸钙的K 方法如下。
sp
Ⅰ.六水合碘酸钙的制备
85℃
已知:2KClO +I +HCl KIO ⋅HIO +Cl ↑+KCl。
3 2 3 3 2
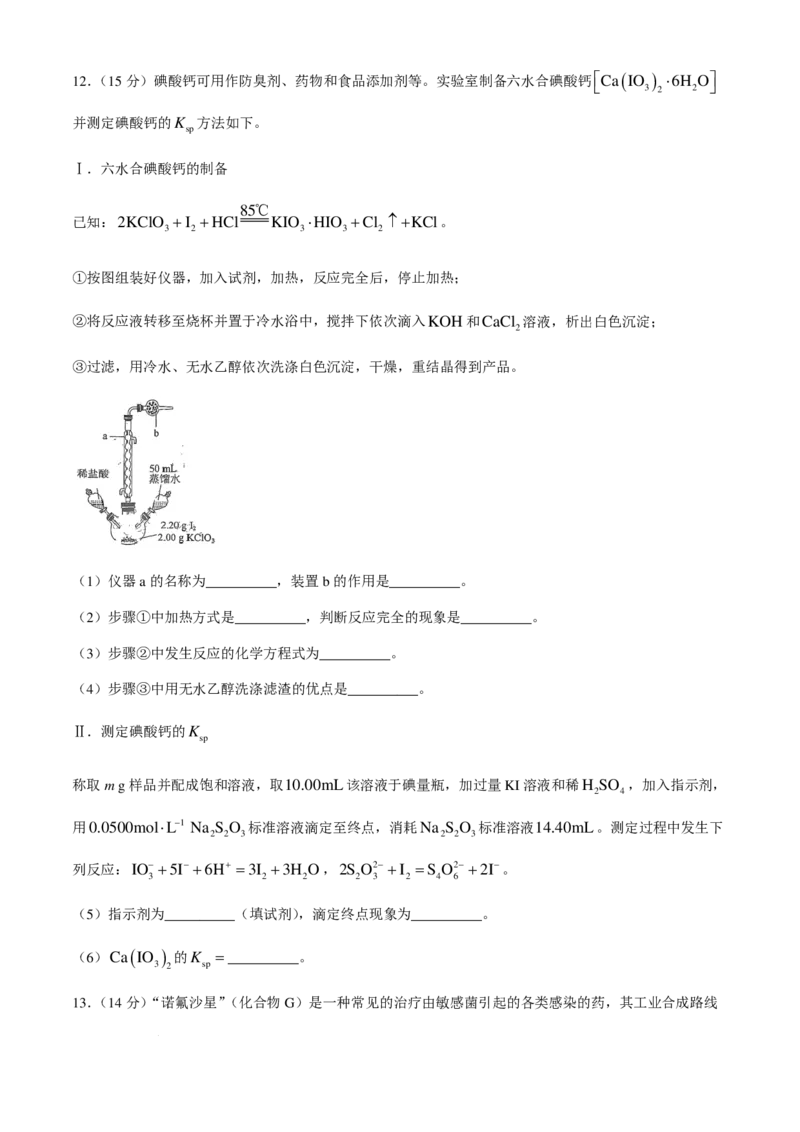
①按图组装好仪器,加入试剂,加热,反应完全后,停止加热;
②将反应液转移至烧杯并置于冷水浴中,搅拌下依次滴入KOH和CaCl 溶液,析出白色沉淀;
2
③过滤,用冷水、无水乙醇依次洗涤白色沉淀,干燥,重结晶得到产品。
(1)仪器a的名称为__________,装置b的作用是__________。
(2)步骤①中加热方式是__________,判断反应完全的现象是__________。
(3)步骤②中发生反应的化学方程式为__________。
(4)步骤③中用无水乙醇洗涤滤渣的优点是__________。
Ⅱ.测定碘酸钙的K
sp
称取m g样品并配成饱和溶液,取10.00mL该溶液于碘量瓶,加过量KI溶液和稀H SO ,加入指示剂,
2 4
用0.0500mol⋅L−1 Na S O 标准溶液滴定至终点,消耗Na S O 标准溶液14.40mL。测定过程中发生下
2 2 3 2 2 3
列反应:IO− +5I− +6H+ =3I +3H O,2S O2− +I =S O2− +2I−。
3 2 2 2 3 2 4 6
(5)指示剂为__________(填试剂),滴定终点现象为__________。
(6)Ca ( IO ) 的K =__________。
3 2 sp
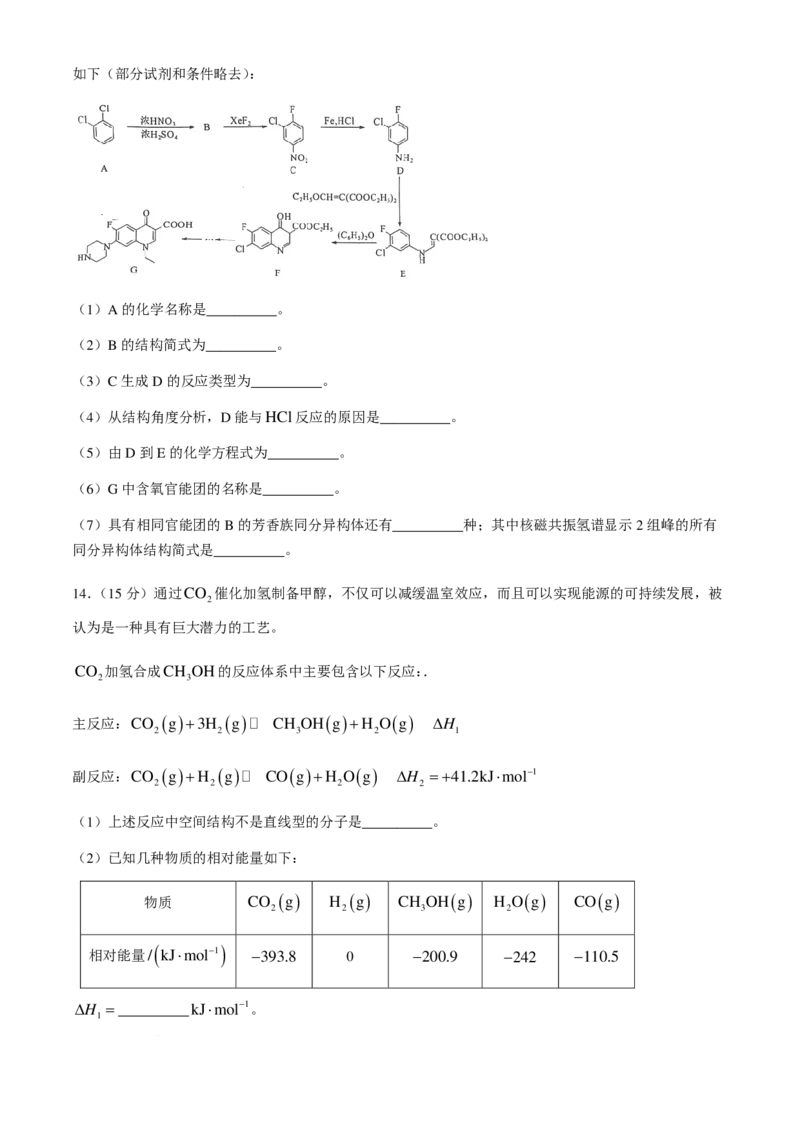
13.(14分)“诺氟沙星”(化合物G)是一种常见的治疗由敏感菌引起的各类感染的药,其工业合成路线
学科网(北京)股份有限公司如下(部分试剂和条件略去):
(1)A的化学名称是__________。
(2)B的结构简式为__________。
(3)C生成D的反应类型为__________。
(4)从结构角度分析,D能与HCl反应的原因是__________。
(5)由D到E的化学方程式为__________。
(6)G中含氧官能团的名称是__________。
(7)具有相同官能团的B的芳香族同分异构体还有__________种;其中核磁共振氢谱显示2组峰的所有
同分异构体结构简式是__________。
14.(15分)通过CO 催化加氢制备甲醇,不仅可以减缓温室效应,而且可以实现能源的可持续发展,被
2
认为是一种具有巨大潜力的工艺。
CO 加氢合成CH OH的反应体系中主要包含以下反应:.
2 3
主反应:CO ( g )+3H ( g ) CH OH ( g )+H O ( g ) ∆H
2 2 3 2 1
副反应:CO ( g )+H ( g ) CO ( g )+H O ( g ) ∆H =+41.2kJ⋅mol−1
2 2 2 2
(1)上述反应中空间结构不是直线型的分子是__________。
(2)已知几种物质的相对能量如下:
( ) ( ) ( ) ( ) ( )
物质 CO g H g CH OH g H O g CO g
2 2 3 2
相对能量/ ( kJ⋅mol−1 ) −393.8 0 −200.9 −242 −110.5
∆H =__________kJ⋅mol−1。
1
学科网(北京)股份有限公司(3)若在恒温恒容容器中同时发生主反应和副反应,下列能说明该体系已达到平衡状态的是__________
(填标号)。
a.气体的密度不再随时间而变化
b.容器内CH OH的浓度保持不变
3
c.反应体系的总压强保持不变
d.单位时间内消耗CO 和生成H O的速率之比为1:1
2 2
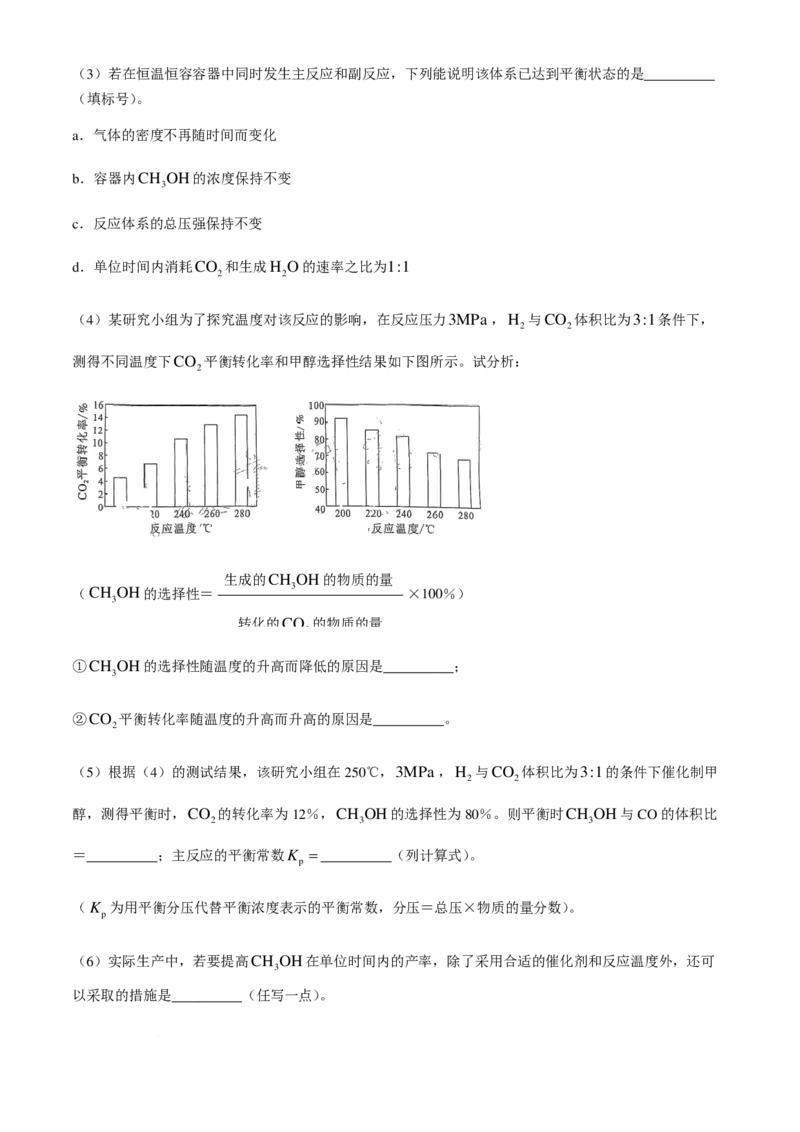
(4)某研究小组为了探究温度对该反应的影响,在反应压力3MPa,H 与CO 体积比为3:1条件下,
2 2
测得不同温度下CO 平衡转化率和甲醇选择性结果如下图所示。试分析:
2
生成的CH OH的物质的量
3
(CH OH的选择性= ×100%)
3
转化的CO 的物质的量
2
①CH OH的选择性随温度的升高而降低的原因是__________;
3
②CO 平衡转化率随温度的升高而升高的原因是__________。
2
(5)根据(4)的测试结果,该研究小组在250℃,3MPa,H 与CO 体积比为3:1的条件下催化制甲
2 2
醇,测得平衡时,CO 的转化率为12%,CH OH的选择性为80%。则平衡时CH OH与CO的体积比
2 3 3
=__________;主反应的平衡常数K =__________(列计算式)。
p
(K 为用平衡分压代替平衡浓度表示的平衡常数,分压=总压×物质的量分数)。
p
(6)实际生产中,若要提高CH OH在单位时间内的产率,除了采用合适的催化剂和反应温度外,还可
3
以采取的措施是__________(任写一点)。
学科网(北京)股份有限公司