文档内容
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 B D A D B A B
题号 8 9 10 11 12 13 14
答案 C B D D C D D
【解析】
1.单晶硅属于共价晶体,A正确。酚醛树脂是由酚类和甲醛缩聚成的,不含酯基,不属于聚
酯,B 错误。碳纳米管与石墨烯互为同素异形体,C 正确。砷化镓属于新型无机非金属材
料,D正确。
2.N 的电子式为 ,A 正确。Cl 中的共价键由 2 个 Cl 原子各提供 1 个未成对电子的
2 2
3p原子轨道重叠形成,为p−p σ键,B正确。NH ClO 中阳离子NH的中心N原子为sp3
4 4 4
杂化,且孤电子对数为0,ClO的中心Cl原子为sp3杂化,且孤电子对数也为0,故NH、
4 4
ClO的VSEPR模型和空间结构都相同,C正确。根据化合价升降变化判断可知氧化产物
4
为N 和O ,还原产物为Cl ,故氧化产物与还原产物的物质的量之比为3∶1,D错误。
2 2 2
3.氯化钠(食盐的主要成分)和谷氨酸钠(味精的主要成分)均可用作食用调味品,A正确。
Cu 和 S 反应生成 Cu S,B 错误。油脂是由高级脂肪酸与甘油形成的酯,不属于高分子化
2
合物,C错误。聚乳酸只能由乳酸分子一种单体通过缩聚反应制得,D错误。
4.K+、NH、I−、NO能大量共存,但因I−有较强还原性,通入Cl 后I−会被氧化,故不能
4 3 2
维持大量存在,A 错误。HCO与[Al(OH) ]−因生成 Al(OH) 沉淀不能大量共存,同时通
3 4 3
入 CO 后,[Al(OH) ]−与 CO 反应生成 Al(OH) 沉淀,B 错误。Fe3与 SCN−发生络合生
2 4 2 3
成Fe(SCN) 不能大量共存,同时通入SO 后,Fe3与SO 发生氧化还原反应而不能大量
3 2 2
存在,C 错误。NH、CH COO−、Cl−、CO2能大量共存,且通入 NH 后仍能维持大量
4 3 3 3
共存,D正确。
化学参考答案·第1页(共7页)5.液体向细口容器转移,需用玻璃棒引流,特别是向容量瓶转移时,玻璃棒末端需在刻度线
以下,确保刻度线以上区域无液体,图中玻璃棒末端在刻度线以上,操作错误,A错误。
已知浓度的NaOH标准溶液滴定未知浓度的CH COOH,滴定终点溶液呈碱性,应该用酚
3
酞作指示剂,氢氧化钠可盛放在耐腐蚀的聚四氟乙烯材质的滴定管中,B 正确。乙二醇滴
入足量的酸性高锰酸钾溶液中会被氧化成CO ,C错误。烧碱(NaOH)与石英(SiO )会
2 2
发生反应,D错误。
6.短周期中Q电负性最小,故Q为Na元素;又五种元素原子序数依次增大且分别位于三个
不同周期,则W必为H元素;基态Y原子的核外电子有5种空间运动状态,则Y为第二
周期的N元素;X、Y、Z相邻,故X为C元素,Z为O元素。据此作答。XW为CH,
3 3
其中C原子的杂化类型为sp3,CH的空间结构为三角锥形,由于C原子还有1个孤电子
3
对,故键角小于109°28′;XW为CH,其中C原子的杂化类型为sp2,CH的空间结构
3 3 3
为平面三角形,键角为 120°,则键角:XW>XW,A 错误。C H 为直线形分子,分子
3 3 2 2
结构对称,分子中正电中心和负电中心重合,故为非极性分子;H O 分子结构不对称,分
2 2
子中正电中心和负电中心不重合,故为极性分子,因此,两者极性的大小关系为
X W O>C,A正确。三聚氰胺分子中所有碳原子均采取sp2杂化,而
—NH 中N原子采用sp3杂化,B错误。1个三聚氰酸分子中含有3个氮氢σ键,3个碳氧
2
σ键,6个碳氮σ键,所以1mol该分子中含有12mol σ键,C正确。二维超分子中相邻的
三聚氰胺和三聚氰酸之间形成3个氢键,D正确。
8.1−溴丁烷和沸石加入NaOH的乙醇溶液中,微热,乙醇会挥发,乙醇能使酸性高锰酸钾溶
液褪色,故无法检验1−溴丁烷的消去产物,C错误。
9.根据反应Ⅱ为制取漂白粉的原理,可推知乙为 Ca(OH) 。若反应Ⅰ为化合反应,且甲属于
2
碱性氧化物,故甲为CaO,则反应Ⅰ的化学方程式为CaO+H O=Ca(OH) ,A正确。若
2 2
反应Ⅰ是实验室制备某气体的反应,该气体分子为14e−结构,应是乙炔,故反应Ⅰ应为碳
化学参考答案·第2页(共7页)化钙和水的反应,其反应的化学方程式可为 CaC +2H O→Ca(OH) +C H ↑。同时 O 分子
2 2 2 2 2 2
为 16e−结构,不符合题意,B 错误。反应Ⅱ为制取漂白粉的原理,其反应化学方程式是
2Cl +2Ca(OH) =Ca(ClO) +CaCl +2H O,C 正确。氯水中含有 HCl 和 HClO:
2 2 2 2 2
Cl +H O
HCl+HClO,在饱和氯水中加块状石灰石,碳酸钙和盐酸反应生成氯化钙、
2 2
二氧化碳和水,促进上述平衡右移,从而能制得较浓 HClO 溶液,反应的离子方程式是
2Cl +H O+CaCO =Ca2++2Cl−+2HClO+CO ,D正确。
2 2 3 2
10.L−多巴和D−多巴互为同分异构体,属于立体异构,A正确。多巴胺分子结构中只含有苯
环不饱和结构,而氨基酸类分子结构含有羧基和氨基官能团,其中羧基为不饱和结构,
故不可能存在含苯环结构的氨基酸类同分异构体,B 正确。L−多巴、D−多巴和多巴胺三
者均含有酚羟基,均能与 FeCl 溶液发生显色反应,C 正确。L−多巴、D−多巴和多巴胺
3
三者均含有碱性基团氨基,能与盐酸反应,但酚羟基不能与NaHCO 反应,D错误。
3
1 1
11.在CeO 理想晶胞中,含Ce4+个数为8 6 4,含O2−个数为8。从图甲中可以看出CeO
2 2
8 3
理想晶胞中,与面心的Ce4+最近且相等的O2−有4个,则在另一晶胞中,与Ce4+等距离的O2−
还有4个,则Ce4+的配位数为8,A正确。若CeO 理想晶胞边长为a nm,N 为阿伏加德罗
2 A
4172g/mol 688
常数的值,则 CeO 晶体的密度为 1021gcm3,B 正确。设
2 (a107cm)3N mol1 a3N
A A
Ce4+和 Ce3+个数分别为 x、y,根据原子守恒有x y8,根据化合价代数和为 0 有
4x3y152,解的x6、y2,Ce4+和Ce3+个数比为3∶1,C正确。CeO 能在Ce4+
2
和 Ce3+之间改变氧化状态,将 NO 氧化为 NO ,并引起氧空位的形成,得到新的铈氧化
2
物(Ce O ),反应原理为8CeO NO=Ce O NO ,氧化标准状况下11.2L NO气体,
8 15 2 8 15 2
则生成0.5mol Ce O ,D错误。
8 15
12.反应ii为H 0,S 0,由GH TS 0推知,故反应ⅱ在高温条件下可自发进
行,A正确。400℃后,BaS的物质的量分数变化不大,BaS基本反应完全,C、CO 的量
2
减少,CO的量增加,故反应后组分的变化是由C(s)+CO (g)2CO(g)的移动导致的,
2
B正确。为使硫酸钡得到充分还原,需要加入过量的碳,故反应过程中生成的CO 和CO
2
的物质的量之和小于投入C的物质的量,C错误。CO的物质的量分数为α,则分压为αp,
化学参考答案·第3页(共7页)则 CO 的物质的量分数为(1),容器中只有 CO 和 CO 两种气体,所以 CO 的分压为
2 2 2
(1)4
(1)p,所以K ,D正确。
p 4
13.电池工作时,Li失电子,所以Li作负极,C作正极,故Li+移向正极,A正确。由图可知,
I 在反应过程中被消耗又生成,故I 为催化剂,B正确。放电时,正极上SOCl 得到电子
2 2 2
发生还原转化为S、SO ,故正极电极反应为2SOCl +4e−+4Li+=SO ↑+S+4LiCl,C正
2 2 2
确。电子只能通过导线,不能通过电解质溶液,D错误。
14.溶液中加入40ml盐酸溶液时,Ⅰ中的溶质为氯化钠和氯化铵,Ⅱ中的溶质为氯化钠和醋
酸,根据K (CH COOH)K (NH H O)1.8105,醋酸根离子、铵根离子的水解程度
a 3 b 3 2
小于醋酸、一水合氨的电离程度,氯化钠显中性,醋酸和氯化铵在浓度相同时,醋酸溶
液的酸性更强,故Ⅰ对应的滴定曲线为 M,Ⅱ对应的滴定曲线为 N,A 正确。根据分析
可知a点的溶质为氯化钠和氯化铵,铵根离子发生水解,溶液的pH接近6,由水电离的
c(H)c(OH),数量级接近106,B正确。当V(NaOH)30.00mL时,Ⅱ中的溶质为氯
化钠、醋酸钠、醋酸,且醋酸钠和醋酸的浓度相同,根据分析可知醋酸根离子的水解程
度小于醋酸的电离程度,故c(Na+)>c(CH COO−)>c(CH COOH),C正确。根据元素守恒,
3 3
n(CH COOH)、n(CH COO)之和等于n(NH H O)、n(NH)之和,根据图像,pH7时,
3 3 3 2 4
Ⅱ所加盐酸较少,溶液体积较小,故Ⅰ中 c(NH H O)、c(NH) 之和小于Ⅱ中
3 2 4
c(CH COOH)、c(CH COO)之和,D错误。
3 3
二、非选择题:本题共4小题,共58分。
15.(除特殊标注外,每空2分,共14分)
(1)800℃(1分)
(2)Fe(OH) 、SiO 重结晶
3 2
(3)使 Fe2+完全转化为 Fe3+,且不引入新的杂质(1 分),减少双氧水的分解,提高原料
的利用率(1分)
(4)利用同离子效应降低硫酸铝铵的溶解度,促进其析出,增大产率
(5)①A(1分) ②NH Al(SO ) ·12H O
4 4 2 2
化学参考答案·第4页(共7页)(6)原子晶体(或共价晶体)(1分)
AlN晶体中的化学键比Al O 的化学键更强(1分)
2 3
【解析】(2)提出固体的方法为重结晶。
(3)双氧水具有较强的氧化性,能氧化亚铁离子生成铁离子,且其产物为水,足量双氧
水可以保证将Fe2+完全氧化,所以步骤中,双氧水需足量的原因为使Fe2+完全转化为Fe3+,
且不引入新的杂质,而分批加入可以减少双氧水的分解,提高原料的利用率。
(4)制备硫酸铝铵使硫酸铵稍微过量可增大铵根离子浓度,利用同离子效应降低硫酸铝
铵的溶解度,促进产品析出,增大产率。
(5)①因为物质为中性,各离子所带电荷的代数和为 0,所以必须测出阴离子SO2的物
4
质的量;
0.102g
②根据AlO 的质量为0.102g,可得Al元素物质的量为 20.002mol,根据BaSO
2 3 4
102g/mol
0.932g
质量为0.932g,可得SO2的物质的量为 0.004mol,浓硫酸增加的质量为NH 的质
4 233g/mol 3
0.0340g
量,所以0.906g铵明矾样品含NH物质的量为 0.002mol,铵明矾样品含结晶水的
4 17g/mol
0.906g0.002mol27g/mol0.004mol96g/mol0.002mol18g/mol
物质的量为
18g/mol
0.024mol,所以铵明矾的化学式为NH Al(SO ) ·12H O。
4 4 2 2
(6)由题给信息氮化铝属类金刚石氮化物及熔点可知,AlN属于共价(或原子)晶体,所
以熔点比离子晶体氧化铝高。
16.(除特殊标注外,每空2分,共15分)
(1)E→D→C(填“E→D”可给1分)
(2)将F中的四氯化碳吹入到E中参与反应(1分)
(3)COCl +4OH−=CO2+2Cl−+2H O
2 3 2
(4)BD
(5)产物可及时脱离反应体系,反应物能充分有效地接触,有利于提高产率
3(1分)
(6)THF易挥发,易燃,遇明火可能发生爆炸(1分)
化学参考答案·第5页(共7页)(7)过滤CrCl 和Zn粉,防止堵塞虹吸管
3
(8)61.42%
【解析】由上述分析可知,实验装置合理的连接顺序为A→C→F→E→D→C→B。
(2)本实验A中产生的N 的目的是赶走体系中原有的空气和将四氯化碳吹入到E中参与
2
反应。
(3)尾气处理时,NaOH 溶液与COCl 发生反应生成碳酸钠和氯化钠,离子方程式为:
2
COCl +4OH−=CO2+2Cl−+2H O。
2 3 2
(4)为除去四氢呋喃的水,可先加入干燥剂,再加入金属钠反应掉剩余的少量水,但不
可使用浓硫酸作干燥剂,浓硫酸与四氢呋喃反应,故答案选BD。
(5)CrCl 不溶于THF中,纸质反应管可以过滤掉CrCl ,因此将无水CrCl 和锌粉放在
3 3 3
纸质反应管内的好处是:产物可及时脱离反应体系,反应物能充分有效地接触,有利于
提高产率,根据虹吸原理,管3利用虹吸原理回流,管2是平衡气压的,故答案为3。
(6)用电加热而不用明火加热是因为THF易挥发,易燃,遇明火可能发生爆炸。
(7)CrCl 和Zn粉不溶于THF中,故纸质反应管可以过滤掉CrCl ,故答案为过滤CrCl ,
3 3 3
防止堵塞虹吸管。
CrO ~ 2CrCl ~ 2CrCl (THF)
2 3 3 3 3
(8) 152 749 求得x7.49g,故CrCl (THF) 的产率为:
3 3
1.52g x
4.6g
100%61.42%。
7.49g
17.(每空2分,共14分)
(1)BD
(2)<
(3)>
(4)当温度高于 300℃,以反应 ii 为主,反应 ii 为吸热反应,升高温度平衡正向移动,
CO 平衡转化率升高
2
(5)18.3% 0.0136
(6)CO +6e−+6H+=CH OH+H O
2 3 2
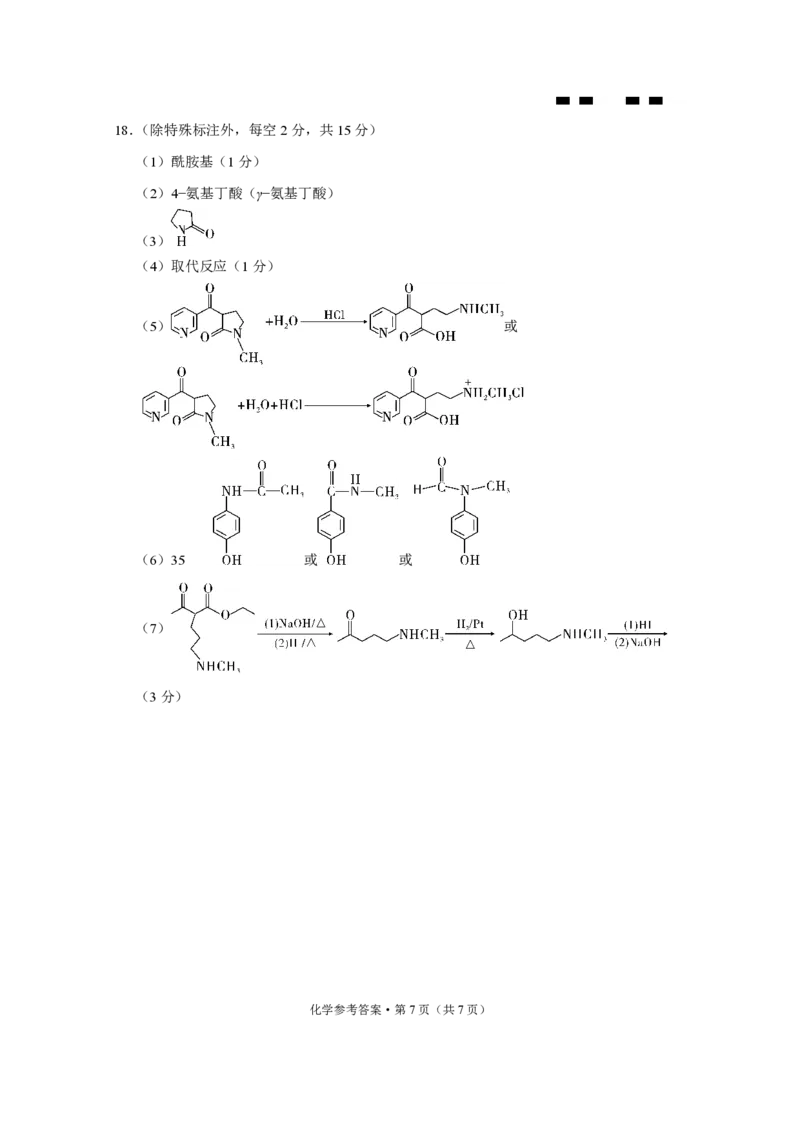
化学参考答案·第6页(共7页)18.(除特殊标注外,每空2分,共15分)
(1)酰胺基(1分)
(2)4−氨基丁酸(γ−氨基丁酸)
(3)
(4)取代反应(1分)
(5) 或
(6)35 或 或
(7)
(3分)
化学参考答案·第7页(共7页)