文档内容
2023-2024学年高三化学下学期开学摸底考(新高考七省专用)
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮
擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.测试范围:高考全部内容。
可能用到的相对原子质量:H 1 B 11 C 12 O 16 Fe 56
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.化学促进了生活、生产、科研的发展,下列相关说法错误的是
A.在葡萄酒中添加SO 作为抗氧化剂食品保鲜,SO 在保鲜时体现了氧化性
2 2
B.华为Mate60手机高清镜头中使用的COC/COP(环状聚烯烃)是高分子化合物,也是混合物
C.中国自主研发的首个5G微基站射频芯片的主要材料是Si
D.高铁动车的车厢厢体由不锈钢和铝合金制成,不锈钢和铝合金均属于金属材料
2.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.pH=2的硫酸溶液中,含氢离子数目为0.01N
A
B.在常温常压下,11.2LCO 分子中含氧原子数目小于N
2 A
C.21gC H 分子中含σ键数目一定是4N
3 6 A
D.在 中,每生成 ,转移的电子数为6N
A
3.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示。下列说法正确的是
A.不存在手性碳原子 B.分子中含有酯基
C.能与饱和溴水发生取代反应和加成反应 D.1mol甘草素最多能与2molNaOH反应
4.鎏金是古代常用的镀金工艺,将金汞合金涂于器物表面,加热使汞挥发,便形成一层光亮的金镀层。
下列关于青铜器鎏金工艺的说法不正确的是
A.用电化学方法也可实现铜上覆金
B.鎏金除了改善外观,还可保护青铜器,使其不易生锈
C.若表面的金镀层破损,暴露出的青铜表面会更易生锈
D.鎏金工艺的镀金过程是一种化学变化
5.室温下,下列各组离子在指定溶液中能大量共存的是
A. 的溶液中: 、 、 、
B.含有大量 的溶液中: 、 、 、
C. 的溶液中: 、 、 、
D.酚酞变红色的溶液中: 、 、 、
6.已知电离常数:K(HCN)=5×10-10,HCO:K =4.3×10-7,K =5.6×10-11,下列离子方程式书写正确的是
a 2 3 a1 a2
学科网(北京)股份有限公司A.向KCN(aq)中通入少量的CO 气体:CO+H O+2CN-=2HCN+CO
2 2 2
B.少量SO 通入Ca(ClO) 溶液中:SO +H O+Ca2++2ClO-=CaSO ↓+2HClO
2 2 2 2 3
C.氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH) +6H++2I-=2Fe2++6H O+I
3 2 2
D.向Ba(OH) 溶液中加入少量的NaHCO 溶液:2HCO +Ba2++2OH-=BaCO ↓+CO +2H O
2 3 3 2
7.下列化学用语表示正确的是
A. 的空间结构: (正四面体形)
B.甲烷的标准燃烧热 为 ,则甲烷燃烧的热化学方程式可表示为
C. 离子结构示意图:
D.NaHCO =Na++H++CO 2-
3 3
8.下列有关物质结构与性质的比较正确的是
A.分子的极性: B.酸性:
C.键角: D.基态原子未成对电子数:Mn>Cr
9.为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
实验目的 主要仪器 试剂
A 分离 和 混合物 分液漏斗、烧杯 和 混合物、蒸馏水
B 检验淀粉是否水解 试管、烧杯、酒精灯 淀粉的稀硫酸溶液、银氨溶液
C 鉴别碳酸钠和碳酸氢钠溶液 试管、胶头滴管 澄清石灰水
D 测定 溶液浓度 酸式滴定管、锥形瓶、烧杯 溶液、0.1000 草酸溶液
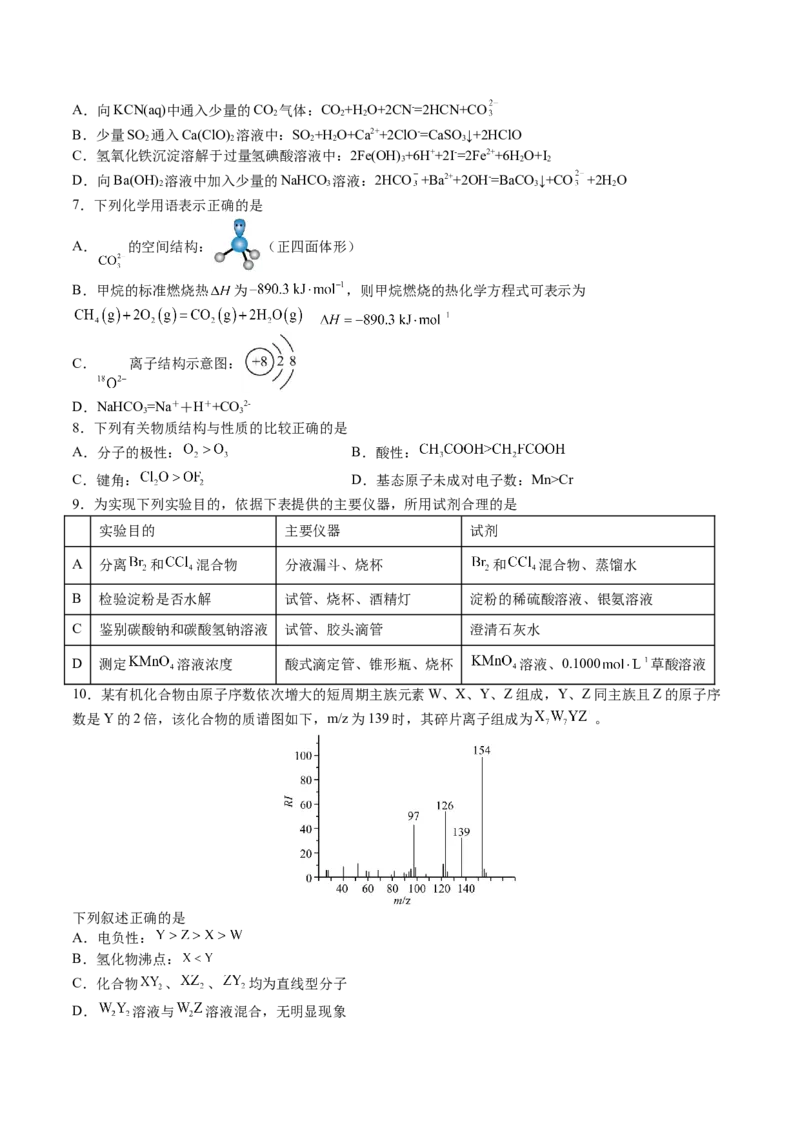
10.某有机化合物由原子序数依次增大的短周期主族元素W、X、Y、Z组成,Y、Z同主族且Z的原子序
数是Y的2倍,该化合物的质谱图如下,m/z为139时,其碎片离子组成为 。
下列叙述正确的是
A.电负性:
B.氢化物沸点:
C.化合物 、 、 均为直线型分子
D. 溶液与 溶液混合,无明显现象
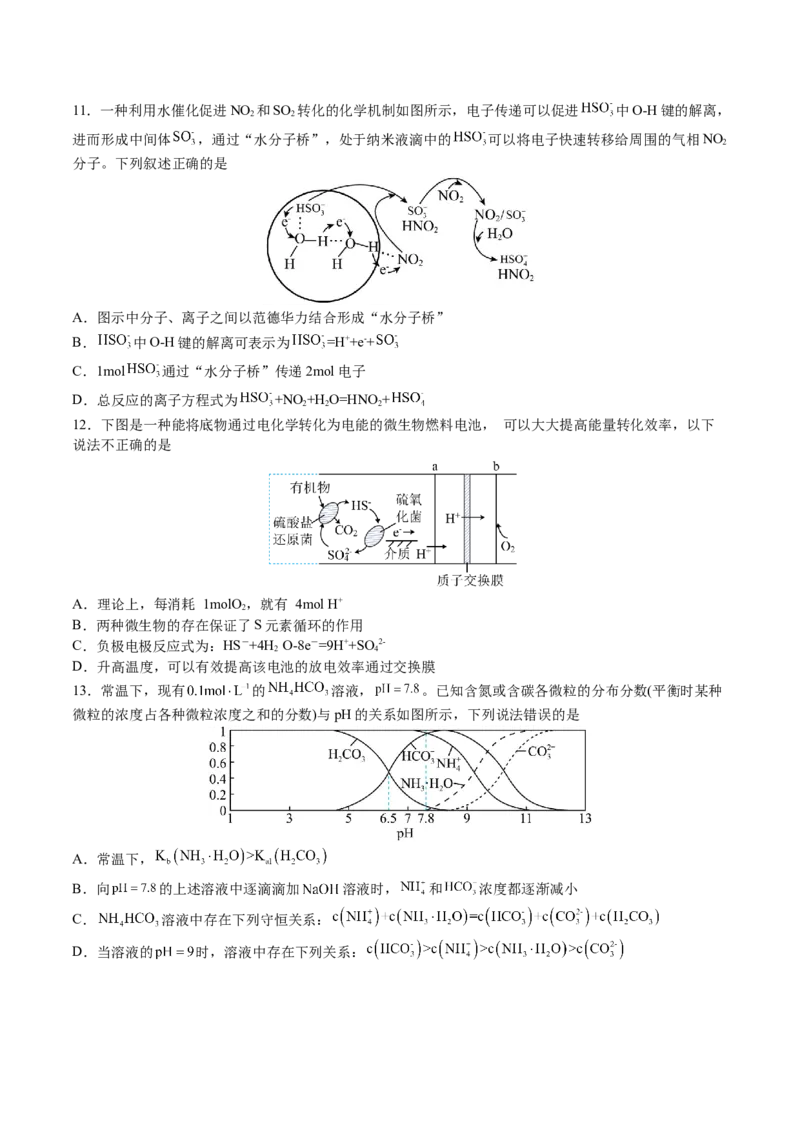
学科网(北京)股份有限公司11.一种利用水催化促进NO 和SO 转化的化学机制如图所示,电子传递可以促进 中O-H键的解离,
2 2
进而形成中间体 ,通过“水分子桥”,处于纳米液滴中的 可以将电子快速转移给周围的气相NO
2
分子。下列叙述正确的是
A.图示中分子、离子之间以范德华力结合形成“水分子桥”
B. 中O-H键的解离可表示为 =H++e-+
C.1mol 通过“水分子桥”传递2mol电子
D.总反应的离子方程式为 +NO+H O=HNO +
2 2 2
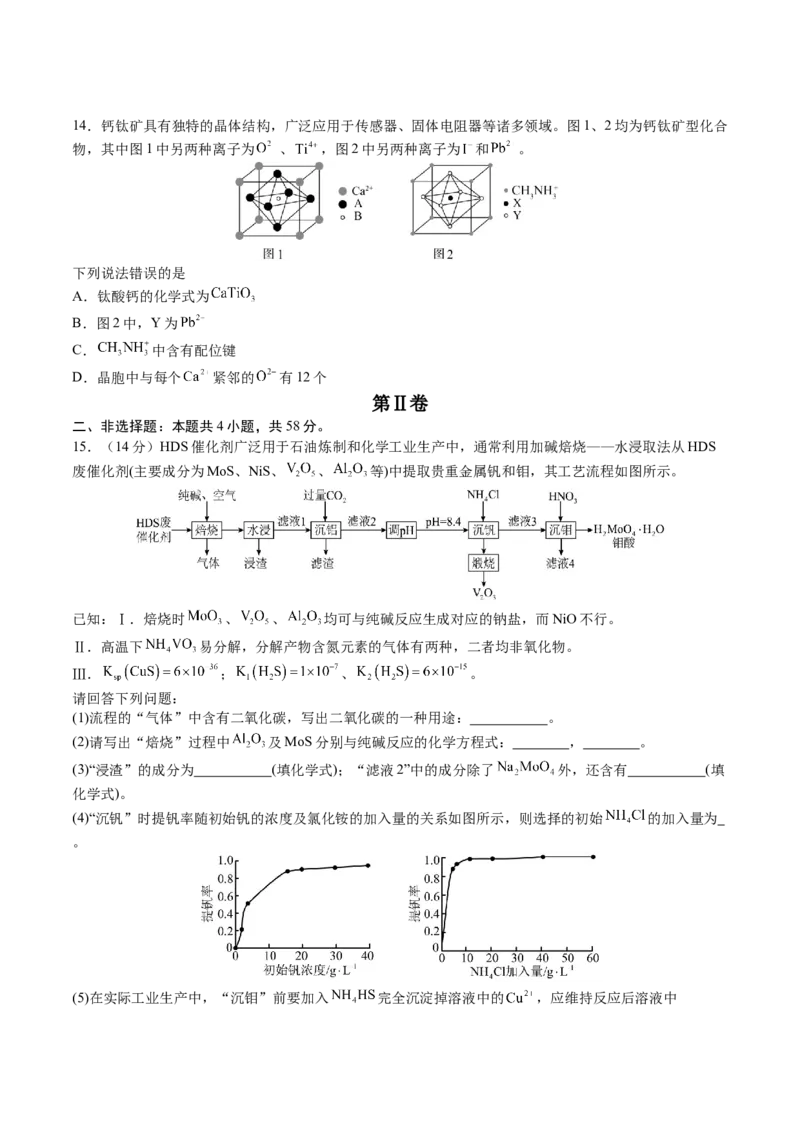
12.下图是一种能将底物通过电化学转化为电能的微生物燃料电池, 可以大大提高能量转化效率,以下
说法不正确的是
A.理论上,每消耗 1molO ,就有 4mol H+
2
B.两种微生物的存在保证了S元素循环的作用
C.负极电极反应式为:HS-+4H O-8e-=9H++SO2-
2 4
D.升高温度,可以有效提高该电池的放电效率通过交换膜
13.常温下,现有 的 溶液, 。已知含氮或含碳各微粒的分布分数(平衡时某种
微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示,下列说法错误的是
A.常温下,
B.向 的上述溶液中逐滴滴加 溶液时, 和 浓度都逐渐减小
C. 溶液中存在下列守恒关系:
D.当溶液的 时,溶液中存在下列关系:
学科网(北京)股份有限公司14.钙钛矿具有独特的晶体结构,广泛应用于传感器、固体电阻器等诸多领域。图1、2均为钙钛矿型化合
物,其中图1中另两种离子为 、 ,图2中另两种离子为 和 。
下列说法错误的是
A.钛酸钙的化学式为
B.图2中,Y为
C. 中含有配位键
D.晶胞中与每个 紧邻的 有12个
第Ⅱ卷
二、非选择题:本题共4小题,共58分。
15.(14分)HDS催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从HDS
废催化剂(主要成分为MoS、NiS、 、 等)中提取贵重金属钒和钼,其工艺流程如图所示。
已知:Ⅰ.焙烧时 、 、 均可与纯碱反应生成对应的钠盐,而NiO不行。
Ⅱ.高温下 易分解,分解产物含氮元素的气体有两种,二者均非氧化物。
Ⅲ. ; 、 。
请回答下列问题:
(1)流程的“气体”中含有二氧化碳,写出二氧化碳的一种用途: 。
(2)请写出“焙烧”过程中 及MoS分别与纯碱反应的化学方程式: , 。
(3)“浸渣”的成分为 (填化学式);“滤液2”中的成分除了 外,还含有 (填
化学式)。
(4)“沉钒”时提钒率随初始钒的浓度及氯化铵的加入量的关系如图所示,则选择的初始 的加入量为
。
(5)在实际工业生产中,“沉钼”前要加入 完全沉淀掉溶液中的 ,应维持反应后溶液中
学科网(北京)股份有限公司,的范围是 。
(6)“沉钒”时生成 沉淀,请写出“煅烧”中发生反应的化学方程式: 。
16.(14分)磁性材料Fe S 与石墨烯构成的复合材料,用于高性能锂硫电池。某化学小组按如下装置测
x y
定该磁性材料Fe S 的组成。
x y
(1)仪器N的名称是 ,其作用是 。
(2)实验时管式炉中产生的气体能使品红溶液褪色,三颈烧瓶中产生白色沉淀,三颈烧瓶中发生反应的离子
方程式是 。
(3)若管式炉内反应的温度为600~700℃,长玻璃管M除了导气外还有的作用是 ,若没有长玻
璃管会导致测定的y值 (填“偏大”“偏小”或“无影响”)。
(4)取2.960g试样放入管式炉充分反应后,再通入O 一段时间,然后将三颈烧瓶中的固体过滤,洗涤,干
2
燥称量得到9.320g,操作过程中,检验沉淀已洗涤干净的方法是 。小组成员提出用浓硝酸代
替HO,其他小组成员提出反驳意见,反驳的理由是 。
2 2
(5)充分反应后,取管式炉中固体溶于足量的稀硫酸中,取少量反应后的溶液,加入 (填试剂名
称),溶液变红,证明溶液中含有Fe3+;另取少量溶液,加入K[Fe(CN) ]溶液,没有明显变化,则管式炉中
3 6
固体的颜色是 ,管式炉中发生的化学反应方程式为 。
17.(15分)我国提出2060年前实现碳中和,为有效降低大气CO 中的含量,以CO 为原料制备甲烷、
2 2
戊烷、甲醇等能源物质具有较好的发展前景。CO 在固体催化剂表面加氢合成甲烷过程中发生如下反应:
2
Ⅰ.主反应:CO(g)+4H(g) CH(g)+2HO(g) ∆H=-156.9 kJ·mol-l
2 2 4 2 1
Ⅱ.副反应:CO(g)+H(g) CO(g)+HO(g) ∆H=+41.1 kJ·mol-l
2 2 2 2
(1)已知:Ⅲ.2H(g)+O(g)=2HO(g) ∆H=-395.6 kJ·mol-l
2 2 2 3
Ⅳ.CH(g)+2O(g)=CO (g)+2HO(g) ∆H= 。
4 2 2 2 4
(2)CO 加氢合成甲烷时,通常控制温度为500°C左右,其可能的原因为_______。
2
A.反应速率快 B.平衡转化率高
C.催化剂活性高 D.主反应催化剂选择性好
(3)500°C时,向1 L恒容密闭容器中充入4 mol CO 和12 mol H,初始压强为p,20 min时主、副反应
2 2
都达到平衡状态,测得c(H O)=5mol·L-1,体系压强为3/4p,则0~20min内 (CH)= mol·L-1·min-1,平
2 4
衡时CH 选择性= (CH 选择性= ×100%,计算保留三位有效数字,下同),副反应的K=
4 4 c
。
(4)以CO 催化加氢合成的甲醇为原料,在催化剂作用下可以制取丙烯,反应的化学方程式为3CHOH(g)
2 3
C H(g)+3HO(g)。该反应的Arrhenius经验公式的实验数据如图中曲线a所示,已知Arhenius经验公式
3 6 2
,(Ea为活化能,k为速率常数,R和C为常数)。当改变外界条件时,实验数据如图中的曲
线b所示,则实验可能改变的外界条件是 。
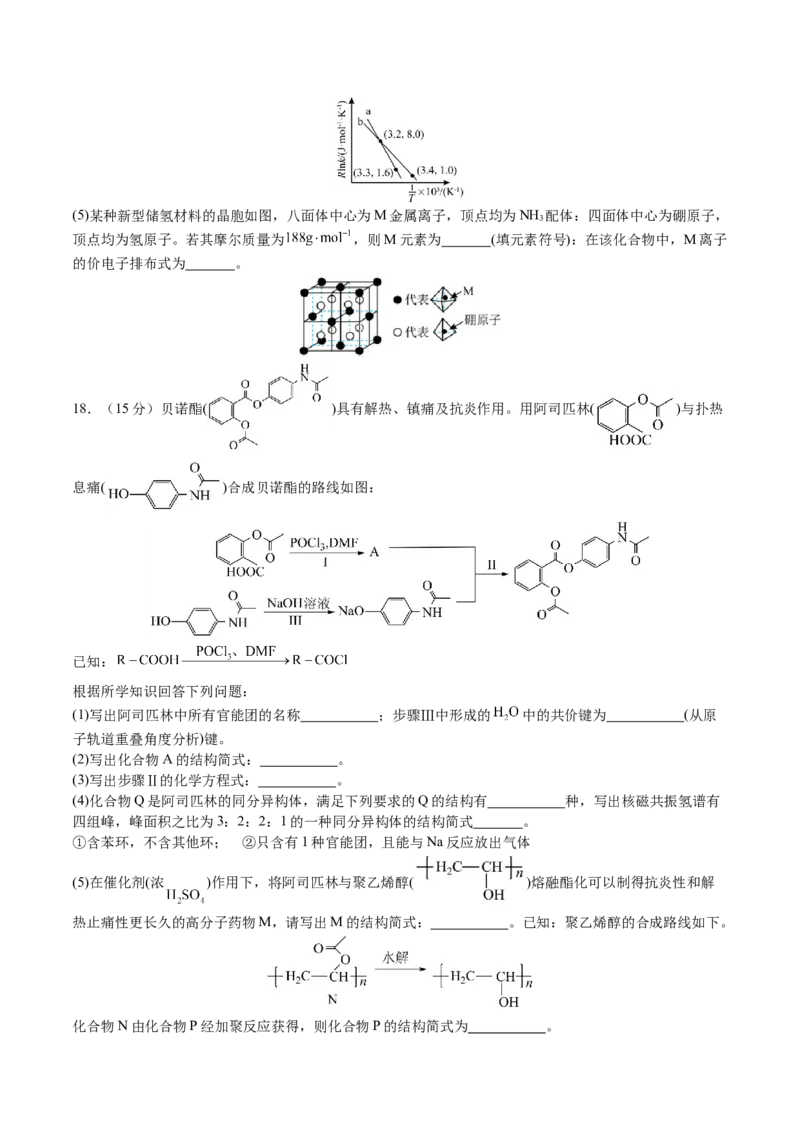
学科网(北京)股份有限公司(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为NH 配体:四面体中心为硼原子,
3
顶点均为氢原子。若其摩尔质量为 ,则M元素为 (填元素符号):在该化合物中,M离子
的价电子排布式为 。
18.(15分)贝诺酯( )具有解热、镇痛及抗炎作用。用阿司匹林( )与扑热
息痛( )合成贝诺酯的路线如图:
已知:
根据所学知识回答下列问题:
(1)写出阿司匹林中所有官能团的名称 ;步骤Ⅲ中形成的 中的共价键为 (从原
子轨道重叠角度分析)键。
(2)写出化合物A的结构简式: 。
(3)写出步骤Ⅱ的化学方程式: 。
(4)化合物Q是阿司匹林的同分异构体,满足下列要求的Q的结构有 种,写出核磁共振氢谱有
四组峰,峰面积之比为3:2:2:1的一种同分异构体的结构简式 。
①含苯环,不含其他环; ②只含有1种官能团,且能与Na反应放出气体
(5)在催化剂(浓 )作用下,将阿司匹林与聚乙烯醇( )熔融酯化可以制得抗炎性和解
热止痛性更长久的高分子药物M,请写出M的结构简式: 。已知:聚乙烯醇的合成路线如下。
化合物N由化合物P经加聚反应获得,则化合物P的结构简式为 。
学科网(北京)股份有限公司学科网(北京)股份有限公司