文档内容
第四章 章末测试
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
一、单选题(每题3分,共14题42分)
1.(2020·江苏月考)短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高价氧化物固态时可用
作人工降雨剂或用于冷藏食品,X、Y的最外层电子数之和与W的最外层电子数相等,W的简单氢化物与
Z的单质混合光照可生成Z的氢化物和油状混合物。下列说法正确的是
A.原子半径:W>X>Y>Z
B.X、Y的简单离子的电子层结构相同
C.W的简单氢化物的稳定性比Z的强
D.Z分别与W、X形成的化合物中所含化学键类型相同
2.(2020·伊美区第二中学开学考试)如图所示,a、b、c、d、e 为元素周期表中前 4 周期的一部分元素,
下列有关叙述正确的是( )
A.元素 b 位于第ⅥA 族,有+6、-2 价两种常见化合价
B.五种元素中,元素 e 的性质最稳定
C.元素 c 和 d 的最高价氧化物对应的水化物的酸性:c>d
D.元素 c 和 e 的气态氢化物的稳定性:c>e
3.(2020·北京市朝阳区人大附中朝阳分校高三月考)已知X、Y、Z、W、M 均为短周期元素。25℃时,
其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不
正确的是
A.Z元素最高价氧化物的化学式为ZO
3
B.简单离子半径大小顺序:X>MC.简单气态氢化物的稳定性:Z>W>Y
D.X、Z的最简单气态氢化物反应有白烟生成
4.(2020·全国高一课时练习)下列微粒中半径最小的是( )
A.Na B.F— C.Al3+ D.Cl—
5.(2020·扬州市江都区大桥高级中学高三月考)用化学用语表示 NH + HCl NH Cl中的相关微粒,
3 4
其中正确的是( )
A.中子数为8的氮原子: B.HCl 的电子式:
C.NH 的结构式: D.Cl−的结构示意图:
3
6.(2020·全国高一课时练习)下列物质中,既含有非极性共价键又含有极性共价键的是
A.NaOH B.CO C.N D.NH
2 2 2 4
7.(2020·全国高一课时练习)短周期元素 、 、 、 的原子序数依次增大, 与 、 与 分
别位于同一主族, 与 可形成共价化合物 , 原子的内层电子总数是其最外层电子数的2.5倍。
下列叙述不正确的是( )
A. 分子中的所有原子最外层都为8电子结构
B. 、 的化学键类型相同
C. 是共价化合物
D.原子半径:
8.(2020·全国高一课时练习)元素X、Y、Z的原子序数之和为36,X、Y在同一周期,X+与Z2-具有相
同的核外电子排布。下列推测不正确的是( )
A.同周期元素中X的金属性最强
B.原子半径:X>Y,离子半径:X+>Z2-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
9.(2020·全国高一课时练习)短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同主族,Y原
子的最外层电子数等于X原子的电子总数。Z原子的电子总数等于W、X、Y原子的电子数之和,Z的最高价氧化物对应水化物的化学式为 。W、X、Y三种元素组成的一种化合物的结构如图所示。下
列说法错误的是( )
A.W的最高正价和最低负价的代数和为0
B.W的离子半径一定小于X的简单离子半径
C.Y的最高价氧化物对应的水化物属于两性化合物
D.Z的单质的水溶液需保存在棕色试剂瓶中
10.(2020·全国高一课时练习)下列各分子中,所有原子都满足最外层为8电子结构的是( )。
A.HO B.BF C.PCl D.NO
2 3 3 2
11.(2020·全国高一课时练习)下列各组大小顺序不正确的是
A.酸性:HSiO﹤HPO ﹤HSO B.热稳定性:HSe﹤HS﹤H O
2 3 3 4 2 4 2 2 2
C.还原性:HI﹥HBr﹥HCl D.金属的还原性:Na﹤Mg﹤Al
12.(2020·全国高一课时练习)下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形
成的反应是( )
A.H+CuO=Cu+HO B.2NaO+2H O=4NaOH+O ↑
2 2 2 2 2 2
C.H+Cl=2HCl D.2NaOH+Cl =NaCl+NaClO+H O
2 2 2 2
13.(2020·霍邱县第二中学高一月考)短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四
种元素原子的最外层电子数之和为21。下列关系正确的是( )
W X
Y Z
A.氢化物沸点:W < Z B.氧化物对应水化物的酸性:Y > W
C.化合物熔点:YX < YZ D.简单离子的半径:Y < X
2 3 3
14.(2020·辽宁葫芦岛·高三二模)短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是
由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K
是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示。下
列说法正确的是A.原子半径:WY>X
C.化合物XZ 中所有原子均满足8电子稳定结构
2
D.X、 Z的单质分别直接与Y的单质反应,都能生成两种氧化物。
二、解答题(共5题58分)
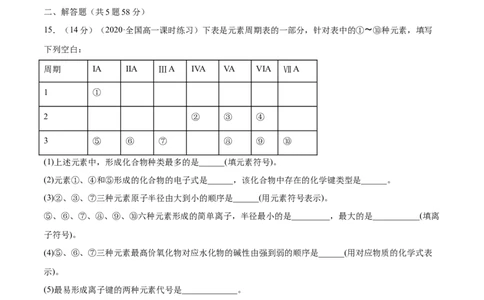
15.(14分)(2020·全国高一课时练习)下表是元素周期表的一部分,针对表中的①〜⑩种元素,填写
下列空白:
周期 IA IIA ⅢA IVA VA VIA ⅦA
1 ①
2 ② ③ ④
3 ⑤ ⑥ ⑦ ⑧ ⑨ ⑩
(1)上述元素中,形成化合物种类最多的是______(填元素符号)。
(2)元素①、④和⑤形成的化合物的电子式是______,该化合物中存在的化学键类型是______。
(3)②、③、⑦三种元素原子半径由大到小的顺序是______(用元素符号表示)。
⑤、⑥、⑦、⑧、⑨、⑩六种元素形成的简单离子,半径最小的是_________,最大的是___________(填离
子符号)。
(4)⑤、⑥、⑦三种元素最髙价氧化物对应水化物的碱性由强到弱的顺序是______(用对应物质的化学式表
示)。
(5)最易形成离子键的两种元素代号是_____________。
(6)能比较元素⑨和⑩非金属性强弱的实验事实是______(填字母序号)。
a.⑨的氢化物的酸性比⑩的氢化物的酸性弱
b.⑩的单质R 与H 化合比⑨的单质Q与H 化合容易,且HR的稳定性比HQ强
2 2 2 2
c.在⑨的氢化物HQ的水溶液中通少量⑩的单质R 气体可置换出单质Q
2 2
16.(14分)(2020·全国高一单元测试)Ⅰ.按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是_。
(2)写出下列物质的电子式: ______, ______, ____。(3)用电子式表示下列化合物的形成过程: :____. :____。
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是____(填化学式)。
(2)10种元素中,原子半径最小的是______(填序号)。
(3)元素⑦的简单氢化物与元素③的单质反应的离子方程式为______。
(4)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为______。
(5)元素①的原子序数为______,其单质与元素⑦的简单氢化物在高温下反应的化学方程式为___。
(6)元素②的单质易溶于元素⑥与③形成的化合物中,所得溶液颜色为______色。
17.(10分)(2020·新疆新区·乌鲁木齐市第70中高三月考)已知A、B、D、E、G、H、J都是周期表中
前四周期的元素,它们的原子序数依次增大。其中A元素原子的最外层电子数是次外层电子数的2倍,B
元素的最髙正价与最低负价代数和为2,D是非金属性最强的元素,D、H同主族,E是同周期元素中离子
半径最小的元素,G元素的最高价含氧酸为二元强酸,J是第Ⅷ族元素,是生活中最常用的金属元素。请
回答:
(1)阴离子GAB-与CO 结构相似,GAB-的电子式为_______。
2
(2)用电子式表示B 的形成过程__________________________________ 。
2
(3)D的氢化物水溶液中存在的氢键有_______种,画出其中一种_______。(用“ ”表示氢键,用短线表
示共价键)
(4)检验J3+的离子方程式为______________________________________。
(5)H与E能形成化合物乙。在1.01105Pa、T℃时,气体摩尔体积为53.4L/mol,实验测得乙的气态密度为
1
5.00g/L,则此时乙的分子式为_______。
18.(12分)(2020·广东禅城·佛山一中高一期末)下表是元素周期表的一部分,针对表中的①~⑩中元
素,请用化学用语填空回答以下问题:
主族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
二 ① ②三 ③ ④ ⑤ ⑥ ⑦ ⑧
四 ⑨ ⑩
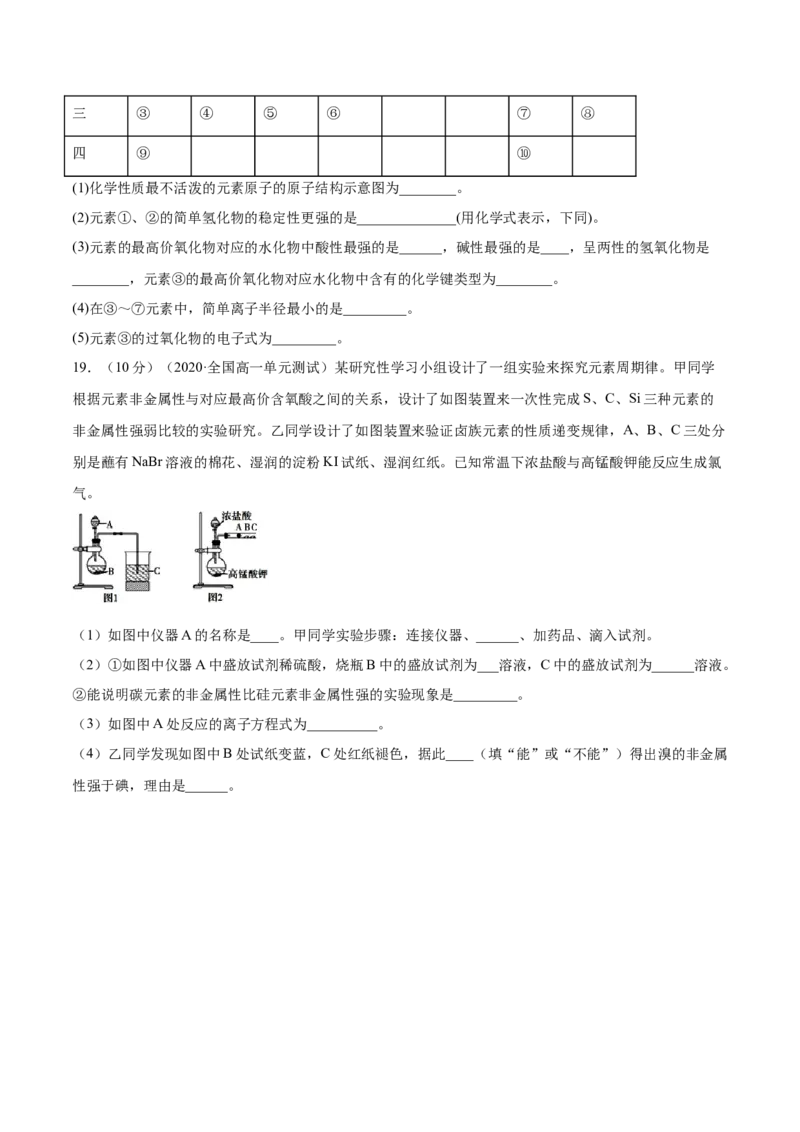
(1)化学性质最不活泼的元素原子的原子结构示意图为________。
(2)元素①、②的简单氢化物的稳定性更强的是______________(用化学式表示,下同)。
(3)元素的最高价氧化物对应的水化物中酸性最强的是______,碱性最强的是____,呈两性的氢氧化物是
________,元素③的最高价氧化物对应水化物中含有的化学键类型为________。
(4)在③~⑦元素中,简单离子半径最小的是_________。
(5)元素③的过氧化物的电子式为_________。
19.(10分)(2020·全国高一单元测试)某研究性学习小组设计了一组实验来探究元素周期律。甲同学
根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成S、C、Si三种元素的
非金属性强弱比较的实验研究。乙同学设计了如图装置来验证卤族元素的性质递变规律,A、B、C三处分
别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯
气。
(1)如图中仪器A的名称是____。甲同学实验步骤:连接仪器、______、加药品、滴入试剂。
(2)①如图中仪器A中盛放试剂稀硫酸,烧瓶B中的盛放试剂为___溶液,C中的盛放试剂为______溶液。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是_________。
(3)如图中A处反应的离子方程式为__________。
(4)乙同学发现如图中B处试纸变蓝,C处红纸褪色,据此____(填“能”或“不能”)得出溴的非金属
性强于碘,理由是______。