文档内容
湖北省荆门市2018年中考化学真题试题
1. 学化学、用化学。下列说法正确的是
A. 提倡少开私家车大力推广共享单车、共享汽车,与我们倡导的“低碳”生活一致
B. 为增加节日氛围,节日期间提倡大量燃放烟花炮竹
C. 醋酸除水垢利用的是物理变化
D. 农业上提倡使用农家肥,因此农民可以在田间焚烧秸秆作为农田耙料
【答案】A
【解析】A. 提倡少开私家车大力推广共享单车、共享汽车,与我们倡导的“低碳”生活一致,正确;B. 大量
燃放烟花炮竹,会造成空气污染,错误;C. 用醋酸除水垢有新物质生成,利用的是化学变化,错误;D. 在田
间焚烧秸秆,会造成空气污染,错误。故选A。
2. 化学是一门以实验为基础的学科。下列实验操作正确的是
A. 少量的酒精洒在桌面上燃烧起来,应立即用湿抹布扑盖
B. 用镊子小心的将块状固体放入垂直的试管中
C. 用100mL量简量取9.5mLNaCl溶液
D. 用托盘天平称量某固体样品的质量为5.00克
【答案】A
【解析】A. 少量的酒精洒在桌面上燃烧起来,应立即用湿抹布扑盖,使酒精与空气隔绝,达到灭火的目的,正
确;B. 用镊子小心的将块状固体放入水平放置的试管口,然后将试管慢慢地竖立起来,错误;C. 用10mL量
简量取9.5mLNaCl溶液,错误;D. 用托盘天平称量固体的质量,一般精确到0.1g,错误。故选A。
3. 下列说法不正确的是
A. CO、O、CH、氟氯代烷等都能产生温室效应
2 3 4
B. 液化气、汽油、煤油都是石油的加工产品
C. 超市里卖的纯净水是纯净物
D. 露天焚烧垃圾会增加空气中的PM2.5
【答案】C
【解析】A. CO、O、CH、氟氯代烷等都能产生温室效应,正确;B. 液化气、汽油、煤油都是石油的加工产品,正
2 3 4
确;C. 超市里卖的纯净水中含有不同种物质,属于混合物,错误;D. 露天焚烧垃圾会增加空气中的PM2.5,
正确。故选C。
4. 下列描述正确的是
A. 铁丝在O 中燃绕火星四射,有黑色固体产生
2
1B. 金属铝在空气中具有抗腐蚀性,是因为金属铝不与空气反应
C. 加热高锰酸钾可以制取O,液化空气也可以制取O,两者都属于化学变化
2 2
D. 硫在O 中燃烧发出微弱的淡蓝色火焰,并生成有刺激性气味的气体
2
【答案】A
【解析】A. 铁丝在O 中燃绕火星四射,有黑色固体产生,正确;B. 金属铝在空气中具有抗腐蚀性,是因为金
2
属铝与空气中的氧气反应,其表面形成了一层致密的氧化物薄膜,从而阻止铝进一步氧化,错误;C. 加热高
锰酸钾可以制取O,液化空气也可以制取O,前者属于化学变化,后者属于物理变化,错误;D. 硫在O 中燃
2 2 2
烧发出明亮的蓝紫色火焰,并生成有刺激性气味的气体,错误。故选A。
5. 下列有关元素、微粒以及物质的描述正确的是
A. 金刚石、石墨、C 都是由碳元素组成的结构不同、但性质相同的单质
60
B. “富硒大米”中的硒指的是元素
C. 电解水可以制取氢气,说明水中含有氢气
D. O2-、Na+质子数和电子数都不同
【答案】B
【解析】A. 金刚石、石墨、C 都是由碳元素组成的结构不同、性质也不相同的单质,错误;B. “富硒大米”中
60
的硒指的是元素,正确;C. 电解水可以制取氢气,说明水中含有氢元素,错误;D. O2-、Na+质子数分别是8、
11,核外电子数都是10,错误。故选B。
6. 石油裂解气中含有CH 和CH,二者以任意比例混和时,下列判断不正确的是
2 4 4 8
A. 完全燃烧时生成CO 和HO的质量比为定值
2 2
B. 不完全燃烧时生成CO、CO 和HO,若产物HO、CO 分别为18g、22g,则CO为l4g
2 2 2 2
C. 混合气体中碳的质量分数为
D. 混合气体总质量一定时,消耗的O 不一定为定值
2
【答案】D
【解析】A. CH 和CH 中碳、氢元素的质量比相等,所以完全燃烧时生成CO 和HO的质量比为定值,正确;B.
2 4 4 8 2 2
CH 和CH 中碳、氢元素的质量比相等,为:(12×2):(1×4)=6:1,18gHO中氢元素的质量是18g× =2g,
2 4 4 8 2
22gCO 中碳元素的质量是:22g× =6g,l4gCO中碳元素是质量是:l4g× =6g,碳元素的质量:6g+6g=12g,
2
氢元素的质量是2g,碳元素与氢元素的质量比为:12g:2g=6:1,正确;C. 混合气体中碳的质量分数为
2= ,正确;
D. 因为CH 和CH 中碳、氢元素的质量比相等,所以混合气体总质量一定时,消耗的O 一定为定值,错误。故
2 4 4 8 2
选D。
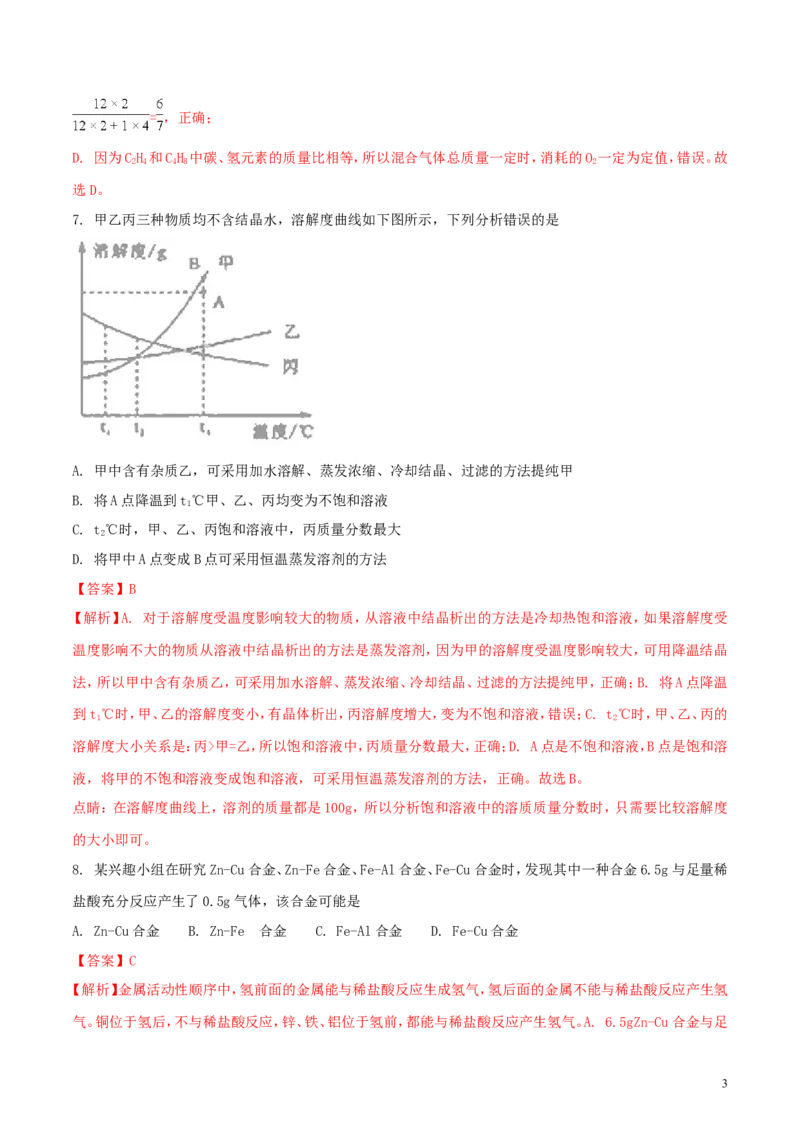
7. 甲乙丙三种物质均不含结晶水,溶解度曲线如下图所示,下列分析错误的是
A. 甲中含有杂质乙,可采用加水溶解、蒸发浓缩、冷却结晶、过滤的方法提纯甲
B. 将A点降温到t℃甲、乙、丙均变为不饱和溶液
1
C. t℃时,甲、乙、丙饱和溶液中,丙质量分数最大
2
D. 将甲中A点变成B点可采用恒温蒸发溶剂的方法
【答案】B
【解析】A. 对于溶解度受温度影响较大的物质,从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受
温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂,因为甲的溶解度受温度影响较大,可用降温结晶
法,所以甲中含有杂质乙,可采用加水溶解、蒸发浓缩、冷却结晶、过滤的方法提纯甲,正确;B. 将A点降温
到t℃时,甲、乙的溶解度变小,有晶体析出,丙溶解度增大,变为不饱和溶液,错误;C. t℃时,甲、乙、丙的
1 2
溶解度大小关系是:丙>甲=乙,所以饱和溶液中,丙质量分数最大,正确;D. A点是不饱和溶液,B点是饱和溶
液,将甲的不饱和溶液变成饱和溶液,可采用恒温蒸发溶剂的方法,正确。故选B。
点睛:在溶解度曲线上,溶剂的质量都是100g,所以分析饱和溶液中的溶质质量分数时,只需要比较溶解度
的大小即可。
8. 某兴趣小组在研究Zn-Cu合金、Zn-Fe合金、Fe-Al合金、Fe-Cu合金时,发现其中一种合金6.5g与足量稀
盐酸充分反应产生了0.5g气体,该合金可能是
A. Zn-Cu合金 B. Zn-Fe 合金 C. Fe-Al合金 D. Fe-Cu合金
【答案】C
【解析】金属活动性顺序中,氢前面的金属能与稀盐酸反应生成氢气,氢后面的金属不能与稀盐酸反应产生氢
气。铜位于氢后,不与稀盐酸反应,锌、铁、铝位于氢前,都能与稀盐酸反应产生氢气。A. 6.5gZn-Cu合金与足
3量稀盐酸充分反应产生氢气的质量少于0.2g,不符合题意;B. 6.5gZn与足量稀盐酸充分反应产生氢气的质
量是0.2g,6.5gFe与足量稀盐酸充分反应产生氢气的质量是0.23g,所以6.5gZn-Fe合金与足量稀盐酸充分
反应产生氢气的质量大于0.2g,少于0.23g,不符合题意;C. 6.5gFe-Al合金与足量稀盐酸充分反应产生氢
气的质量大于0.23g,少于0.72g,符合题意;D. 6.5g Fe-Cu合金与足量稀盐酸充分反应产生氢气的质量少
于0.23g,不符合题意。故选C。
点睛:金属活动性顺序中,氢前面的金属能与稀盐酸反应生成氢气,氢后面的金属不能与稀盐酸反应产生氢
气。先计算出6.5g某纯净的金属单质与酸反应产生氢气的质量,当6.5g两种金属都与酸反应时,则产生氢
气的质量介于一种金属单质与酸反应产生氢气的质量之间。
9. 化学使我们的生结丰富多彩,生活中处处有化学。请用化学知识回答下列问题:
(1)画出O2-的结构示意图______。
(2)浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,然后再涂上3%-5%的____(填名称)的溶液。
(3)乙醇______(填“能”或“不能”)导电
(4)干冰_______(填“是“或者“不是”)冰
(5)电解水时加少量NaOH以增强导电性,在电解过程中NaOH不发生反应,则电解后溶液的pH_______ (填”
增大”、“减小”或者“不变”)
(6)氧化钙与水反应、镁与盐酸反应均_______(填“放出”或“吸收”)热量。
【答案】 (1). ; (2). 碳酸氨钠; (3). 不能; (4). 不是; (5). 增大;
(6). 放出
【解析】(1)O2-的核内有8个质子,核外有10个电子,第一层排两个电子,第二层有10个电子。(2)皮肤上沾有
酸溶液,用水冲洗后,然后再涂上3%-5%的碳酸氨钠的溶液。(3)乙醇中不存在自由移动的带有电荷的粒子,
所以乙醇不能导电。(4)干冰是二氧化碳固体,不是冰。(5)电解水时加少量NaOH以增强导电性,在电解过程
中NaOH不发生反应,电解后溶液的碱性增强,pH增大。(6)氧化钙与水反应、镁与盐酸反应均放出热量。
10. 请从H、C、N、O、Na、Cl、K、Ca中选取相关元素,用合适的化学用语填空。
(1)已知NO-,请标出N(NO) 中加点N的化合价________
2 2 3
(2)含有2核10电子的阴离子________
(3)厨房最常见的调味品________(填化学式,以下均同)
(4)可作复合肥的盐_________.
(5)实验室中可在MnO 催化下制O 的物质_________(含2种元素)、________(含3种元素)
2 2
(6)可作补钙剂的物质________。
4【答案】 (1). +3; (2). OH-; (3). NaCl; (4). KNO; (5). HO (6). KClO;
3 2 2 3
(7). CaCO
3
【解析】(1)化合物中各元素化合价的代数和为零,NO-的化合价是-1,所以N(NO) 中N的化合价为+3。(2)含
2 2 3
有2核10电子的阴离子是含有2个原子核,即含有2个原子,10个电子的阴离子,是OH-。(3)厨房最常见的
调味品是NaCl。(4) KNO 是可作复合肥的盐。(5)实验室中可在MnO 催化下制O 的物质(含2种元素)的是
3 2 2
HO,(含3种元素)的物质是KClO。(6)CaCO 可作补钙剂。
2 2 3 3
11. A~I均为初中化学常见物貭,它们之间的转化关系如下图,部分产物己略去。己知A是人体胃酸的主要
成分,B是大理石的主要成分,D为液体,F为气体,I能与A反应生成个数比为1:2的+2价、+3价铁盐。
(1)写出下列物质的化学式C________、H_________ 。
(2)上述①②③④⑤中属于化合反应的是________、属于分解反应的是________
(3)写出G→H的化学反应方程式________。
(4)写出I和A反应的化学反应方程式________。
【答案】 (1). CaCl; (2). Fe; (3). ③⑤ (4). ② (5). 3CO+FeO 2Fe+3CO
2 2 3 2
(6). FeO+8HCl== FeCl+ 2FeCl + 4HO
3 4 2 3 2
5点睛:要顺利解答推断题,就要熟悉物质的性质、用途、常发生的化学反应、与其它物质之间的相互转化、甚
至反应条件等,该类题是综合性较强的题,要求必须能把知识系统起来。
12. 实验探究题:
已知某生铁合金除了含有铁、碳外,还含有硅或者铝中的一种。
某化学兴趣小组对该生铁合金产生了浓厚的兴趣,于是探究到底是含有硅还是铝。
【查阅资料】
硅不能与盐酸反应,但能与NaOH溶液反应:Si+2NaOH+HO=NaSiO+2H↑。
2 2 3 2
铝与NaOH溶液反应生成NaAlO 与H,则铝与NaOH溶液反应的化学方程式为____________。
2 2
【提出猜想】
猜想一:该生铁合金除了含有铁、碳外,还含有硅。
猜想二:该生铁合金除了含有铁、碳外,还含有________
实验步骤及现象:
①取一定生铁合金,加入过量的________,充分反应后,合金部分溶解,并有无色气体产生。
②取步骤①中的滤渣,加入过最的________,充分反应后,滤渣部分溶解,并有气体放出。
实验结论:猜想_____正确。若步骤②中实验现象为无现象,则猜想_____正确。
【答案】 (1). 2Al+2NaOH+2HO=2NaAlO+3H↑; (2). 铝 (3). 盐酸 (4). NaOH溶液 (5).
2 2 2
一 (6). 二
【解析】【查阅资料】根据题给信息,铝与NaOH溶液反应的化学方程式为:2Al+2NaOH+2HO=2NaAlO+3H↑。【提
2 2 2
6出猜想】猜想二:根据题给信息,该生铁合金除了含有铁、碳外,还含有铝。实验步骤及现象:①因为硅不能与
盐酸反应,但能与NaOH溶液反应,所以先加入足量的盐酸,除去能与酸反应的金属单质,再加入NaOH溶液,
如果滤渣部分溶解,并有气体放出,说明猜想一正确,若步骤②中无实验现,则猜想二正确。
13. 计算题:
某固体样品可能含有NaCl、NaHCO、NaCO 中的一种、二种或三种。某兴趣小组取出100g固体与足量的稀硫酸
3 2 3
反应,将产生的气体通入足量的澄清石灰水,生成沉淀100g。然后又取出等质量的样品加水溶解,再加入足
量的CaCl 生成沉淀50g(己知:NaHCO 与CaCl 不反应).
2 3 2
(1)该固体样品成分是________。
(2)求该固体样品中NaCO 质量分数为多少___________? (写出计算过程)
2 3
【答案】 (1). NaC1.NaHCO.NaCO (2). 53%.
3 2 3
NaCO + CaCl == CaCO↓+ 2NaCl
2 3 2 3
106 100
x 50g
= ,解得x=53g
NaCO + 2HCl == 2NaCl + HO + CO↑,NaHCO + HCl == NaCl + HO + CO↑,CO + Ca(OH) == CaCO↓+
2 3 2 2 3 2 2 2 2 3
HO
2
所以100g-50g=50g沉淀是NaHCO 发生有关反应生成的,设样品中NaHCO 的质量是y。
3 3
NaHCO ---- CaCO
3 3
84 100
y 100g-50g=50g
= ,解得y=42g
53g+42g=95g<100g,所以样品是由碳酸钠、碳酸氢钠、氯化钠组成的。
(2)固体样品中NaCO 质量分数为: ×100%=53%
2 3
7点睛:要顺利解答此题,首先要从题中获取信息,根据题给信息,结合化学方程式的计算,确定出样品的成分,
获取信息是解答此题的关键。
8