文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
秘密★启用前
2024 年遂宁市初中毕业暨高中阶段学校招生考试
理科综合试卷
注意事项:
1.理科综合共200分,包括物理90分、化学70分、生物学40分。考试时间共150分钟。
2.答题前,考生务必将自己的学校、姓名和准考证号用 0.5毫米的黑色墨迹签字笔填写在答
题卡对应位置上,并检查条形码粘贴是否正确。
3.选择题使用2B铅笔涂在答题卡对应位置上,非选择题用 0.5毫米黑色墨迹签字笔书写在
答题卡对应位置上,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
4.保持答题卡卡面清洁,不折叠、不破损。考试结束后,将本试卷和答题卡一并交回。
化学部分
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
一、选择题(本题包括7个小题,每小题3分,共21分,每小题只有一个选项符合题意)
1. 遂宁射洪市享有“子昂故里、诗酒之乡”的美誉,当地的蒸馏酒传统酿造技艺是国家级非物质文化遗产
之一,对于研究我国传统生物发酵工业具有极高的价值。下列过程涉及化学变化的是
A. 研磨 B. 发酵 C. 蒸馏 D. 灌装
【答案】B
【解析】
【详解】A、研磨只是物质的形态发生改变,没有新物质生成,属于物理变化,不符合题意;
B、发酵过程中生成酒精,有新物质生成,属于化学变化,符合题意;
C、蒸馏主要是利用物质沸点不同进行分离,此过程中只是物质的状态发生改变,没有新物质生成,属于
物理变化,不符合题意;
D、灌装只是物质的转移和存放,没有新物质生成,属于物理变化,不符合题意。
故选B。
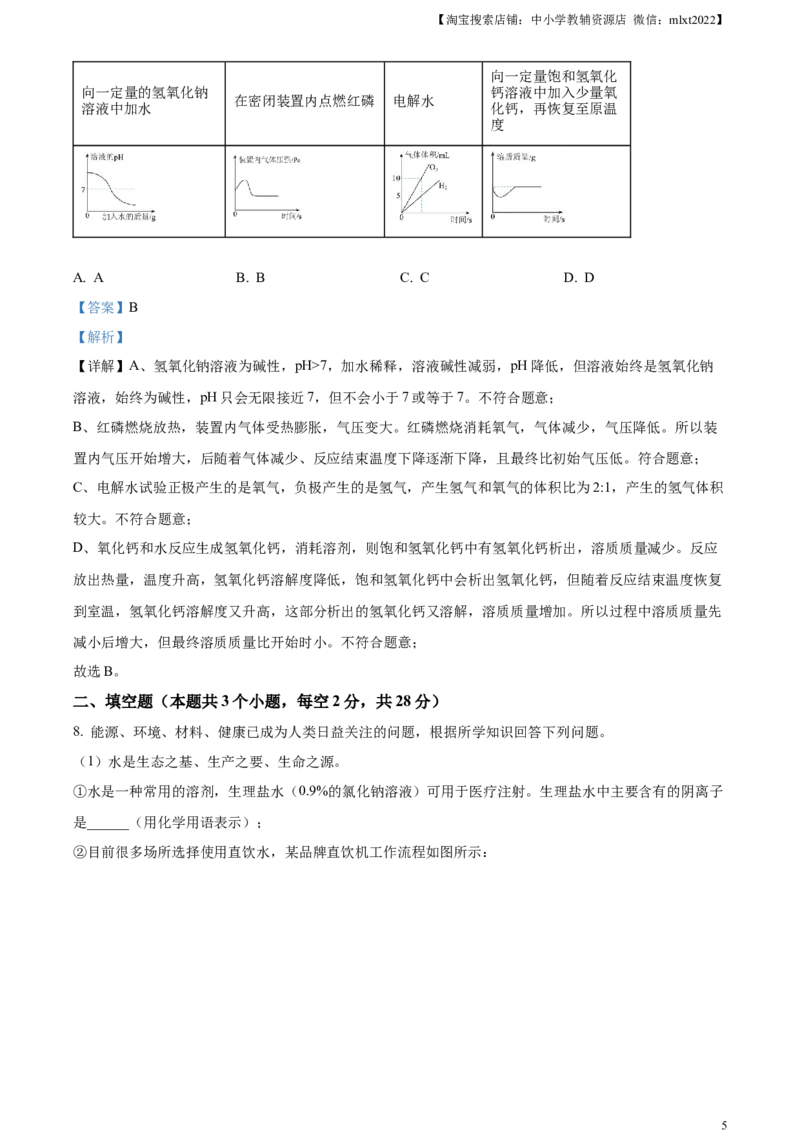
2. 规范操作是实验成功的保证。以下实验基本操作正确的是
A. 稀释浓硫酸 B. 测定溶液的pH
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C. 滴加液体 D. 检查装置的气密性
【答案】D
【解析】
【详解】A、稀释浓硫酸,需要将浓硫酸沿烧杯壁缓缓倒入水中,并用玻璃棒不断搅拌散热,不能将水倒
入浓硫酸中 。不符合题意;
B、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,
与标准比色卡对比来确定pH。不能把pH试纸直接伸入待测溶液中,以免污染待测液。不符合题意;
C、使用胶头滴管滴液时,滴管竖直放在容器口的正上方,不得伸入容器内,更不能接触容器内壁。不符
合题意;
D、检查装置气密性,先将导管放入水中,然后用手捂住试管,如导管口有气泡冒出则装置气密性良好。
符合题意;
故选D。
3. 归纳总结是学习化学的基本方法,下列知识点归纳有错误的一组是
A.化学与农业 B.化学与能源
①可用熟石灰改良酸性土壤 ①化石燃料使用便捷,我们无需开发新能源
②合理使用化肥提高粮食产量 ②煤、石油和天然气都属于可再生能源
C.化学与环境 D.化学与生活
①垃圾分类回收,实现资源再利用
①洗涤剂除油污是利用了洗涤剂的乳化作用
②推行使用可降解塑料,可减少“白色污
②炒菜时油锅不慎着火,立即盖上锅盖灭火
染”
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、①熟石灰氢氧化钙为碱性,能和酸性土壤中的酸性物质反应,可用熟石灰改良酸性土壤。②
化肥中含有植物生长需求较多的氮磷钾等元素,合理使用化肥提高粮食产量且可以避免因为过量使用引起
的土壤和水污染。归纳正确;
B、①化石燃料是不可再生能源,储量有限。且化石燃料燃烧排放大量污染气体和二氧化碳,导致空气污
染和温室效应加剧,我们应开发新能源。②煤、石油和天然气短时间内无法得到补充,都属于不可再生能
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
源。归纳错误;
C、①垃圾分类回收,实现资源(如塑料、金属等)再利用,节约资源和能源,同时可以减少环境污染。
②“白色污染”是由于塑料等不易降解产生的污染,推行使用可降解塑料,可减少“白色污染”。归纳正
确;
D、①洗涤剂对油污有乳化作用,可将油污分散为小液滴,形成乳浊液除去。洗涤剂除油污是利用了洗涤
剂的乳化作用。②炒菜时油锅不慎着火,立即盖上锅盖灭火,利用隔绝空气的原理灭火。归纳正确;
故选B。
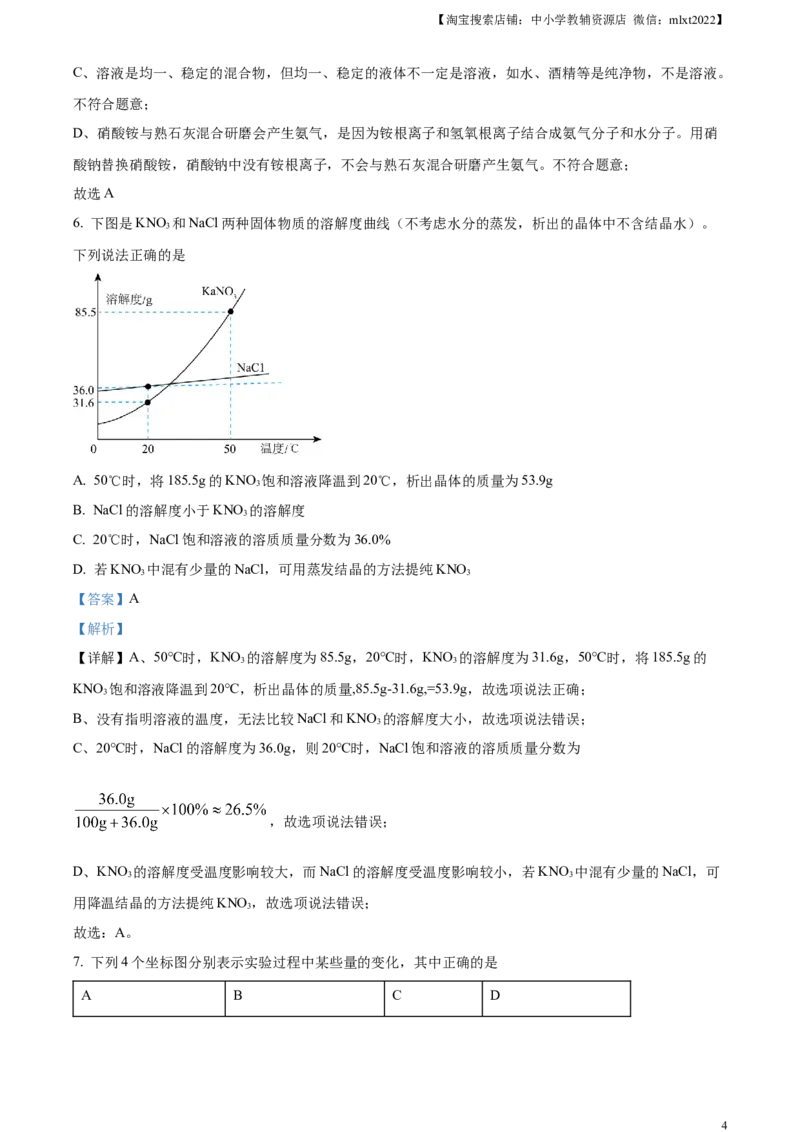
4. 2024年以“创新预见6G未来”为主题的全球6G技术大会在南京召开。氮化镓是制造芯片的材料之一。
镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是
A. 镓元素为非金属元素 B. 镓原子的中子数是31
C. 图中X的数值是8 D. 镓的相对原子质量是69.72g
【答案】C
【解析】
【详解】A、镓是“钅”字旁,所以镓元素为金属元素。不符合题意;
B、元素周期表一格左上角数字为原子序数=质子数,最下方数字为相对原子质量。相对原子质量≈质子数
+中子数,所以镓原子的中子数是70-31=39。不符合题意;
C、原子中质子数=核外电子数,所以31=2+X+18+3,X=8。符合题意;
D、相对原子质量的单位是“1”不是“g”,镓的相对原子质量是69.72。不符合题意;
故选C。
5. 逻辑推理是学习化学常用的思维方法,下列推理正确的是
A. 在室温下,碱溶液的pH>7,但pH>7的溶液不一定是碱溶液
B. 离子是带电荷的微粒,所以带电荷的微粒一定是离子
C. 溶液是均一、稳定的,因此均一、稳定的液体一定是溶液
.
D 硝酸铵与熟石灰混合研磨会产生氨气,所以用硝酸钠替换硝酸铵也会产生氨气
【答案】A
【解析】
【详解】A、在室温下,碱溶液的pH>7,但pH>7的溶液不一定是碱溶液,如室温下,碳酸钠溶液的
pH>7,但碳酸钠溶液是盐溶液。符合题意;
B、离子是带电荷的微粒,但带电荷的微粒不一定是离子,如电子带负电荷,但不是离子。不符合题意;
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
C、溶液是均一、稳定的混合物,但均一、稳定的液体不一定是溶液,如水、酒精等是纯净物,不是溶液。
不符合题意;
D、硝酸铵与熟石灰混合研磨会产生氨气,是因为铵根离子和氢氧根离子结合成氨气分子和水分子。用硝
酸钠替换硝酸铵,硝酸钠中没有铵根离子,不会与熟石灰混合研磨产生氨气。不符合题意;
故选A 。
6. 下图是KNO 和NaCl两种固体物质的溶解度曲线(不考虑水分的蒸发,析出的晶体中不含结晶水)。
3
下列说法正确的是
A. 50℃时,将185.5g的KNO 饱和溶液降温到20℃,析出晶体的质量为53.9g
3
B. NaCl的溶解度小于KNO 的溶解度
3
C. 20℃时,NaCl饱和溶液的溶质质量分数为36.0%
D. 若KNO 中混有少量的NaCl,可用蒸发结晶的方法提纯KNO
3 3
【答案】A
【解析】
【详解】A、50℃时,KNO 的溶解度为85.5g,20℃时,KNO 的溶解度为31.6g,50℃时,将185.5g的
3 3
KNO 饱和溶液降温到20℃,析出晶体的质量,85.5g-31.6g,=53.9g,故选项说法正确;
3
B、没有指明溶液的温度,无法比较NaCl和KNO 的溶解度大小,故选项说法错误;
3
C、20℃时,NaCl的溶解度为36.0g,则20℃时,NaCl饱和溶液的溶质质量分数为
,故选项说法错误;
D、KNO 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,若KNO 中混有少量的NaCl,可
3 3
用降温结晶的方法提纯KNO,故选项说法错误;
3
故选:A。
7. 下列4个坐标图分别表示实验过程中某些量的变化,其中正确的是
A B C D
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
向一定量饱和氢氧化
向一定量的氢氧化钠 钙溶液中加入少量氧
在密闭装置内点燃红磷 电解水
溶液中加水 化钙,再恢复至原温
度
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、氢氧化钠溶液为碱性,pH>7,加水稀释,溶液碱性减弱,pH降低,但溶液始终是氢氧化钠
溶液,始终为碱性,pH只会无限接近7,但不会小于7或等于7。不符合题意;
B、红磷燃烧放热,装置内气体受热膨胀,气压变大。红磷燃烧消耗氧气,气体减少,气压降低。所以装
置内气压开始增大,后随着气体减少、反应结束温度下降逐渐下降,且最终比初始气压低。符合题意;
C、电解水试验正极产生的是氧气,负极产生的是氢气,产生氢气和氧气的体积比为2:1,产生的氢气体积
较大。不符合题意;
D、氧化钙和水反应生成氢氧化钙,消耗溶剂,则饱和氢氧化钙中有氢氧化钙析出,溶质质量减少。反应
放出热量,温度升高,氢氧化钙溶解度降低,饱和氢氧化钙中会析出氢氧化钙,但随着反应结束温度恢复
到室温,氢氧化钙溶解度又升高,这部分析出的氢氧化钙又溶解,溶质质量增加。所以过程中溶质质量先
减小后增大,但最终溶质质量比开始时小。不符合题意;
故选B。
二、填空题(本题共3个小题,每空2分,共28分)
8. 能源、环境、材料、健康已成为人类日益关注的问题,根据所学知识回答下列问题。
(1)水是生态之基、生产之要、生命之源。
①水是一种常用的溶剂,生理盐水(0.9%的氯化钠溶液)可用于医疗注射。生理盐水中主要含有的阴离子
是______(用化学用语表示);
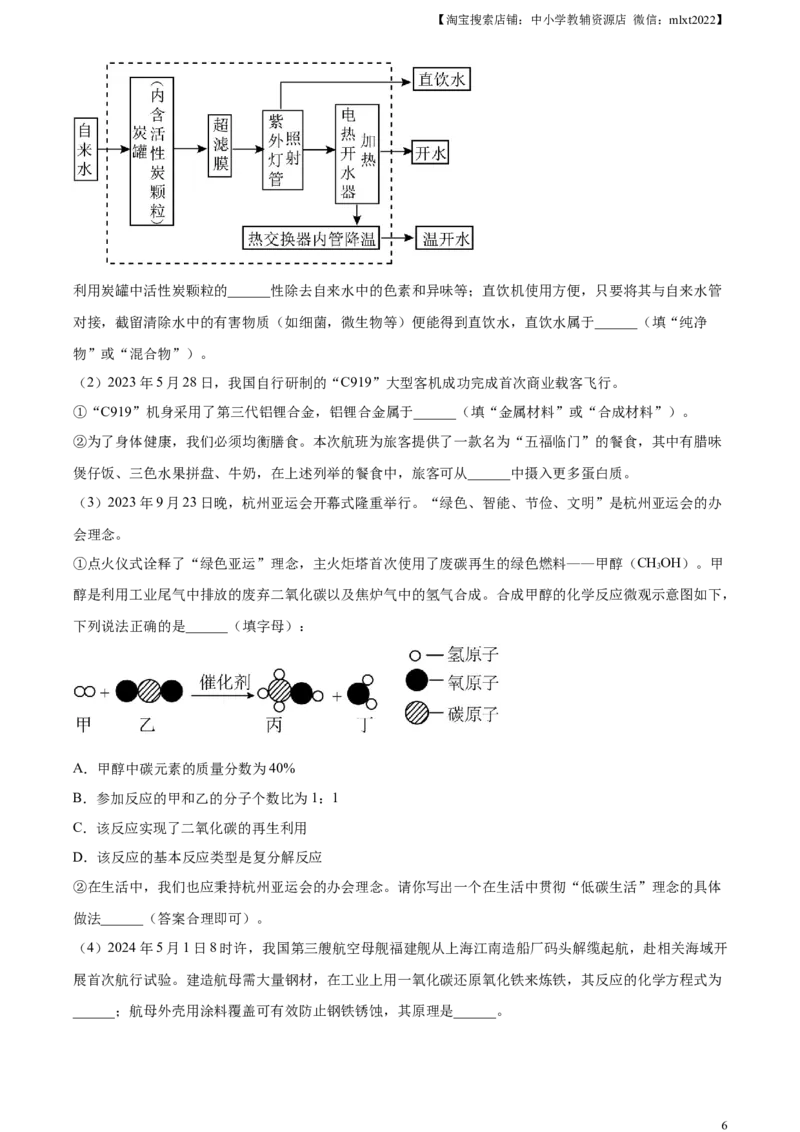
②目前很多场所选择使用直饮水,某品牌直饮机工作流程如图所示:
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
利用炭罐中活性炭颗粒的______性除去自来水中的色素和异味等;直饮机使用方便,只要将其与自来水管
对接,截留清除水中的有害物质(如细菌,微生物等)便能得到直饮水,直饮水属于______(填“纯净
物”或“混合物”)。
(2)2023年5月28日,我国自行研制的“C919”大型客机成功完成首次商业载客飞行。
①“C919”机身采用了第三代铝锂合金,铝锂合金属于______(填“金属材料”或“合成材料”)。
②为了身体健康,我们必须均衡膳食。本次航班为旅客提供了一款名为“五福临门”的餐食,其中有腊味
煲仔饭、三色水果拼盘、牛奶,在上述列举的餐食中,旅客可从______中摄入更多蛋白质。
(3)2023年9月23日晚,杭州亚运会开幕式隆重举行。“绿色、智能、节俭、文明”是杭州亚运会的办
会理念。
①点火仪式诠释了“绿色亚运”理念,主火炬塔首次使用了废碳再生的绿色燃料——甲醇(CHOH)。甲
3
醇是利用工业尾气中排放的废弃二氧化碳以及焦炉气中的氢气合成。合成甲醇的化学反应微观示意图如下,
下列说法正确的是______(填字母):
A.甲醇中碳元素的质量分数为40%
B.参加反应的甲和乙的分子个数比为1:1
C.该反应实现了二氧化碳的再生利用
D.该反应的基本反应类型是复分解反应
②在生活中,我们也应秉持杭州亚运会的办会理念。请你写出一个在生活中贯彻“低碳生活”理念的具体
做法______(答案合理即可)。
(4)2024年5月1日8时许,我国第三艘航空母舰福建舰从上海江南造船厂码头解缆起航,赴相关海域开
展首次航行试验。建造航母需大量钢材,在工业上用一氧化碳还原氧化铁来炼铁,其反应的化学方程式为
______;航母外壳用涂料覆盖可有效防止钢铁锈蚀,其原理是______。
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【答案】(1) ①. Cl- ②. 吸附 ③. 混合物
(2) ①. 金属材料 ②. 牛奶
(3) ①. C ②. 绿色出行
(4) ①. ②. 使铁与氧气和水隔绝
【解析】
【小问1详解】
①氯化钠由钠离子和氯离子构成,所以生理盐水中主要含有的阴离子是氯离子,其离子符号为Cl-;
②活性炭具有疏松多孔的结构,具有吸附性,利用炭罐中活性炭颗粒的吸附性除去自来水中的色素和异味
等;直饮水中含有水和一些矿物质,属于混合物;
【小问2详解】
①铝锂合金为合金,属于金属材料;
②腊味煲仔饭中富含淀粉,淀粉属于糖类,三色水果拼盘中富含维生素,牛奶中富含蛋白质,所以旅客可
从牛奶中摄入更多蛋白质;
【小问3详解】
①由微观示意图可知,二氧化碳和氢气在催化剂的催化作用下生成甲醇和水,反应的化学方程式为:
;
A、甲醇中碳元素的质量分数为 ,故选项说法错误;
B、由反应的化学方程式可知,参加反应的甲和乙的分子个数比为3:1,故选项说法错误;
C、该反应实现了二氧化碳的再生利用,故选项说法正确;
D、该反应不是两种化合物互相交换成分生成了另外两种化合物,不属于复分解反应,故选项说法错误;
故选:C;
②在生活中,绿色出行可减少化石燃料的使用,符合“低碳生活”理念。
【
小问4详解】
一氧化碳和氧化铁在高温条件下生成铁和二氧化碳,反应的化学方程式为:
;航母外壳用涂料覆盖可有效防止钢铁锈蚀,其原理是使铁与氧气和水隔
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
绝。
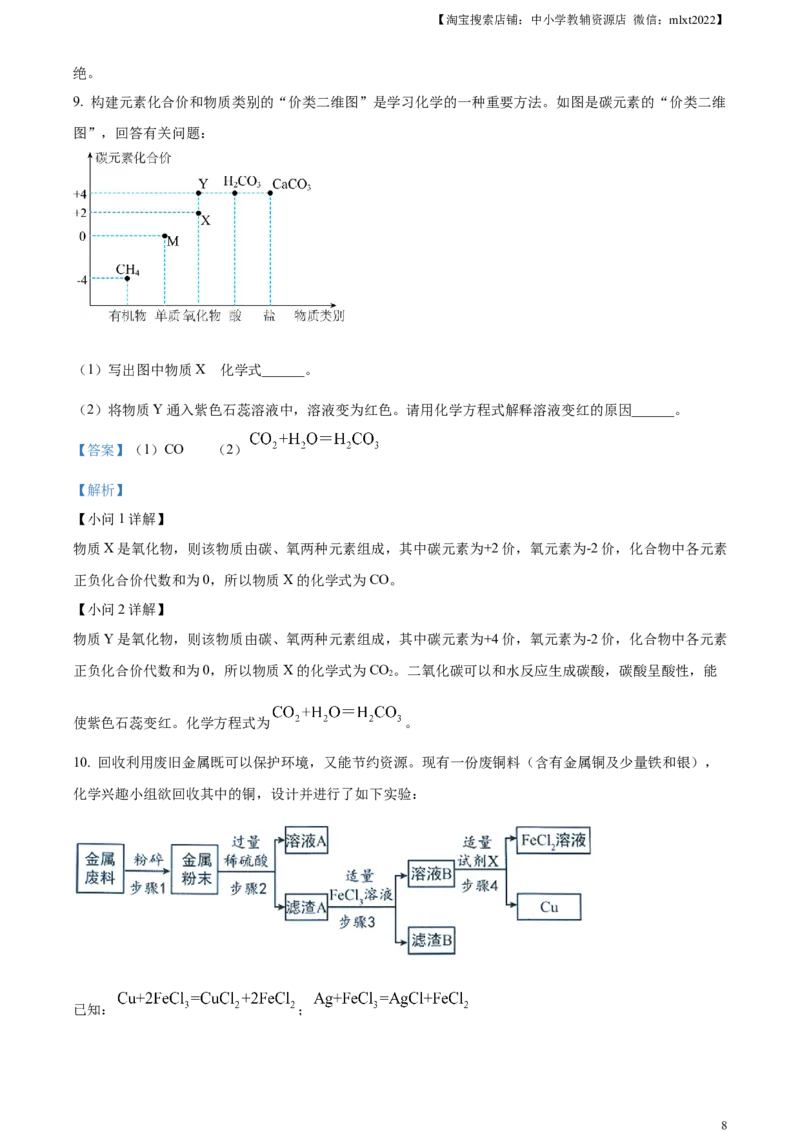
9. 构建元素化合价和物质类别的“价类二维图”是学习化学的一种重要方法。如图是碳元素的“价类二维
图”,回答有关问题:
的
(1)写出图中物质X 化学式______。
(2)将物质Y通入紫色石蕊溶液中,溶液变为红色。请用化学方程式解释溶液变红的原因______。
【答案】(1)CO (2)
【解析】
【小问1详解】
物质X是氧化物,则该物质由碳、氧两种元素组成,其中碳元素为+2价,氧元素为-2价,化合物中各元素
正负化合价代数和为0,所以物质X的化学式为CO。
【小问2详解】
物质Y是氧化物,则该物质由碳、氧两种元素组成,其中碳元素为+4价,氧元素为-2价,化合物中各元素
正负化合价代数和为0,所以物质X的化学式为CO。二氧化碳可以和水反应生成碳酸,碳酸呈酸性,能
2
使紫色石蕊变红。化学方程式为 。
10. 回收利用废旧金属既可以保护环境,又能节约资源。现有一份废铜料(含有金属铜及少量铁和银),
化学兴趣小组欲回收其中的铜,设计并进行了如下实验:
已知: ;
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
完成下列各题:
(1)步骤2中涉及的操作名称是______。
(2)溶液A中的溶质是______。
(3)步骤4中反应的化学方程式是______。
【答案】(1)过滤 (2)硫酸、硫酸亚铁
(3)
【解析】
【分析】废铜料中有铜、铁、银,稀硫酸可以和铁反应生成硫酸亚铁和氢气,和铜、银不反应。则溶液A
中溶质是过量的硫酸和生成的硫酸亚铁。滤渣A中有银和铜。加入氯化铁,氯化铁和铜反应生成氯化铜和
氯化亚铁,和银反应生成氯化银(不溶于水)和氯化亚铁,所以滤渣B为氯化银,溶液B中有氯化铜、氯
化亚铁,加入试剂X得到氯化亚铁和铜,则试剂X和氯化铜反应生成氯化亚铁和铜,则试剂X是铁。
【小问1详解】
步骤2将固体和液体分离,是过滤操作。
【小问2详解】
根据分析,溶液A中的溶质是过量的硫酸和生成的硫酸亚铁。
【小问3详解】
根据分析,步骤4是铁和氯化铜反应生成氯化亚铁和铜,化学方程式为 。
三、实验探究题(本题共2个小题,每空2分,共14分)
11. 根据下列实验装置图,回答问题:
(1)装置B中仪器a的名称是______。
(2)实验室用过氧化氢溶液制取并收集40mL干燥的氧气,应选择的装置是______(填装置的字母序号);
其反应的化学方程式为______。
(3)实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷气体,应选择的发生装置是______(填
装置的字母序号)。
【答案】(1)酒精灯 (2) ①. AFG ②.
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(3)B
【解析】
【小问1详解】
仪器a的名称是酒精灯。
【小问2详解】
过氧化氢溶液制取氧气不需要加热,是固液不加热型反应,发生装置选择A。排水法收集的氧气不干燥,
则不能使用E排水法收集。氧气密度比空气大,可使用向上排空气法收集,虽然排空气法收集气体干燥,
但并不能收集一定量的氧气,所以不选择装置C、D收集。G装置中,氧气从短管通入,将植物油排入量
筒,可收集干燥的氧气,同时排出的植物油的体积与收集的氧气的体积相同,则量筒中有40mL植物油时
说明收集了40mL氧气,此时停止收集即可。因为制取的氧气中带有水蒸气,需要使用F浓硫酸干燥,除
去水蒸气。所以应选择的装置是AFG。
过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为 。
【小问3详解】
加热无水醋酸钠和碱石灰的固体混合物制取甲烷气体,是固体加热型反应,发生装置选择B。
12. 同学们学习了盐的相关知识后,知道BaCO 为白色固体,难溶于水;BaSO 为白色固体,难溶于水和
3 4
盐酸。他们运用所学知识分组设计并完成了“检验碳酸钠溶液中是否混有硫酸钠”的实验,请你帮助他们完
成以下实验报告单并进行交流评价(温馨提示:本题中番号①~③为答题卡上的序号)。
化学实验报告单
姓名:明明 合作者:芳芳
班级:九年级一班 日期:2024.3。25
【实验名称】检验碳酸钠溶液中是否混有硫酸钠
【实验目的】NaCO 与NaSO 的区别
2 3 2 4
【实验仪器】试管2支、试管架、试管刷、胶头滴管、抹布、盛放废弃物的大烧杯等
【实验药品】待测溶液、氯化钡溶液、稀盐酸
【实验过程】
(1)
实验步骤 实验现象 实验结论
1、取待测溶液1-2mL于试管中,向试管中加入足量氯化钡溶 产生白色沉
液,振荡 淀
NaCO 溶液中混有
2 3
NaSO
2 4
2、向步骤1的试管中滴加少量的稀盐酸 ______
10【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
【交流评价】
(2)其他组同学认为实验步骤2不够严谨,不能证明混合溶液中一定存在硫酸钠,其理由是______;则步
骤1中一定发生反应的化学方程式为______。
【反思拓展】
进行物质的检验时,除了根据物质的不同性质选择恰当的试剂和方法,还应充分考虑加入试剂的用量。
【答案】(1)白色沉淀部分溶解
( 2 ) ① . 滴 加 少 量 稀 盐 酸 , 生 成 碳 酸 钡 可 能 没 有 反 应 完 全 ② .
【解析】
【小问1详解】
1、实验步骤:取待测溶液1-2mL于试管中,向试管中加入足量氯化钡溶液,振荡,实验现象:产生白色
沉淀;
2、实验步骤:向步骤1的试管中滴加少量的稀盐酸,实验结论:NaCO 溶液中混有NaSO ,碳酸钠溶液
2 3 2 4
与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,硫酸钠溶液和氯化钡溶液反应生成硫酸钡沉淀和氯化钠,碳
酸钡与稀盐酸反应生成氯化钡、水和二氧化碳,实验现象:白色沉淀部分溶解。
【小问2详解】
其他组同学认为实验步骤2不够严谨,不能证明混合溶液中一定存在硫酸钠,其理由是滴加少量稀盐酸,
生成碳酸钡可能没有反应完全,假设碳酸钠溶液中没有混有硫酸钠,碳酸钠溶液和氯化钡溶液反应生成碳
酸钡白色沉淀,碳酸钡与少量稀盐酸反应,碳酸钡有剩余,此时白色沉淀部分溶解。溶液中一定含有碳酸
钠、不一定含有硫酸钠,碳酸钠溶液与氯化钡溶液反应生成碳酸钡沉淀和氯化钠,该反应化学方程式:
。
六、计算题(本题共1个小题,共7分)
13. 我国力争在2060年前实现“碳中和”,实现二氧化碳的相对“零排放”。使用氢能源汽车可以有效减
少二氧化碳的排放。氢化钙(CaH)是一种重要的制氢剂,氢化钙可与物质M反应生成氢气,反应的化学
2
方程式为: ,请完成下列各题:
(1)CaH 中钙元素和氢元素的质量比为______(化为最简整数比)。
2
(2)M的化学式为______。
(3)若制取8kg氢气,计算理论上需要CaH 的质量(写出计算过程)。
2
【答案】(1)20:1
11【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
(2)HO (3)解:设需要CaH 的质量为x
2 2
答:理论上需要CaH 的质量是84kg。
2
【解析】
【小问1详解】
CaH 中钙元素和氢元素的质量比为40:(1×2)=20:1;
2
【小问2详解】
化学反应前后原子的种类和数目不变,反应前有1Ca、2H,反应后有1Ca、6H、2O,则2M中有4H、
2O,M为HO。
2
【小问3详解】
详见答案。
12