文档内容
班级 姓名 学号 分数
第 06 单元 化学反应与能量
(B 卷•提升能力)
(时间:90分钟,满分:100分)
一、选择题(本题共16小题,每小题3分,共48分)
1.下列说法正确的是( )
A.化学键的变化必然会引起能量变化,所以能量变化也一定会引起化学变化
B.所有化学变化的能量都可以通过原电池转化为电能
C.所有化学变化一定遵循质量守恒和能量守恒
D.化学变化一定会引起物质种类的变化,所以反应体系内物质种类变化一定是发生化学变化
【答案】C
【解析】能量变化不一定会引起化学变化,如物质的三态变化是物理变化,A错误;只有自发进行的氧化
还原反应才能设计成原电池,B错误;物质种类发生变化不一定是发生了化学变化,D错误。
2.一种环保型燃料——丙烷,其燃烧时发生反应的化学方程式为 C H +5O――→3CO +4HO。下列说
3 8 2 2 2
法中不正确的是( )
A.火炬燃烧时化学能只转化为热能
B.所有的化学反应都会伴随着能量变化,有能量变化的物质变化不一定是化学反应
C.1 mol C H 和5 mol O 所具有的总能量大于3 mol CO 和4 mol H O所具有的总能量
3 8 2 2 2
D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料
【答案】A
【解析】火炬燃烧时化学能转化为热能和光能等,A错;物质发生化学反应一定伴随着能量变化,伴随着
能量变化的物质变化却不一定是化学变化,如物质的“三态”变化、核变化也都伴随能量变化,B正确;
可燃物的燃烧属于放热反应,放热反应反应物总能量大于生成物总能量,C正确;丙烷燃烧产物为CO 和
2
HO,无污染,D正确。
2
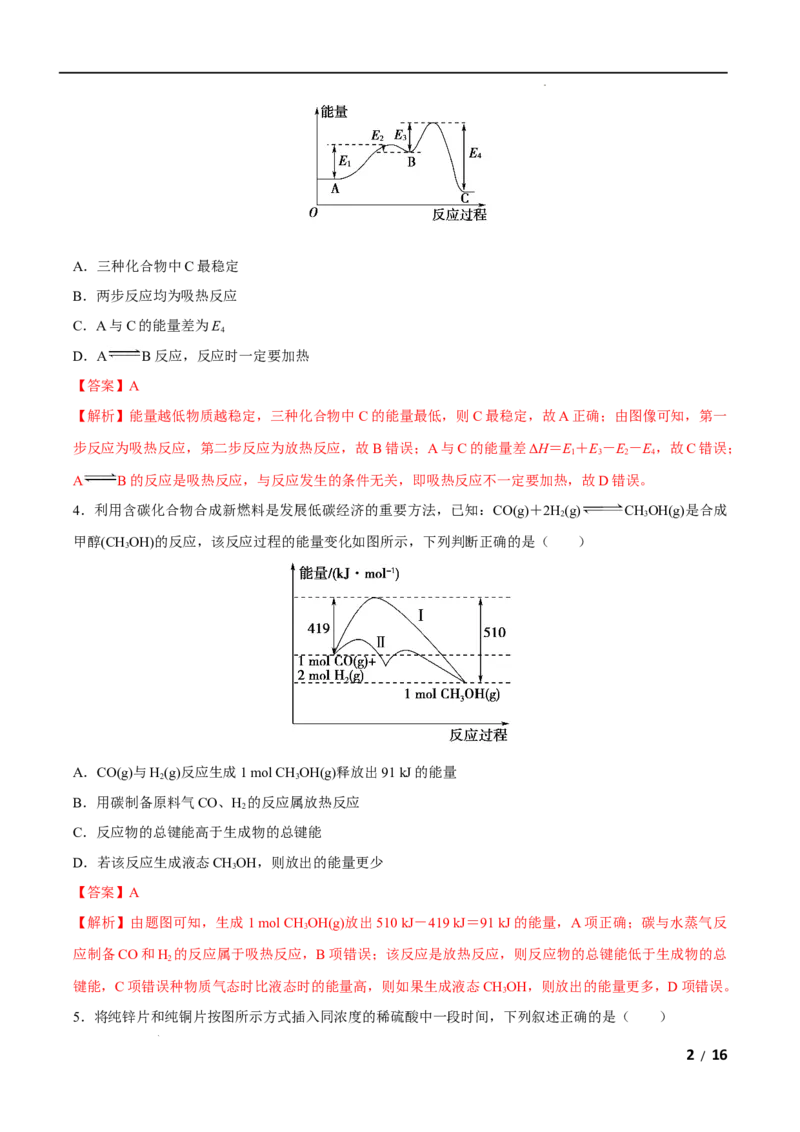
3.某反应由两步反应A B C构成,它的反应能量曲线如图,下列叙述正确的是( )
1 / 16
学科网(北京)股份有限公司A.三种化合物中C最稳定
B.两步反应均为吸热反应
C.A与C的能量差为E
4
D.A B反应,反应时一定要加热
【答案】A
【解析】能量越低物质越稳定,三种化合物中C的能量最低,则C最稳定,故A正确;由图像可知,第一
步反应为吸热反应,第二步反应为放热反应,故B错误;A与C的能量差ΔH=E+E-E-E,故C错误;
1 3 2 4
A B的反应是吸热反应,与反应发生的条件无关,即吸热反应不一定要加热,故D错误。
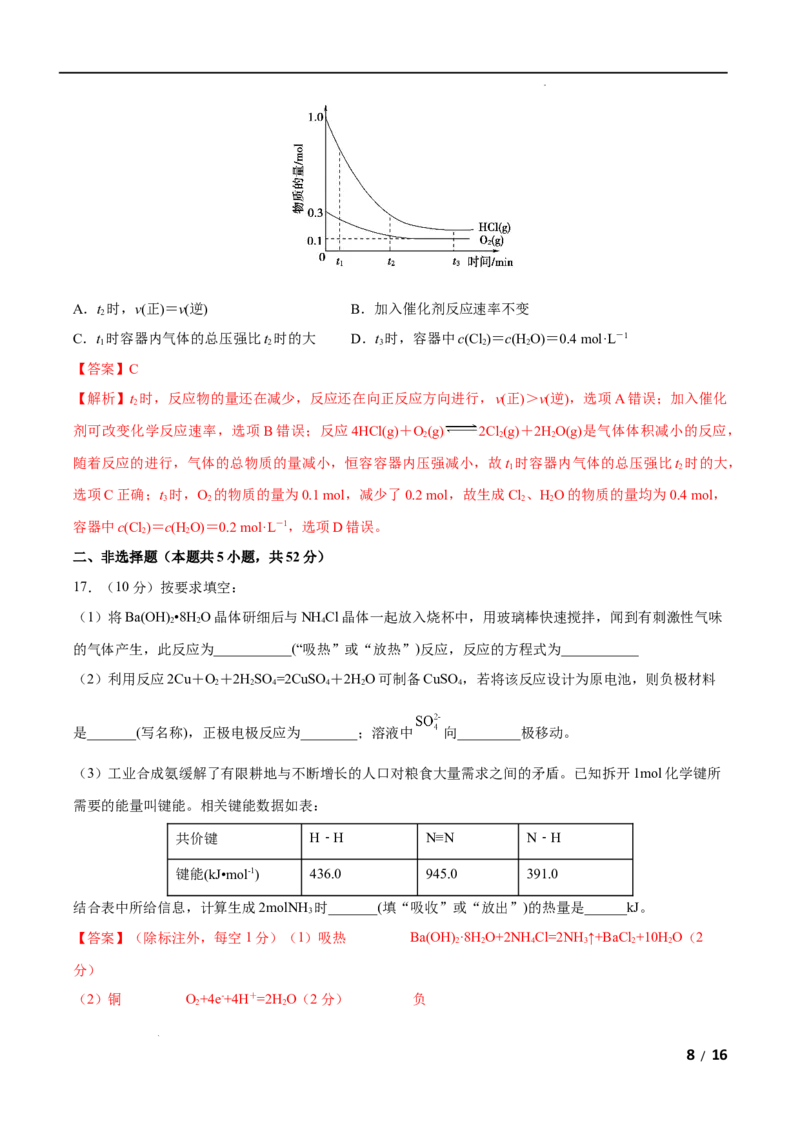
4.利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知:CO(g)+2H(g) CHOH(g)是合成
2 3
甲醇(CHOH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )
3
A.CO(g)与H(g)反应生成1 mol CH OH(g)释放出91 kJ的能量
2 3
B.用碳制备原料气CO、H 的反应属放热反应
2
C.反应物的总键能高于生成物的总键能
D.若该反应生成液态CHOH,则放出的能量更少
3
【答案】A
【解析】由题图可知,生成1 mol CH OH(g)放出510 kJ-419 kJ=91 kJ的能量,A项正确;碳与水蒸气反
3
应制备CO和H 的反应属于吸热反应,B项错误;该反应是放热反应,则反应物的总键能低于生成物的总
2
键能,C项错误种物质气态时比液态时的能量高,则如果生成液态CHOH,则放出的能量更多,D项错误。
3
5.将纯锌片和纯铜片按图所示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是( )
2 / 16
学科网(北京)股份有限公司A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速率甲比乙慢
【答案】C
【解析】由题图可知,甲中形成闭合回路,符合形成原电池的条件,铜的活泼性比锌的弱,故铜作正极,
发生的电极反应为2H++2e-===H ↑;乙不能形成闭合回路,不能形成原电池,只在锌片上发生反应:Zn
2
+2H+===Zn2++H↑,由于两者都消耗H+,故两烧杯中溶液的pH都增大。由于原电池的形成,故甲中产
2
生气泡的速率比乙快。
6.一种新型绿色燃料电池是把H 、CO、CH 的混合气体和空气不断输入,将化学能转化为电能,被称为
2 4
“21世纪的绿色发电站”。关于这种燃料电池的说法不正确的是( )
A.通入空气的一极为正极
B.H、CO、CH 的混合气体在电池内部燃烧,放出大量的热,然后电池将热能转化为电能
2 4
C.电池实际工作时的电解液应选择碱性溶液
D.电池的正极反应式为O+4e-+2H O 4OH-
2 2
【答案】B
【解析】正极上得电子发生还原反应,所以通入空气的电极为正极,A正确;燃料电池中不存在燃料的燃烧
反应,燃料在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,将化学能直接转化为电能,B
错误;该反应中有二氧化碳生成,用碱性物质作电解质溶液可以吸收二氧化碳,避免电池内部压强过大而产
生安全隐患,C正确;用碱液作电解液,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为 O+4e-
2
+2H O 4OH-,D正确。
2
7.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
3 / 16
学科网(北京)股份有限公司甲 乙
丙 丁
A.图甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增大
B.图乙:正极的电极反应式为Ag O+2e-+HO===2Ag+2OH-
2 2
C.图丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.图丁:电池放电过程中,硫酸浓度不断减小
【答案】A
【解析】图甲为Zn、Cu、HSO 溶液构成的原电池,锌为负极,铜为正极,锌失去电子生成锌离子,Zn2+
2 4
向Cu电极方向移动,在铜电极上氢离子得到电子生成氢气,故Cu电极附近溶液中H+浓度减小,A错误;
锌为负极,电解质溶液为碱性溶液,所以正极的电极反应式为Ag O+2e-+HO===2Ag+2OH-,B正确;
2 2
锌筒作负极,失去电子,发生氧化反应,电极反应式为Zn-2e-===Zn2+,锌溶解,锌筒会变薄,C正确;
电池放电过程中,电池总反应为Pb+PbO +2HSO ===2PbSO +2HO,消耗硫酸,硫酸浓度不断减小,D
2 2 4 4 2
正确。
8.一种直接铁燃料电池(电池反应:3Fe+2O===Fe O)的装置如图所示,下列说法正确的是( )
2 3 4
A.Fe极作正极
B.KOH溶液为电池的电解质溶液
4 / 16
学科网(北京)股份有限公司C.电子由多孔碳极沿导线流向Fe极
D.5.6 g Fe参与反应时,导线中流过1.204×1023个电子
【答案】B
【解析】铁燃料电池中铁失去电子,发生氧化反应,作负极,A错误;KOH溶液为电解质溶液,B正确;
电子由负极(Fe极)沿导线流向正极(多孔碳极),C错误;根据电池反应:3Fe+2O===Fe O 可知,3 mol铁
2 3 4
参与反应时转移8 mol e-,故5.6 g Fe参与反应时,导线中流过约1.605×1023个电子,D错误。
9.在恒温恒容的密闭容器中进行反应2SO +O 2SO ,若反应物浓度由0.1 mol·L-1降到0.06 mol·L-1
2 2 3
需20 s,那么由0.06 mol·L-1降到0.024 mol·L-1需要的反应时间为( )
A.等于18 s B.等于12 s C.大于18 s D.小于18 s
【答案】C
10.将4 mol A和2 mol B在2 L的密闭容器中混合,并在一定条件下发生如下反应:2A(s)+B(g)
2C(g),反应2 s 后测得C的浓度为0.6 mol·L-1。下列说法正确的是( )
A.用物质A表示2 s内的平均反应速率为0.3 mol·L-1·s-1
B.用物质B表示2 s内的平均反应速率为0.6 mol·L-1·s-1
C.2 s时v(C)=0.3 mol·L-1·s-1
D.2 s时物质B的浓度为0.7 mol·L-1
【答案】D
【解析】不能用固体物质表示化学反应速率,A错误;化学反应速率是平均值不是瞬时值,C错误;据题
目条件知v(C)=0.6 mol·L-1÷2 s=0.3 mol·L-1·s-1,则v(B)=0.3 mol·L-1·s-1÷2=0.15 mol·L-1·s-1,则2 s时
物质B的浓度为2 mol÷2 L-0.6 mol·L-1÷2=0.7 mol·L-1,B错误,D正确。
11.NO 和 CO 都是汽车尾气里的有害物质,它们能缓慢地反应生成氮气和二氧化碳气体:2NO+
2CO===N +2CO。对此反应,下列叙述正确的是( )
2 2
A.使用催化剂能加快反应速率
B.压强增大不影响化学反应速率
C.冬天气温低,反应速率降低,对人体危害减小
D.无论外界条件怎样改变,均对此化学反应的速率无影响
【答案】A
【解析】中学阶段,一般催化剂默认为正催化剂,使用(正)催化剂能加快反应速率,A正确;增大压强反
应速率增大,B错误;冬天气温低,反应速率降低,因为NO、CO都有毒,对人类危害增大,C错误;改
变温度、压强等外界条件,化学反应速率会改变,D错误。
5 / 16
学科网(北京)股份有限公司12.硫代硫酸钠溶液与稀硫酸反应的化学方程式为NaSO+H SO NaSO +SO↑+S↓+H O,下列各组实
2 2 3 2 4 2 4 2 2
验中最先出现浑浊的是( )
NaSO 溶液 稀硫酸 HO
2 2 3 2
实验
反应 V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
A 25 5 0.1 10 0.1 5
B 25 5 0.2 5 0.2 10
C 35 5 0.1 10 0.1 5
D 35 5 0.2 5 0.2 10
【答案】D
【解析】本题考查浓度和温度两个因素对化学反应速率的影响,只要抓住浓度越大,温度越高,反应速率
就越大,因此D项最先出现浑浊。
13.把镁条投入盛有盐酸的敞口容器中,产生氢气的速率变化曲线如图所示。下列因素中,影响该反应速
率的主要因素是( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①③ D.②③
【答案】C
【解析】镁与盐酸反应的离子方程式为Mg+2H+===Mg2++H↑,与H+有关,与Cl-无关。在镁与盐酸的
2
反应中,刚开始时H+的浓度最大,反应速率应最大,但由于此反应为放热反应,温度升高,化学反应速
率还会增大,随着化学反应的进行,H+浓度逐渐减小,化学反应速率又逐渐减慢。镁条的表面积在此反应
中不是主要因素。
14.一定条件下,对于反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c 、c 、c(均不为零)。
1 2 3
达平衡时,X、Y、Z 浓度分别为 0.1 mol·L-1、0.3 mol·L-1和 0.08 mol·L-1,则下列判断不合理的是
( )
①c∶c =1∶3 ②平衡时,Y和Z的生成速率之比为2∶3 ③平衡时X和Y的转化率不相等 ④c 的取
1 2 1
值范围为00,反应又是可逆的,④正确。
1 1
15.某温度时,在容积为3 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
由图中数据分析,下列结论错误的是( )
A.该反应的化学方程式为2Z+Y 3X
B.反应开始至2 min末,X的化学反应速率为0.2 mol·L-1·s-1
C.该反应是由正、逆反应同时开始的,最终建立平衡
D.若增加或减少X的物质的量,化学反应速率一定会发生明显的变化
【答案】B
【解析】从题图中横、纵坐标及曲线的变化趋势可找到X、Y、Z转化的物质的量之比,即可写出该反应
的化学方程式:2Z+Y 3X,故A项正确;根据化学反应速率的计算公式,可求出X的化学反应速率:v(X)=
≈0.0011mol·L-1·s-1,故B项错误;根据题图中曲线均不通过原点,可判断该可逆反应是由
正、逆反应同时开始的,故C项正确。因容器容积一定,改变X的物质的量,必然会导致其浓度的改变,
因此化学反应速率也会随之改变,故D项正确。
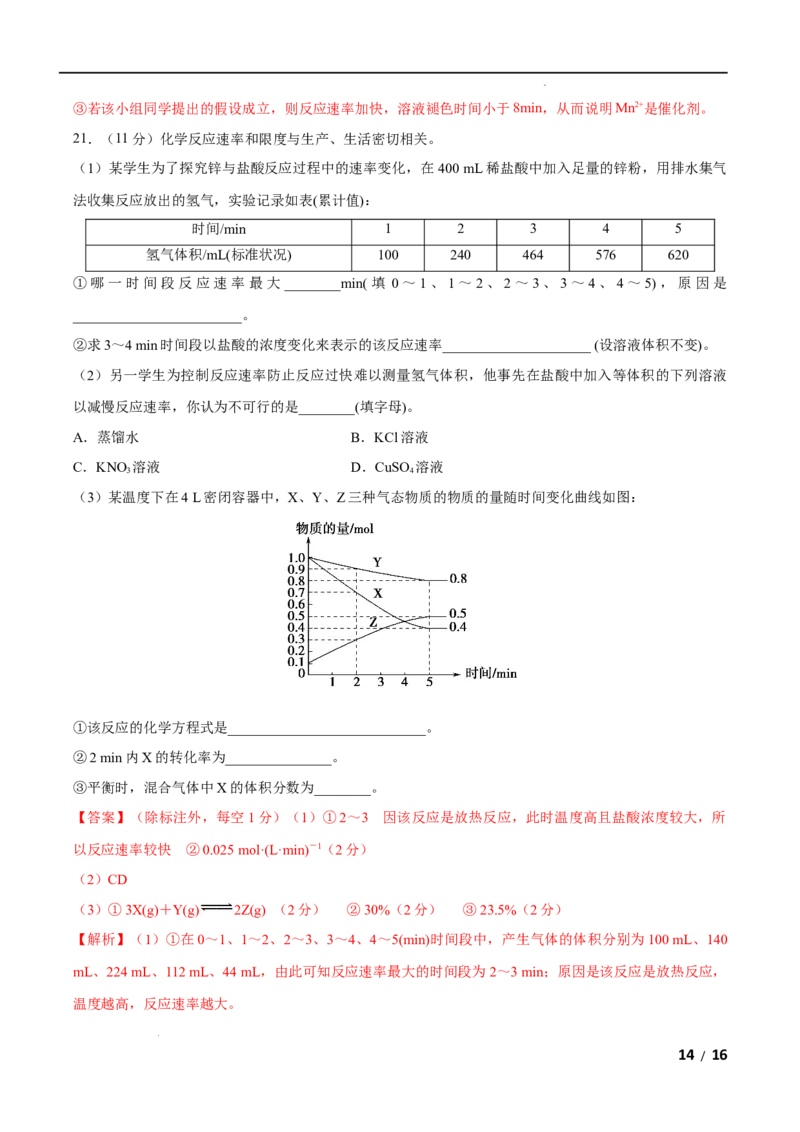
16.在2.0 L恒温恒容密闭容器中充入 1.0 mol HCl和0.3 mol O ,加入催化剂发生反应 4HCl(g)+O(g)
2 2
2Cl(g)+2HO(g),HCl、O 的物质的量随时间的变化曲线如图所示。下列说法正确的是( )
2 2 2
7 / 16
学科网(北京)股份有限公司A.t 时,v(正)=v(逆) B.加入催化剂反应速率不变
2
C.t 时容器内气体的总压强比t 时的大 D.t 时,容器中c(Cl )=c(H O)=0.4 mol·L-1
1 2 3 2 2
【答案】C
【解析】t 时,反应物的量还在减少,反应还在向正反应方向进行,v(正)>v(逆),选项A错误;加入催化
2
剂可改变化学反应速率,选项B错误;反应4HCl(g)+O(g) 2Cl(g)+2HO(g)是气体体积减小的反应,
2 2 2
随着反应的进行,气体的总物质的量减小,恒容容器内压强减小,故t 时容器内气体的总压强比t 时的大,
1 2
选项C正确;t 时,O 的物质的量为0.1 mol,减少了0.2 mol,故生成Cl 、HO的物质的量均为0.4 mol,
3 2 2 2
容器中c(Cl )=c(H O)=0.2 mol·L-1,选项D错误。
2 2
二、非选择题(本题共5小题,共52分)
17.(10分)按要求填空:
(1)将Ba(OH) •8H O晶体研细后与NH Cl晶体一起放入烧杯中,用玻璃棒快速搅拌,闻到有刺激性气味
2 2 4
的气体产生,此反应为___________(“吸热”或“放热”)反应,反应的方程式为___________
(2)利用反应2Cu+O+2HSO =2CuSO+2HO可制备CuSO ,若将该反应设计为原电池,则负极材料
2 2 4 4 2 4
是_______(写名称),正极电极反应为________;溶液中 向_________极移动。
(3)工业合成氨缓解了有限耕地与不断增长的人口对粮食大量需求之间的矛盾。已知拆开1mol化学键所
需要的能量叫键能。相关键能数据如表:
共价键 H﹣H N≡N N﹣H
键能(kJ•mol-1) 436.0 945.0 391.0
结合表中所给信息,计算生成2molNH 时_______(填“吸收”或“放出”)的热量是______kJ。
3
【答案】(除标注外,每空1分)(1)吸热 Ba(OH) ·8H O+2NH Cl=2NH ↑+BaCl +10H O(2
2 2 4 3 2 2
分)
(2)铜 O+4e-+4H+=2H O(2分) 负
2 2
8 / 16
学科网(北京)股份有限公司(3)放出 93.0(2分)
【解析】(1)闻到刺激性气味的气体,烧杯壁温度下降,可知发生反应生成氨气且吸热,即
Ba(OH) ·8H O晶体与NH Cl晶体的反应是吸热反应,Ba(OH) ·8H O与NH Cl反应生成氨气、水、氯化钡,
2 2 4 2 2 4
其化学方程式为Ba(OH) ·8H O+2NH Cl=2NH ↑+BaCl +10H O。
2 2 4 3 2 2
(2)由2Cu+O+2HSO =2CuSO+2HO可知,该反应中Cu元素化合价由0价变为+2价、O元素化合价
2 2 4 4 2
由0价变为-2价,要将该反应设计成原电池,铜作负极,电极反应为Cu-2e-=Cu2+,正极上氧气得电子发生
还原反应,又因为在酸性条件下,所以氧气得电子和氢离子反应生成水,电极反应式为4H++O +4e-
2
═2H O,原电池工作是时,阴离子向负极(铜)移动,即 向负极移动。
2
(3)合成氨的反应为N(g)+3H(g) 2NH (g),焓变△H=反应物键能和-生成物键能和=(945.0kJ/
2 2 3
mol+3×436.0kJ/mol)-6×391.0kJ/mol=-93.0kJ/mol,热化学方程式为N(g)+3H(g) 2NH (g) H=-93.0kJ/
2 2 3
△
mol,即生成2molNH 时放出93.0kJ热量。
3
18.(10分)化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,
下同)。
A.KOH+HCl=KCl+HO B.Cu+Fe3+=Fe2++Cu2+
2
C.NaO+HO=2NaOH D.Fe+HSO =FeSO +H↑
2 2 2 4 4 2
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现
象,下列说法正确的是_______。
A.图Ⅰ中温度计的示数高于图Ⅱ的示数
B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温
C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面
D.图Ⅱ中产生气体的速率比Ⅰ慢
9 / 16
学科网(北京)股份有限公司(3)请利用反应“Cu+2Ag+= 2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),该电池的负极材料是
_______,发生的电极反应是____________________________,电解质溶液是______________。
(4)正极上出现的现象是__________________________________________。
(5)若导线上转移电子1 mol,则生成银_______g,理论上电解质溶液质量变化_______g。
【答案】(除标注外,每空1分)(1)D
(2)A
(3)Cu Cu - 2e- = Cu2+(2分) AgNO
3
(4)有银白色固体析出
(5)108 76(2分)
【解析】(1)原电池是将化学能转变为电能的装置,只有自发的氧化还原反应才有电子的转移,而B、D
为氧化还原反应,但反应B离子方程式未配平,AC为非氧化还原反应,不可以设计成原电池,故答案为:
D;
(2)图Ⅰ锌和稀硫酸反应生成硫酸锌和氢气,离子方程式为Zn+2H+═Zn2++H ↑;稀硫酸和锌的反应是放
2
热反应导致溶液温度逐渐升高,化学能转化为热能;图Ⅱ该装置构成原电池,Zn易失电子作负极,Cu作
正极,正极上氢离子得电子生成氢气;温度计指示的温度变化不明显,是因为化学能没有全部转化为热能,
大多数转化为电能,所以图Ⅰ中气泡产生在锌棒表面,Ⅱ中产生在铜棒表面;构成原电池加快化学反应速
率,则图Ⅱ中产生气体的速度比Ⅰ快;图Ⅰ中温度计的示数高于图Ⅱ的示数,故答案为:A;
(3)原电池中失电子的物质作负极,负极发生氧化反应,根据反应方程式知,Cu作负极,电极反应式为:
Cu-2e-=Cu2+,电解质溶液中含有得电子的Ag+,可用AgNO 溶液作电解质溶液;
3
(4)正极发生Ag++e-=Ag,正极上出现的现象是碳棒上出现银白色物质;
(5)根据知Ag++e-=Ag,转移1mol电子生成1molAg,m(Ag)=1mol×108g/mol=108g,由Cu-2e-=Cu2+,溶
液中增加Cu的质量为1/2mol×64g/mol=32g,则溶液减少的质量为108-32=76g。
19.(13分)电池是人类生产和生活中重要的能量来源,电池的发明是化学对人类的一项重大贡献。
(1)依据NaOH与HCl的反应原理设计原电池,你认为是否可行?__________(填“是”或“否”),理由
是____________________________________________________。
(2)一种以肼(N H)为液体燃料的电池装置如图所示。该电池用空气中的氧气作氧化剂,KOH作电解质。
2 4
负极反应式为_____________________________,正极反应式为_________________________________。
10 / 16
学科网(北京)股份有限公司(3)Li—SOCl 电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl —SOCl 。电
2 4 2
池的总反应可表示为:4Li+2SOCl =4LiCl+S+SO ↑。请回答下列问题:
2 2
①电池的负极材料为__________。
②电池正极发生的电极反应为_______________________________。
③SOCl 易挥发,实验室中常用NaOH溶液吸收SOCl ,有NaSO 和NaCl生成。如果把少量水滴到SOCl
2 2 2 3 2
中,实验现象是________________________,反应的化学方程式为_______________________________。
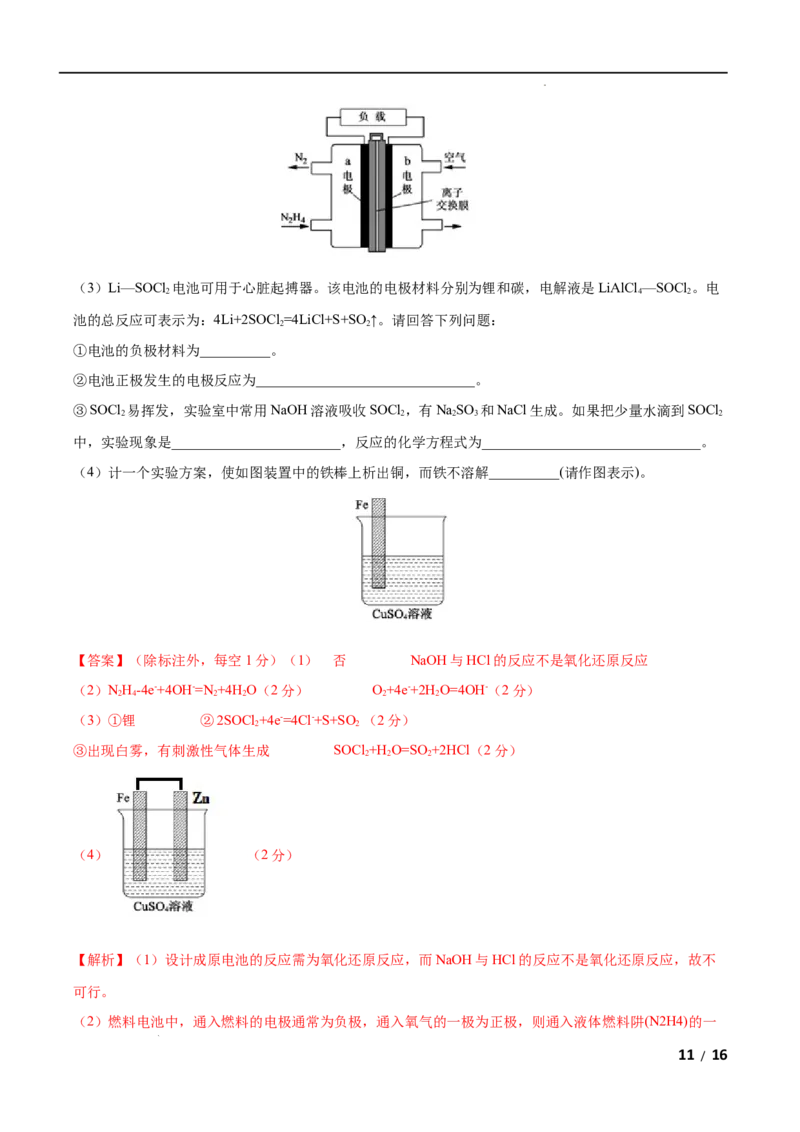
(4)计一个实验方案,使如图装置中的铁棒上析出铜,而铁不溶解__________(请作图表示)。
【答案】(除标注外,每空1分)(1) 否 NaOH与HCl的反应不是氧化还原反应
(2)NH-4e-+4OH-=N +4H O(2分) O+4e-+2H O=4OH-(2分)
2 4 2 2 2 2
(3)①锂 ②2SOCl +4e-=4Cl-+S+SO (2分)
2 2
③出现白雾,有刺激性气体生成 SOCl +H O=SO +2HCl(2分)
2 2 2
(4) (2分)
【解析】(1)设计成原电池的反应需为氧化还原反应,而NaOH与HCl的反应不是氧化还原反应,故不
可行。
(2)燃料电池中,通入燃料的电极通常为负极,通入氧气的一极为正极,则通入液体燃料阱(N2H4)的一
11 / 16
学科网(北京)股份有限公司极为负极,负极发生氧化反应,由图可知负极上有N2生成,电极反应式为:NH-4e-+4OH-=N +4H O;通
2 4 2 2
入氧气的一极为正极,正极发生还原反应,电极反应式为:O+4e-+2H O=4OH-。
2 2
(3)①从电池反应4Li+2SOCl =4LiCl+S+SO,可以看出,Li由0价升高到+1价,所以电池的负极材料为
2
Li,失去电子生成Li产物。
②SOCl 中的S元素显+4价,产物中S为0价,所以一部分SOCl 中的S元素得电子生成S,一部分SOCl
2 2 2
生成SO ,同时氯元素转化为Cl-,电池正极发生的电极反应为2SOCl +4e-=4Cl-+S+SO 。
2 2 2
③用NaOH溶液吸收SOCl ,生成NaSO 和NaCl,若将NaOH换成HO,产物为HSO 和HCl,则如果把
2 2 3 2 2 3
少量水滴到SOCl 中,则生成SO 和HCl,HCl遇水蒸气产生白雾,实验现象是出现白雾,有刺激性气体
2 2
生成,反应的化学方程式为SOCl +H O=SO +2HCl。
2 2 2
(4)铁棒上析出铜即电解质溶液为硫酸铜溶液,铜离子在正极得电子生成铜单质,而铁不溶解即铁为正
极,负极为比铁活泼且可做电极的金属单质如锌单质,原电池的总反应为Zn+Cu2+=Zn2++Cu,则该原电池
中,Zn为负极,负极反应Zn-2e-=Zn2+,铁为正极,正极发生还原反应,电极反应式为Cu2++2e-=Cu。
20.(8分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO +5H C O+3H SO ==2MnSO +10CO ↑+8H O+KSO
4 2 2 4 2 4 4 2 2 2 4
(实验内容及记录)
室温下,试管中所加试剂及其用量/mL
实验 室温下溶液褪色至
编号 0.6 mol/L HO 0.1 mol/L 3 mol/L 无色所需时间/min
2
HC O 溶液 KMnO 溶液 HSO 溶液
2 2 4 4 2 4
1 3.0 13.0 2.0 2.0 8.0
2 2.0 14.0 2.0 2.0 10.4
3 1.0 V V 2.0 12.8
1 2
请回答:
(1)请完成上述实验设计表:V=_________,V=__________。
1 2
(2)根据上表中的实验数据,可以得到的结论是_________________________________。
(3)利用实验1中数据计算,反应速率为v(KMnO)=_________________________。
4
(4)该小组同学依据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实
验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了
新的假设,并继续进行实验探究。
12 / 16
学科网(北京)股份有限公司①该小组同学提出的假设是____________________________________________________。
②请你帮助该小组同学完成实验方案,并填写表中空白。
室温下,试管中所加试剂及其用量
室温下溶液褪色
实验
至无色所需时
编号 0.6 mol/L 0.1 mol/L 3 mol/L
HO 间/min
HC O 溶液 2 KMnO 溶液 HSO 溶液
2 2 4 4 2 4 少量
__________
4 3.0mL 13.0mL 2.0mL 2.0mL t
③若该小组同学提出的假设成立,应观察到的现象是_______________________________。
【答案】(除标注外,每空1分)(1)15.0 2.0
(2)草酸浓度越来越小,褪色时间越来越长,说明反应速率越来越慢
(3) (2分)
(4)①生成物中的MnSO 或Mn2+为该反应的催化剂 ②MnSO ③与实验1相比,溶液褪色所需时
4 4
间短(或所用时间小于8min)
【解析】探究草酸浓度不同对反应速率的影响,变量为草酸浓度,其他都是固定的,溶液的总体积相等,
根据褪色时间长短来分析实验结论,根据速率公式计算速率,根据实际情况来分析可能是锰离子对反应速
率其催化作用。
(1)通过图中信息得到实验探究草酸浓度对反应速率的影响,因此整个溶液的体积相同,只能改变草酸
的浓度,其他的浓度不能改变,因此上述实验设计表:V=15.0,V=2.0。
1 2
(2)根据上表中的实验数据,可以得到的结论是草酸浓度越来越小,褪色时间越来越长,说明反应速率
越来越慢;故答案为:草酸浓度越来越小,褪色时间越来越长,说明反应速率越来越慢。
(3)利用实验1中数据计算,反应速率为υ(KMnO)=
4
。
(4)①由图乙可知反应开始后速率增大得比较快,说明生成物中的MnSO 或Mn2+为该反应的催化剂。
4
②与实验1相比,则加入的硫酸锰的量不同,其他条件必须相同,所以加入的少量固体硫酸锰。
13 / 16
学科网(北京)股份有限公司③若该小组同学提出的假设成立,则反应速率加快,溶液褪色时间小于8min,从而说明Mn2+是催化剂。
21.(11分)化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在 400 mL稀盐酸中加入足量的锌粉,用排水集气
法收集反应放出的氢气,实验记录如表(累计值):
时间/min 1 2 3 4 5
氢气体积/mL(标准状况) 100 240 464 576 620
①哪一时间段反应速率最大________min(填 0~1、1~2、2~3、3~4、4~5),原因是
________________________。
②求3~4 min时间段以盐酸的浓度变化来表示的该反应速率_____________________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液
以减慢反应速率,你认为不可行的是________(填字母)。
A.蒸馏水 B.KCl溶液
C.KNO 溶液 D.CuSO 溶液
3 4
(3)某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图:
①该反应的化学方程式是____________________________。
②2 min内X的转化率为_______________。
③平衡时,混合气体中X的体积分数为________。
【答案】(除标注外,每空1分)(1)①2~3 因该反应是放热反应,此时温度高且盐酸浓度较大,所
以反应速率较快 ②0.025 mol·(L·min)-1(2分)
(2)CD
(3)①3X(g)+Y(g) 2Z(g) (2分) ②30%(2分) ③23.5%(2分)
【解析】(1)①在0~1、1~2、2~3、3~4、4~5(min)时间段中,产生气体的体积分别为100 mL、140
mL、224 mL、112 mL、44 mL,由此可知反应速率最大的时间段为2~3 min;原因是该反应是放热反应,
温度越高,反应速率越大。
14 / 16
学科网(北京)股份有限公司②在3~4 min时间段内,n(H )=0.112 L÷22.4 L·mol-1=0.005 mol,根据2HCl~H ,计算消耗盐酸的物质
2 2
的量为0.01 mol,则v(HCl)=0.01 mol÷0.4 L÷1 min=0.025 mol·(L·min)-1。
(2)A可行:加入蒸馏水,H+浓度减小,反应速率减小且不减少产生氢气的量;B可行:加入KCl溶液,
H+浓度减小,反应速率减小且不减少产生氢气的量;C不可行:因酸性溶液中有NO,具有强氧化性,与
Zn反应无氢气生成;D不可行:加入CuSO 溶液,Zn置换出Cu,构成原电池,反应速度增大,且影响生
4
成氢气的量。
(3)①由图像可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,
当反应进行到5 min时,Δn(Y)=0.2 mol、Δn(Z)=0.4 mol、Δn(X)=0.6 mol,则Δn(Y)∶Δn(Z)∶Δn(X)=
1∶2∶3,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为 3X(g)+Y(g)
2Z(g)。
②2 min内X的转化率=×100%=×100%=30%。
③X的体积分数=X的物质的量分数=×100%≈23.5%。
15 / 16
学科网(北京)股份有限公司16 / 16
学科网(北京)股份有限公司