文档内容
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 S-32 C1-35.5 Cu-64 Ag- 108
五、选择题(本题包括12小题,每小题2分,共24分。每小题只有一个选项符合题意)
24.每年的5月31日是“世界无烟日”。下列说法不正确的是
A.吸烟损害大脑,使人记忆力减退
B.长期吸烟易患肺气肿、肺癌等疾病
C.吸烟有害健康,但“二手烟”对人体无害
D.香烟烟气中的CO、尼古丁等对人体危害很大
25.下列过程中包含化学变化的是
A.酒精挥发 B.冰雪融化 C.干冰升华 D.金属氧化
26.下列图示实验操作中,正确的是
27.下列化学用语表示正确的是
A.3个铁离子:3Fe2+ B.1个臭氧分子:O
3
C.锰酸钾的化学式:KMnO D.氟离子的结构示意图:
4
28.下列几种物质中,其重要成分不属于人体所需基本营养素的是
A.白糖 B.白面 C.白酒 D.白开水
29.下列有关物质的性质与用途具有对应关系的是
A.铬耐磨、耐腐蚀,可镀在钢铁制品表面防生锈
B.石墨很软,有光泽和滑腻感,可用于制作电极
C.乙醇易挥发、易溶于水,可掺入汽油中作燃料
D.聚四氟乙烯塑料密度小,可用作不粘锅的内衬
30.已知:金属X在常温下能与空气中的氧气反应,而金属Y和Z不能;将Y 、Z分别投入稀
盐酸中,Y溶解并产生气泡,Z无变化。下列说法正确的是A.X氧化物的化学式只能表示为XO B.Y能将X从它的盐溶液中置换出来
C.Z在自然界中只能以单质形式存在 D.三种金属的活动性顺序:X>Y>Z
31.下列排序正确的是
A.空气中物质的含量:
B.溶液的pH:
C.氮元素的化合价:
D.硫元素的质量分数:
32.物质a和b在一定条件下反应生成e和d的微观示意图如下:
下列说法正确的是
A.物质c是一氧化碳 B.该反应不符合质量守恒定律
C.该反应前后,原子的种类发生改变 D.该反应前后,分子的个数保持不变
33.下列各组实验方案中,不能达到实验目的的是
选项 实验目的 实验方案
A 稀释浓硫酸 将浓硫酸缓慢注入水中,并不断搅拌
B 除去CO 气体中的HCl 将气体通过盛有足量NaOH溶液的洗气瓶
2
C 鉴别化肥KNO 和NH4NO 取样,加Ca(OH) 固体混合研磨,闻气味
3 3 2
D 除去FeCl 溶液中的CuCl 加入过量的Fe粉,充分反应后过滤
2 2
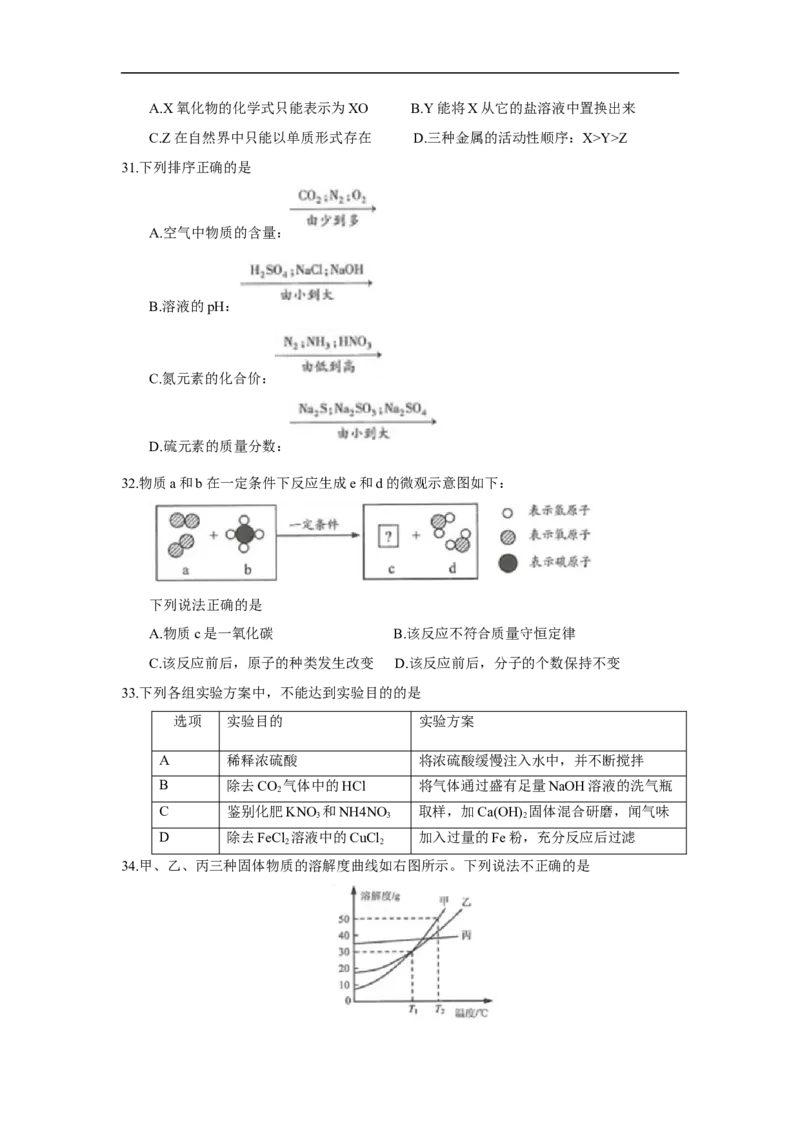
34.甲、乙、丙三种固体物质的溶解度曲线如右图所示。下列说法不正确的是A. T℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙
2
B. T℃时,将甲、乙的饱和溶液均降温到T℃,得到的溶液仍饱和
2 1
C.若甲中混有少量的丙,可采用降温结晶的方法提纯甲
D. T℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液
2
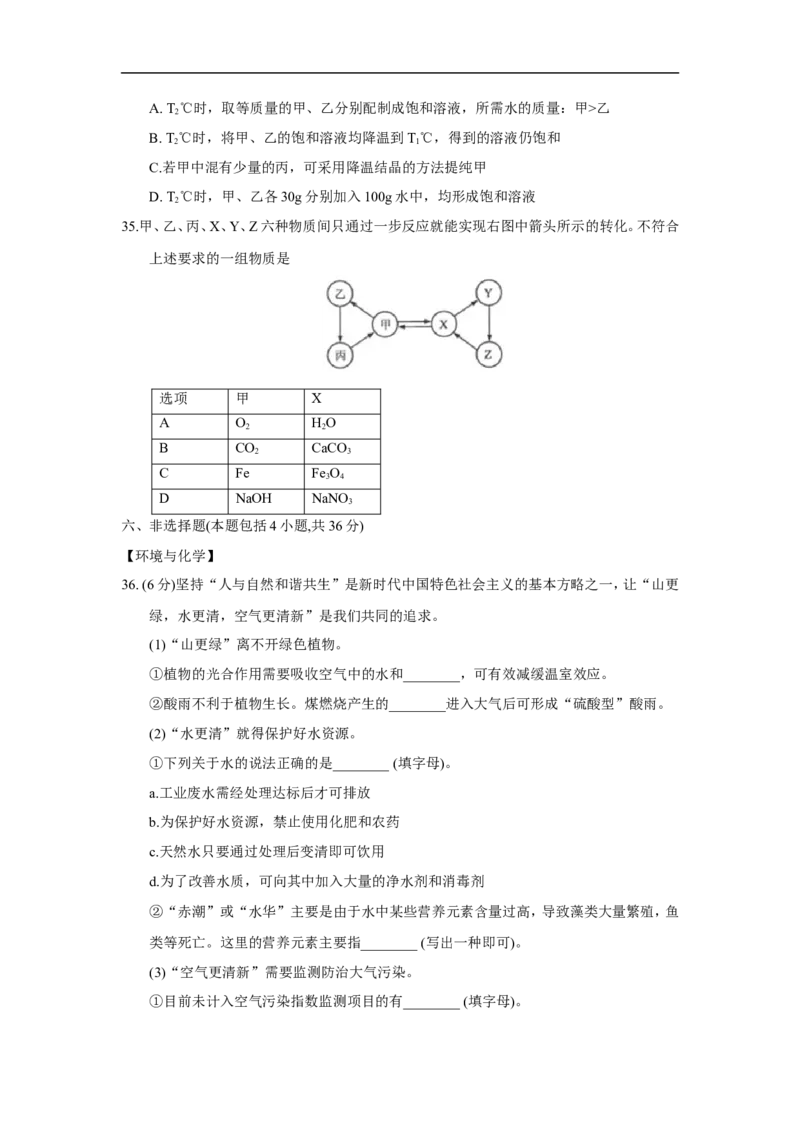
35.甲、乙、丙、X、Y、Z六种物质间只通过一步反应就能实现右图中箭头所示的转化。不符合
上述要求的一组物质是
选项 甲 X
A O HO
2 2
B CO CaCO
2 3
C Fe Fe O
3 4
D NaOH NaNO
3
六、非选择题(本题包括4小题,共36分)
【环境与化学】
36. (6分)坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更
绿,水更清,空气更清新”是我们共同的追求。
(1)“山更绿”离不开绿色植物。
①植物的光合作用需要吸收空气中的水和________,可有效减缓温室效应。
②酸雨不利于植物生长。煤燃烧产生的________进入大气后可形成“硫酸型”酸雨。
(2)“水更清”就得保护好水资源。
①下列关于水的说法正确的是________ (填字母)。
a.工业废水需经处理达标后才可排放
b.为保护好水资源,禁止使用化肥和农药
c.天然水只要通过处理后变清即可饮用
d.为了改善水质,可向其中加入大量的净水剂和消毒剂
②“赤潮”或“水华”主要是由于水中某些营养元素含量过高,导致藻类大量繁殖,鱼
类等死亡。这里的营养元素主要指________ (写出一种即可)。
(3)“空气更清新”需要监测防治大气污染。
①目前未计入空气污染指数监测项目的有________ (填字母)。a.一氧化碳 b.二氧化氮 c.可吸人颗粒物 d.稀有气体
②硝酸工厂排放的尾气中常含有NO、NO 等有害气体,可用氢氧化钠溶液来吸收:
2
NO+NO +2NaOH=2X+HO。 X的化学式为________。
2 2
【厨房中的化学】
37. (8分)
(1)炒菜时油锅着火可用锅盖盖灭,其灭火原理是________。
(2)家用液化气的主要成分之一是丙烷(C H),丙烷属于________ (填字母)。
3 8
a.氧化物 b.化合物 c.无机物 d.有机物
(3)热水壶中水垢的主要成分是CaCO 和________ (填化学式), 可用食醋洗涤。食醋的
3
重要成分是醋酸(设其化学式为HA),写出其与CaCO 反应的化学方程式:________。
3
(4)利用厨房中的物品鉴別食盐和苏打:取一固体于碗中,加入________(填物质名称),
若有________,则该固体为苏打;若无此现象,则为食盐。
【生产中的化学】
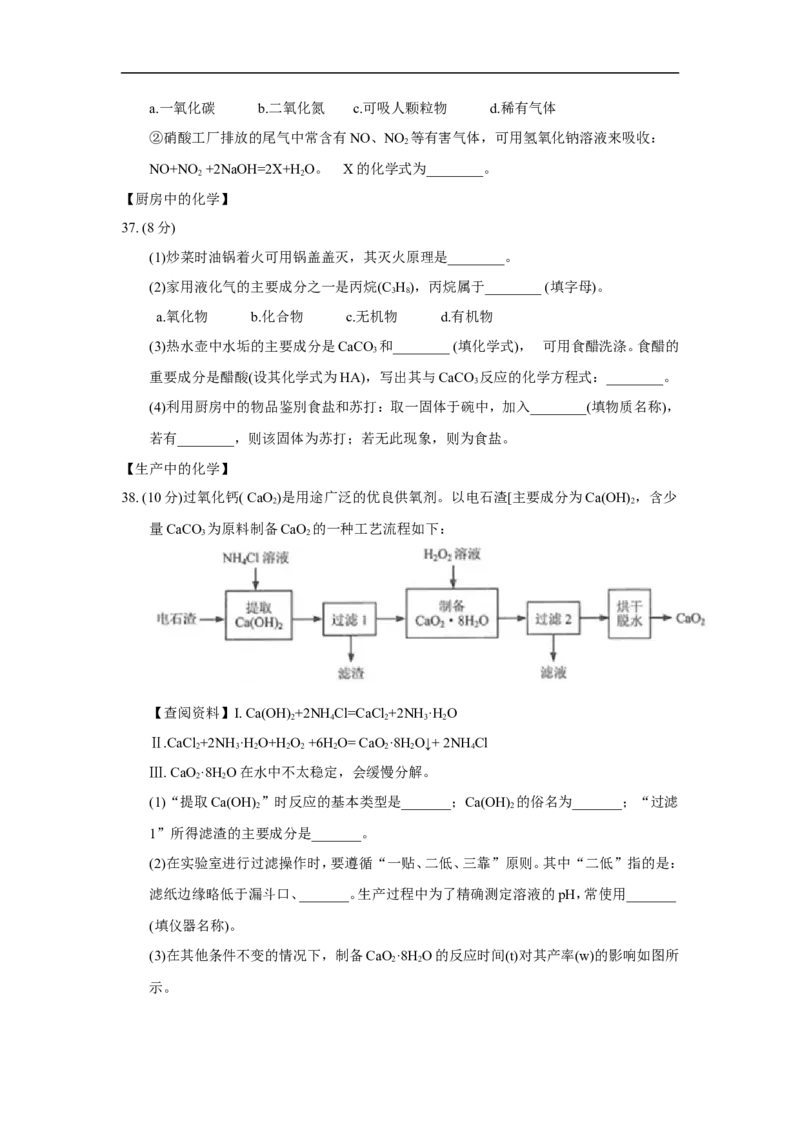
38. (10分)过氧化钙( CaO)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH) ,含少
2 2
量CaCO 为原料制备CaO 的一种工艺流程如下:
3 2
【查阅资料】I. Ca(OH) +2NHCl=CaCl +2NH·HO
2 4 2 3 2
Ⅱ.CaCl +2NH·HO+HO +6H O= CaO·8HO↓+ 2NH Cl
2 3 2 2 2 2 2 2 4
Ⅲ. CaO·8HO在水中不太稳定,会缓慢分解。
2 2
(1)“提取Ca(OH) ”时反应的基本类型是_______;Ca(OH) 的俗名为_______;“过滤
2 2
1”所得滤渣的主要成分是_______。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:
滤纸边缘略低于漏斗口、_______。生产过程中为了精确测定溶液的pH,常使用_______
(填仪器名称)。
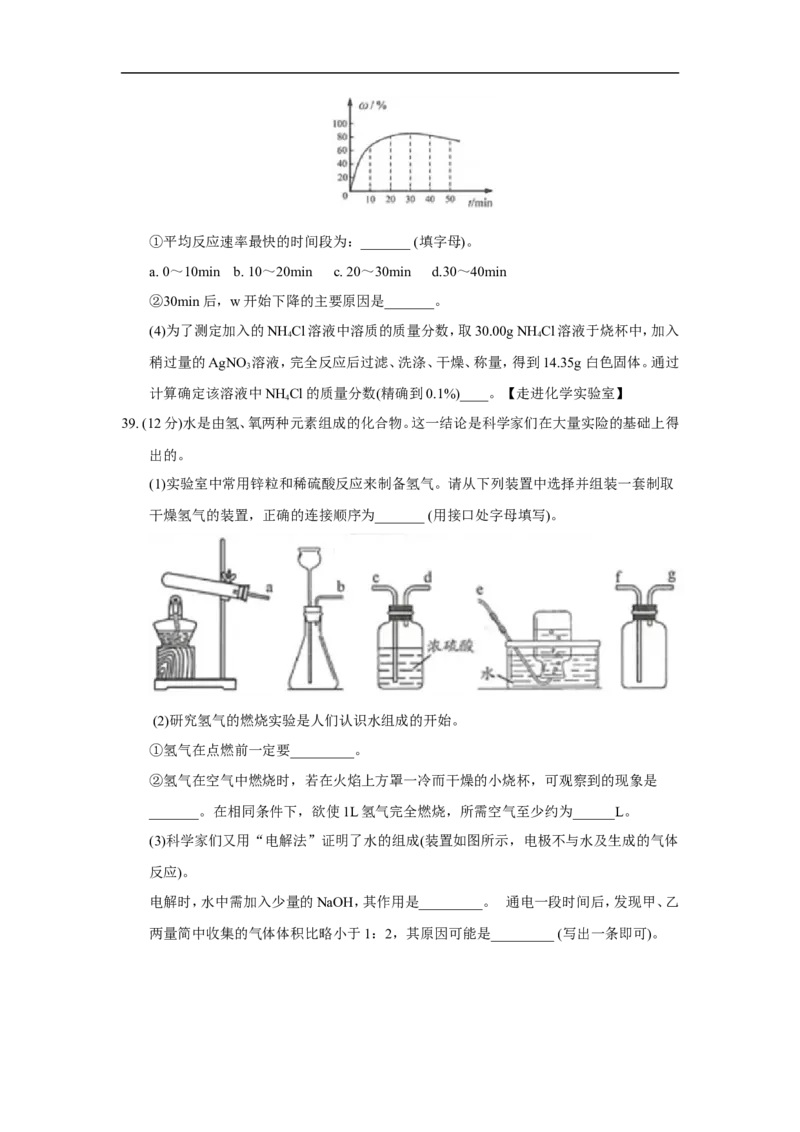
(3)在其他条件不变的情况下,制备CaO·8HO的反应时间(t)对其产率(w)的影响如图所
2 2
示。①平均反应速率最快的时间段为:_______ (填字母)。
a. 0~10min b. 10~20min c. 20~30min d.30~40min
②30min后,w开始下降的主要原因是_______。
(4)为了测定加入的NH Cl溶液中溶质的质量分数,取30.00g NH Cl溶液于烧杯中,加入
4 4
稍过量的AgNO 溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过
3
计算确定该溶液中NH Cl的质量分数(精确到0.1%)____。【走进化学实验室】
4
39. (12分)水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得
出的。
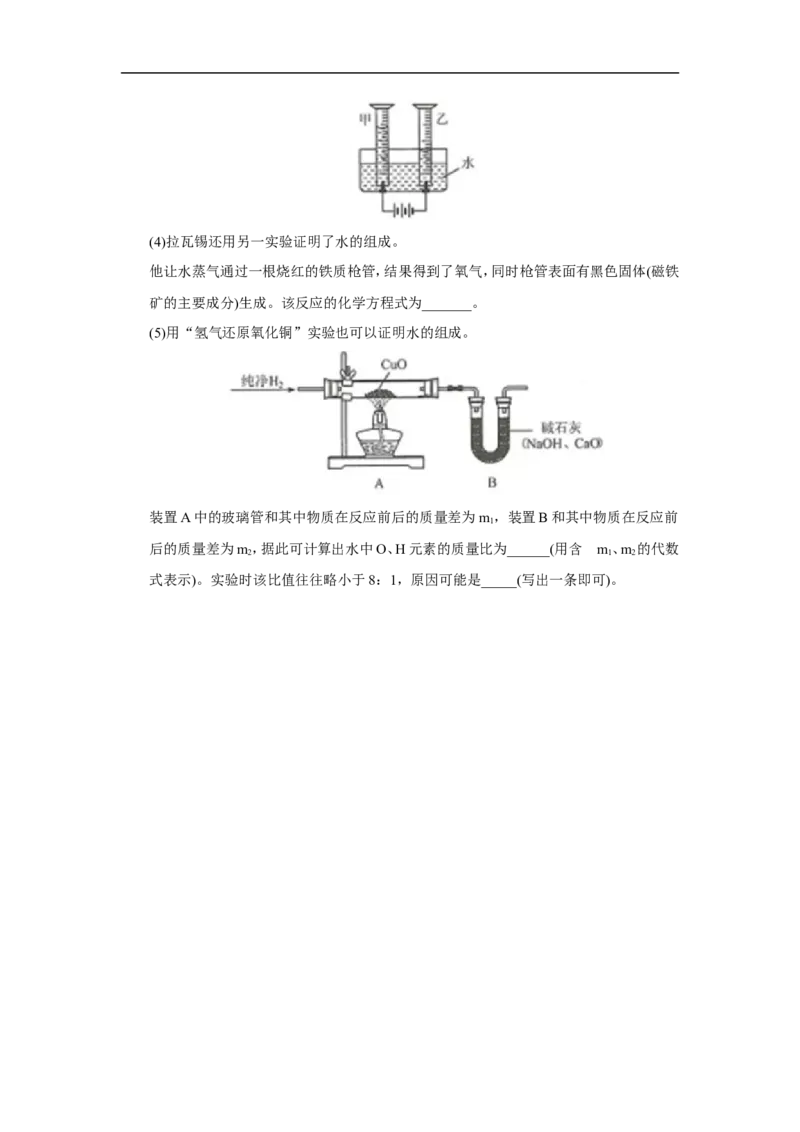
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取
干燥氢气的装置,正确的连接顺序为_______ (用接口处字母填写)。
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要_________。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是
_______。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为______L。
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体
反应)。
电解时,水中需加入少量的NaOH,其作用是_________。 通电一段时间后,发现甲、乙
两量简中收集的气体体积比略小于1:2,其原因可能是_________ (写出一条即可)。(4)拉瓦锡还用另一实验证明了水的组成。
他让水蒸气通过一根烧红的铁质枪管,结果得到了氧气,同时枪管表面有黑色固体(磁铁
矿的主要成分)生成。该反应的化学方程式为_______。
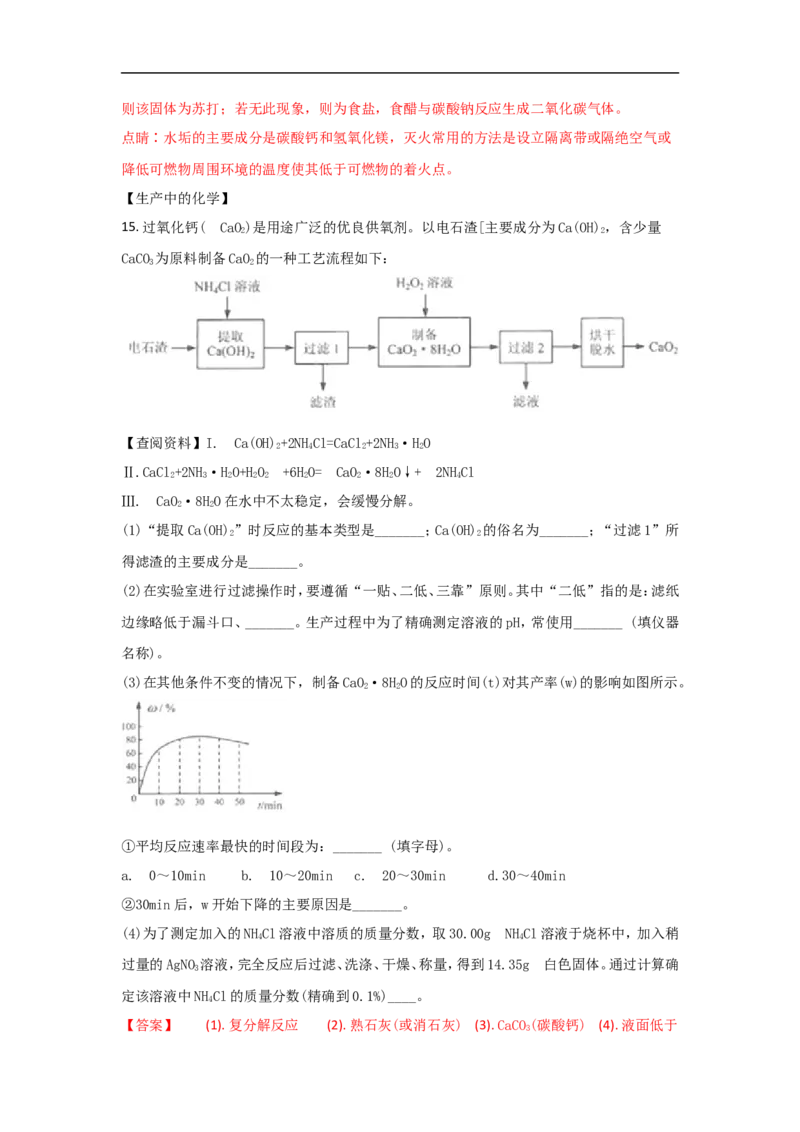
(5)用“氢气还原氧化铜”实验也可以证明水的组成。
装置A中的玻璃管和其中物质在反应前后的质量差为m,装置B和其中物质在反应前
1
后的质量差为m,据此可计算出水中O、H元素的质量比为______(用含 m、m 的代数
2 1 2
式表示)。实验时该比值往往略小于8:1,原因可能是_____(写出一条即可)。五、选择题(本题包括12小题,每小题2分,共24分。每小题只有一个选项符合题意)
24-28:CDABC 29-35:ADBDB AD
六、非选择题(本题包括4小题,共36分)
36.(6分,每空1分)
(1)①CO2(二氧化碳) ②S02(二氧化硫) (2)①a ②N(氮)或P(磷)
(3)①d ②NaNO2
37.(8分)
(1)隔绝空气(或氧气)(1分) (2)b、d(2分)
(3)Mg(OH) CaCO +2HA = CaA+CO ↑+H O(3分)
2 3 2 2 2
(4)食醋(或白醋) 气泡产生(2分)
38.(10分)
(1)复分解反应 熟石灰(或消石灰) CaCO (碳酸钙)(3分)
3
(2)液面低于滤纸边缘 pH 计(酸度计或pH测定仪)(2分)
(3)①a ②CuO·8HO在水中不太稳定会缓慢分解(2分)
2 2
(4) 17.8%(1分)
39.(12分)
(1)b、c、d、g(2分)
(2)①验纯 ②烧杯内壁有水珠(或雾滴)产生 2.5(或2.38)(2分)
(3)增强导电性(1分) 在相同条件下,O 较H 稍易溶于水(1分)
2 2
(4)3Fe+4H O 高温 F e O+ 4H(2分)
2 3 4 2
(5) (2分)
空气中的HO、CO 等进入B中(或装置A中生成的Cu又部分被氧化)(1分)
2 2江苏省连云港市 2018 年中考
化学试题
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 S-32 C1-35.5 Cu-64
Ag- 108
一、选择题(本题包括12小题,每小题2分,共24分。每小题只有一个选项符合题
意)
1. 每年的5月31日是“世界无烟日”。下列说法不正确的是
A. 吸烟损害大脑,使人记忆力减退
B. 长期吸烟易患肺气肿、肺癌等疾病
C. 吸烟有害健康,但“二手烟”对人体无害
D. 香烟烟气中的CO、尼古丁等对人体危害很大
【答案】C
【解析】A、吸烟损害大脑,使人记忆力减退,故A正确;B、长期吸烟易患肺气肿、肺癌等疾病,
故B正确;C、吸烟有害健康,但“二手烟”对人体危害更大,故C错误;D、香烟烟气中的CO、
尼古丁等对人体危害很大,故D正确。
点睛∶吸烟危害健康,尽量少吸烟或不吸烟,特别是在公共场所不要吸烟。
2. 下列过程中包含化学变化的是
A. 酒精挥发 B. 冰雪融化 C. 干冰升华 D. 金属氧化
【答案】D
【解析】化学变化是指变化时生成了其他物质的变化,物理变化是指没有生成其他物质的变
化。A、酒精挥发,仅是物质状态的变化,没有生成其他物质,属于物理变化;B、冰雪融化,仅
是物质状态的变化,没有生成其他物质,属于物理变化;C、干冰升华,仅是物质状态的变化,
没有生成其他物质,属于物理变化;D、金属氧化,生成了其他物质,属于化学变化。
点睛∶物理变化和化学变化的本质区别是有无其他物质生成,有其他物质生成属于化学变化,
没有其他物质生成属于物理变化。
3. 下列图示实验操作中,正确的是A. A B. B C. C D. D
【答案】A
【解析】A、酒精灯应用火柴点燃,故A正确;B、量筒读数应平视,视线应与凹液面最低处保
持水平,故B错误;C、倾倒液体,试管应倾斜,标签对着手掌心,瓶塞倒放,故C错误;D、滴
管应悬空竖直,以免污染药品,故D错误。
点睛∶严格按照实验要求规范实验操作是顺利完成实验的重要保证。
4. 下列化学用语表示正确的是
A. 3个铁离子:3Fe2+ B. 1个臭氧分子:O
3
C. 锰酸钾的化学式:KMnO D. 氟离子的结构示意图:
4
【答案】B
【解析】A、3个铁离子是3Fe3+ ,Fe2+ 是亚铁离子, 故A错误;B、1个臭氧分子是O,故B正确;
3
C、高锰酸钾的化学式是KMnO,锰酸钾的化学式是KMnO ,故C错误;D、氯原子的结构示意
4 2 4
图: ,故D错误。
点睛∶高锰酸钾的化学式是KMnO,锰酸钾的化学式是KMnO。铁离子是3Fe3+ ,Fe2+ 是亚铁离
4 2 4
子。
5. 下列几种物质中,其重要成分不属于人体所需基本营养素的是
A. 白糖 B. 白面 C. 白酒 D. 白开水
【答案】C
【解析】不属于人体所需基本营养素的是白酒,.白糖、白面、白开水均是人体所需基本营养素。
故选C。
6. 下列有关物质的性质与用途具有对应关系的是
A. 铬耐磨、耐腐蚀,可镀在钢铁制品表面防生锈
B. 石墨很软,有光泽和滑腻感,可用于制作电极C. 乙醇易挥发、易溶于水,可掺入汽油中作燃料
D. 聚四氟乙烯塑料密度小,可用作不粘锅的内衬
【答案】A
【解析】A、铬耐磨、耐腐蚀,可镀在钢铁制品表面防生锈,故A正确;B、石墨很软,有光泽和滑
腻感,可用于制作铅笔芯,故B错误;C、乙醇易挥发、易溶于汽油,具有可燃性,可掺入汽油
中作燃料,故C错误;D、聚四氟乙烯塑料熔点高,可用作不粘锅的内衬,故D错误。
点睛∶物质的结构决定物质的性质,物质的性质决定物质的用途。
7. 已知:金属X在常温下能与空气中的氧气反应,而金属Y和Z不能;将Y 、Z分别投入稀盐
酸中,Y溶解并产生气泡,Z无变化。下列说法正确的是
A. X氧化物的化学式只能表示为XO B. Y能将X从它的盐溶液中置换出来
C. Z在自然界中只能以单质形式存在 D. 三种金属的活动性顺序:X>Y>Z
【答案】D
【解析】金属X在常温下能与空气中的氧气反应,而金属Y和Z不能,说明金属x比金属Y和Z
活泼;将Y 、Z分别投入稀盐酸中,Y溶解并产生气泡,Z无变化,说明金属Y比Z活泼。A、X
氧化物的化学式不一定只能表示为XO,故A错误;B、Y不能将X从它的盐溶液中置换出来,故
B错误;C、Z在自然界中不一定只能以单质形式存在,也可能以化合物 形式存在,故C错误;
D、三种金属的活动性顺序:X>Y>Z,故D正确。
点睛∶金属在自然界中通常以两种形式存在一种是以单质形式存在,另一种是以化合物 形
式存在。
8. 下列排序正确的是
A. 空气中物质的含量:
B. 溶液的pH:
C. 氮元素的化合价:
D. 硫元素的质量分数:
【答案】B
【解析】A、空气中物质的含量由少到多的是二氧化碳﹙0.03%﹚,氧气﹙21%﹚,氮气﹙78%﹚,故A错误;B、溶液的pH值由小到大的是硫酸﹙pH<7﹚,氯化钠﹙pH=7﹚,氢氧
化钠﹙pH>7﹚,故B正确;C、氮元素的化合价由低到高的是氨气﹙-3﹚,氮气﹙0﹚,硝酸
﹙+5﹚,故C错误;D、硫元素的质量分数由小到大的是硫酸钠﹙22.5%﹚,亚硫酸钠
﹙25.4%﹚,硫化钠﹙41%﹚,故D错误。
点睛∶pH>7溶液呈碱性,pH<7溶液呈酸性,pH=7溶液呈中性。
9. 物质a和b在一定条件下反应生成e和d的微观示意图如下:
下列说法正确的是
A. 物质c是一氧化碳 B. 该反应不符合质量守恒定律
C. 该反应前后,原子的种类发生改变 D. 该反应前后,分子的个数保持不变
【答案】D
【解析】根据所学知识和题中信息知,O +CH c+HO。A、根据质量守恒定律知,
2 4 2
物质c不一定是一氧化碳,也可能是二氧化碳,故A错误;B、该反应符合质量守恒定律,任何
一个化学反应都必然遵循质量守恒定律,故B错误;C、该反应前后,原子的种类没有发生改
变,故C错误;D、该反应前后,分子的个数不一定保持不变,故D错误。
点睛∶任何一个化学反应都必然遵循质量守恒定律,化学变化的实质是分子的划分,原子的
重新组合。
10. 下列各组实验方案中,不能达到实验目的的是
选项 实验目的 实验方案
A 稀释浓硫酸 将浓硫酸缓慢注入水中,并不断搅拌
B 除去CO 气体中的HCl 将气体通过盛有足量NaOH溶液的洗气瓶
2
C 鉴别化肥KNO 和NHNO 取样,加Ca(OH) 固体混合研磨,闻气味
3 4 3 2
D 除去FeCl 溶液中的CuCl 加入过量的Fe粉,充分反应后过滤
2 2
A. A B. B C. C D. D
【答案】B【解析】
选项 实验目的 实验方案
将浓硫酸缓慢注入水中,并不断搅拌,浓硫酸密度比水大,稀释时
A 稀释浓硫酸
放热,故A正确;
将气体通过盛有足量NaOH溶液的洗气瓶,二氧化碳和氯化氢均
B 除去CO 气体中的HCl
2 与NaOH溶液反应,故B错误;
取样,加Ca(OH) 固体混合研磨,闻气味,硝酸铵与Ca(OH) 反应
C 鉴别化肥KNO 和NHNO 2 2
3 4 3 生成有刺激性气味的气体,故C正确;
加入过量的Fe粉,充分反应后过滤,铁与CuCl 反应生成氯化亚
D 除去FeCl 溶液中的CuCl 2
2 2 铁和铜,故D正确。
点睛∶铵盐遇到氢氧化钙发生产生氨气,这是我们检验铵盐常用的方法。活泼的金属可以把
不活泼的金属从它的盐溶液中置换出来。
11. 甲、乙、丙三种固体物质的溶解度曲线如右图所示。下列说法不正确的是
A. T℃时,取等质量的甲、乙分别配制成饱和溶液,所需水的质量:甲>乙
2
B. T℃时,将甲、乙的饱和溶液均降温到T℃,得到的溶液仍饱和
2 1
C. 若甲中混有少量的丙,可采用降温结晶的方法提纯甲
D. T℃时,甲、乙各30g分别加入100g水中,均形成饱和溶液
2
【答案】AD点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解度或溶解度随温度变化的
情况;②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的
大小。若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;③根据溶解度
曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;④根据溶解度曲线能进
行有关的计算。
12. 甲、乙、丙、X、Y、Z六种物质间只通过一步反应就能实现右图中箭头所示的转化。不符合
上述要求的一组物质是
选项 甲 X
A O HO
2 2
B CO CaCO
2 3
C Fe FeO
3 4
D NaOH NaNO
3
A. A B. B C. C D. D
【答案】D
学。科。网...学。科。网...学。科。网...学。科。网...学。科。网...
选项 甲 XA O HO,氢气燃烧生成水,水通电分解生成氧气,故A正确;
2 2
CaCO,二氧化碳通入石灰水生成碳酸钙白色沉淀,碳酸钙高温分解
B CO 3
2 生成二氧化碳,故B正确;
FeO,铁丝在氧气中燃烧生成四氧化三铁,FeO 与氢气或二氧化碳
C Fe 3 4 3 4
高温反应生成铁,故C正确;
NaNO,NaOH与稀酸反应生成硝酸钠,硝酸钠不可能一步通过反应生
D NaOH 3
成氢氧化钠,故D错误。
点睛∶掌握常见物质的性质是顺利完成本题的重要保证。水通电分解生成氧气和氢气,FeO
3 4
与氢气或二氧化碳高温反应生成铁,碳酸钙高温分解生成二氧化碳。
二、非选择题(本题包括4小题,共36分)
【环境与化学】
13. 坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,
水更清,空气更清新”是我们共同的追求。
(1)“山更绿”离不开绿色植物。
①植物的光合作用需要吸收空气中的水和________,可有效减缓温室效应。
②酸雨不利于植物生长。煤燃烧产生的________进入大气后可形成“硫酸型”酸雨。
(2)“水更清”就得保护好水资源。
①下列关于水的说法正确的是________ (填字母)。
a.工业废水需经处理达标后才可排放
b.为保护好水资源,禁止使用化肥和农药
c.天然水只要通过处理后变清即可饮用
d.为了改善水质,可向其中加入大量的净水剂和消毒剂
②“赤潮”或“水华”主要是由于水中某些营养元素含量过高,导致藻类大量繁殖,鱼类等
死亡。这里的营养元素主要指________ (写出一种即可)。
(3)“空气更清新”需要监测防治大气污染。
①目前未计入空气污染指数监测项目的有________ (填字母)。
a.一氧化碳 b.二氧化氮 c.可吸人颗粒物 d.稀有气体
②硝酸工厂排放的尾气中常含有NO、NO 等有害气体,可用氢氧化钠溶液来吸收:NO+NO +2
2 2
NaOH=2X+HO。 X的化学式为________。
2
【答案】 (1). CO(二氧化碳) (2). S0(二氧化硫) (3). a (4). N(氮)或P(磷) (5). d (6).
2 2
NaNO
2【解析】(1)“山更绿”离不开绿色植物。①植物的光合作用需要吸收空气中的水和CO(二氧
2
化碳),可有效减缓温室效应,水和CO 是植物光合作用的原料,二氧化碳是产生温室效应的
2
主要气体。②酸雨不利于植物生长。煤燃烧产生的S0(二氧化硫) 进入大气后可形成“硫酸
2
型”酸雨,二氧化硫与水反应生成亚硫酸,亚硫酸具有酸性。(2)“水更清”就得保护好水资
源。①a、工业废水需经处理达标后才可排放,以免污染环境,故a正确;b、为保护好水资源,
合理使用化肥和农药,不是禁止使用化肥和农药,故b错误;c、天然水通过处理后变清不一
定就能即可饮用,可能溶有有些杂质或细菌,故c错误;d、为了改善水质,可向其中加入适量
的净水剂和消毒剂,不可过量,故d错误。②“赤潮”或“水华”主要是由于水中某些营养
元素含量过高,导致藻类大量繁殖,鱼类等死亡。这里的营养元素主要指N(氮)或P(磷),
N(氮)或P(磷)是藻类生长所需的营养元素。(3)“空气更清新”需要监测防治大气污染。①
目前未计入空气污染指数监测项目的有稀有气体,一氧化碳、二氧化氮、可吸人颗粒物均属
于空气污染指数监测项目。②硝酸工厂排放的尾气中常含有NO、NO 等有害气体,可用氢氧化
2
钠溶液来吸收,NO+NO+2NaOH=2X+HO。根据质量守恒定律知,X的化学式为NaNO。
2 2 2
点睛∶保护环境人人有责。山更绿离不开绿色植物,水更清就得保护好水资源,空气更清新
需要监测防治大气污染。藻类大量繁殖的主要原因是N(氮)或P(磷) 营养元素的大量富集。
【厨房中的化学】
14. (1)炒菜时油锅着火可用锅盖盖灭,其灭火原理是________。
(2)家用液化气的主要成分之一是丙烷(CH),丙烷属于________ (填字母)。
3 8
a.氧化物 b.化合物 c.无机物 d.有机物
(3)热水壶中水垢的主要成分是CaCO 和________ (填化学式), 可用食醋洗涤。食醋的重
3
要成分是醋酸(设其化学式为HA),写出其与CaCO 反应的化学方程式:________。
3
(4)利用厨房中的物品鉴別食盐和苏打:取一固体于碗中,加入________(填物质名称),若有
________,则该固体为苏打;若无此现象,则为食盐。
【答案】 (1). 隔绝空气(或氧气) (2). b、d (3). Mg(OH) (4).
2
CaCO+2HA = CaA+CO↑+HO (5). 食醋(或白醋) (6). 气泡产生
3 2 2 2
【解析】(1)炒菜时油锅着火可用锅盖盖灭,其灭火原理是隔绝空气(或氧气),这是灭火所采
取的措施之一。(2)家用液化气的主要成分之一是丙烷(CH),丙烷属于有机物化合物。故选
3 8
b、d。(3)热水壶中水垢的主要成分是CaCO 和Mg(OH),可用食醋洗涤。食醋的重要成分是醋
3 2
酸(设其化学式为HA),其与CaCO 反应的化学方程式是CaCO+2HA = CaA+CO↑+HO。(4)
3 3 2 2 2
利用厨房中的物品鉴別食盐和苏打:取一固体于碗中,加入食醋(或白醋) ,若有气泡产生,则该固体为苏打;若无此现象,则为食盐,食醋与碳酸钠反应生成二氧化碳气体。
点睛∶水垢的主要成分是碳酸钙和氢氧化镁,灭火常用的方法是设立隔离带或隔绝空气或
降低可燃物周围环境的温度使其低于可燃物的着火点。
【生产中的化学】
15. 过氧化钙( CaO)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH),含少量
2 2
CaCO 为原料制备CaO 的一种工艺流程如下:
3 2
【查阅资料】I. Ca(OH)+2NHCl=CaCl+2NH·HO
2 4 2 3 2
Ⅱ.CaCl+2NH·HO+HO +6HO= CaO·8HO↓+ 2NHCl
2 3 2 2 2 2 2 2 4
Ⅲ. CaO·8HO在水中不太稳定,会缓慢分解。
2 2
(1)“提取Ca(OH)”时反应的基本类型是_______;Ca(OH) 的俗名为_______;“过滤1”所
2 2
得滤渣的主要成分是_______。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸
边缘略低于漏斗口、_______。生产过程中为了精确测定溶液的pH,常使用_______ (填仪器
名称)。
(3)在其他条件不变的情况下,制备CaO·8HO的反应时间(t)对其产率(w)的影响如图所示。
2 2
①平均反应速率最快的时间段为:_______ (填字母)。
a. 0~10min b. 10~20min c. 20~30min d.30~40min
②30min后,w开始下降的主要原因是_______。
(4)为了测定加入的NHCl溶液中溶质的质量分数,取30.00g NHCl溶液于烧杯中,加入稍
4 4
过量的AgNO 溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确
3
定该溶液中NHCl的质量分数(精确到0.1%)____。
4
【答案】 (1). 复分解反应 (2). 熟石灰(或消石灰) (3). CaCO(碳酸钙) (4). 液面低于
3滤纸边缘 (5). pH 计(酸度计或pH测定仪) (6). a (7). CuO·8HO在水中不太稳定会缓
2 2
慢分解 (8). 17.8%
【解析】根据所学知识和题中信息知,(1)“提取Ca(OH)”时反应的基本类型是复分解反应;
2
Ca(OH) 的俗名为熟石灰(或消石灰)。“过滤1”所得滤渣的主要成分是CaCO(碳酸钙)。(2)
2 3
在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边
缘略低于漏斗口、液面低于滤纸边缘。生产过程中为了精确测定溶液的pH,常使用pH计(酸
度计或pH测定仪)。(3)由图中信息知,①平均反应速率最快的时间段为0~10min,故选a。
②30min后,w开始下降的主要原因是CuO·8HO在水中不太稳定会缓慢分解。(4)测定加入
2 2
的NHCl溶液中溶质的质量分数∶
4
NHCl+AgNO=AgCl↓+NHNO
4 3 4 3
53.5 143.5
30.0g×x 14.35g
= ,x=17.8%。
点睛∶Ca(OH) 的俗名为熟石灰(或消石灰)。精确测定溶液的pH,常使用pH计(酸度计或pH
2
测定仪)。
【走进化学实验室】
16. 水是由氢、氧两种元素组成的化合物。这一结论是科学家们在大量实险的基础上得出的。
(1)实验室中常用锌粒和稀硫酸反应来制备氢气。请从下列装置中选择并组装一套制取干燥
氢气的装置,正确的连接顺序为_______ (用接口处字母填写)。
(2)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要_________。
②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,可观察到的现象是_______。
在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为______L。
(3)科学家们又用“电解法”证明了水的组成(装置如图所示,电极不与水及生成的气体反应)。
电解时,水中需加入少量的NaOH,其作用是_________。 通电一段时间后,发现甲、乙两量
简中收集的气体体积比略小于1:2,其原因可能是_________ (写出一条即可)。
(4)拉瓦锡还用另一实验证明了水的组成。
他让水蒸气通过一根烧红的铁质枪管,结果得到了氧气,同时枪管表面有黑色固体(磁铁矿
的主要成分)生成。该反应的化学方程式为_______。
(5)用“氢气还原氧化铜”实验也可以证明水的组成。
装置A中的玻璃管和其中物质在反应前后的质量差为m,装置B和其中物质在反应前后的质
1
量差为m,据此可计算出水中O、H元素的质量比为______(用含 m、m 的代数式表示)。实验
2 1 2
时该比值往往略小于8:1,原因可能是_____(写出一条即可)。
【答案】 (1). b、c、d、g (2). 验纯 (3). 烧杯内壁有水珠(或雾滴)产生 (4). 2.5(或
2.38) (5). 增强导电性 (6). 在相同条件下,O 较H 稍易溶于水 (7). 3Fe+4HO
2 2 2
FeO+4H (8). (9). 空气中的HO、CO 等进入B中(或装置A中生成的Cu又部分被氧
3 4 2 2 2
化)
【解析】(1)实验室中常用锌粒和稀硫酸反应来制备氢气。制取干燥氢气的装置,正确的连接
顺序为b、c、d、g。(2)研究氢气的燃烧实验是人们认识水组成的开始。①氢气在点燃前一定
要验纯,若不纯,有可能爆炸。②氢气在空气中燃烧时,若在火焰上方罩一冷而干燥的小烧杯,
可观察到的现象是烧杯内壁有水珠(或雾滴)产生,氢气燃烧生成了水。在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为∶0.5L÷21%=2.38 L。(3) 电解时,水中需加入少量
的NaOH,其作用是增强导电性。通电一段时间后,发现甲、乙两量简中收集的气体体积比略小
于1:2,其原因可能是在相同条件下,O 较H 稍易溶于水。(4)拉瓦锡还用另一实验证明了水
2 2
的组成。水蒸气通过一根烧红的铁质枪管,结果得到了氧气,同时枪管表面有黑色固体(磁铁
矿的主要成分)生成。该反应的化学方程式为3Fe+4HO FeO+4H。(5)用“氢气还原氧化
2 3 4 2
铜”实验也可以证明水的组成。出水中O、H元素的质量比为 。实验时该比值往往略小
于8:1,原因可能是空气中的HO、CO 等进入B中(或装置A中生成的Cu又部分被氧化)。
2 2
点睛∶水是由氢、氧两种元素组成的化合物。电解时,水中需加入少量的NaOH,其作用是增强
导电性。