文档内容
【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
扬州市 2025 年初中毕业升学考试
化学
注意事项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共6页,满分为100分,考试时间为100分钟。考试结束后,请将本试卷和答题卡一
并交回。
2.答题前,务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题卡的
规定位置,在试卷第一面的右下角填写好座位号。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4.答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦
干净后,再选涂其他答案。答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上的指
定位置作答,在其他位置作答一律无效。
5.如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。
可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 Ca40
一、单项选择题:共20题,每题2分,共40分。每题只有一个选项最符合题意。
1. 下列是我国几位科学家及其部分研究领域,其中研究领域主要涉及能量的储存与释放的是
A. 徐光宪,稀土元素分离技术研究 B. 屠呦呦,抗疟药物研究
C. 王泽山,火炸药等高能材料研究 D. 侯德榜,制碱工艺研究
2. 科学发展常以如题图所示的方式推进、循环。公元前5世纪,有哲学家猜想:万物是由极其微小的、不
可分割的“原子”构成。这属于
A. 观察现象 B. 提出问题 C. 建立假说 D. 实验验证
3. 食品包装袋内充入某气体可以避免食物因氧化而变质,该气体可以是
A. B. C. D.
4. 锌肥是一种微量元素肥料,能够提高作物的产量。下列物质属于锌肥的是
1【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. B. C. D.
5. 可用于自来水的杀菌消毒。 属于
A. 氧化物 B. 酸 C. 碱 D. 盐
6. 四氯化钛 是制备钛白粉的主要原料。 中钛元素的化合价为
A. +1 B. +2 C. +3 D. +4
7. 俗名往往反映了物质的组成、性质或用途。下列对物质俗名的理解正确的是
A. 铜绿:单质铜为绿色 B. 干冰:干净无杂质的冰
C. 石灰石: 经煅烧可制备生石灰 D. 水银:汞 是液态的银
8. 常温下,测得生活中一些物质的pH如下,其中能使紫色石蕊试液变红的是
A. 柠檬汁:pH=2.5 B. 食盐水:pH=7 C. 肥皂水:pH=10.2 D. 油污净:pH=11.2
9. 碘是生命活动必需的微量元素,碘在元素周期表中的信息如题图所示。下列说法不正确的是
的
A. 碘 元素符号为I B. 碘属于非金属元素
C. 碘原子核内有53个中子 D. 碘的相对原子质量为126.9
10. 构成物质的微观粒子有分子、原子、离子等。下列物质由分子构成的是
A. 氧化镁 B. 金
C. 金刚石 D. 水
11. 《天工开物》记载:“凡蓝五种,皆可为淀。”“蓝淀”用于染布,色泽浓郁且洗涤不易掉色,其主
要成分的化学式为C H NO,下列关于C H NO 的说法正确的是
16 10 2 2 16 10 2 2
2【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 易溶于水 B. 分子中含氧分子(O)
2
C. 由C、H、N、O四种元素组成 D. C、H两种元素的质量比为8∶5
12. 红磷在O 中燃烧生成PO,其转化可表示为 在给定条件下,下列物质间的转化不能实
2 2 5 .
现的是
.
A Fe FeSO B. NH HCO NH
4 4 3 3
C. H HO D. CuO Cu(OH)
2 2 2
13. 汽车尾气净化装置中发生反应:2CO+2X N+2CO ,X的化学式为
2 2
A. NO B. NO C. NO D. NO
2 2 4 2
14. 下列实验方案能达到实验目的的是
选
实验方案 实验目的
项
A 加热KMnO 固体,并用向下排空气法收集产生的气体 制备并收集O
4 2
B 将燃着的木条靠近集气瓶口,观察现象 收集CO 时,检验是否集满
2
C 用玻璃棒蘸取NaOH溶液滴在湿润的pH试纸上,与标准比色卡对照 测定NaOH溶液的pH
D 将粗盐溶解后,蒸发结晶 去除粗盐中的难溶性杂质
A. A B. B C. C D. D
15. 下列实验操作不正确的是
A. 读取液体体积 B. 稀释浓硫酸
C. 过滤沉淀 D. 干燥氢气
3【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
阅读下列材料,完成下面小题。
SO 是空气污染物之一,也是重要的化工原料。燃煤烟气中含少量的SO ,可用NaSO 处理,方法如下:
2 2 2 3
步骤一,将烟气通入NaSO 溶液,发生反应①NaSO +SO+H O=2NaHSO ;步骤二,加热NaHSO 溶液,
2 3 2 3 2 2 3 3
发生反应②2NaHSO NaSO +SO↑+H O。
3 2 3 2 2
16. 下列物质的排放会引起酸雨的是
A. SO B. CO C. CO D. CH
2 2 4
17. 步骤二中反应②的类型是
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
18. 关于用NaSO 处理烟气中SO 的方法,下列说法不正确的是
2 3 2
A. 步骤一的作用是吸收烟气中的SO
2
B. 向NaSO 溶液中快速通入热的烟气,有利于SO 的吸收
2 3 2
C. 与烟气中的SO 相比,步骤二释放出的SO 较为纯净
2 2
D. 该处理方法中NaSO 可循环使用
2 3
19. 下列对实验现象的解释正确的是
选
实验现象 解释
项
25℃时,向某蔗糖溶液中加入少量蔗糖,蔗糖逐渐 原溶液是25℃时,蔗糖的
A
消失 饱和溶液
80℃的NH Cl饱和溶液冷却至20℃时,有晶体析 温度降低,NH Cl的溶解度
B 4 4
出 增大
将铁丝浸入CuSO 溶液,一段时间后,铁丝表面
C 4 Cu的金属活动性比Fe强
有红色固体出现
将干冷的烧杯罩在蜡烛火焰上方,烧杯内有黑烟和
D 蜡烛中含有碳元素、氢元素
水雾
A. A B. B C. C D. D
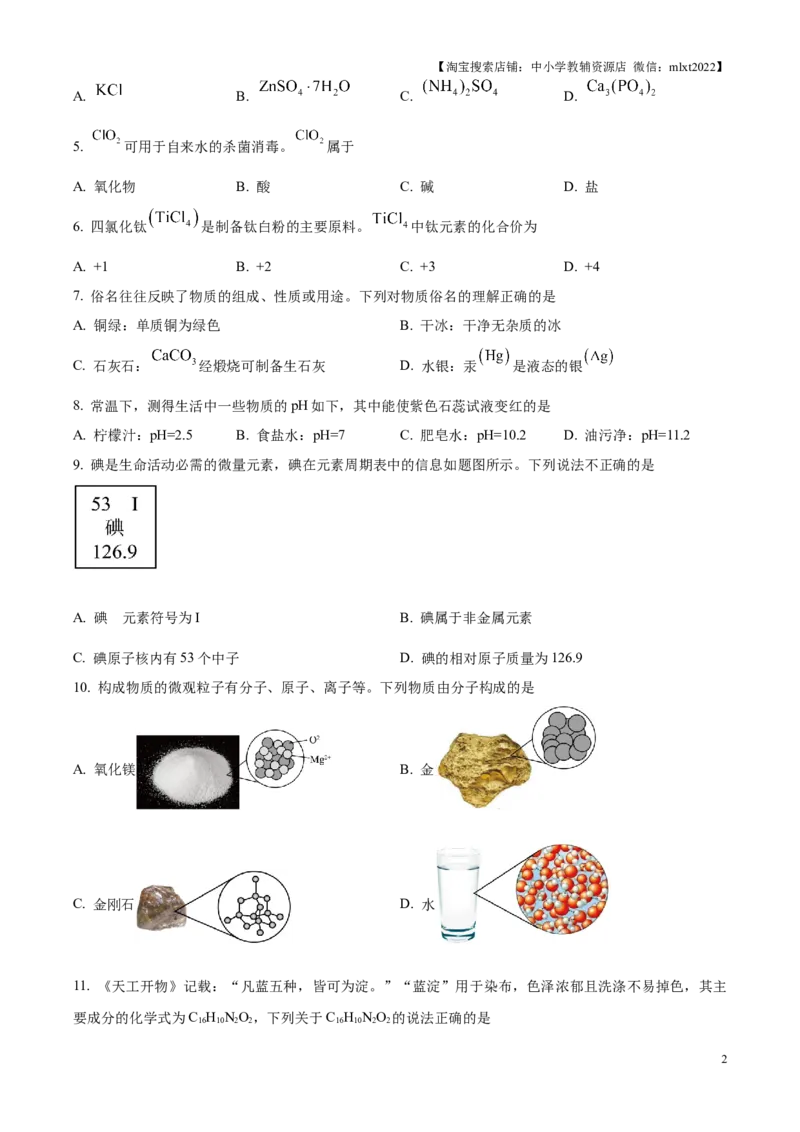
20. 某催化剂可实现HO与O 反应制备HO。向容器中加入100gHO和适量催化剂,并不断通入O,保
2 2 2 2 2 2
的
持其他条件不变,分别在20℃、40℃和60℃下进行实验①、②、③,测得HO 产量随时间的变化如题
2 2
图所示。下列说法不正确的是
4【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
A. 设计实验①、②、③的目的是探究温度对该催化反应的影响
B. 实验①说明:20℃,在0~3h内,随着时间的增加,该催化反应持续进行
C. 比较实验①、②可知,在0~3h内,40℃比20℃对该催化反应更有利
D. 实验③中2h后,HO与O 不再反应,生成的HO 开始分解
2 2 2 2
二、非选择题:共5题,共60分。
21. 被誉为“中国运河第一城”的扬州,既有深厚文化底蕴,又充满创新活力。
(1)“产业科创名城”激发澎湃动能。
①特种工程塑料用于制作无人机起落架。塑料属于______(填“无机物”或“有机物”)。
②夏季穿着智能纤维制作的衣物,出汗后衣物的透气性变好,有利于吸湿排汗,说明汗水会使智能纤维的
孔隙______(填“变大”“不变”或“变小”)。
(2)“生态宜居名城”绘就崭新图景。
①小秦淮河保护更新工程使水质提升。在河道中种植合适的水生植物后,河水中硝酸盐含量降低,避免了
河水的富营养化,说明该植物在生长过程中能够吸收的营养元素为______(填元素符号)。
②扬州市将瘦西湖打造为“零碳”景区,用清洁能源代替化石燃料,助力实现碳中和目标。这里的“零
碳”指的是______。
(3)“文化旅游名城”展示独特魅力。
①古文献《食经》中记载了“碎金饭”的做法,制作时用到的食材有鸡蛋、食用油、大米,其中富含淀粉
的是______。
②隋炀帝墓葬考古发现了铜铺首(题图)、萧后凤冠等文物。铜铺首采用了鎏金工艺,即在青铜表面镀金。
通常条件下,铜、金两种金属中耐腐蚀性能更好的是______。铜铺首材料中属于合金的是______(填
“金”或“青铜”)。凤冠表面有一种疏松的“粉状锈”,主要成分为Cu (OH)Cl。为避免“粉状锈”
2 3
蔓延,可用氧化银进行脱氯处理,氧化银的化学式为______。
(4)“崇文尚教名城”赋能时代新篇。博物馆科普研学活动中,同学们对“粉状锈的产生展开研究。有
同学提出:导致青铜器产生“粉状锈”的因素,除了O 和HO外,还有含氯离子的物质。为验证该观点,
2 2
5【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
设计以下实验,请补充完整实验方案:实验1,将青铜片置于潮湿空气环境中;实验2,将青铜片置于
______的环境中,相同时间后观察现象。
22. 太空中,宇航员的每一次呼吸都离不开一系列精心设计的化学反应。
(1)空间站模拟地球的大气环境。
①法拉第认为,空气进入肺部,碳与氧立即结合,即使外面天寒地冻,我们也能通过呼吸迅速产生二氧化
碳。一切反应都恰到好处地进行着。呼吸与燃烧有着巧妙且惊人的相似之处。”他的观点是,伴随呼吸过
程会______(填“吸收”或“放出”)热量,从而维持人体的体温正常。
②成年人每次呼吸时,吸入的空气和呼出的气体的成分(部分)质量变化如图-1所示。图中成分B的化学
式为______。
③快速深呼吸时,人体血液中的CO 含量会减小,此时人体血液的碱性会______(填“增强”或“减
2
弱”)。
(2)空间站源源不断为呼吸提供O 备用装置可应急提供O,其原理是:NaClO 固体受热分解产生O;
2. 2 3 2
均匀添加于其中的适量金属锰(Mn)在O 中燃烧生成氧化物,有助于快速产生O 添加金属Mn的作用是
2 2.
______。
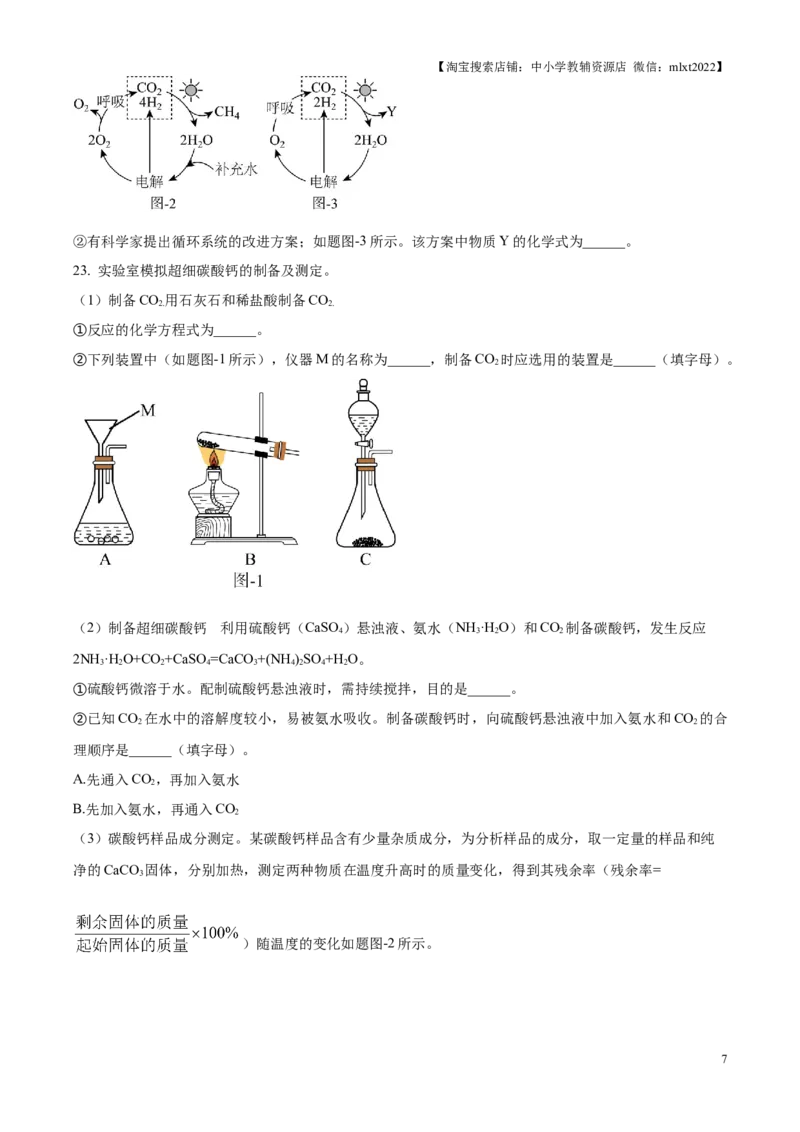
(3)空间站需及时处理产生的CO
2.
①中国空间站构建了高效循环的生命保障系统,如题图-2所示。该系统中发生反应CO+4H
2 2
CH+2H O。每转化44gCO,需从外界补充水的质量为______g。
4 2 2
6【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
②有科学家提出循环系统的改进方案;如题图-3所示。该方案中物质Y的化学式为______。
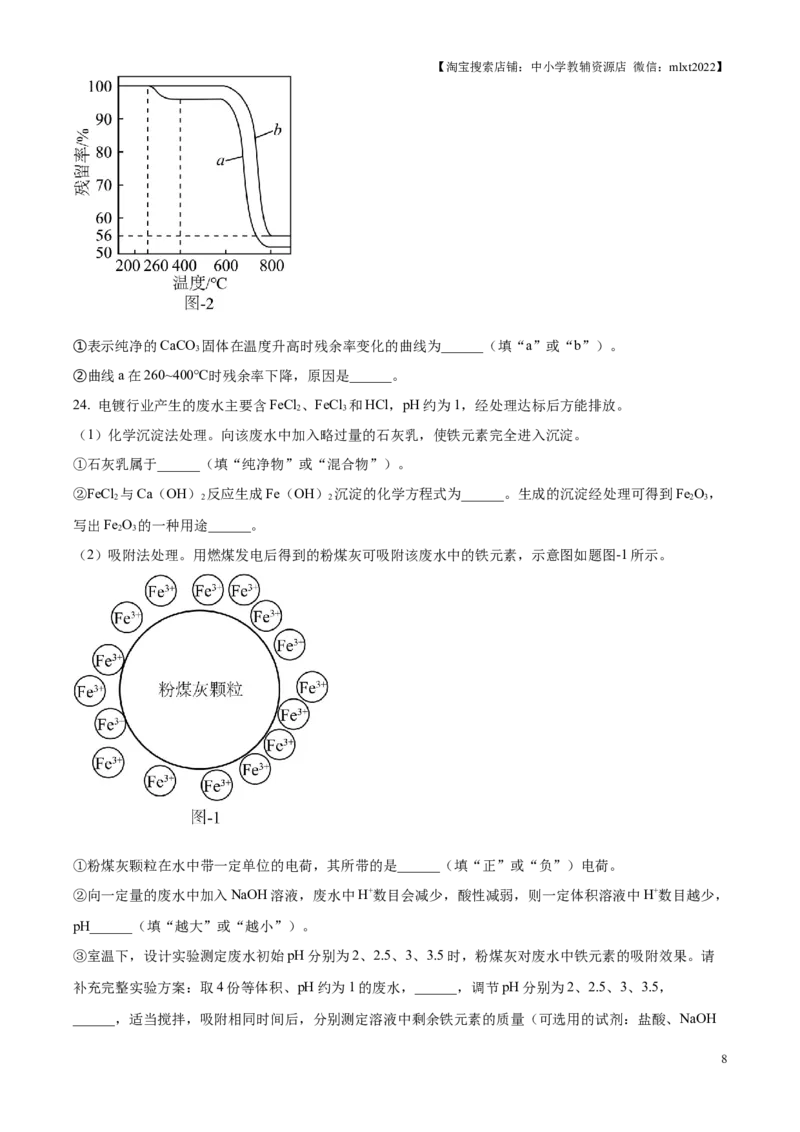
23. 实验室模拟超细碳酸钙的制备及测定。
(1)制备CO 用石灰石和稀盐酸制备CO
2. 2.
①反应的化学方程式为______。
②下列装置中(如题图-1所示),仪器M的名称为______,制备CO 时应选用的装置是______(填字母)。
2
(2)制备超细碳酸钙 。利用硫酸钙(CaSO)悬浊液、氨水(NH ·H O)和CO 制备碳酸钙,发生反应
4 3 2 2
2NH ·H O+CO+CaSO =CaCO +(NH)SO +H O。
3 2 2 4 3 4 2 4 2
①硫酸钙微溶于水。配制硫酸钙悬浊液时,需持续搅拌,目的是______。
②已知CO 在水中的溶解度较小,易被氨水吸收。制备碳酸钙时,向硫酸钙悬浊液中加入氨水和CO 的合
2 2
理顺序是______(填字母)。
A.先通入CO,再加入氨水
2
B.先加入氨水,再通入CO
2
(3)碳酸钙样品成分测定。某碳酸钙样品含有少量杂质成分,为分析样品的成分,取一定量的样品和纯
净的CaCO 固体,分别加热,测定两种物质在温度升高时的质量变化,得到其残余率(残余率=
3
)随温度的变化如题图-2所示。
7【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①表示纯净的CaCO 固体在温度升高时残余率变化的曲线为______(填“a”或“b”)。
3
②曲线a在260~400℃时残余率下降,原因是______。
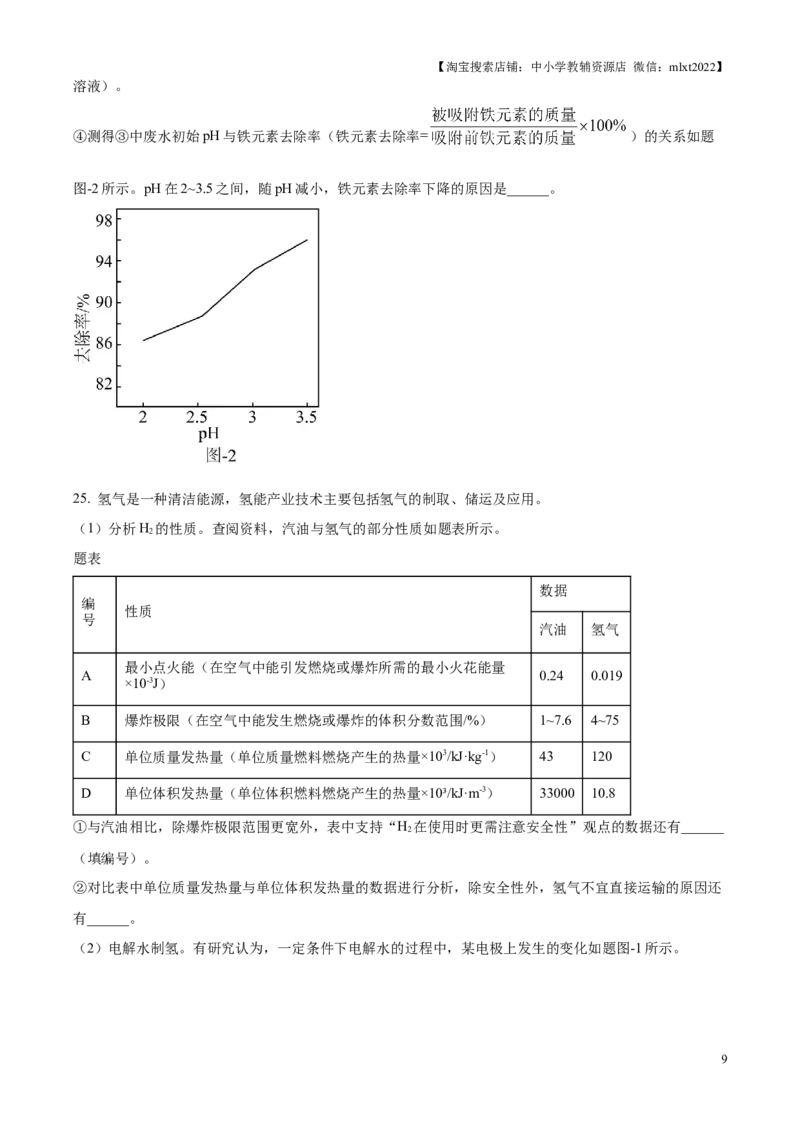
24. 电镀行业产生的废水主要含FeCl 、FeCl 和HCl,pH约为1,经处理达标后方能排放。
2 3
(1)化学沉淀法处理。向该废水中加入略过量的石灰乳,使铁元素完全进入沉淀。
①石灰乳属于______(填“纯净物”或“混合物”)。
②FeCl 与Ca(OH) 反应生成Fe(OH) 沉淀的化学方程式为______。生成的沉淀经处理可得到Fe O,
2 2 2 2 3
写出Fe O 的一种用途______。
2 3
(2)吸附法处理。用燃煤发电后得到的粉煤灰可吸附该废水中的铁元素,示意图如题图-1所示。
①粉煤灰颗粒在水中带一定单位的电荷,其所带的是______(填“正”或“负”)电荷。
②向一定量的废水中加入NaOH溶液,废水中H+数目会减少,酸性减弱,则一定体积溶液中H+数目越少,
pH______(填“越大”或“越小”)。
③室温下,设计实验测定废水初始pH分别为2、2.5、3、3.5时,粉煤灰对废水中铁元素的吸附效果。请
补充完整实验方案:取4份等体积、pH约为1的废水,______,调节pH分别为2、2.5、3、3.5,
______,适当搅拌,吸附相同时间后,分别测定溶液中剩余铁元素的质量(可选用的试剂:盐酸、NaOH
8【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
溶液)。
④测得③中废水初始pH与铁元素去除率(铁元素去除率= )的关系如题
图-2所示。pH在2~3.5之间,随pH减小,铁元素去除率下降的原因是______。
25. 氢气是一种清洁能源,氢能产业技术主要包括氢气的制取、储运及应用。
(1)分析H 的性质。查阅资料,汽油与氢气的部分性质如题表所示。
2
题表
数据
编
性质
号
汽油 氢气
最小点火能(在空气中能引发燃烧或爆炸所需的最小火花能量
A 0.24 0.019
×10-3J)
B 爆炸极限(在空气中能发生燃烧或爆炸的体积分数范围/%) 1~7.6 4~75
C 单位质量发热量(单位质量燃料燃烧产生的热量×103/kJ·kg-1) 43 120
D 单位体积发热量(单位体积燃料燃烧产生的热量×10³/kJ·m-3) 33000 10.8
①与汽油相比,除爆炸极限范围更宽外,表中支持“H 在使用时更需注意安全性”观点的数据还有______
2
(填编号)。
②对比表中单位质量发热量与单位体积发热量的数据进行分析,除安全性外,氢气不宜直接运输的原因还
有______。
(2)电解水制氢。有研究认为,一定条件下电解水的过程中,某电极上发生的变化如题图-1所示。
9【淘宝搜索店铺:中小学教辅资源店 微信:mlxt2022】
①“阶段一”中,生成的“ ”是一种阴离子,其离子符号为______。
②“阶段三”中,气泡从电极表面脱离后,在溶液中向上运动时,所受压强逐渐减小,体积逐渐增大。从
的
微观粒子 视角,对气泡体积增大进行解释:______。
③相同条件下,若电极表面的气泡难以脱离,则不利于氢气的产生。原因是______。
(3)甲酸(HCOOH)分解制氢。常温下,甲酸是一种液态物质,可通过反应Ⅰ制备H,化学方程式为
2
HCOOH CO↑+H ↑。
2 2
①制备H 时,部分甲酸会发生反应Ⅱ:HCOOH分解为HO和另一种有毒气体。该气体的化学式为______。
2 2
②仅考虑以上两个反应,若有92%的甲酸发生反应Ⅰ,计算500吨(t)甲酸可制得H₂的质量______(写出
计算过程)。
(4)高效利用能源。为实现可持续发展,用可再生能源如太阳能、风能等发电引起人们的关注。但太阳
能、风能等无法实现及时或稳定的能源供应,通过它们产生的过剩电能制氢,再供给有能源需求的地区使
用,如题图-2所示,可实现能源的高效利用。
该过程中HCOOH的作用是______。
10