文档内容
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO 2﹣)>c(NH +)
2008 年北京市高考化学试卷 4 4
B.两种醋酸溶液的物质的量浓度分别为c 和c ,pH分别为a和a+1,则c =10c
1 2 1 2
一、选择题(共7小题,每小题6分,满分42分)
C.pH=11的NaOH溶液与pH=3醋酸溶液等体积混合,滴入石蕊试液呈红色
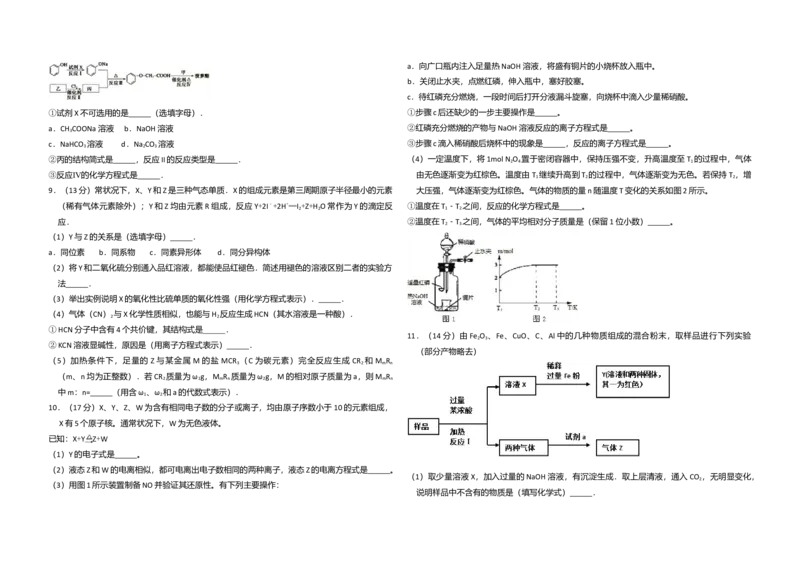
1.(6分)对H O的电离平衡不产生影响的粒子是( )
2
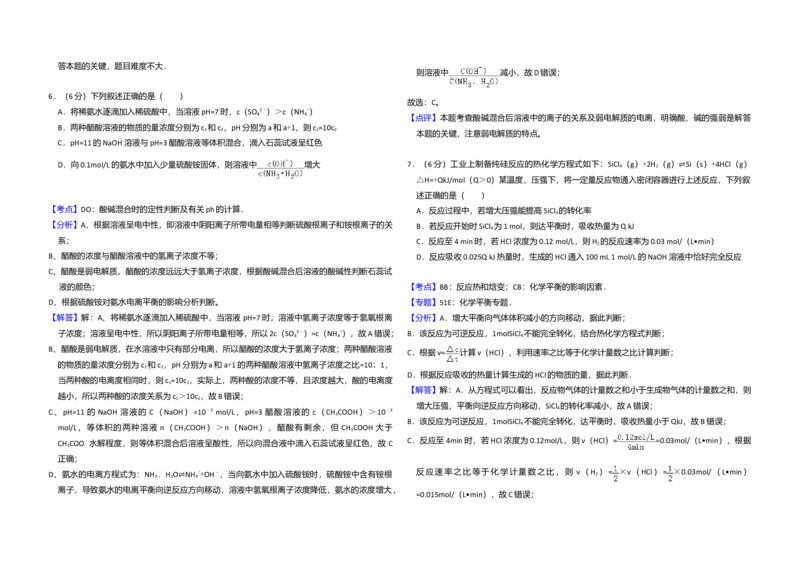
D.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中 增大
A. B. M3+ C. D.
26
7.(6分)工业上制备纯硅反应的热化学方程式如下:SiCl (g)+2H (g) Si(s)+4HCl(g)
4 2
2.(6分)1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体
△H=+QkJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行
⇌
上述反应,下列叙
物质后冷却,残留的固体物质是( )
述正确的是( )
A.Na CO B.Na O Na CO
2 3 2 2 2 3 A.反应过程中,若增大压强能提高SiCl 的转化率
4
C.NaOH Na CO D.Na O NaOH Na CO
2 3 2 2 3 3 B.若反应开始时SiCl 为1 mol,则达平衡时,吸收热量为Q kJ
4
3.(6分)下列叙述正确的是( )
C.反应至4 min时,若HCl浓度为0.12 mol/L,则H 的反应速率为0.03 mol/(L•min)
2
A.金属与盐溶液的反应都是置换反应
D.反应吸收0.025Q kJ热量时,生成的HCl通入100 mL 1 mol/L的NaOH溶液中恰好完全反应
B.阴离子都只有还原性
C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
二、解答题(共4小题,满分60分)
D.分子晶体中都存在范德华力,可能不存在共价键
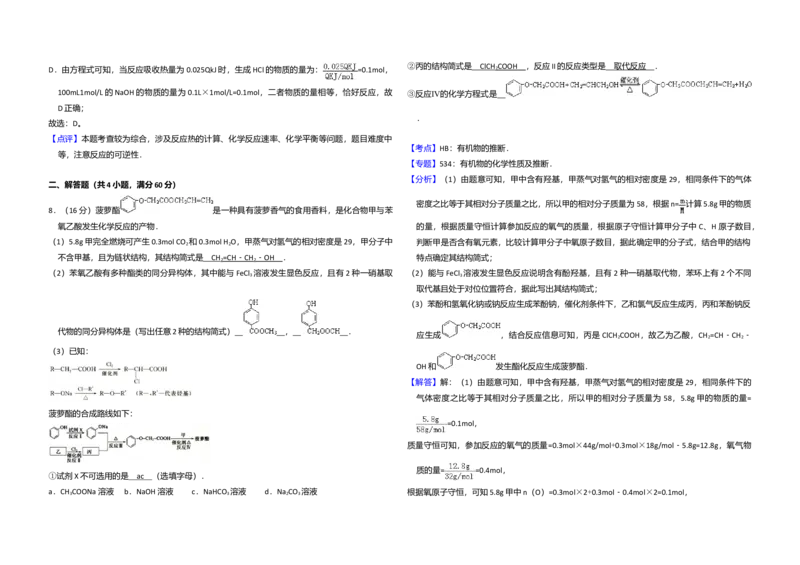
4.(6分)下列各组物质的无色溶液,不用其它试剂即可鉴别的是( ) 8.(16分)菠萝酯 是一种具有菠萝香气的食用香料,是化合物甲与苯
①KOH、Na SO 、AlCl 氧乙酸发生化学反应的产物.
2 4 3
②NaHCO 、Ba(OH) 、H SO (1)5.8g甲完全燃烧可产生0.3mol CO 和0.3mol H O,甲蒸气对氢气的相对密度是29,甲分子中
3 2 2 4 2 2
③HCl、NaAlO 、NaHSO 不含甲基,且为链状结构,其结构简式是 .
2 4
④Ca(OH) 2 、Na 2 CO 3 、BaCl 2 . (2)苯氧乙酸有多种酯类的同分异构体,其中能与 FeCl 3 溶液发生显色反应,且有2种一硝基取
A.①② B.②③ C.①③④ D.①②④ 代物的同分异构体是(写出任意2种的结构简式) , .
5.(6分)X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确 (3)已知:
的是( )
A.由 Xa+与 Yb﹣,得m+a=n﹣b
m n
B.X2﹣的还原性一定大于Y﹣
C.X、Y一定不是同周期元素 菠萝酯的合成路线如下:
D.若X的原子半径大于Y,则气态氢化物的稳定性H X一定大于H Y
m n
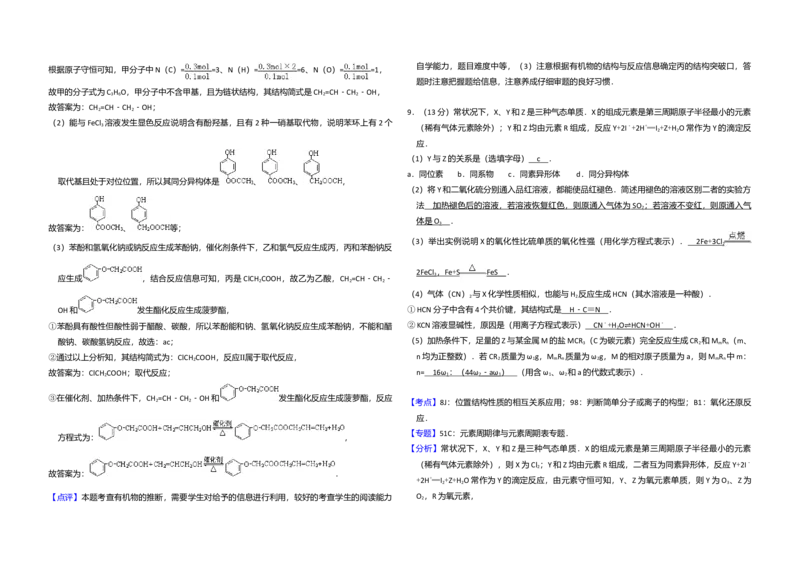
6.(6分)下列叙述正确的是( )a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①试剂X不可选用的是 (选填字母). ①步骤c后还缺少的一步主要操作是 。
a.CH COONa溶液 b.NaOH溶液 ②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是 。
3
c.NaHCO 溶液 d.Na CO 溶液 ③步骤c滴入稀硝酸后烧杯中的现象是 ,反应的离子方程式是 。
3 2 3
②丙的结构简式是 ,反应II的反应类型是 . (4)一定温度下,将1mol N O 置于密闭容器中,保持压强不变,升高温度至T 的过程中,气体
2 4 1
③反应Ⅳ的化学方程式是 . 由无色逐渐变为红棕色。温度由 T 继续升高到T 的过程中,气体逐渐变为无色。若保持 T ,增
1 2 2
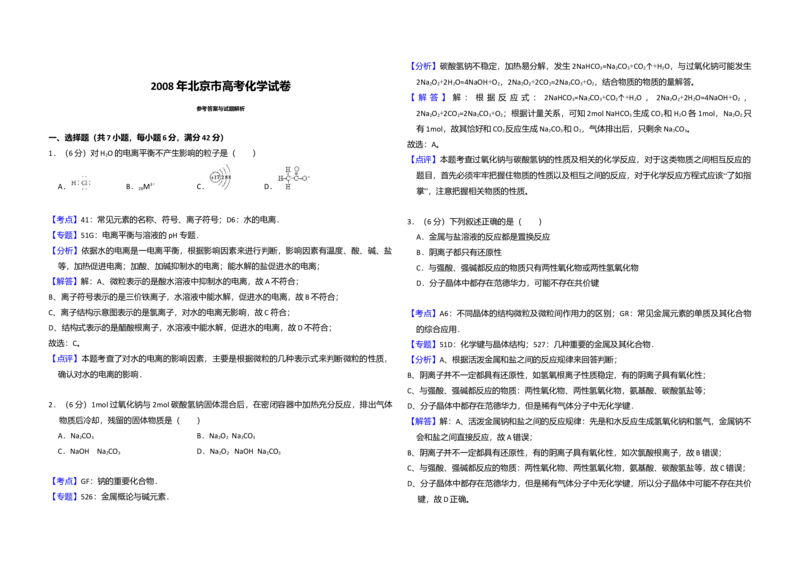
9.(13分)常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素 大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图2所示。
(稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I﹣+2H+═I +Z+H O常作为Y的滴定反 ①温度在T ﹣T 之间,反应的化学方程式是 。
2 2 1 2
应. ②温度在T ﹣T 之间,气体的平均相对分子质量是(保留1位小数) 。
2 3
(1)Y与Z的关系是(选填字母) .
a.同位素 b.同系物 c.同素异形体 d.同分异构体
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别二者的实验方
法 .
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示). .
(4)气体(CN) 与X化学性质相似,也能与H 反应生成HCN(其水溶液是一种酸).
2 2
①HCN分子中含有4个共价键,其结构式是 .
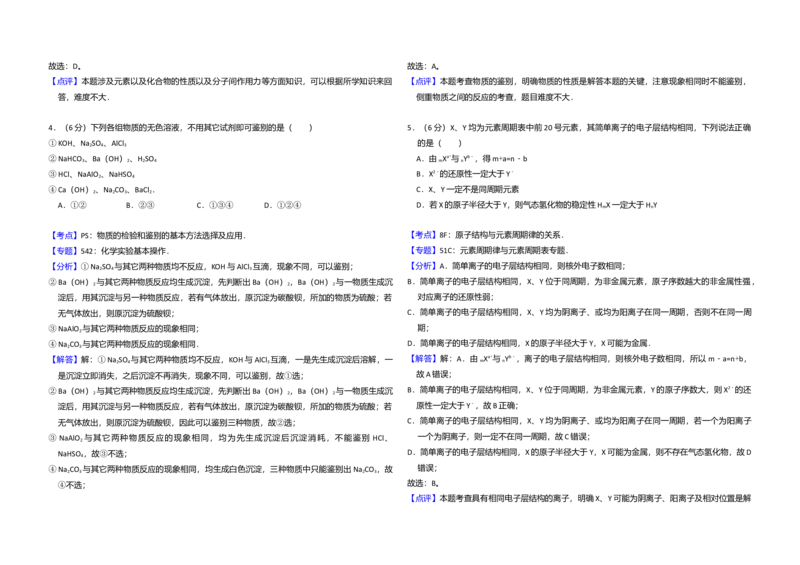
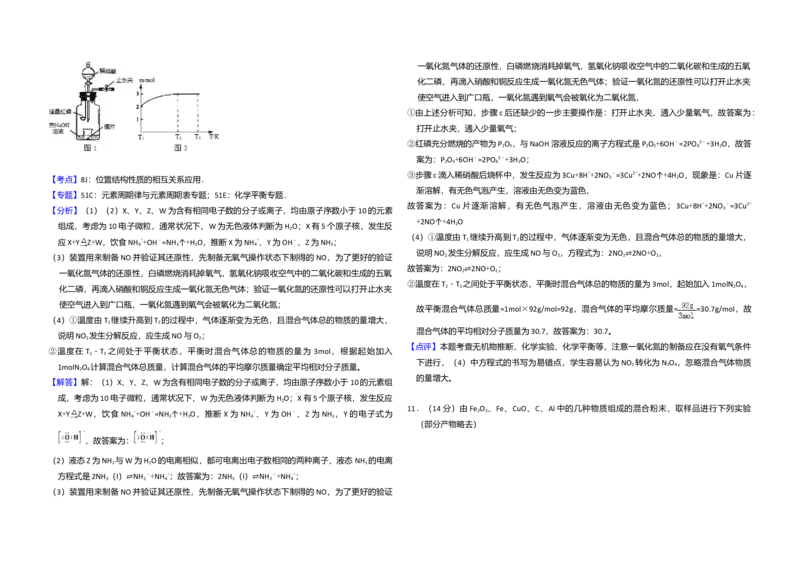
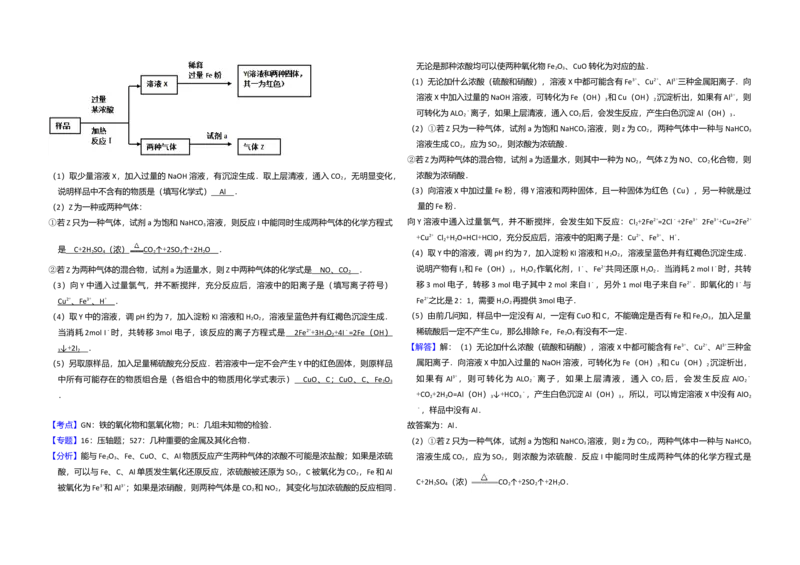
11.(14分)由 Fe O 、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验
2 3
②KCN溶液显碱性,原因是(用离子方程式表示) .
(部分产物略去)
(5)加热条件下,足量的 Z 与某金属 M 的盐 MCR (C 为碳元素)完全反应生成 CR 和 M R
3 2 m n
(m、n均为正整数).若CR 质量为ω g,M R 质量为ω g,M的相对原子质量为a,则M R
2 1 m n 2 m n
中m:n= (用含ω 、ω 和a的代数式表示).
1 2
10.(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,
X有5个原子核。通常状况下,W为无色液体。
已知:X+Y Z+W
(1)Y的电子式是 。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是 。
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入 CO ,无明显变化,
2
(3)用图1所示装置制备NO并验证其还原性。有下列主要操作:
说明样品中不含有的物质是(填写化学式) .(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO 溶液,则反应I中能同时生成两种气体的化学方程式
3
是 .
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是 .
(3)向Y中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)
.
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H O ,溶液呈蓝色并有红褐色沉淀生成.
2 2
当消耗2mol I﹣时,共转移3mol电子,该反应的离子方程式是 .
(5)另取原样品,加入足量稀硫酸充分反应.若溶液中一定不会产生Y中的红色固体,则原样品
中所有可能存在的物质组合是(各组合中的物质用化学式表示) .【分析】碳酸氢钠不稳定,加热易分解,发生 2NaHCO =Na CO +CO ↑+H O,与过氧化钠可能发生
3 2 3 2 2
2Na O +2H O=4NaOH+O ,2Na O +2CO =2Na CO +O ,结合物质的物质的量解答。
2008 年北京市高考化学试卷 2 2 2 2 2 2 2 2 3 2
【 解 答 】 解 : 根 据 反 应 式 : 2NaHCO =Na CO +CO ↑+H O , 2Na O +2H O=4NaOH+O ,
3 2 3 2 2 2 2 2 2
参考答案与试题解析
2Na O +2CO =2Na CO +O ;根据计量关系,可知2mol NaHCO 生成CO 和H O各1mol,Na O 只
2 2 2 2 3 2 3 2 2 2 2
有1mol,故其恰好和CO 反应生成Na CO 和O ,气体排出后,只剩余Na CO 。
2 2 3 2 2 3
一、选择题(共7小题,每小题6分,满分42分)
故选:A。
1.(6分)对H O的电离平衡不产生影响的粒子是( )
2
【点评】本题考查过氧化钠与碳酸氢钠的性质及相关的化学反应,对于这类物质之间相互反应的
题目,首先必须牢牢把握住物质的性质以及相互之间的反应,对于化学反应方程式应该“了如指
A. B. M3+ C. D.
26 掌”,注意把握相关物质的性质。
【考点】41:常见元素的名称、符号、离子符号;D6:水的电离. 3.(6分)下列叙述正确的是( )
菁优网版权所有
【专题】51G:电离平衡与溶液的pH专题. A.金属与盐溶液的反应都是置换反应
【分析】依据水的电离是一电离平衡,根据影响因素来进行判断,影响因素有温度、酸、碱、盐 B.阴离子都只有还原性
等,加热促进电离;加酸、加碱抑制水的电离;能水解的盐促进水的电离; C.与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物
【解答】解:A、微粒表示的是酸水溶液中抑制水的电离,故A不符合; D.分子晶体中都存在范德华力,可能不存在共价键
B、离子符号表示的是三价铁离子,水溶液中能水解,促进水的电离,故B不符合;
C、离子结构示意图表示的是氯离子,对水的电离无影响,故C符合; 【考点】A6:不同晶体的结构微粒及微粒间作用力的区别;GR:常见金属元素的单质及其化合物
D、结构式表示的是醋酸根离子,水溶液中能水解,促进水的电离,故D不符合; 的综合应用.
菁优网版权所有
故选:C。 【专题】51D:化学键与晶体结构;527:几种重要的金属及其化合物.
【点评】本题考查了对水的电离的影响因素,主要是根据微粒的几种表示式来判断微粒的性质, 【分析】A、根据活泼金属和盐之间的反应规律来回答判断;
确认对水的电离的影响. B、阴离子并不一定都具有还原性,如氢氧根离子性质稳定,有的阴离子具有氧化性;
C、与强酸、强碱都反应的物质:两性氧化物、两性氢氧化物,氨基酸、碳酸氢盐等;
2.(6分)1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体 D、分子晶体中都存在范德华力,但是稀有气体分子中无化学键.
物质后冷却,残留的固体物质是( ) 【解答】解:A、活泼金属钠和盐之间的反应规律:先是和水反应生成氢氧化钠和氢气,金属钠不
A.Na 2 CO 3 B.Na 2 O 2 Na 2 CO 3 会和盐之间直接反应,故A错误;
C.NaOH Na 2 CO 3 D.Na 2 O 2 NaOH Na 3 CO 3 B、阴离子并不一定都具有还原性,有的阴离子具有氧化性,如次氯酸根离子,故B错误;
C、与强酸、强碱都反应的物质:两性氧化物、两性氢氧化物,氨基酸、碳酸氢盐等,故C错误;
【考点】GF:钠的重要化合物.
D、分子晶体中都存在范德华力,但是稀有气体分子中无化学键,所以分子晶体中可能不存在共价
菁优网版权所有
【专题】526:金属概论与碱元素.
键,故D正确。故选:D。 故选:A。
【点评】本题涉及元素以及化合物的性质以及分子间作用力等方面知识,可以根据所学知识来回 【点评】本题考查物质的鉴别,明确物质的性质是解答本题的关键,注意现象相同时不能鉴别,
答,难度不大. 侧重物质之间的反应的考查,题目难度不大.
4.(6分)下列各组物质的无色溶液,不用其它试剂即可鉴别的是( ) 5.(6分)X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确
①KOH、Na SO 、AlCl 的是( )
2 4 3
②NaHCO 、Ba(OH) 、H SO A.由 Xa+与 Yb﹣,得m+a=n﹣b
3 2 2 4 m n
③HCl、NaAlO 、NaHSO B.X2﹣的还原性一定大于Y﹣
2 4
④Ca(OH) 、Na CO 、BaCl . C.X、Y一定不是同周期元素
2 2 3 2
A.①② B.②③ C.①③④ D.①②④ D.若X的原子半径大于Y,则气态氢化物的稳定性H X一定大于H Y
m n
【考点】PS:物质的检验和鉴别的基本方法选择及应用. 【考点】8F:原子结构与元素周期律的关系.
菁优网版权所有 菁优网版权所有
【专题】542:化学实验基本操作. 【专题】51C:元素周期律与元素周期表专题.
【分析】①Na SO 与其它两种物质均不反应,KOH与AlCl 互滴,现象不同,可以鉴别; 【分析】A.简单离子的电子层结构相同,则核外电子数相同;
2 4 3
②Ba(OH) 与其它两种物质反应均生成沉淀,先判断出Ba(OH) ,Ba(OH) 与一物质生成沉 B.简单离子的电子层结构相同,X、Y位于同周期,为非金属元素,原子序数越大的非金属性强,
2 2 2
淀后,用其沉淀与另一种物质反应,若有气体放出,原沉淀为碳酸钡,所加的物质为硫酸;若 对应离子的还原性弱;
无气体放出,则原沉淀为硫酸钡; C.简单离子的电子层结构相同,X、Y均为阴离子、或均为阳离子在同一周期,否则不在同一周
③NaAlO 与其它两种物质反应的现象相同; 期;
2
④Na CO 与其它两种物质反应的现象相同. D.简单离子的电子层结构相同,X的原子半径大于Y,X可能为金属.
2 3
【解答】解:①Na SO 与其它两种物质均不反应,KOH与AlCl 互滴,一是先生成沉淀后溶解,一 【解答】解:A.由 Xa+与 Yb﹣,离子的电子层结构相同,则核外电子数相同,所以m﹣a=n+b,
2 4 3 m n
是沉淀立即消失,之后沉淀不再消失,现象不同,可以鉴别,故①选; 故A错误;
②Ba(OH) 与其它两种物质反应均生成沉淀,先判断出Ba(OH) ,Ba(OH) 与一物质生成沉 B.简单离子的电子层结构相同,X、Y位于同周期,为非金属元素,Y的原子序数大,则X2﹣的还
2 2 2
淀后,用其沉淀与另一种物质反应,若有气体放出,原沉淀为碳酸钡,所加的物质为硫酸;若 原性一定大于Y﹣,故B正确;
无气体放出,则原沉淀为硫酸钡,因此可以鉴别三种物质,故②选; C.简单离子的电子层结构相同,X、Y均为阴离子、或均为阳离子在同一周期,若一个为阳离子
③ NaAlO 与其它两种物质反应的现象相同,均为先生成沉淀后沉淀消耗,不能鉴别 HCl、 一个为阴离子,则一定不在同一周期,故C错误;
2
NaHSO ,故③不选; D.简单离子的电子层结构相同,X的原子半径大于Y,X可能为金属,则不存在气态氢化物,故D
4
④Na CO 与其它两种物质反应的现象相同,均生成白色沉淀,三种物质中只能鉴别出Na CO ,故 错误;
2 3 2 3
④不选; 故选:B。
【点评】本题考查具有相同电子层结构的离子,明确X、Y可能为阴离子、阳离子及相对位置是解答本题的关键,题目难度不大.
则溶液中 减小,故D错误;
6.(6分)下列叙述正确的是( )
故选:C。
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO 2﹣)>c(NH +)
4 4
【点评】本题考查酸碱混合后溶液中的离子的关系及弱电解质的电离,明确酸、碱的强弱是解答
B.两种醋酸溶液的物质的量浓度分别为c 和c ,pH分别为a和a+1,则c =10c
1 2 1 2
本题的关键,注意弱电解质的特点。
C.pH=11的NaOH溶液与pH=3醋酸溶液等体积混合,滴入石蕊试液呈红色
D.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中 增大 7.(6分)工业上制备纯硅反应的热化学方程式如下:SiCl (g)+2H (g) Si(s)+4HCl(g)
4 2
△H=+QkJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行
⇌
上述反应,下列叙
述正确的是( )
【考点】DO:酸碱混合时的定性判断及有关ph的计算. A.反应过程中,若增大压强能提高SiCl 的转化率
菁优网版权所有 4
【分析】A、根据溶液呈电中性,即溶液中阴阳离子所带电量相等判断硫酸根离子和铵根离子的关 B.若反应开始时SiCl 为1 mol,则达平衡时,吸收热量为Q kJ
4
系; C.反应至4 min时,若HCl浓度为0.12 mol/L,则H 的反应速率为0.03 mol/(L•min)
2
B、醋酸的浓度与醋酸溶液中的氢离子浓度不等; D.反应吸收0.025Q kJ热量时,生成的HCl通入100 mL 1 mol/L的NaOH溶液中恰好完全反应
C、醋酸是弱电解质,醋酸的浓度远远大于氢离子浓度,根据酸碱混合后溶液的酸碱性判断石蕊试
液的颜色; 【考点】BB:反应热和焓变;CB:化学平衡的影响因素.
菁优网版权所有
D、根据硫酸铵对氨水电离平衡的影响分析判断。 【专题】51E:化学平衡专题.
【解答】解:A、将稀氨水逐滴加入稀硫酸中,当溶液 pH=7时,溶液中氢离子浓度等于氢氧根离 【分析】A.增大平衡向气体体积减小的方向移动,据此判断;
子浓度;溶液呈电中性,所以阴阳离子所带电量相等,所以2c(SO 2﹣)=c(NH +),故A错误; B.该反应为可逆反应,1molSiCl 不能完全转化,结合热化学方程式判断;
4 4 4
B、醋酸是弱电解质,在水溶液中只有部分电离,所以醋酸的浓度大于氢离子浓度;两种醋酸溶液
C.根据v= 计算v(HCl),利用速率之比等于化学计量数之比计算判断;
的物质的量浓度分别为c 和c ,pH分别为a和a+1的两种醋酸溶液中氢离子浓度之比=10:1,
1 2
D.根据反应吸收的热量计算生成的HCl的物质的量,据此判断.
当两种酸的电离度相同时,则c =10c ,实际上,两种酸的浓度不等,且浓度越大,酸的电离度
1 2
【解答】解:A.从方程式可以看出,反应物气体的计量数之和小于生成物气体的计量数之和,则
越小,所以两种酸的浓度关系为c >10c ,故B错误;
1 2
增大压强,平衡向逆反应方向移动,SiCl 的转化率减小,故A错误;
C、pH=11 的 NaOH 溶液的 C(NaOH)=10﹣3 mol/L,pH=3 醋酸溶液的 c(CH COOH)>10﹣3 4
3
B.该反应为可逆反应,1molSiCl 不能完全转化,达平衡时,吸收热量小于QkJ,故B错误;
4
mol/L,等体积的两种溶液 n(CH COOH)>n(NaOH),醋酸有剩余,但 CH COOH 大于
3 3
C.反应至4min时,若HCl浓度为0.12mol/L,则v(HCl)= =0.03mol/(L•min),根据
CH COO﹣水解程度,则等体积混合后溶液呈酸性,所以向混合液中滴入石蕊试液呈红色,故 C
3
正确;
D、氨水的电离方程式为:NH .H O NH ++OH﹣,当向氨水中加入硫酸铵时,硫酸铵中含有铵根 反应速率之比等于化学计量数之比,则 v(H 2 )= ×v(HCl)= ×0.03mol/(L•min)
3 2 4
离子,导致氨水的电离平衡向逆反应方向移动,溶液中氢氧根离子浓度降低,氨水的浓度增大,
⇌
=0.015mol/(L•min),故C错误;②丙的结构简式是 ClCH COOH ,反应II的反应类型是 取代反应 .
D.由方程式可知,当反应吸收热量为 0.025QkJ时,生成HCl的物质的量为: =0.1mol, 2
100mL1mol/L的NaOH的物质的量为0.1L×1mol/L=0.1mol,二者物质的量相等,恰好反应,故 ③反应Ⅳ的化学方程式是
D正确;
.
故选:D。
【点评】本题考查较为综合,涉及反应热的计算、化学反应速率、化学平衡等问题,题目难度中
【考点】HB:有机物的推断.
等,注意反应的可逆性. 菁优网版权所有
【专题】534:有机物的化学性质及推断.
【分析】(1)由题意可知,甲中含有羟基,甲蒸气对氢气的相对密度是 29,相同条件下的气体
二、解答题(共4小题,满分60分)
密度之比等于其相对分子质量之比,所以甲的相对分子质量为 58,根据n= 计算5.8g甲的物质
8.(16分)菠萝酯 是一种具有菠萝香气的食用香料,是化合物甲与苯
氧乙酸发生化学反应的产物. 的量,根据质量守恒计算参加反应的氧气的质量,根据原子守恒计算甲分子中 C、H原子数目,
(1)5.8g甲完全燃烧可产生0.3mol CO 和0.3mol H O,甲蒸气对氢气的相对密度是29,甲分子中 判断甲是否含有氧元素,比较计算甲分子中氧原子数目,据此确定甲的分子式,结合甲的结构
2 2
不含甲基,且为链状结构,其结构简式是 CH =CH﹣CH ﹣OH . 特点确定其结构简式;
2 2
(2)苯氧乙酸有多种酯类的同分异构体,其中能与 FeCl 溶液发生显色反应,且有2种一硝基取 (2)能与FeCl 溶液发生显色反应说明含有酚羟基,且有 2种一硝基取代物,苯环上有 2个不同
3 3
取代基且处于对位位置符合,据此写出其结构简式;
(3)苯酚和氢氧化钠或钠反应生成苯酚钠,催化剂条件下,乙和氯气反应生成丙,丙和苯酚钠反
代物的同分异构体是(写出任意2种的结构简式) , .
应生成 ,结合反应信息可知,丙是 ClCH COOH,故乙为乙酸,CH =CH﹣CH ﹣
2 2 2
(3)已知:
OH和 发生酯化反应生成菠萝酯.
【解答】解:(1)由题意可知,甲中含有羟基,甲蒸气对氢气的相对密度是 29,相同条件下的
气体密度之比等于其相对分子质量之比,所以甲的相对分子质量为 58,5.8g甲的物质的量=
菠萝酯的合成路线如下:
=0.1mol,
质量守恒可知,参加反应的氧气的质量=0.3mol×44g/mol+0.3mol×18g/mol﹣5.8g=12.8g,氧气物
质的量= =0.4mol,
①试剂X不可选用的是 ac (选填字母).
a.CH COONa溶液 b.NaOH溶液 c.NaHCO 溶液 d.Na CO 溶液 根据氧原子守恒,可知5.8g甲中n(O)=0.3mol×2+0.3mol﹣0.4mol×2=0.1mol,
3 3 2 3自学能力,题目难度中等,(3)注意根据有机物的结构与反应信息确定丙的结构突破口,答
根据原子守恒可知,甲分子中N(C)= =3、N(H)= =6、N(O)= =1,
题时注意把握题给信息,注意养成仔细审题的良好习惯.
故甲的分子式为C H O,甲分子中不含甲基,且为链状结构,其结构简式是CH =CH﹣CH ﹣OH,
3 6 2 2
故答案为:CH =CH﹣CH ﹣OH;
2 2 9.(13分)常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素
(2)能与FeCl 溶液发生显色反应说明含有酚羟基,且有 2种一硝基取代物,说明苯环上有 2个
3 (稀有气体元素除外);Y和Z均由元素R组成,反应Y+2I﹣+2H+═I +Z+H O常作为Y的滴定反
2 2
应.
(1)Y与Z的关系是(选填字母) c .
a.同位素 b.同系物 c.同素异形体 d.同分异构体
取代基且处于对位位置,所以其同分异构体是 、 、 ,
(2)将Y和二氧化硫分别通入品红溶液,都能使品红褪色.简述用褪色的溶液区别二者的实验方
法 加热褪色后的溶液,若溶液恢复红色,则原通入气体为 SO ;若溶液不变红,则原通入气
2
体是 O .
3
故答案为: 、 等;
(3)举出实例说明X的氧化性比硫单质的氧化性强(用化学方程式表示). 2Fe + 3C l
2
(3)苯酚和氢氧化钠或钠反应生成苯酚钠,催化剂条件下,乙和氯气反应生成丙,丙和苯酚钠反
2FeCl , Fe + S FeS .
3
应生成 ,结合反应信息可知,丙是 ClCH COOH,故乙为乙酸,CH =CH﹣CH ﹣
2 2 2
(4)气体(CN) 与X化学性质相似,也能与H 反应生成HCN(其水溶液是一种酸).
2 2
OH和 发生酯化反应生成菠萝酯, ①HCN分子中含有4个共价键,其结构式是 H﹣C ≡ N .
①苯酚具有酸性但酸性弱于醋酸、碳酸,所以苯酚能和钠、氢氧化钠反应生成苯酚钠,不能和醋 ②KCN溶液显碱性,原因是(用离子方程式表示) CN ﹣ + H O HCN + OH ﹣ .
2
酸钠、碳酸氢钠反应,故选:ac; (5)加热条件下,足量的Z与某金属M的盐MCR 3 (C为碳元素 ⇌ )完全反应生成CR 2 和M m R n (m、
②通过以上分析知,其结构简式为:ClCH COOH,反应Ⅱ属于取代反应, n均为正整数).若CR 质量为ω g,M R 质量为ω g,M的相对原子质量为a,则M R 中m:
2 2 1 m n 2 m n
故答案为:ClCH COOH;取代反应; n= 16ω :( 44ω ﹣aω ) (用含ω 、ω 和a的代数式表示).
2 1 2 1 1 2
③在催化剂、加热条件下,CH =CH﹣CH ﹣OH和 发生酯化反应生成菠萝酯,反应
2 2 【考点】8J:位置结构性质的相互关系应用;98:判断简单分子或离子的构型;B1:氧化还原反
应.
菁优网版权所有
【专题】51C:元素周期律与元素周期表专题.
方程式为: ,
【分析】常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元素
(稀有气体元素除外),则 X为Cl ;Y和Z均由元素R组成,二者互为同素异形体,反应 Y+2I﹣
2
故答案为: .
+2H+═I +Z+H O常作为Y的滴定反应,由元素守恒可知,Y、Z为氧元素单质,则Y为O 、Z为
2 2 3
【点评】本题考查有机物的推断,需要学生对给予的信息进行利用,较好的考查学生的阅读能力 O 2 ,R为氧元素,(1)O 、O 都由氧元素形成的结构不同的单质,互为同位素;
3 2 物质的量之比为 1:1,则 =m× ,整理得 m:n=16ω :(44ω ﹣
1 2
(2)二氧化硫使品红溶液褪色,生成不稳定的无色物质,受热容易分解又恢复红色,臭氧具有强
氧化性,将品红氧化使其褪色,不能恢复红色.
aω ),
1
(3)可以利用与变价金属反应或氯气置换硫单质说明氯气的氧化性更强;
故答案为:16ω :(44ω ﹣aω ).
1 2 1
(4)气体(CN) 与Cl 化学性质相似,能与H 反应生成HCN(其水溶液是一种酸,则HCN中为
2 2 2
【点评】本题考查物质推断、漂白原理、盐类水解、氧化性比较、信息迁移及化学计算等,(5)
H﹣CN形式,HCN含有4个共价键,则C与N原子之间形成三键;CN﹣水解使KCN溶液显碱性;
注意利用原子守恒进行计算,难度中等.
(5)由盐MCO (C为碳元素)化学式,根据原子数守恒可知,CO 中C原子与M R 中M原子的
3 2 m n
物质的量之比为1:1,据此解答.
10.(17分)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,
【解答】解:常状况下,X、Y和Z是三种气态单质.X的组成元素是第三周期原子半径最小的元
X有5个原子核。通常状况下,W为无色液体。
素(稀有气体元素除外),则 X为Cl ;Y和Z均由元素R组成,二者互为同素异形体,反应
2 已知:X+Y Z+W
Y+2I﹣+2H+═I +Z+H O常作为Y的滴定反应,由元素守恒可知,Y、Z为氧元素单质,则Y为O 、
2 2 3
(1)Y的电子式是 。
Z为O ,R为氧元素,
2
(1)Y为O 、Z为O ,由氧元素形成的结构不同的单质,二者核外同素异形体,故选:c; (2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是 2NH
3 2 3
(2)加热褪色后的溶液,若溶液恢复红色,则原通入气体为 SO ;若溶液不变红,则原通入气体 ( l ) NH ﹣ + NH + 。
2 2 4
是O
3
, (3)用
⇌
图1所示装置制备NO并验证其还原性。有下列主要操作:
故答案为:加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO ;若溶液不变红,则原通 a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
2
入气体是O ; b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
3
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
(3)利用与变价金属反应说明氯气的氧化性更强,反应方程式为:2Fe+3Cl 2FeCl ,Fe+S
2 3
①步骤c后还缺少的一步主要操作是 打开止水夹,通入少量氧气 。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是 P O + 6OH ﹣ =2PO 3﹣ + 3H O 。
FeS, 2 5 4 2
③步骤c滴入稀硝酸后烧杯中的现象是 Cu 片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色
故答案为:2Fe+3Cl 2FeCl ,Fe+S FeS ,反应的离子方程式是 3Cu + 8H + + 2NO ﹣ =3Cu 2 + + 2NO↑ + 4H O 。
2 3 3 2
(4)一定温度下,将1mol N O 置于密闭容器中,保持压强不变,升高温度至T 的过程中,气体
2 4 1
(4)①气体(CN) 与Cl 化学性质相似,能与H 反应生成HCN(其水溶液是一种酸,则HCN中
2 2 2
由无色逐渐变为红棕色。温度由 T 继续升高到T 的过程中,气体逐渐变为无色。若保持 T ,增
1 2 2
为H﹣CN形式,HCN含有4个共价键,则 C与N原子之间形成三键,故 HCN的结构式为 H﹣
大压强,气体逐渐变为红棕色。气体的物质的量n随温度T变化的关系如图2所示。
C≡N,故答案为:H﹣C≡N;
①温度在T ﹣T 之间,反应的化学方程式是 2NO 2NO+O 。
1 2 2 2
② CN﹣水解 CN﹣+H O HCN+OH﹣,破坏水的电离平衡,使 KCN 溶液显碱性,故答案为:CN﹣
2
②温度在T ﹣T 之间,气体的平均相对分子质量是(保留1位小数) 30.7 。
2 3 ⇌
+H 2 O HCN+OH﹣; ⇌
(5)由盐MCO (C为碳元素)化学式,根据原子数守恒可知,CO 中C原子与M O 中M原子的
⇌ 3 2 m n一氧化氮气体的还原性,白磷燃烧消耗掉氧气,氢氧化钠吸收空气中的二氧化碳和生成的五氧
化二磷,再滴入硝酸和铜反应生成一氧化氮无色气体;验证一氧化氮的还原性可以打开止水夹
使空气进入到广口瓶,一氧化氮遇到氧气会被氧化为二氧化氮,
①由上述分析可知,步骤c后还缺少的一步主要操作是:打开止水夹,通入少量氧气,故答案为:
打开止水夹,通入少量氧气;
②红磷充分燃烧的产物为P O ,与NaOH溶液反应的离子方程式是P O +6OH﹣=2PO 3﹣+3H O,故答
2 5 2 5 4 2
案为:P O +6OH﹣=2PO 3﹣+3H O;
2 5 4 2
③步骤c滴入稀硝酸后烧杯中,发生反应为3Cu+8H++2NO ﹣=3Cu2++2NO↑+4H O,现象是:Cu片逐
【考点】8J:位置结构性质的相互关系应用. 3 2
菁优网版权所有
渐溶解,有无色气泡产生,溶液由无色变为蓝色,
【专题】51C:元素周期律与元素周期表专题;51E:化学平衡专题.
故答案为:Cu 片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色;3Cu+8H++2NO ﹣=3Cu2+
【分析】(1)(2)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于 10的元素 3
+2NO↑+4H O
组成,考虑为10电子微粒,通常状况下,W为无色液体判断为H O;X有5个原子核,发生反 2
2
(4)①温度由T 继续升高到T 的过程中,气体逐渐变为无色,且混合气体总的物质的量增大,
应X+Y Z+W,饮食NH ++OH﹣=NH ↑+H O,推断X为NH +、Y为OH﹣、Z为NH ; 1 2
4 3 2 4 3
说明NO 发生分解反应,应生成NO与O ,方程式为:2NO 2NO+O ,
(3)装置用来制备NO并验证其还原性,先制备无氧气操作状态下制得的 NO,为了更好的验证 2 2 2 2
故答案为:2NO 2NO+O ;
一氧化氮气体的还原性,白磷燃烧消耗掉氧气,氢氧化钠吸收空气中的二氧化碳和生成的五氧 2 2 ⇌
②温度在T ﹣T 之间处于平衡状态,平衡时混合气体总的物质的量为3mol,起始加入1molN O ,
化二磷,再滴入硝酸和铜反应生成一氧化氮无色气体;验证一氧化氮的还原性可以打开止水夹 2 3 ⇌ 2 4
使空气进入到广口瓶,一氧化氮遇到氧气会被氧化为二氧化氮;
故平衡混合气体总质量=1mol×92g/mol=92g,混合气体的平均摩尔质量= =30.7g/mol,故
(4)①温度由T 继续升高到T 的过程中,气体逐渐变为无色,且混合气体总的物质的量增大,
1 2
混合气体的平均相对分子质量为30.7,故答案为:30.7。
说明NO 发生分解反应,应生成NO与O ;
2 2
【点评】本题考查无机物推断、化学实验、化学平衡等,注意一氧化氮的制备应在没有氧气条件
②温度在 T ﹣T 之间处于平衡状态,平衡时混合气体总的物质的量为 3mol,根据起始加入
2 3
下进行,(4)中方程式的书写为易错点,学生容易认为NO 转化为N O ,忽略混合气体物质
1molN O 计算混合气体总质量,计算混合气体的平均摩尔质量确定平均相对分子质量。 2 2 4
2 4
的量增大。
【解答】解:(1)X、Y、Z、W为含有相同电子数的分子或离子,均由原子序数小于 10的元素组
成,考虑为10电子微粒,通常状况下,W为无色液体判断为H O;X有5个原子核,发生反应
2
11.(14分)由 Fe O 、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验
X+Y Z+W,饮食 NH ++OH﹣=NH ↑+H O,推断 X 为 NH +、Y 为 OH﹣、Z 为 NH ,Y 的电子式为 2 3
4 3 2 4 3
(部分产物略去)
,故答案为: ;
(2)液态Z为NH 与W为H O的电离相似,都可电离出电子数相同的两种离子,液态 NH 的电离
3 2 3
方程式是2NH (l) NH ﹣+NH +;故答案为:2NH (l) NH ﹣+NH +;
3 2 4 3 2 4
(3)装置用来制备NO并验证其还原性,先制备无氧气操作状态下制得的 NO,为了更好的验证
⇌ ⇌无论是那种浓酸均可以使两种氧化物Fe O 、CuO转化为对应的盐.
2 3
(1)无论加什么浓酸(硫酸和硝酸),溶液 X中都可能含有Fe3+、Cu2+、Al3+三种金属阳离子.向
溶液X中加入过量的NaOH溶液,可转化为Fe(OH) 和Cu(OH) 沉淀析出,如果有Al3+,则
3 2
可转化为ALO ﹣离子,如果上层清液,通入CO 后,会发生反应,产生白色沉淀Al(OH) .
2 2 3
(2)①若Z只为一种气体,试剂a为饱和NaHCO 溶液,则z为CO ,两种气体中一种与NaHCO
3 2 3
溶液生成CO ,应为SO ,则浓酸为浓硫酸.
2 2
②若Z为两种气体的混合物,试剂a为适量水,则其中一种为NO ,气体Z为NO、CO 化合物,则
2 2
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入 CO ,无明显变化, 浓酸为浓硝酸.
2
说明样品中不含有的物质是(填写化学式) A l . (3)向溶液X中加过量Fe粉,得Y溶液和两种固体,且一种固体为红色(Cu),另一种就是过
(2)Z为一种或两种气体: 量的Fe粉.
①若Z只为一种气体,试剂a为饱和NaHCO 溶液,则反应I中能同时生成两种气体的化学方程式 向 Y 溶液中通入过量氯气,并不断搅拌,会发生如下反应:Cl +2Fe2+=2Cl﹣+2Fe3+ 2Fe3++Cu=2Fe2+
3 2
+Cu2+ Cl +H O=HCl+HClO,充分反应后,溶液中的阳离子是:Cu2+、Fe3+、H+.
2 2
是 C + 2H SO (浓) CO ↑ + 2SO ↑ + 2H O .
2 4 2 2 2 (4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H O ,溶液呈蓝色并有红褐色沉淀生成.
2 2
②若Z为两种气体的混合物,试剂a为适量水,则Z中两种气体的化学式是 NO 、 CO . 说明产物有I 和Fe(OH) ,H O 作氧化剂,I﹣、Fe2+共同还原H O .当消耗2 mol I﹣时,共转
2 2 3 2 2 2 2
(3)向 Y 中通入过量氯气,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号) 移3 mol 电子,转移 3 mol 电子其中 2 mol 来自 I﹣,另外 1 mol 电子来自 Fe2+.即氧化的 I﹣与
Cu 2 + 、 Fe 3 + 、 H + . Fe2+之比是2:1,需要H O 再提供3mol电子.
2 2
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H O ,溶液呈蓝色并有红褐色沉淀生成. (5)由前几问知,样品中一定没有Al,一定有CuO和C,不能确定是否有Fe和Fe O ,加入足量
2 2 2 3
当消耗 2mol I﹣时,共转移 3mol 电子,该反应的离子方程式是 2Fe 2 + + 3H O + 4 I ﹣ =2Fe ( OH ) 稀硫酸后一定不产生Cu,那么排除Fe,Fe O 有没有不一定.
2 2 2 3
↓ + 2I . 【解答】解:(1)无论加什么浓酸(硫酸和硝酸),溶液 X中都可能含有Fe3+、Cu2+、Al3+三种金
3 2
(5)另取原样品,加入足量稀硫酸充分反应.若溶液中一定不会产生Y中的红色固体,则原样品 属阳离子.向溶液X中加入过量的NaOH溶液,可转化为Fe(OH) 和Cu(OH) 沉淀析出,
3 2
中所有可能存在的物质组合是(各组合中的物质用化学式表示) CuO 、 C ; CuO 、 C 、 Fe O 如果有 Al3+,则可转化为 ALO ﹣离子,如果上层清液,通入 CO 后,会发生反应 AlO ﹣
2 3 2 2 2
. +CO +2H O=Al(OH) ↓+HCO ﹣,产生白色沉淀Al(OH) ,所以,可以肯定溶液 X中没有AlO
2 2 3 3 3 2
﹣,样品中没有Al.
【考点】GN:铁的氧化物和氢氧化物;PL:几组未知物的检验. 故答案为:Al.
菁优网版权所有
【专题】16:压轴题;527:几种重要的金属及其化合物. (2)①若Z只为一种气体,试剂a为饱和NaHCO 溶液,则z为CO ,两种气体中一种与NaHCO
3 2 3
【分析】能与Fe O 、Fe、CuO、C、Al物质反应产生两种气体的浓酸不可能是浓盐酸;如果是浓硫 溶液生成 CO ,应为 SO ,则浓酸为浓硫酸.反应 I 中能同时生成两种气体的化学方程式是
2 3 2 2
酸,可以与Fe、C、Al单质发生氧化还原反应,浓硫酸被还原为 SO ,C被氧化为CO ,Fe和Al
2 2
C+2H SO (浓) CO ↑+2SO ↑+2H O.
被氧化为Fe3+和Al3+;如果是浓硝酸,则两种气体是 CO 和NO ,其变化与加浓硫酸的反应相同. 2 4 2 2 2
2 2故答案为:C+2H SO (浓) CO ↑+2SO ↑+2H O.
2 4 2 2 2
②若Z为两种气体的混合物,试剂a为适量水,则其中一种为NO ,气体Z为NO、CO 化合物,则
2 2
浓酸为浓硝酸.
故答案为:NO、CO
2
(3)向溶液X中加过量Fe粉,得Y溶液和两种固体,且一种固体为红色(Cu),另一种就是过
量的Fe粉,这个过程发生了置换反应:Cu2++Fe=Cu+Fe2+,向Y溶液中通入过量氯气,并不断搅
拌,会发生如下反应:Cl +2Fe2+=2Cl﹣+2Fe3+,2Fe3++Cu=2Fe2++Cu2+,Cl +H O=HCl+HClO,充分反应
2 2 2
后,溶液中的阳离子是:Cu2+、Fe3+、H+(特别注意没有了Fe2+).
故答案为:Cu2+、Fe3+、H+.
(4)取Y中的溶液,调pH约为7,加入淀粉KI溶液和H O ,溶液呈蓝色并有红褐色沉淀生成.I
2 2
﹣、Fe2+共同还原H O .当消耗2 mol I﹣时,共转移3 mol电子,转移3 mol电子其中2 mol 来自I
2 2
﹣,另外1 mol电子来自Fe2+.即氧化的I﹣与Fe2+之比是2:1,需要H O 再提供3mol电子.这
2 2
反应方程式:2Fe2++3H O +4I﹣=2Fe(OH) ↓+2I .
2 2 3 2
故答案为:2Fe2++3H O +4I﹣=2Fe(OH) ↓+2I .
2 2 3 2
(5)根据前面分析可知,样品中一定没有Al,一定有CuO和C,不能确定是否有Fe和Fe O ,加
2 3
入足量稀硫酸后一定不产生 Cu,那么排除 Fe,符合整个设问的组合只有两种为:CuO、C;
CuO、C、Fe O .
2 3
故答案为:CuO、C;CuO、C、Fe O .
2 3
【点评】无机推断题为主体的综合题,主要考查金属单质、金属氧化物、非金属单质的性质.本
题综合性强,涉及知识面广,难度较大.