文档内容
2011 年普通高等学校招生全国统一考试(安徽卷)(化学)
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分第Ⅰ卷第 1页至第5页,第
Ⅱ卷第6页至第12页。全卷满分300分
第Ⅰ卷(选择题 共 120 分)
本试卷共20小题,每小题6分,共120分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
以下数据可供解题时参考:
相对原子质量(原子量):C 12 N 14 O 16 Mn 55
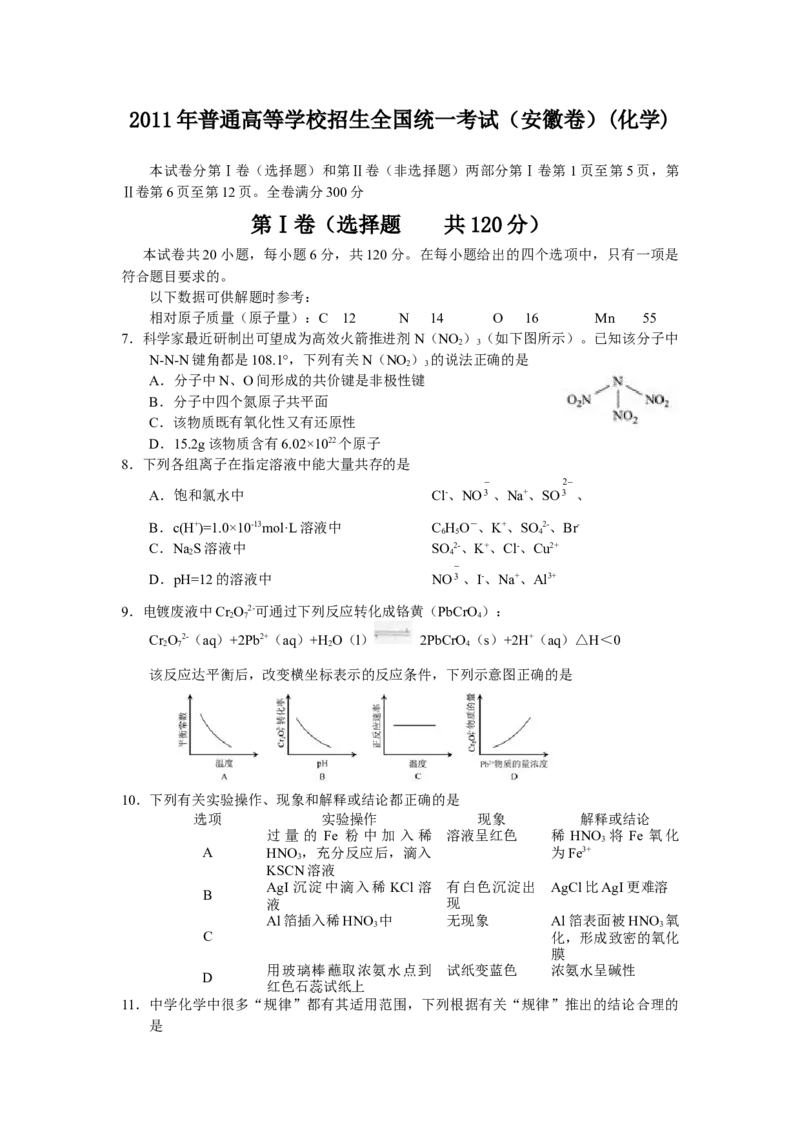
7.科学家最近研制出可望成为高效火箭推进剂N(NO )(如下图所示)。已知该分子中
2 3
N-N-N键角都是108.1°,下列有关N(NO ) 的说法正确的是
2 3
A.分子中N、O间形成的共价键是非极性键
B.分子中四个氮原子共平面
C.该物质既有氧化性又有还原性
D.15.2g该物质含有6.02×1022个原子
8.下列各组离子在指定溶液中能大量共存的是
2
A.饱和氯水中 Cl-、NO3、Na+、SO3 、
B.c(H+)=1.0×10-13mol·L溶液中 C HO-、K+、SO 2-、Br-
6 5 4
C.NaS溶液中 SO 2-、K+、Cl-、Cu2+
2 4
D.pH=12的溶液中 NO3、I-、Na+、Al3+
9.电镀废液中Cr O2-可通过下列反应转化成铬黄(PbCrO ):
2 7 4
Cr O2-(aq)+2Pb2+(aq)+H O(l) 2PbCrO (s)+2H+(aq)△H<0
2 7 2 4
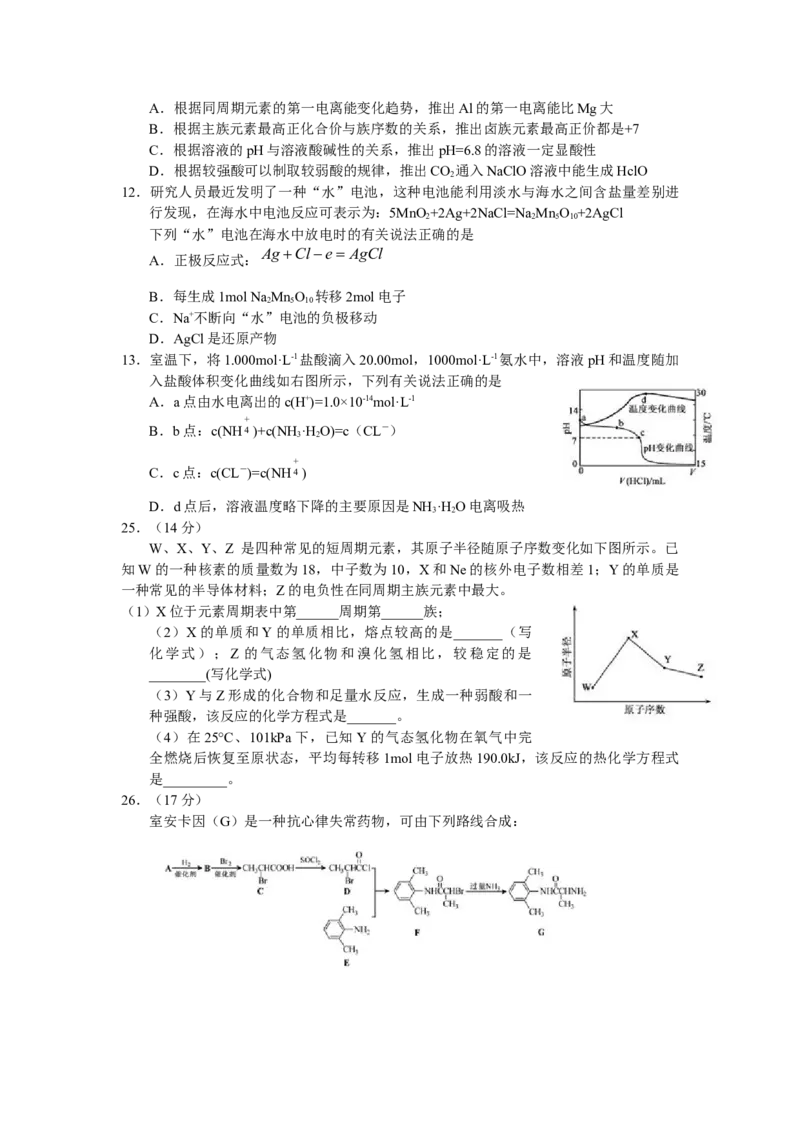
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是
10.下列有关实验操作、现象和解释或结论都正确的是
选项 实验操作 现象 解释或结论
过 量 的 Fe 粉 中 加 入 稀 溶液呈红色 稀 HNO 将 Fe 氧化
3
A HNO ,充分反应后,滴入 为Fe3+
3
KSCN溶液
AgI 沉淀中滴入稀 KCl 溶 有白色沉淀出 AgCl比AgI更难溶
B
液 现
Al箔插入稀HNO 中 无现象 Al箔表面被HNO 氧
3 3
C 化,形成致密的氧化
膜
用玻璃棒蘸取浓氨水点到 试纸变蓝色 浓氨水呈碱性
D
红色石蕊试纸上
11.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的
是A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.根据溶液的pH与溶液酸碱性的关系,推出pH=6.8的溶液一定显酸性
D.根据较强酸可以制取较弱酸的规律,推出CO 通入NaClO溶液中能生成HclO
2
12.研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进
行发现,在海水中电池反应可表示为:5MnO +2Ag+2NaCl=Na MnO +2AgCl
2 2 5 10
下列“水”电池在海水中放电时的有关说法正确的是
AgCle AgCl
A.正极反应式:
B.每生成1mol Na MnO 转移2mol电子
2 5 10
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
13.室温下,将1.000mol·L-1盐酸滴入20.00mol,1000mol·L-1氨水中,溶液pH和温度随加
入盐酸体积变化曲线如右图所示,下列有关说法正确的是
A.a点由水电离出的c(H+)=1.0×10-14mol·L-1
B.b点:c(NH4)+c(NH·H O)=c(CL-)
3 2
C.c点:c(CL-)=c(NH4)
D.d点后,溶液温度略下降的主要原因是NH ·H O电离吸热
3 2
25.(14分)
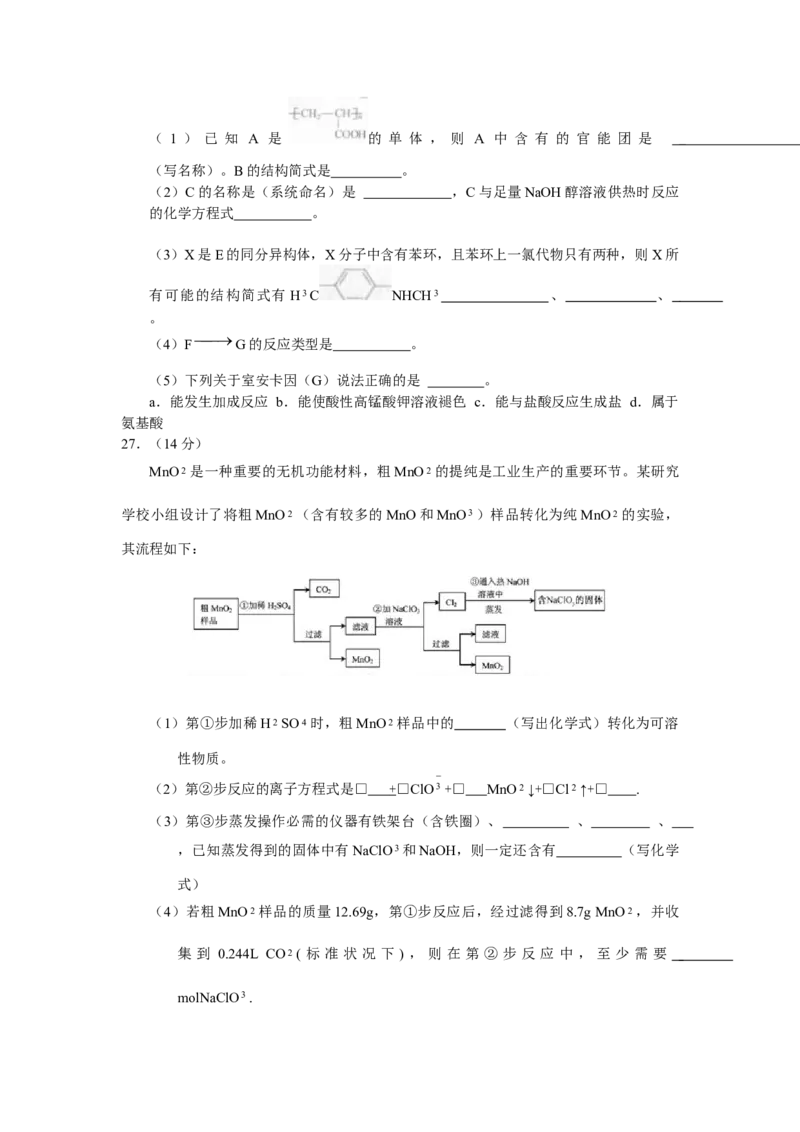
W、X、Y、Z 是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已
知W的一种核素的质量数为18,中子数为10,X和Ne的核外电子数相差1;Y的单质是
一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
(1)X位于元素周期表中第______周期第______族;
(2)X的单质和Y的单质相比,熔点较高的是_______(写
化学式);Z 的气态氢化物和溴化氢相比,较稳定的是
________(写化学式)
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一
种强酸,该反应的化学方程式是_______。
(4)在25°C、101kPa下,已知Y的气态氢化物在氧气中完
全燃烧后恢复至原状态,平均每转移1mol电子放热190.0kJ,该反应的热化学方程式
是_________。
26.(17分)
室安卡因(G)是一种抗心律失常药物,可由下列路线合成:( 1 ) 已 知 A 是 的 单 体 , 则 A 中 含 有 的 官 能 团 是
(写名称)。B的结构简式是 。
(2)C的名称是(系统命名)是 ,C与足量NaOH醇溶液供热时反应
的化学方程式 。
(3)X是E的同分异构体,X分子中含有苯环,且苯环上一氯代物只有两种,则X所
有可能的结构简式有 H3C NHCH3 、 、
。
(4)F G的反应类型是 。
(5)下列关于室安卡因(G)说法正确的是 。
a.能发生加成反应 b.能使酸性高锰酸钾溶液褪色 c.能与盐酸反应生成盐 d.属于
氨基酸
27.(14分)
MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究
学校小组设计了将粗MnO2(含有较多的MnO和MnO3)样品转化为纯MnO2的实验,
其流程如下:
(1)第①步加稀H2SO4时,粗MnO2样品中的 (写出化学式)转化为可溶
性物质。
(2)第②步反应的离子方程式是□ +□ClO3+□ MnO2↓+□Cl2↑+□ .
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、 、 、
,已知蒸发得到的固体中有NaClO3和NaOH,则一定还含有 (写化学
式)
(4)若粗MnO2样品的质量12.69g,第①步反应后,经过滤得到8.7g MnO2,并收
集 到 0.244L CO2( 标 准 状 况 下 ) , 则 在 第 ② 步 反 应 中 , 至 少 需 要
molNaClO3.28.(13分)
地下水中硝酸盐造成的氮污染已成为一个世界性的
环境问题。文献报道某课题组模拟地下水脱氮过程,利
用Fe粉和KNO 溶液反应,探究脱氮原理及相关因素
3
对脱氮速率的影响。
(1)实验前:①先用0.1mol·L-1HSO 洗涤Fe粉,
2 4
其目的是_________,然后用蒸馏水洗涤至中
性;②将KNO 溶液的pH调至2.5;③为防止
3
空气中的O 对脱氮的影响,应向 KNO 溶液
2 3
中通入_________(写化学式)。
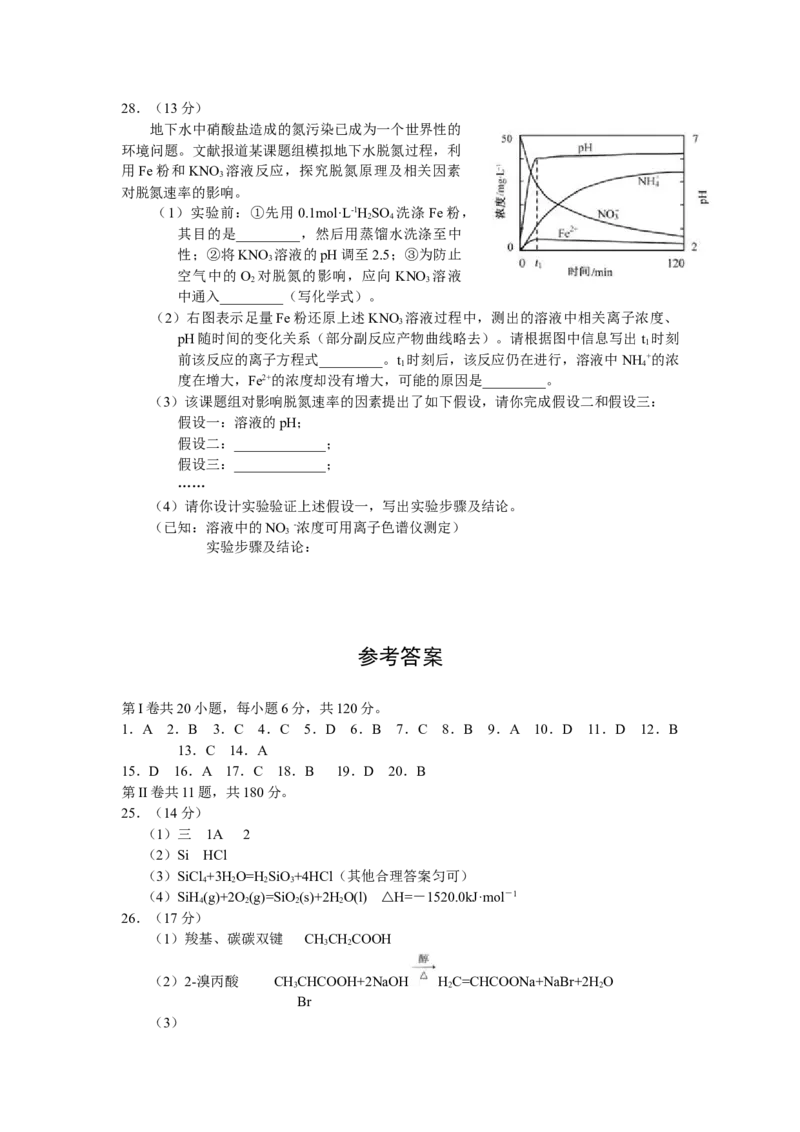
(2)右图表示足量Fe粉还原上述KNO 溶液过程中,测出的溶液中相关离子浓度、
3
pH随时间的变化关系(部分副反应产物曲线略去)。请根据图中信息写出 t 时刻
1
前该反应的离子方程式_________。t 时刻后,该反应仍在进行,溶液中NH +的浓
1 4
度在增大,Fe2+的浓度却没有增大,可能的原因是_________。
(3)该课题组对影响脱氮速率的因素提出了如下假设,请你完成假设二和假设三:
假设一:溶液的pH;
假设二:_____________;
假设三:_____________;
……
(4)请你设计实验验证上述假设一,写出实验步骤及结论。
(已知:溶液中的NO -浓度可用离子色谱仪测定)
3
实验步骤及结论:
参考答案
第I卷共20小题,每小题6分,共120分。
1.A 2.B 3.C 4.C 5.D 6.B 7.C 8.B 9.A 10.D 11.D 12.B
13.C 14.A
15.D 16.A 17.C 18.B 19.D 20.B
第II卷共11题,共180分。
25.(14分)
(1)三 1A 2
(2)Si HCl
(3)SiCl +3H O=HSiO+4HCl(其他合理答案匀可)
4 2 2 3
(4)SiH(g)+2O(g)=SiO (s)+2HO(l) △H=-1520.0kJ·mol-1
4 2 2 2
26.(17分)
(1)羧基、碳碳双键 CHCHCOOH
3 2
(2)2-溴丙酸 CHCHCOOH+2NaOH HC=CHCOONa+NaBr+2H O
3 2 2
Br
(3)(4)取代反应
(5)a、b、c
27.(14分)(1)MnO 、MnCO
2 3
(2)5Mn2+ 2 4H O 5 1 8H+
2
(3)酒精灯 蒸发皿 玻璃棒 NaCl
(4)0.02
28.(13分)
(1)去除铁粉表面的氧化物等杂质 N
2
(2)4Fe+NO3+10H+=4Fe2++NH4+3H O 生成Fe2+水解(或和溶液中的OH-结合)
2
(3)温度 铁粉颗粒大小
(4)
实验步骤及结论:
①分别取等体积、等浓度的KNO 溶液于不同的试管中;
3
②调节溶液呈酸性且pH各不相同,并通入N;
2
③分别向上述溶液中加入足量等质量的同种Fe粉;
④用离子色谱仪测定相同反应时间时各溶液中NO3的浓度。
若pH不同的KNO 溶液中,测出的NO3浓度不同,表明pH对脱氮速率有影响,否
3
则无影响。
(本题属于开放性试题,合理答案均可)