文档内容
2013年广东卷高考理综试卷化学部分
一、 单项选择题:本大题共16小题,每小题4分,满分64分.在每小题
给出的四个选项中,只有一项是符合题目要求的.选对的得4分,选错或不
答的得0分。
7.下列说法正确的是
A.糖类化合物都具有相同的官能团 B.酯类物质是形成水果香咪的主要成分
C.油脂的皂化反应生成脂肪酸和丙醇 D.蛋白质的水解产物都含有羧基和羟基
8.水溶解中能大量共存的一组离子是
A.Na+、Al3+、Cl-、CO 2- B.H+、Na+、Fe2+、MnO -
3 4
C.K+、Ca2+、Cl-、NO - B. K+、NH +、OH-、SO 2-
3 4 4
9.设n 为阿弗加德罗常数的数值,下列说法正确的是
A
A.常温常压下,8gO 含有4n 个电子
2 A
B.1L0.1molL-1的氨水中有n 个NH +
A 4
C.标准状况下,22.4L盐酸含有n 个HCl分子
A
D.1molNa被完全氧化生成Na O ,失去个2n 电子
2 2 A
10.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
11.下列措施不合理的是
A.用SO 漂白纸浆和草帽辫
2
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO 制取粗硅
2
12.50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:c(H+)=4.0molL-1
B.饱和小苏打溶液中:c(Na+)= c(HCO -)
3
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D. pH=12的纯碱溶液中:c(OH-)=1.0×10-2molL-1
二、双项选择题:本大题共9小题,每小题6分,共54分。在每小题给出的四
个选项中,有两个选项符合题目要求,全部选对的得6分,只选1个且正确
的得3分,有选错或者不答的得0分。
22.元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单
质在暗处与H 剧烈化合并发生爆炸。则下列判断正确的是
2
A.非金属性:ZQ
23.下列实验的现象与对应结论均正确的是
选项 操作 现象 结论
A 将浓硫酸滴到蔗糖表面 固体变黑膨胀 浓硫酸有脱水性和强氧化性B 常温下将Al片放入浓硝酸中 无明显变化 Al与浓硝酸不反应
C 将一小块Na放入无水乙醇中 产生气泡 Na能置换出醇羟基中的氢
D 将水蒸气通过灼热的铁粉 粉末变红 铁与水在高温下发生反应
三、非选择题:本大题共11小题,共182分。按题目要求作答。解答题应写出必
要的文字说明、方程式和重要演算步骤,只写出最后答案的不能得分。有数值
计算的题,答案中必须明确写出数值和单位。
30.(16分)脱水偶联反应是一种新型的直接烷基化反应,例如:
(1)化合物Ⅰ的分子式为_____,1mol该物质完全燃烧最少需要消耗_____molO
2.
(2)化合物Ⅱ可使____溶液(限写一种)褪色;化合物Ⅲ(分子式为C H C1)可
10 11
与NaOH水溶液共热生成化合物Ⅱ,相应的化学方程式为______.
(3)化合物Ⅲ与NaOH乙醇溶液工热生成化合物Ⅳ,Ⅳ的核磁共振氢谱除苯环峰外还有
四组峰,峰面积之比为为1:1:1:2,Ⅳ的结构简式为_______.
(4)由CH COOCH CH 可合成化合物Ⅰ.化合物Ⅴ是CH COOCH CH 的一种无支链同
3 2 3 3 2 3
分异构体,碳链两端呈对称结构,且在Cu催化下与过量O 反应生成能发生银镜反
2
应的化合物Ⅵ. Ⅴ的结构简式为______,Ⅵ的结构简式为______.
(5)一定条件下,
也可以发生类似反应①的反应,有机
产物的结构简式为_____.
31.(16分)
大气中的部分碘源于O 对海水中Ⅰ-的氧化。将O 持续通入NaⅠ溶液中进行模拟研究.
3 3
(1)O 将Ⅰ-氧化成Ⅰ 的过程由3步反应组成:
3 2
①Ⅰ-(aq)+ O (g)=ⅠO-(aq)+O(g)△H
3 2 1
②ⅠO-(aq)+H+(aq) HOⅠ(aq) △H
2
总反应的化学方程式为______,其反应△H=______
(2)在溶液中存在化学平衡: ,其平衡常数
表达式为_______.
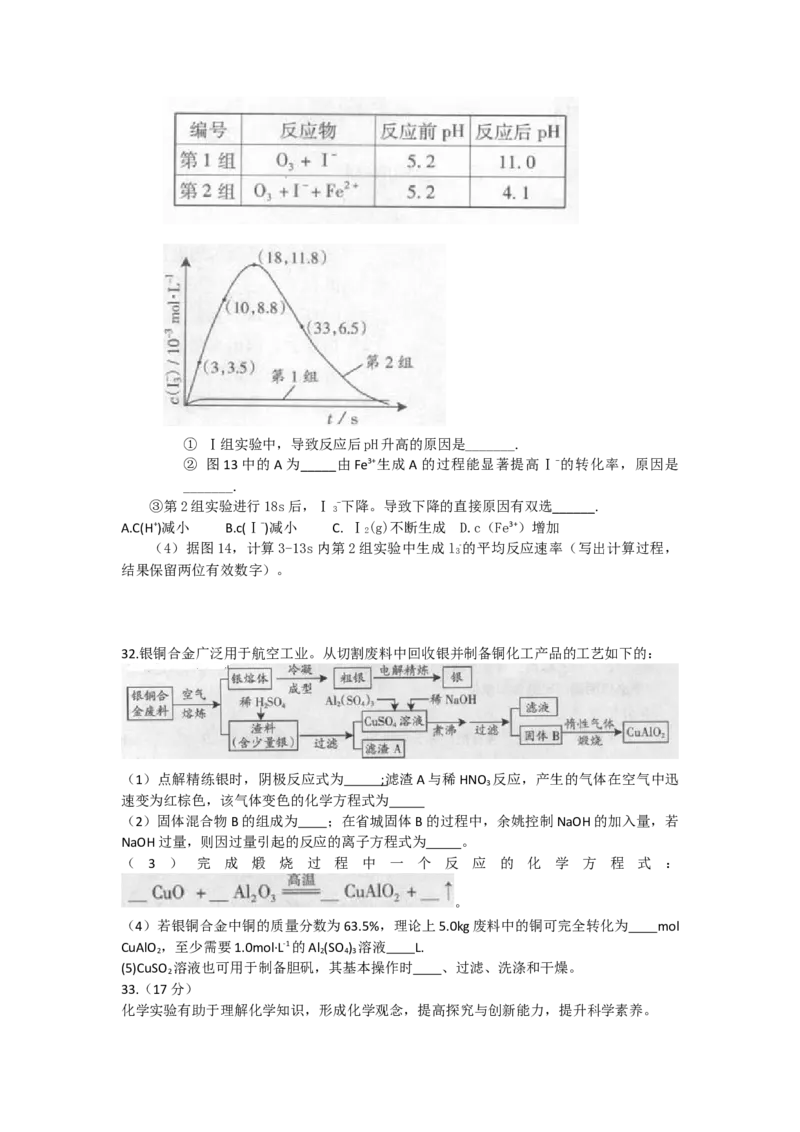
(3) 为探究Fe2+对氧化Ⅰ-反应的影响(反应体如图13),某研究小组测定两组实验
中Ⅰ -浓度和体系pH,结果见图14和下表。
3① Ⅰ组实验中,导致反应后pH升高的原因是_______.
② 图13中的A为_____由Fe3+生成A的过程能显著提高Ⅰ-的转化率,原因是
_______.
③第2组实验进行18s后,Ⅰ -下降。导致下降的直接原因有双选______.
3
A.C(H+)减小 B.c(Ⅰ-)减小 C. Ⅰ(g)不断生成 D.c(Fe3+)增加
2
(4)据图14,计算3-13s内第2组实验中生成l-的平均反应速率(写出计算过程,
3
结果保留两位有效数字)。
32.银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下的:
(1)点解精练银时,阴极反应式为 ;滤渣A与稀HNO 反应,产生的气体在空气中迅
3
速变为红棕色,该气体变色的化学方程式为
(2)固体混合物B的组成为 ;在省城固体B的过程中,余姚控制NaOH的加入量,若
NaOH过量,则因过量引起的反应的离子方程式为 。
( 3 ) 完 成 煅 烧 过 程 中 一 个 反 应 的 化 学 方 程 式 :
。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 mol
CuAlO ,至少需要1.0mol·L-1的Al (SO ) 溶液 L.
2 2 4 3
(5)CuSO 溶液也可用于制备胆矾,其基本操作时 、过滤、洗涤和干燥。
2
33.(17分)
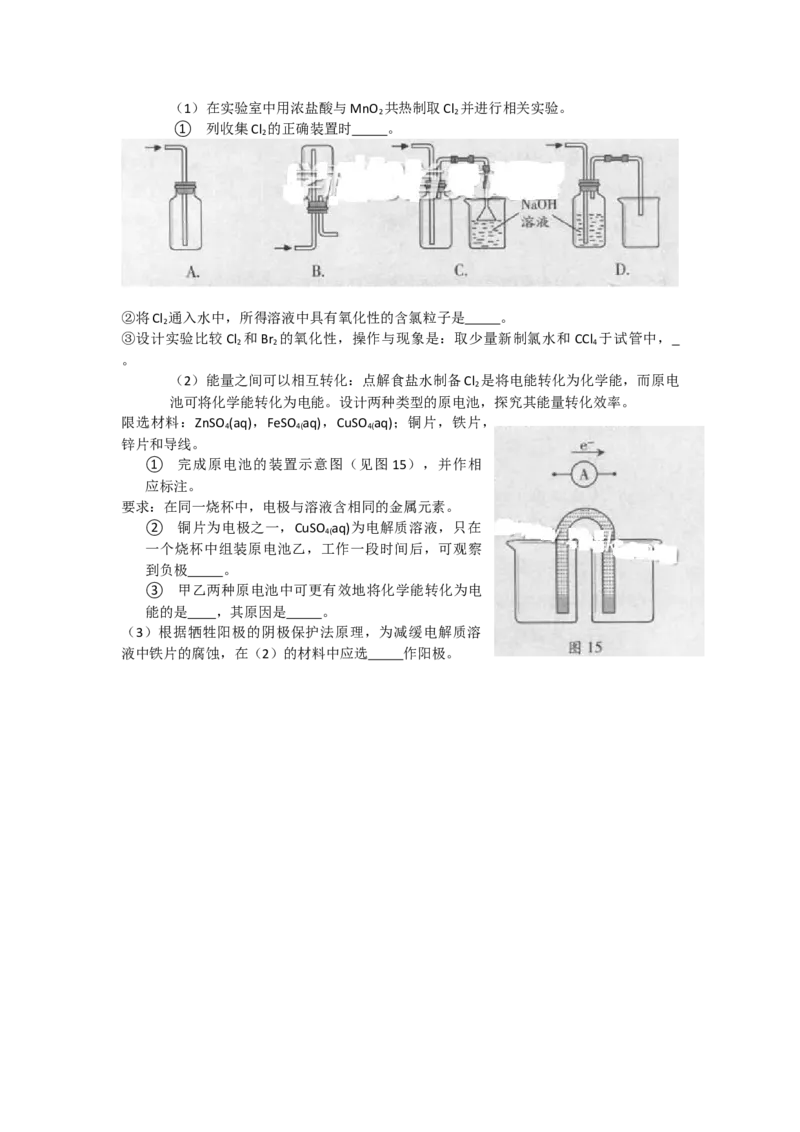
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。(1)在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。
2 2
① 列收集Cl 的正确装置时 。
2
②将Cl 通入水中,所得溶液中具有氧化性的含氯粒子是 。
2
③设计实验比较Cl 和Br 的氧化性,操作与现象是:取少量新制氯水和 CCl 于试管中,
2 2 4
。
(2)能量之间可以相互转化:点解食盐水制备Cl 是将电能转化为化学能,而原电
2
池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。
限选材料:ZnSO (aq),FeSO aq),CuSO aq);铜片,铁片,
4 4( 4(
锌片和导线。
① 完成原电池的装置示意图(见图15),并作相
应标注。
要求:在同一烧杯中,电极与溶液含相同的金属元素。
② 铜片为电极之一,CuSO aq)为电解质溶液,只在
4(
一个烧杯中组装原电池乙,工作一段时间后,可观察
到负极 。
③ 甲乙两种原电池中可更有效地将化学能转化为电
能的是 ,其原因是 。
(3)根据牺牲阳极的阴极保护法原理,为减缓电解质溶
液中铁片的腐蚀,在(2)的材料中应选 作阳极。2013 年广东高考化学部分答案解析
7.【答案】B
【命题透析】本题考查的是常见有机物的性质。
【思路点拨】糖类是多羟基的酮或多羟基的醛,所含的官能团不一定相同,A项错误;水
果香精的主要成分是酯类,B项正确;油脂的皂化反应生成的是硬脂酸和丙三醇,C项错误;
蛋白质的水解产物是氨基酸,所含的官能团是氨基和羧基,D项错误。
8.【答案】C
【命题透析】本题考查的是离子共存问题
【思路点拨】Al3+与CO 2—在水溶液中发生双水解而不能大量共存,A项错误;H+、Fe2+、
3
MnO -在水溶液中因氧化还原反应而不能大量共存,B项错误;NH +、OH-在水溶液中不能大
4 4
量共存,D项错误。
9.【答案】A
【命题透析】本题考查的是阿伏加德罗常数。
【思路点拨】解析:常温常压下,8gO 为0.25mol,1molO2含有的电子数为 16mol,故
2
8gO 含有4n 个电子,A项正确;氨水是弱电解质,1L0.1mol·L-1的氨水中有NH +小于n
2 A 4 A
个,B项错误;盐酸在标况下是液态,C项错误;1molNa被完全氧化生成Na O ,Na从0
2 2
价升高到+1价,失去个n 电子,D项错误。
A
10.【答案】D
【命题透析】本题考查的是常见无机物的性质及其除杂、鉴别、保存等。
【思路点拨】 解析:NH Cl为强酸弱碱盐,加热也可除去NaCl中的N号4Cl,但是二者无
4
因果关系,A项错误;Fe3+具有氧化性,与Fe3+用KSCN溶液的检验无因果关系,B项错误;
CaCO 的溶解度大于Ca(HCO ) ,但是Na CO 溶解大于NaHCO ,C项错误;玻璃的主要
3 3 2 2 3 3
成分是SiO ,SiO 与HF能反应,所以不能用玻璃瓶保存,D项正确。
2 2
11.【答案】B
【命题透析】本题考查的是常见物质的性质及相关反应。
【思路点拨】 SO 具有漂白性,可以漂白纸浆和草帽辫,A项正确;硫酸与CaCO 反应生
2 3
成微溶于水的CaSO ,且硫酸能与铁反应,所以不能用硫酸清洗锅炉,B项错误;高温下焦
4
炭与SiO 反应的得到Si与CO,C项正确;Cu2+和Hg2+与S2—能生成难溶物CuS和HgS,D项
2
正确。
12.【答案】C
【命题透析】本题考查的是溶液中离子浓度的大小计算与关系。
【思路点拨】pH=4的醋酸中:c(H+)=0.0001mol·L-1,A项错误;小苏打溶液中,由于
HCO —的水解,所以c(Na+)>c(HCO -),B项错误;饱和食盐水中:c根据电荷守恒,有
3 3
(Na+)+ c(H+)= c(Cl-)+c(OH-),C项正确;由于题干给的温度不是常温下,所以
pH=12的纯碱溶液中c(OH-)无法计算,D项错误。
二、双项选择题:本大题共9小题,每小题6分,共54分。在每小题给出的四
个选项中,有两个选项符合题目要求,全部选对的得6分,只选1个且正确
的得3分,有选错或者不答的得0分。
22.【答案】BD【命题透析】本题考查的是元素周期表和元素周期律。
【思路点拨】“R单质在暗处与H 剧烈化合并发生爆炸”,则R为F元素;根据图中元素
2
的关系,则X为S元素,T为Cl元素,Z为Ar元素,Q为Br元素。Z为惰性气体元素,故非
金属性的大小比较为F>Cl>Ar,A项错误;Br的原子序数为35,F的原子序数为9,原子序
数只差为26,B项正确;气态氢化物的稳定性为HF>HCl>HBr,C项错误;HClO 的酸性大于
4
HBrO ,D项正确。
4
23.【答案】AC
【命题透析】本题考查的是实验的基本操作与现象分析。
【思路点拨】浓硫酸的脱水性和强氧化性,能与蔗糖固体变黑,A项正确;Al在常温下与
浓硝酸反应发生钝化,钝化也是化学反应,B项错误;Na与无水乙醇反应得到H ,反应原
2
理是 Na 置换出醇羟基中的氢,C 项正确;水蒸气通过灼热的铁粉,得到的是黑色的
Fe O ,D项错误。
3 4
三、非选择题:本大题共11小题,共182分。按题目要求作答。解答题应写出必
要的文字说明、方程式和重要演算步骤,只写出最后答案的不能得分。有数值
计算的题,答案中必须明确写出数值和单位。
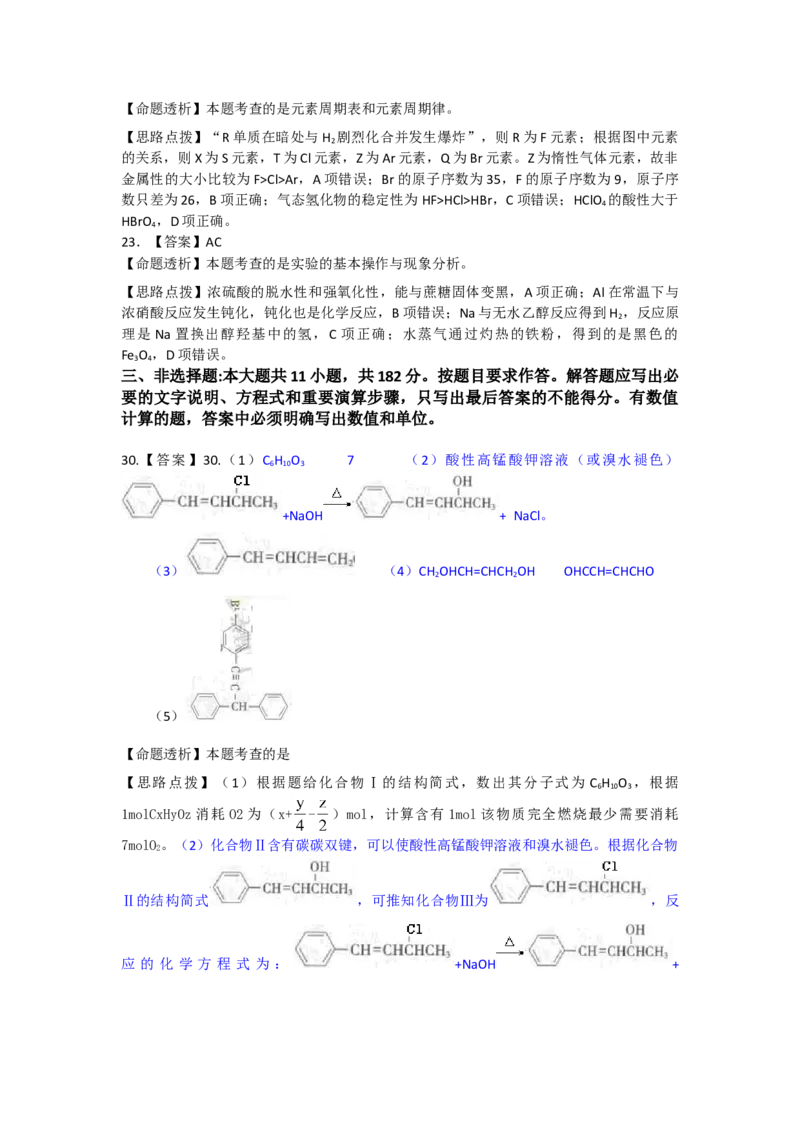
30.【答案】30.(1)C H O 7 (2)酸性高锰酸钾溶液(或溴水褪色)
6 10 3
+NaOH + NaCl。
(3) (4)CH OHCH=CHCH OH OHCCH=CHCHO
2 2
(5)
【命题透析】本题考查的是
【思路点拨】(1)根据题给化合物Ⅰ的结构简式,数出其分子式为 C H O ,根据
6 10 3
1molCxHyOz消耗 O2为(x+ - )mol,计算含有 1mol该物质完全燃烧最少需要消耗
7molO 。(2)化合物Ⅱ含有碳碳双键,可以使酸性高锰酸钾溶液和溴水褪色。根据化合物
2
Ⅱ的结构简式 ,可推知化合物Ⅲ为 ,反
应 的 化 学 方 程 式 为 : +NaOH +NaCl 。 ( 3 ) 在 NaOH 乙 醇 溶 液 中 发 生 消 去 反 应 生 成
,该有机物分子内除苯环外含有四种氢原子,个数之比为
1:1:1:2,即四组峰,峰面积之比为 1:1:1:2。(4)由 V 的结构特征可推知其为
CH OHCH=CHCH OH,其在铜做催化剂的作用下与过量氧气发生催化氧化反应生成
2 2
OHCCH=CHCHO 。(5)根据题给信息只能是脱去羟基和碳碳三键的氢原子生成:
31. ( 1 )
(2) (3)①H+被消耗,其浓度降低;② 结合氢氧根生成氢氧化
铁沉淀,增大了氢离子浓度,使 向
右移动,使 减小;③BD (4)
【解析】本题考查了盖斯定律、化学平衡常数,化学平衡的移动以及化学反应速率的计算
等知识。(1)根据题给信息,总反应为O3氧化I-生成I2,将所给的三个反应:①+②+③可
得 △ H= 。
(2)根据化学反应方程式写出平衡常数表达式。(3)①该反应消耗H+,随反应进行c(H+)
浓度降低,pH升高。②见答案(也有认为该转化是二价铁与三价铁的转化,故 A为Fe2+,
Fe3+氧化 生成I ,使 减小;但是解释不了为什么氢离子浓度减小)。
2
③c(Fe3+)增加, 减小都会使c(I -)急剧减小。(4)3~18s内,
3
v(I -)= 。
3
32.(1)Ag++e-=Ag 2NO+O =2NO
2 2(2)Al(OH) 和CuO的混合物 Al(OH) +OH-=AlO -+2H O
3 3 2 2
(3)4 2 4 O2
(4)50 25
(5)蒸发浓缩、冷却结晶
【解析】本题考查了工艺流程问题。(1)电解精炼时,阴极上Ag+得电子生成金属银,电
极反应式为 Ag++e-=Ag;气体迅速变红是因为生成的 NO 气体被空气氧化为 NO ,
2
2NO+O =2NO 。
2 2
(2)Al (SO ) 和CuSO 溶液中加入NaOH溶液后得到的固体为Al(OH) 和Cu(OH) 的混合
2 4 3 4 3 2
物,但是煮沸后,氢氧化铜在80度即分解,故应该为氢氧化铝和氧化铜的混合物;在该过
程中加入的NaOH过量后会使生成的Al(OH) 溶解,反应的离子方程式为Al(OH) +OH-=AlO -
3 3 2
+2H O。
2
(3)在该未完成的方程式中,产生的气体只能是氧气,故配平后的方程式为
4CuO+2Al O =4CuAlO +O ↑。
2 3 2 2
( 4 ) 根 据 铜 守 恒 可 知 n(CuAlO2)= =50mol ; 因 为
n(Al)=n(Cu)=n(CuAlO )=50mol,故需要溶液的体积为25L。
2
(5)从硫酸铜溶液中得到晶体的过程为,蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
33.(1)①C ②Cl 、HClO、ClO- ③用胶头滴管向试管中滴加溴化钠溶液、震荡使其充分
2
反应,发现溶液出现分层现象,下层溶液变为橙红色。(2)① ;
②电极逐渐溶解;③装置甲,可以避免铁和铜离子的接触,从而避免能量损失,提高电池
效率,提供稳定电流; (3)Zn。
【解析】本题考查化学实验基本操作、非金属性的比较、电化学原理(原电池和电解池)
等知识。(1)①氯气的密度比空气大,应采用向上排空气法,氯气有毒,必须有尾气处理
装置,故只有C合适;②氯气溶于水后有一部分生成了具有强氧化性的HClO,故溶液中具
有氧化性的含氯粒子有Cl 、HClO、ClO-三种;③比较Cl 和Br 的氧化性可以通过两种单质
2 2 2
之间的置换反应来实现。(2)①根据电子的流向可知,左边的烧杯中的电极为负极,右边
烧杯中电极为正极,在原电池中活泼金属做负极,故左边烧杯中盛有 ZnSO4溶液,插入锌
片,右边烧杯中盛有CuSO4 溶液,插入铜片;②由所给的电极材料可知,当铜片做电极时,
铜片一定是正极,则负极是活泼的金属(失电子发生氧化反应),反应的现象是电极逐渐
的溶解;③以Fe和Cu做电极为例,如果不用盐桥则除了电化学反应外还发生Fe和铜的置
换反应,反应放热,会使化学能以热能的形式转化掉,使其不能完全转化为电能,而盐桥
的使用,可以避免铁和铜离子的接触,从而避免能量损失,提高电池效率,提供稳定电流
(3)根据牺牲阳极的阴极保护法,可知被保护的金属作阴极,即Zn作为阳极。