文档内容
2015年普通高等学校招生全国统一考试(四川卷)
理科综合·化学
理科综合考试时间共150分钟,满分300分。其中,物理110分,化学100分,生物90
分。
化学试题卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)。第Ⅰ卷 5至6页,第Ⅱ卷7至8页,
共4页。考生作答时,须将答案答再答题卡上,在本试题卷、草稿纸上答题无效。考试结束
后,将本试题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56
第Ⅰ卷 (选择题 共42分)
注意事项:
必须使用2B铅笔在答题卡上将所选答案对应的标号涂黑。
第Ⅰ卷共7题,每题6分。每题给出的四个选项中,只有一项是符合题目要求的。
1.下列物质在生活中应用时,起还原作用的是
A. 明矾作净水剂 B. 甘油做护肤保湿剂
C. 漂粉精做消毒剂 D. 铁粉作食品袋中的脱氧剂
2.下列有关CuSO 溶液的叙述正确的是
4
A. 该溶液中Na+、NH 、NO 、Mg2+可以大量共存
B. 通入CO 气体产生蓝色沉淀
2
C. 与HS反应的离子方程式:Cu2++S2—=CuS↓
2
D. 与过量浓氨水反应的离子方程式:Cu2++2NH·HO=Cu(OH) ↓+2NH +
2 2 4
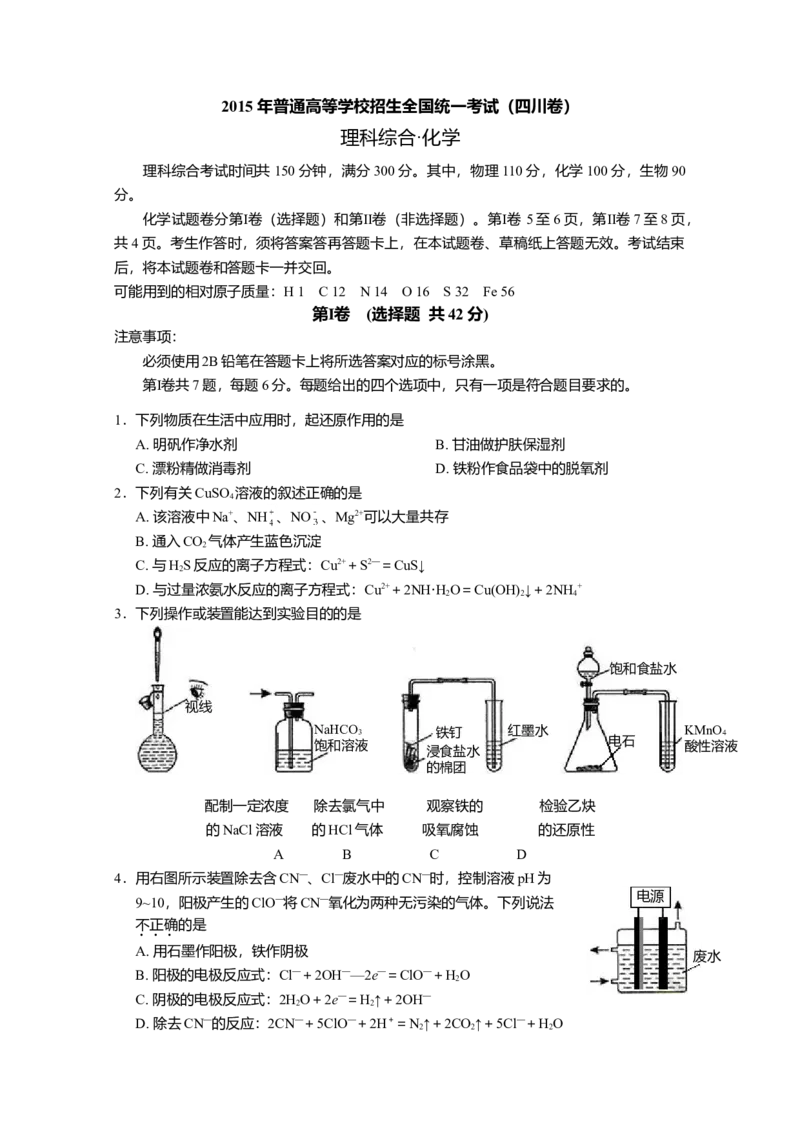
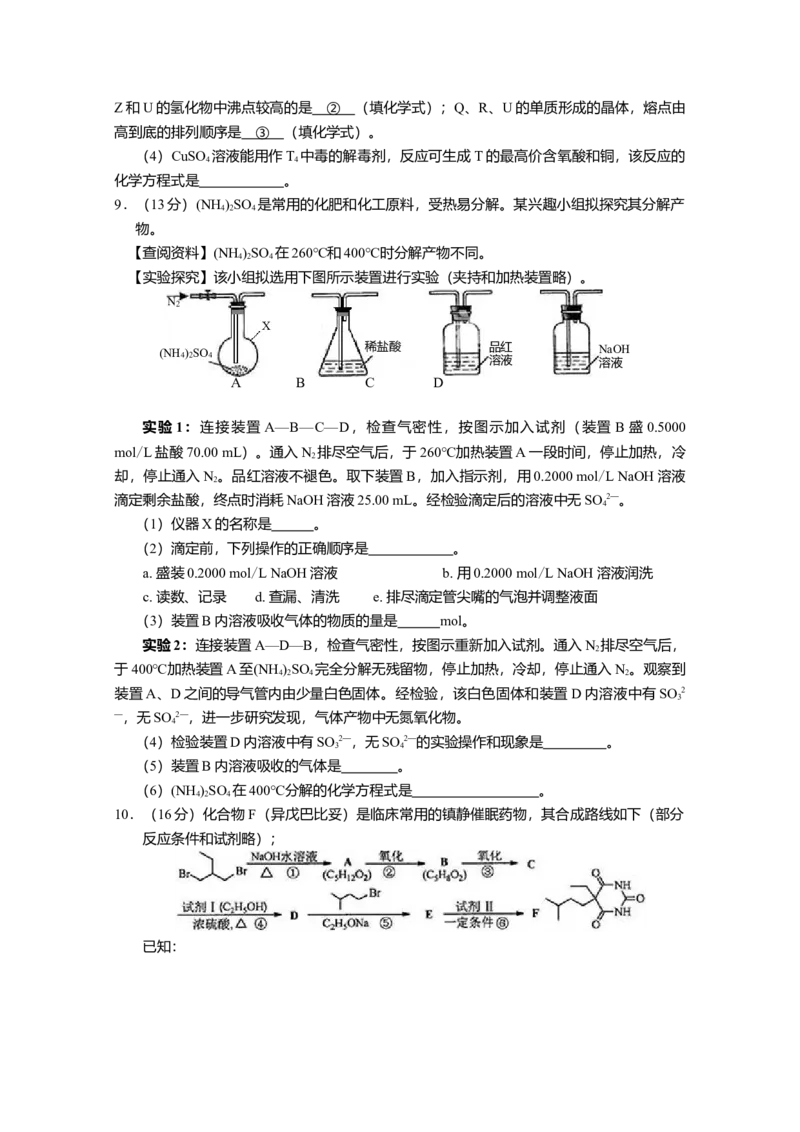
3.下列操作或装置能达到实验目的的是
饱和食盐水
视线
NaHCO 3 铁钉 红墨水 KMnO 4
电石
饱和溶液 酸性溶液
浸食盐水
的棉团
配制一定浓度 除去氯气中 观察铁的 检验乙炔
的NaCl溶液 的HCl气体 吸氧腐蚀 的还原性
A B C D
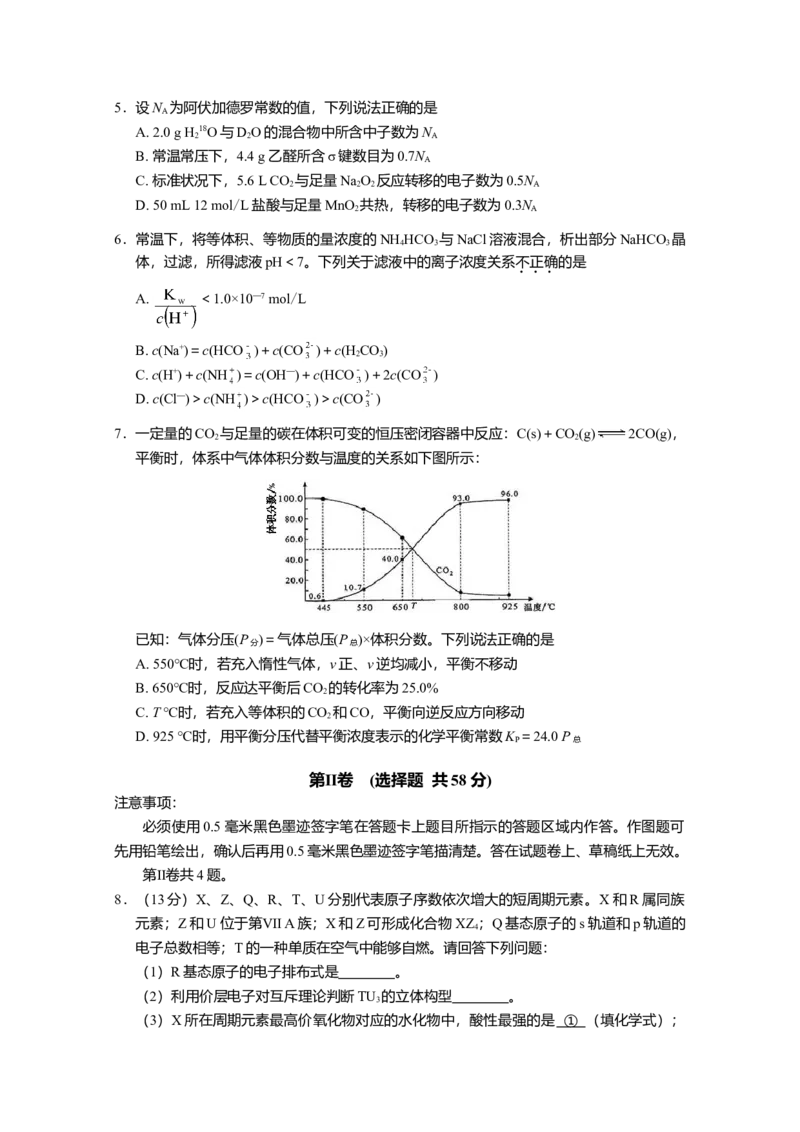
4.用右图所示装置除去含CN—、Cl—废水中的CN—时,控制溶液pH为
电源
9~10,阳极产生的ClO—将CN—氧化为两种无污染的气体。下列说法
不正确的是
A. 用石墨作阳极,铁作阴极
废水
B. 阳极的电极反应式:Cl—+2OH——2e—=ClO—+HO
2
C. 阴极的电极反应式:2HO+2e—=H↑+2OH—
2 2
D. 除去CN—的反应:2CN—+5ClO—+2H+=N↑+2CO↑+5Cl—+HO
2 2 25.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 2.0 g H 18O与DO的混合物中所含中子数为N
2 2 A
B. 常温常压下,4.4 g 乙醛所含σ键数目为0.7N
A
C. 标准状况下,5.6 L CO 与足量NaO 反应转移的电子数为0.5N
2 2 2 A
D. 50 mL 12 mol/L盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
6.常温下,将等体积、等物质的量浓度的NH HCO 与NaCl溶液混合,析出部分NaHCO 晶
4 3 3
体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A. <1.0×10—7 mol/L
B. c(Na+)=c(HCO )+c(CO )+c(H CO)
2 3
C. c(H+)+c(NH )=c(OH—)+c(HCO )+2c(CO )
D. c(Cl—)>c(NH )>c(HCO )>c(CO )
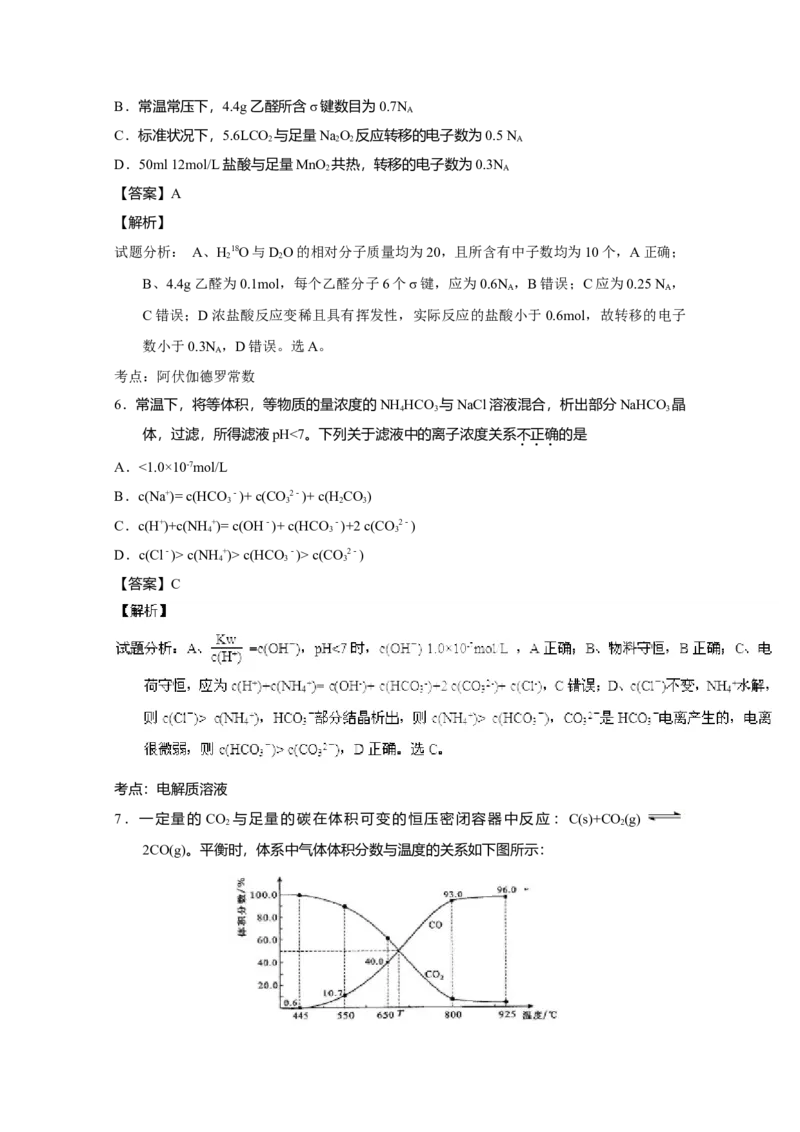
7.一定量的CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g) 2CO(g),
2 2
平衡时,体系中气体体积分数与温度的关系如下图所示:
已知:气体分压(P )=气体总压(P )×体积分数。下列说法正确的是
分 总
A. 550℃时,若充入惰性气体,v正、v逆均减小,平衡不移动
B. 650℃时,反应达平衡后CO 的转化率为25.0%
2
C. T ℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D. 925 ℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0 P
P 总
第Ⅱ卷 (选择题 共58分)
注意事项:
必须使用0.5 毫米黑色墨迹签字笔在答题卡上题目所指示的答题区域内作答。作图题可
先用铅笔绘出,确认后再用0.5毫米黑色墨迹签字笔描清楚。答在试题卷上、草稿纸上无效。
第Ⅱ卷共4题。
8.(13分)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族
元素;Z和U位于第ⅦA族;X和Z可形成化合物XZ ;Q基态原子的s轨道和p轨道的
4
电子总数相等;T的一种单质在空气中能够自燃。请回答下列问题:
(1)R基态原子的电子排布式是 。
(2)利用价层电子对互斥理论判断TU 的立体构型 。
3
(3)X所在周期元素最高价氧化物对应的水化物中,酸性最强的是 ① (填化学式);Z和U的氢化物中沸点较高的是 ② (填化学式);Q、R、U的单质形成的晶体,熔点由
高到底的排列顺序是 ③ (填化学式)。
(4)CuSO 溶液能用作T 中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的
4 4
化学方程式是 。
9.(13分)(NH )SO 是常用的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产
4 2 4
物。
【查阅资料】(NH )SO 在260℃和400℃时分解产物不同。
4 2 4
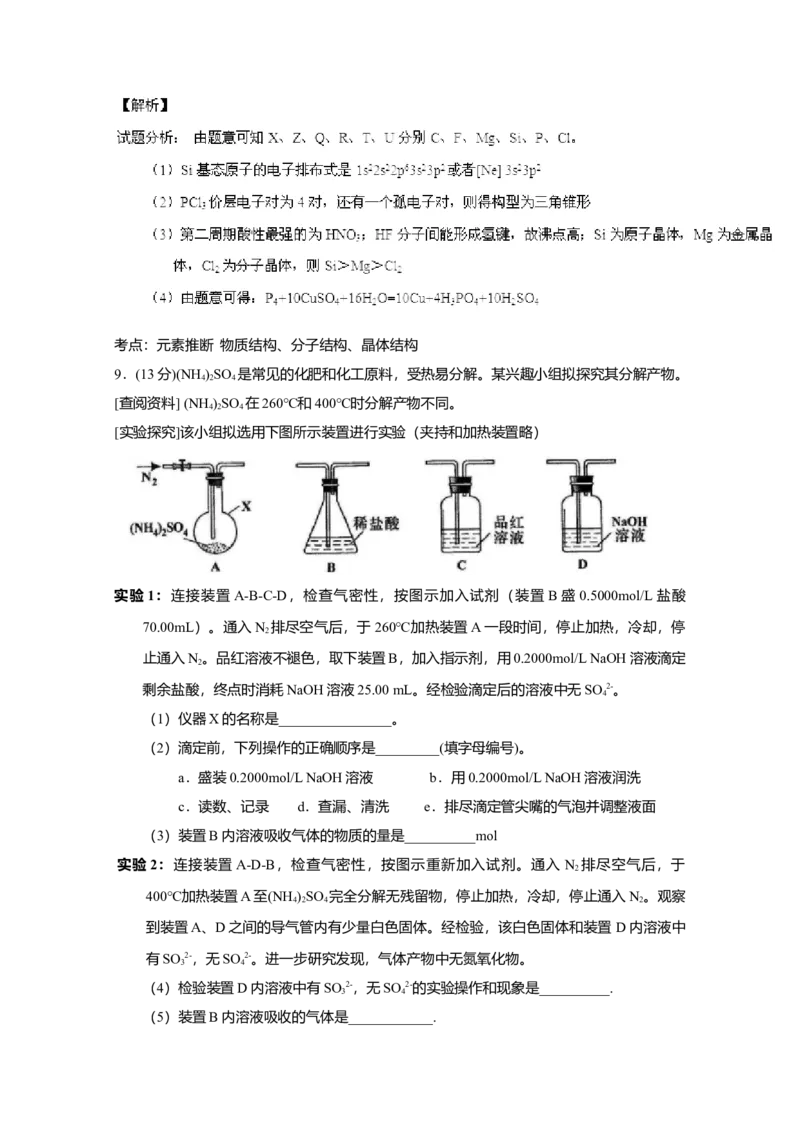
【实验探究】该小组拟选用下图所示装置进行实验(夹持和加热装置略)。
N
2
X
(NH ) SO 稀盐酸 品红 NaOH
4 2 4 溶液 溶液
A B C D
实验 1:连接装置 A—B—C—D,检查气密性,按图示加入试剂(装置 B 盛 0.5000
mol/L盐酸70.00 mL)。通入N 排尽空气后,于260℃加热装置A一段时间,停止加热,冷
2
却,停止通入N 。品红溶液不褪色。取下装置B,加入指示剂,用0.2000 mol/L NaOH溶液
2
滴定剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO 2—。
4
(1)仪器X的名称是 。
(2)滴定前,下列操作的正确顺序是 。
a. 盛装0.2000 mol/L NaOH溶液 b. 用0.2000 mol/L NaOH溶液润洗
c. 读数、记录 d. 查漏、清洗 e. 排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是 mol。
实验2:连接装置A—D—B,检查气密性,按图示重新加入试剂。通入N 排尽空气后,
2
于400℃加热装置A至(NH )SO 完全分解无残留物,停止加热,冷却,停止通入N。观察到
4 2 4 2
装置A、D之间的导气管内由少量白色固体。经检验,该白色固体和装置D内溶液中有SO 2
3
—,无SO 2—,进一步研究发现,气体产物中无氮氧化物。
4
(4)检验装置D内溶液中有SO 2—,无SO 2—的实验操作和现象是 。
3 4
(5)装置B内溶液吸收的气体是 。
(6)(NH )SO 在400℃分解的化学方程式是 。
4 2 4
10.(16分)化合物F(异戊巴比妥)是临床常用的镇静催眠药物,其合成路线如下(部分
反应条件和试剂略);
已知:请回答下列问题:
(1)试剂Ⅰ的化学名称是 ① ,化合物B的官能团名称是 ② ,第4步的化学反应类
型是 ③ 。
(2)第①步反应的化学方程式是 。
(3)第⑤步反应的化学方程式是 。
(4)试剂Ⅱ的相对分子质量为60,其结构简式是 。
(5)化合物B的一种同分异构体G与NaOH溶液共热反应,生成乙醇和化合物H,H在
一定条件下发生聚合反应得到高吸水性树脂,该聚合物的结构简式是 。
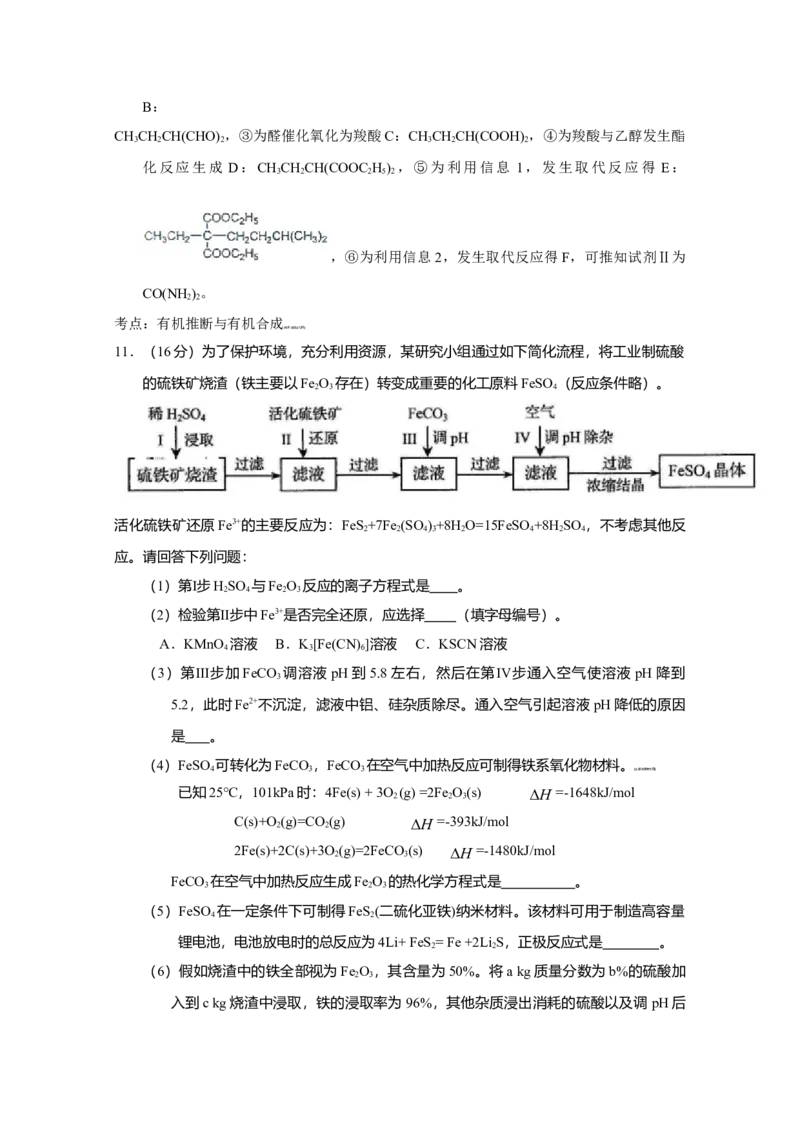
11.(16分)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸
的硫铁矿烧渣(铁主要以Fe O 存在)转变成重要的化工原料FeSO (反应条件略)。
2 3 4
稀H SO 活化硫铁矿 FeCO 空气
2 4 3
Ⅰ 浸取 Ⅱ 还原 Ⅲ 调pH Ⅳ 调pH除杂
硫铁矿烧渣 过滤 滤液 过滤 滤液 过滤 滤液 过滤 FeSO 晶体
4
浓缩结晶
活化硫铁矿还原Fe3+的主要反应为:FeS +7Fe (SO ) +8HO=15FeSO +8HSO ,不考
2 2 4 3 2 4 2 4
虑其它反应。请回答下列问题:
(1)第Ⅰ步HSO 与Fe O 反应的离子方程式是 。
2 4 2 3
(2)检验第Ⅱ步中Fe3+是否完全还原,应选择 (填字母编号)。
A. KMnO 溶液 B. K[Fe(CN) ]溶液 C. KSCN溶液
4 3 6
(3)第Ⅲ步加FeCO 调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH降到5.2,
3
此时Fe2+不沉淀,滤液中铝、硅杂质被除尽。通入空气引起溶液pH降低的原因是
。
(4)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。
4 3 3
已知25℃,101 kPa时:4Fe(s)+3O(g)=2Fe O(s) △H=—1648 kJ/mol
2 2 3
C(s)+O(g)=CO(g) △H=—393 kJ/mol
2 2
2Fe(s)+2C(s)+3O(g)=2FeCO(s) △H=—1480 kJ/mol
2 3
FeCO 在空气中加热反应生成Fe O 的热化学方程式是 。
3 2 3
(5)FeSO 在一定条件下可制得FeS (二硫化亚铁)纳米材料。该材料可用于制造高容
4 2
量锂电池,电池放电时的总反应为4Li+FeS=Fe+2LiS,正极反应式是 。
2 2
(6)假如烧渣中的铁全部视为Fe O,其含量为50%。将a kg质量分数为b %的硫酸加入
2 3
到c kg 烧渣中浸取,铁的浸取率为96%,其它杂质浸出消耗的硫酸以及调pH后溶液呈微酸
性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO kg。
3理科综合·化学试题参考答案
第Ⅰ卷 (包括7题,每题6分,共42分)
1.D 2.A 3.C 4.D 5.A 6.C 7.B
8.(13分)(六种元素分别是C、F、Mg、Si、P、Cl)
(1)1s22s22p63s23p2 或 [Ne] 3s23p2
(2)三角锥形
(3)① HNO ② HF ③ Si、Mg、Cl
3 2
(4)P+10CuSO +16HO=10Cu+4HPO +10HSO
4 4 2 3 4 2 4
9.(13分)
(1)圆底烧瓶
(2)d b a e c
(3)0.03
(4)取少量装置D内溶液于试管中,滴加BaCl 溶液,生成白色沉淀;加入足量稀盐酸后沉
2
淀完全溶解,放出无色刺激性气味气体。
(5)NH 或氨气
3
(6)3(NH )SO 4NH ↑+N↑+3SO ↑+6HO↑
4 2 4 3 2 2 2
400℃
10.(16分)
(1)① 乙醇 ② 醛基 ③ 取代反应(或酯化反应)
(2)CH CH CH(CH Br) +2NaOH 水 CH CH CH(CH OH) +2NaBr
3 2 2 2 3 2 2 2
△
或
COOC
2
H
5
COOC
2
H
5
(3)CH CH —C—H +(CH )CHCH CH Br+C H Na CH CH —C—CH CH CH(CH ) +C H OH+
3 2 3 2 2 2 5 3 2 2 2 3 2 2 5
NaBr
COOC
2
H
5
COOC
2
H
5
(4) (5)
11.(16分)
(1)Fe O+6H+=2Fe3++3HO
2 3 2
(2)C
(3)Fe2+被氧化为Fe3+,Fe3+水解产生H+
(4)4FeCO(s)+O(g)=2Fe O(s)+4CO(g) △H=—260 kJ/mol
3 2 2 3 2
(5)FeS+4Li++4e—=Fe+2LiS 或Fe S+4e— =Fe+2S2—
2 2 2(6)0.0118ab—0.646c或
2015年普通高等学校招生全国统一考试(四川卷)
化学
1.下列物质在生活中应用时,起还原作用的是
A.明矾作净水剂
B.甘油作护肤保湿剂
C.漂粉精作消毒剂
D.铁粉作食品袋内的脱氧剂
【答案】D
【解析】
试题分析:A、明矾净水是因为Al3+水解成Al(OH) 胶体吸附;B、甘油具有强的吸湿性,可
3
以让皮肤上的水分不会太快散发,同时适当从空气中吸收水蒸气,故用作保湿剂;C、
漂粉精具有强氧化性,故可作消毒剂;D、铁粉可以消耗食品袋中的氧气,铁粉自身被
氧化,起还原作用。选D。
考点:氧化还原反应
2.下列有关CuSO 溶液的叙述正确的是
4
A.该溶液中Na+、NH +、NO -、Mg2+可以大量共存
4 3
B.通入CO 气体产生蓝色沉淀
2
C.与HS反应的离子方程式:Cu2++ S2-=CuS↓
2
D.与过量浓氨水反应的离子方程式:Cu2++2NH·H O=Cu(OH) ↓+2NH+
3 2 2 4
【答案】A
考点:离子反应
3.下列操作或装置能达到实验目的的是【答案】C
【解析】
试题分析:A、视线应平视,俯视使浓度偏大;B、氯气要和饱和碳酸氢钠反应,应用饱和食
盐水;D、电石产生的气体中混有 HS等杂质气体也能使酸性高锰酸钾溶液褪色。选
2
C。
考点:实验基本操作
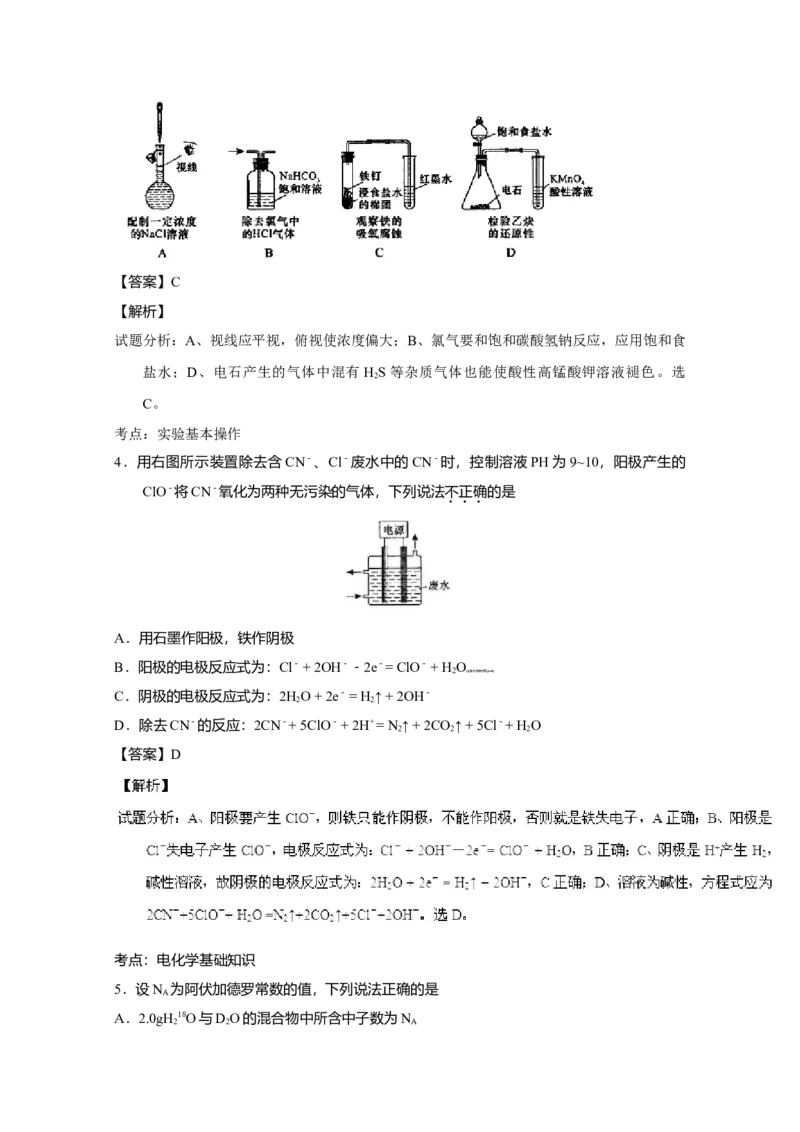
4.用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的
ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H O
2 [来源:学优高考网gkstk]
C.阴极的电极反应式为:2HO + 2e- = H ↑ + 2OH-
2 2
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N ↑ + 2CO ↑ + 5Cl-+ H O
2 2 2
【答案】D
考点:电化学基础知识
5.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.2.0gH 18O与DO的混合物中所含中子数为N
2 2 AB.常温常压下,4.4g乙醛所含σ键数目为0.7N
A
C.标准状况下,5.6LCO 与足量NaO 反应转移的电子数为0.5 N
2 2 2 A
D.50ml 12mol/L盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
【答案】A
【解析】
试题分析: A、H18O与DO的相对分子质量均为20,且所含有中子数均为10个,A正确;
2 2
B、4.4g乙醛为0.1mol,每个乙醛分子6个σ键,应为0.6N ,B错误;C应为0.25 N ,
A A
C错误;D浓盐酸反应变稀且具有挥发性,实际反应的盐酸小于0.6mol,故转移的电子
数小于0.3N ,D错误。选A。
A
考点:阿伏伽德罗常数
6.常温下,将等体积,等物质的量浓度的NH HCO 与NaCl溶液混合,析出部分NaHCO 晶
4 3 3
体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.<1.0×10-7mol/L
B.c(Na+)= c(HCO -)+ c(CO2-)+ c(HCO)
3 3 2 3
C.c(H+)+c(NH+)= c(OH-)+ c(HCO -)+2 c(CO2-)
4 3 3
D.c(Cl-)> c(NH +)> c(HCO -)> c(CO2-)
4 3 3
【答案】C
考点:电解质溶液
7.一定量的 CO 与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO(g)
2 2
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:已知:气体分压(P )=气体总压(P )×体积分数。下列说法正确的是
分 总
A.550℃时,若充入惰性气体,ʋ ,ʋ 均减小,平衡不移动
正 逆
B.650℃时,反应达平衡后CO 的转化率为25.0%
2
C.T℃时,若充入等体积的CO 和CO,平衡向逆反应方向移动
2
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =24.0P
P 总
【答案】B
考点:化学反应速率与化学平衡 化学平衡常数
[来源:gkstk.Com]
8.(13分)X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族
元素;Z和U位于第VIIA族;X和Z可形成化合物XZ ;Q基态原子的s轨道和p轨道
4
的电子总数相等;T的一种单质在空气中能够自燃。
请回答下列问题:
(1)R基态原子的电子排布式是_____________________。
(2)利用价层电子对互斥理论判断TU 的立体构型是______。
3
(3)X所在周期元素最高价氧化物对应的水化物中,酸性最强的是______(填化学式);
Z和U的氢化物中沸点较高的是_____(填化学式);Q、R、U的单质形成的晶体,熔
点由高到低的排列顺序是_______(填化学式)。
(4)CuSO 溶液能用作T 中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应
4 4
的化学方程式是_______________________。
【答案】
(1)1s22s22p63s23p2或者[Ne] 3s23p2
(2)三角锥形
(3)HNO;HF;Si>Mg>Cl
3 2
(4)P+10CuSO+16H O=10Cu+4H PO +10H SO
4 4 2 3 4 2 4考点:元素推断 物质结构、分子结构、晶体结构
9.(13分)(NH )SO 是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
4 2 4
[查阅资料] (NH)SO 在260℃和400℃时分解产物不同。
4 2 4
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)
实验1:连接装置A-B-C-D,检查气密性,按图示加入试剂(装置 B盛0.5000mol/L盐酸
70.00mL)。通入N 排尽空气后,于260℃加热装置A一段时间,停止加热,冷却,停
2
止通入N。品红溶液不褪色,取下装置B,加入指示剂,用0.2000mol/L NaOH溶液滴定
2
剩余盐酸,终点时消耗NaOH溶液25.00 mL。经检验滴定后的溶液中无SO 2-。
4
(1)仪器X的名称是________________。
(2)滴定前,下列操作的正确顺序是_________(填字母编号)。
a.盛装0.2000mol/L NaOH溶液 b.用0.2000mol/L NaOH溶液润洗
c.读数、记录 d.查漏、清洗 e.排尽滴定管尖嘴的气泡并调整液面
(3)装置B内溶液吸收气体的物质的量是__________mol
实验2:连接装置A-D-B,检查气密性,按图示重新加入试剂。通入 N 排尽空气后,于
2
400℃加热装置A至(NH )SO 完全分解无残留物,停止加热,冷却,停止通入N。观察
4 2 4 2
到装置A、D之间的导气管内有少量白色固体。经检验,该白色固体和装置 D内溶液中
有SO 2-,无SO 2-。进一步研究发现,气体产物中无氮氧化物。
3 4
(4)检验装置D内溶液中有SO 2-,无SO 2-的实验操作和现象是__________.
3 4
(5)装置B内溶液吸收的气体是____________.(6)(NH )SO 在400℃分解的化学方程式是______________________.
4 2 4
【答案】
(1)圆底烧瓶
(2)dbaec
(3)0.03 mol
(4)取少量装置D内溶液于试管中,滴加BaCl 溶液,生成白色沉淀;加入足量稀盐酸
2
后沉淀完全溶解,放出无色刺激性气体
(5)NH
3
(6)3(NH )SO △ 4 N H ↑+ N ↑+3SO↑ + 6H O↑
4 2 4 3 2 2 2
(4)取装置D内溶液少许于试管中,加入BaCl 溶液,再加入稀盐酸,若产生白色沉淀
2
且加入盐酸后白色沉淀能完全溶液,则说明原溶液中有SO 2-,无SO 2-
3 4
(5)NH
3
(6)3(NH )SO △ 4 N H ↑+ N ↑+3SO↑ + 6H O
4 2 4 3 2 2 2
考点:实验设计与评价
10.(16分)化合物F(异戊巴比妥)是临床常用的镇静催眠药物,其合成路线如下(部分
反应条件和试剂略);请回答下列问题:
(1)试剂I的化学名称是 ① ,化合物B的官能团名称是 ② ,第④步的化学反应
类型是 ③ 。
[来源:学优高考网gkstk]
(2)第①步反应的化学方程式是 。
(3)第⑤步反应的化学方程式是 。
(4)试剂Ⅱ的相对分子质量为60,其结构简式是 。
(5)化合物B的一种同分异构体G与NaOH溶液共热反应,生成乙醇和化合物H。H
在一定条件下发生聚合反应得到高吸水性树脂,该聚合物的结构简式是 。
【答案】
(1)乙醇,醛基,酯化反应(取代反应)。
(2)
( 3 )
+ C HOH + NaBr
2 5
(4)
(5)
【解析】学优高考网
试题分析: 由题意可知①为卤代烃水解为醇A:CHCHCH(CH OH) ,②为醇催化氧化为醛
3 2 2 2B:
CHCHCH(CHO) ,③为醛催化氧化为羧酸C:CHCHCH(COOH) ,④为羧酸与乙醇发生酯
3 2 2 3 2 2
化反应生成 D:CHCHCH(COOC H) ,⑤为利用信息 1,发生取代反应得 E:
3 2 2 5 2
,⑥为利用信息2,发生取代反应得F,可推知试剂Ⅱ为
CO(NH)。
2 2
考点:有机推断与有机合成
[来源:学优高考网]
11.(16分)为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸
的硫铁矿烧渣(铁主要以Fe O 存在)转变成重要的化工原料FeSO (反应条件略)。
2 3 4
活化硫铁矿还原Fe3+的主要反应为:FeS+7Fe (SO )+8H O=15FeSO +8H SO ,不考虑其他反
2 2 4 3 2 4 2 4
应。请回答下列问题:
(1)第Ⅰ步HSO 与Fe O 反应的离子方程式是 。
2 4 2 3
(2)检验第Ⅱ步中Fe3+是否完全还原,应选择 (填字母编号)。
A.KMnO 溶液 B.K[Fe(CN) ]溶液 C.KSCN溶液
4 3 6
(3)第Ⅲ步加FeCO 调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液 pH降到
3
5.2,此时Fe2+不沉淀,滤液中铝、硅杂质除尽。通入空气引起溶液pH降低的原因
是 。
(4)FeSO 可转化为FeCO,FeCO 在空气中加热反应可制得铁系氧化物材料。
4 3 3 [来源:学优高考网]
已知25℃,101kPa时:4Fe(s) + 3O (g) =2Fe O(s) H =-1648kJ/mol
2 2 3
C(s)+O (g)=CO (g) H =-393kJ/mol
2 2
2Fe(s)+2C(s)+3O (g)=2FeCO (s) H =-1480kJ/mol
2 3
FeCO 在空气中加热反应生成Fe O 的热化学方程式是 。
3 2 3
(5)FeSO 在一定条件下可制得FeS(二硫化亚铁)纳米材料。该材料可用于制造高容量
4 2
锂电池,电池放电时的总反应为4Li+ FeS = Fe +2Li S,正极反应式是 。
2 2
(6)假如烧渣中的铁全部视为Fe O ,其含量为50%。将a kg质量分数为b%的硫酸加
2 3
入到c kg烧渣中浸取,铁的浸取率为96%,其他杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入 FeCO
3
kg。
【答案】
(1)Fe O+6H+=2Fe3++3H O
2 3 2
(2)C
(3)Fe2+被氧化为Fe3+,Fe3+水解产生H+。
(4)4FeCO(s)+O(g) =2Fe O(s)+ 4CO (g) H =-260kJ/mol。
3 2 2 3 2
(5)FeS+4e-= Fe +2S2-
2
(6)-kg。
【解析】学优高考网
试题分析:
(1)Fe O+6H+=2Fe3++3H O
2 3 2
(2)若Fe3+没有完全还原,则可以用KSCN检验。
(3)部分Fe2+被氧化为Fe3+。
(4)根据盖斯定律可得:4FeCO(s)+O(g) =2Fe O(s)+ 4CO (g) H =-260kJ/mol。
3 2 2 3 2
(5)正极得电子,化合价降低,可得正极方程式:FeS+4e- = Fe +2S2-
2
(6)由于最终得到 FeSO ,根据元素守恒,n(Fe)=n(S),Fe 来自于 Fe O 、FeS 、
4 2 3 2
FeCO;S来自于FeS、HSO 则有:
3 2 2 4
( ×2 + ×2×)×96% + = + ×2××2 ×96%
则得答案:-kg。
考点:化学工艺流程 化学反应与能量 元素及化合物 化学计算