文档内容
第 05 讲 化学反应速率
知识导航
小杨老师 15521324728 侵权必究
知识精讲
小杨老师 15521324728 侵权必究
一、化学反应速率的概念及其表示方法
1.定义:衡量化学反应进行_______的物理量。
2.表示方法:单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。
杨sir化学,侵权必究
3.表达式:______________________ 单位: ________________________
二、化学反应速率的测定
资料卡片——除浓度外,反应速率的其他测量量
化学反应速率是可以通过实验测定的。根据化学反应速率表达式,实验中需要测定不同反应时刻
反应物(或生成物)的浓度。实际上任何一种与物质浓度有关的可观测量都可以加以利用,如气体的
体积、体系的压强、颜色的深浅、光的吸收、导电能力等。例如,对于在溶液中进行的反应,当反应
物或生成物本身有比较明显的颜色时,人们常常利用颜色变化与浓度变化间的比例关系来测量反应速
率。
三、“三段式”计算
(1)写出有关反应的化学方程式;
杨sir化学,侵权必究
(2)标出各物质的起始量、变化量、最终量(可用物质的量,也可用浓度);
(3)根据已知条件列方程式计算。
举个例子已知反应:2SO + O 2SO ,4 mol SO 和2 mol O 在2 L的密闭容器中反应2 min 后,SO
2 2 3 2 2 2
的物质的量浓度为1.5 mol/L,求SO 、O、SO 的反应速率。
2 2 3 杨sir化学,侵权必究
思考与交流:比较用SO 、O、SO 表示的反应速率,从中你能得出什么结论?
2 2 3
四、化学反应速率与化学计量数的关系
1.同一反应用不同物质表示化学反应速率时,其数值大小可能不同,但表示的意义相同。
2.对于反应mA(g) + nB(g) === pC(g) + qD(g),当单位相同时,化学反应速率的数值之比等于方程式中
各物质的化学计量数之比,即v (A)∶v (B)∶v (C)∶v (D) = ___________________。
明辨是非
(1)化学反应速率是用来衡量化学反应进行快慢的尺度( )
(2)化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示( )
(3)对任何化学反应来说,反应速率越大,反应现象就越明显( )
(4)在同一个反应中,各物质的反应速率之比等于其化学方程式中的化学计量数之比( )
(5)合成氨的反应中,3v (H ) = 2v (NH ) ( )
2 3
五、化学反应速率的比较方法
1.定性比较
通过观察实验现象,如反应的剧烈程度、产生气泡或沉淀的快慢、固体消失或气体充满所需时间的长短等
来定性判断化学反应的快慢。如K与水反应比Na与水反应剧烈,则反应速率:K>Na。
2.定量比较
杨sir化学,侵权必究
同一化学反应速率用不同物质表示时数值可能不同,比较化学反应速率的快慢不能只看数值大小,还要进
行一定的转化。
(1)“化物质”:将不同物质的化学反应速率转化成同一物质的化学反应速率,或分别除以相应物质的
化学计量数,所得数值大的速率大。
(2)“化单位”:若化学反应速率的单位不一致,需转化为同一单位。对点训练
小杨老师 15521324728 侵权必究
题型一:化学反应速率的含义
杨sir化学,侵权必究
【例1】下列关于化学反应速率的说法正确的是
A.因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的
B.根据化学反应速率的大小可以知道化学反应进行的快慢
C.化学反应速率为“1mol/(L•min)”表示的意思是:时间为1min时,某物质的浓度为1mol/L
D.化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加
【变1-1】化学反应速率(单位可用mol/(L∙s))表示单位时间内反应物或生成物( )
A.体积的变化 B.物质的量的变化
C.质量的变化 D.物质的量浓度的变化
【变1-2】下列对化学反应速率的理解正确的是 ( )
A.化学反应速率表示的是化学反应进行的程度
B.化学反应速率可以用单位时间内反应物浓度的变化来表示
C.化学反应速率可以用任何一种反应物或生成物来表示
D.化学反应速率可以是正值,也可以是负值
题型二:化学反应速率与计量数的关系
杨sir化学,侵权必究
【例2】合成氨的反应为:3H + N 2NH ,其反应的速率可分别表示为v (H )、v (N )、
2 2 3 2 2
v (NH )(单位为),则下列关系正确的是( )
3
A.v (H ) = v (N ) = v (NH ) B.v (H) = 3v (N )
2 2 3 2 2
3
C.v (N ) =2v (NH ) D.v (NH ) = v (H)
2 3 3 2
2【变2-1】已知:4NH (g) + 5O(g) ======= 4NO(g) + 6HO(g),若反应速率分别用v (NH )、v (O )、
3 2 2 3 2
v (NO)、v (H O)表示,则正确的关系是( )
2
A.4/5 v (NH ) = v (O ) B.5/6 v (O ) = v (H O)
3 2 2 2
C.2/3 v (NH ) = v (H O) D.4/5 v (O ) = v (NO)
3 2 2
【变2-2】已知某反应的各物质浓度数据如下:
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是
A.9∶3∶4 B.3∶1∶2 C.2∶1∶3 D.3∶2∶1
题型三:化学反应速率的大小比较
杨sir化学,侵权必究
【例3】对于反应A(g)+2B(g)=3C(s)+2D(g)来说,下列反应速率最快的是( )
A.v(A)=0.32 mol·L-1·min-1 B.v(B)=0.55 mol·L-1·min-1
C.v(C)=0.02 mol·L-1·s-1 D.v(D)=0.01 mol·L-1·s-1
【变3-1】在2A(g)+B(g)=3C(g)+5D(g)反应中,表示该反应速率最快的是( )
杨sir化学,侵权必究
A.v(A)=2mol·L-1·min-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.8mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
【变3-2】反应2A(g)+2B(g)=C(g)+3D(g)在四种不同情况下的反应速率分别为:①v(A)=0.45mol·L-1·min-1
②v(B)=0.6mol·L-1·s-1 ③v(C)=0.4mol·L-1·s-1 ④v(D)=0.5mol·L-1·s-1。该反应进行的快慢顺序为
A.②>④>①>③ B.③>④>②>① C.③>②>④>① D.④>③>②>①
题型四:化学反应速率的计算
杨sir化学,侵权必究
【例4】将4 mol A气体和2 mol B气体在2 L的容器中混合,并在一定条件下发生如下反应:
2A(g) + B(g) 2C(g),若90 s后测得A的浓度为1 mol/L,物质A表示的反应速率正确的是( )
A.2 mol/(L·min) B.0.67 mol/(L·min)
C.1 mol/(L·min) D.0.5 mol/(L·min)【变4-1】某反应2A(g)+B(g) C(g)经10s后A的物质的量浓度为0.2mol/L,B的物质的量浓度降低了
0.02mol/L,则A物质的起始浓⇌度为
A.0.24 mol/L B.0.6 mol/L C.2.4 mol/L D.4.2 mol/L
【变4-2】在N + 3H 2NH 的反应中,经过一段时间后,NH 的浓度增加了0.6 mol/L。在此
2 2 3 3
时间内,用H 表示的平均反应速率为0.45 mol /(L·s),反应所经过的时间是( )
2
A.0.44 s B.1 s C.1.33 s D.2 s
【变4-3】把0.6 mol气体X和0.4 mol气体Y混合于2.0 L的密闭容器中,发生如下反应:3X(g)+Y(g)
nZ(g)+2W(g),测得5 min末生成0.2 mol W,又知以Z表示的平均反应速率为0.01 mol·L-1·min-1,则
n值是
A.1 B.2
C.3 D.4
杨sir化学,侵权必究
【变4-4】在一密闭的2L容器中装有4molSO 和2molO ,在一定条件下开始反应。2min末测得容器中有
2 2
1.6molSO ,请计算:
2
(1)2min末SO 的浓度_______;
3
(2)2min内SO 的平均反应速率_______。
2
(3)2min内O 的转化率_______。
2
题型五:“三段式”的计算
【例5】一定温度下,向2L恒容密闭容器中充入0.4molNH 和0.5molO 发生反应4NH (g)+5O(g)
3 2 3 2
4NO(g)+6H O(g)。4min后,NO的浓度为0.06mol·L-1。下列有关说法错误的是( ) ⇌
2
A.4min末,用NO表示的反应速率为0.03mol·L-1·min-1
B.4min末,NH 的浓度为0.14mol·L-1
3
C.0~4min内,生成的水的质量为3.24g
杨sir化学,侵权必究
D.0~4min内,O 的物质的量减少了0.15mol
2【变5-1】将6 mol A气体和5 mol B气体混合放入4 L密闭容器中,发生下列反应:3A (g) + B (g)
2C (g) + xD (g) ,经过5 min达到化学平衡,此时生成C为2 mol,测得D的反应速率为0.1
mol/(L·min),计算:① x的值;②平衡时B的转化率;③A的平衡浓度。
【变5-2】已知一氧化碳与水蒸气的反应为:CO(g) + H O (g) CO(g) + H (g) ,800℃时,在容积为
2 2 2
2.0 L的密闭容器中充入2.0 mol CO(g)和3.0 mol H O(g),保持温度不变,4 min后反应达到平衡,测得CO
2
的转化率为60%。求(1)4 min内H 的平均化学反应速率;(2)平衡时HO (g)的物质的量。
2 2
题型六:化学反应速率与图像
杨sir化学,侵权必究
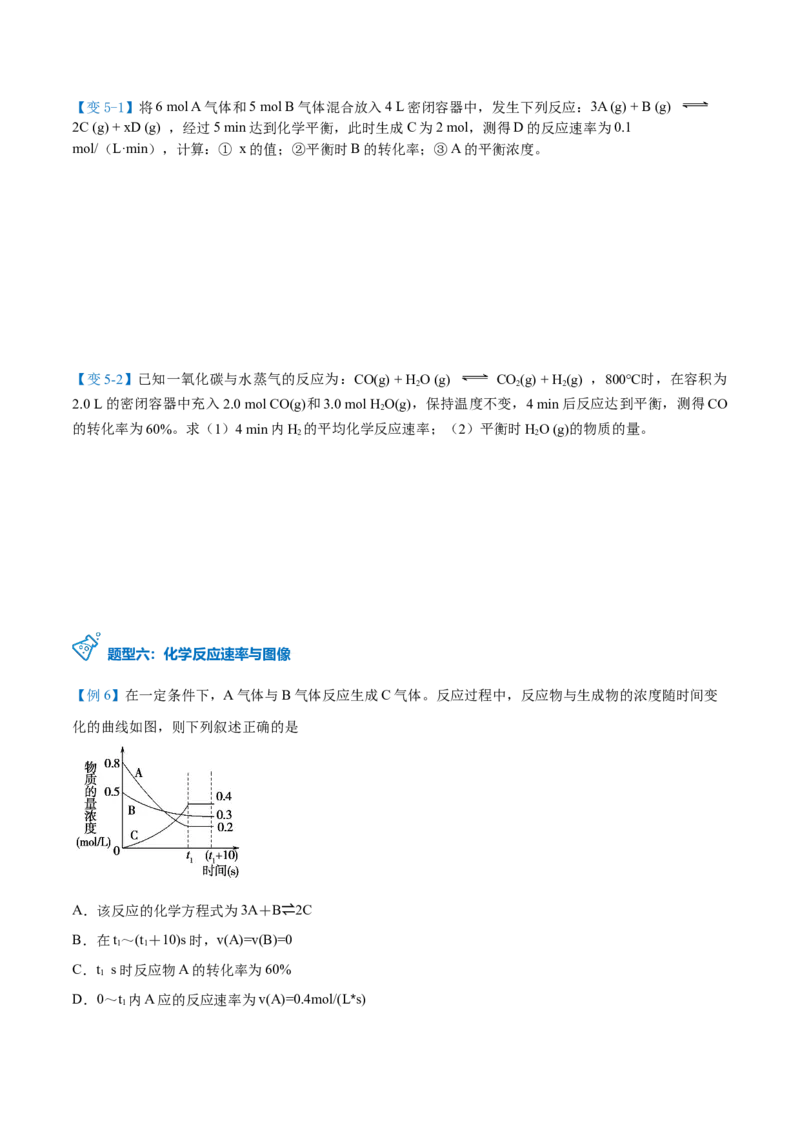
【例6】在一定条件下,A气体与B气体反应生成C气体。反应过程中,反应物与生成物的浓度随时间变
化的曲线如图,则下列叙述正确的是
A.该反应的化学方程式为3A+B⇌2C
B.在t~(t +10)s时,v(A)=v(B)=0
1 1
C.t s时反应物A的转化率为60%
1
D.0~t 内A应的反应速率为v(A)=0.4mol/(L*s)
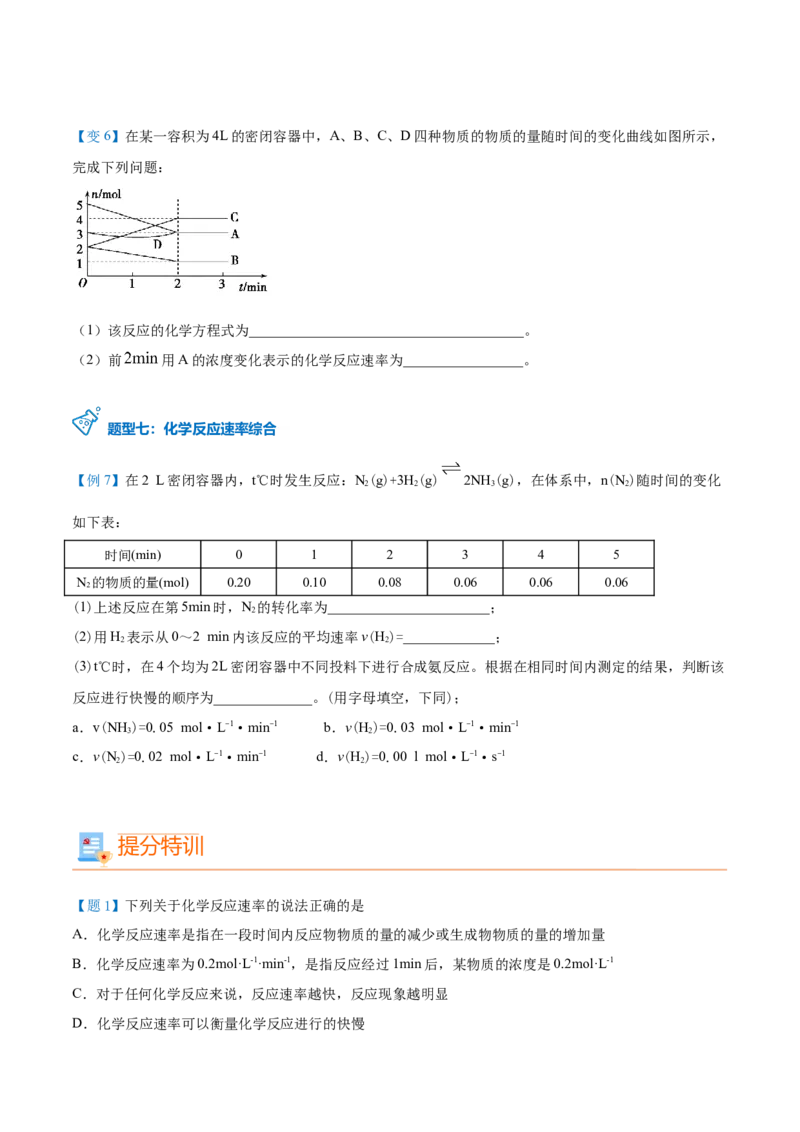
1【变6】在某一容积为4L的密闭容器中,A、B、C、D四种物质的物质的量随时间的变化曲线如图所示,
完成下列问题:
(1)该反应的化学方程式为_______________________________________。
(2)前 用A的浓度变化表示的化学反应速率为_________________。
题型七:化学反应速率综合
杨sir化学,侵权必究
【例7】在2 L密闭容器内,t℃时发生反应:N(g)+3H(g) 2NH (g),在体系中,n(N)随时间的变化
2 2 3 2
如下表:
时间(min) 0 1 2 3 4 5
N 的物质的量(mol) 0.20 0.10 0.08 0.06 0.06 0.06
2
(1)上述反应在第5min时,N 的转化率为_______________________;
2
(2)用H 表示从0~2 min内该反应的平均速率v(H)=_____________;
2 2
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该
反应进行快慢的顺序为______________。(用字母填空,下同);
a.v(NH )=0.05 mol·L-1·min-1 b.v(H)=0.03 mol·L-1·min-1
3 2
c.v(N)=0.02 mol·L-1·min-1 d.v(H)=0.00 l mol·L-1·s-1
2 2
提分特训
小杨老师 15521324728 侵权必究
【题1】下列关于化学反应速率的说法正确的是
A.化学反应速率是指在一段时间内反应物物质的量的减少或生成物物质的量的增加量
B.化学反应速率为0.2mol·L-1·min-1,是指反应经过1min后,某物质的浓度是0.2mol·L-1
C.对于任何化学反应来说,反应速率越快,反应现象越明显
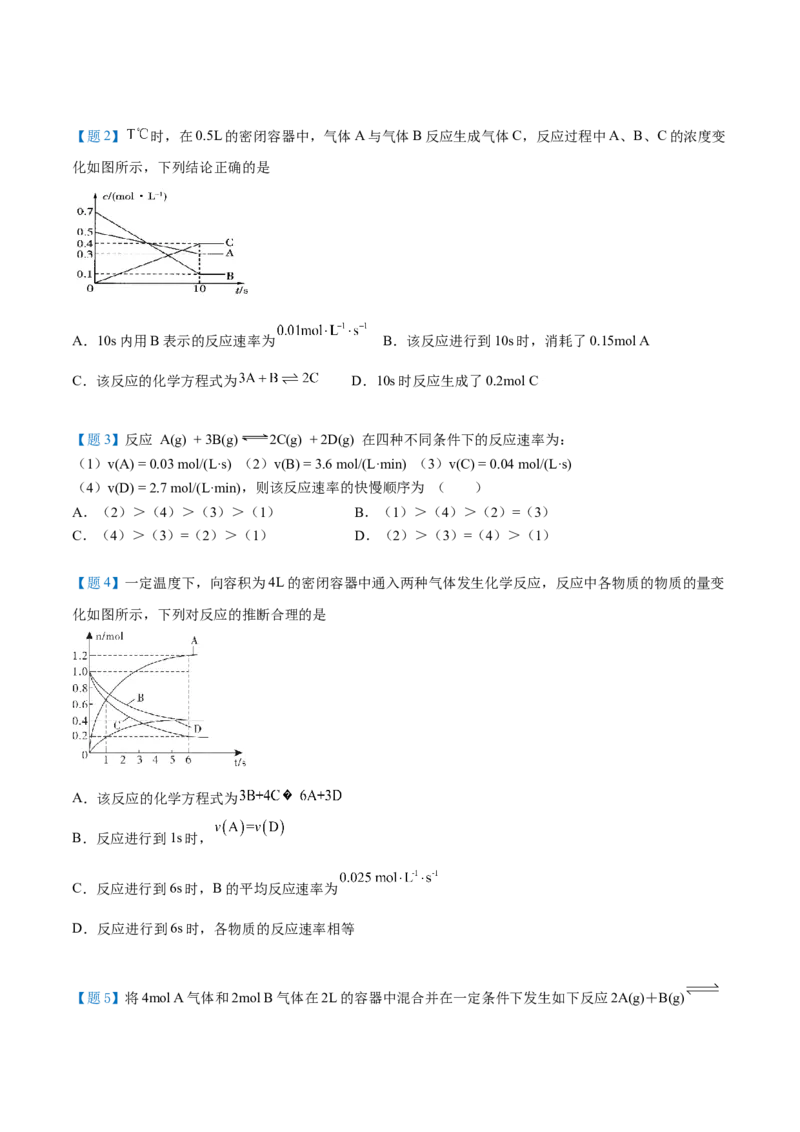
D.化学反应速率可以衡量化学反应进行的快慢【题2】 时,在0.5L的密闭容器中,气体A与气体B反应生成气体C,反应过程中A、B、C的浓度变
化如图所示,下列结论正确的是
A.10s内用B表示的反应速率为 B.该反应进行到10s时,消耗了0.15mol A
C.该反应的化学方程式为 D.10s时反应生成了0.2mol C
杨sir化学,侵权必究
【题3】反应 A(g) + 3B(g) 2C(g) + 2D(g) 在四种不同条件下的反应速率为:
(1)v(A) = 0.03 mol/(L·s) (2)v(B) = 3.6 mol/(L·min) (3)v(C) = 0.04 mol/(L·s)
(4)v(D) = 2.7 mol/(L·min),则该反应速率的快慢顺序为 ( )
A.(2)>(4)>(3)>(1) B.(1)>(4)>(2)=(3)
C.(4)>(3)=(2)>(1) D.(2)>(3)=(4)>(1)
【题4】一定温度下,向容积为4L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变
化如图所示,下列对反应的推断合理的是
A.该反应的化学方程式为
B.反应进行到1s时,
C.反应进行到6s时,B的平均反应速率为
D.反应进行到6s时,各物质的反应速率相等
【题5】将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应2A(g)+B(g)2C(g)若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3
②2s时物质A的转化率为70%
杨sir化学,侵权必究
③2s时物质B的浓度为0.7mol/L
④用物质B表示的反应的平均速率为0.6mol·L-1·s-1
其中正确的是
A.①④ B.①③ C.②③ D.③④
【题6】在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,
请填写下列空⇌白:
(1)x值等于_______。
(2)A的转化率为_______。
(3)生成D的反应速率为_______。
(4)平衡时物质C的体积分数是_______。
杨sir化学,侵权必究
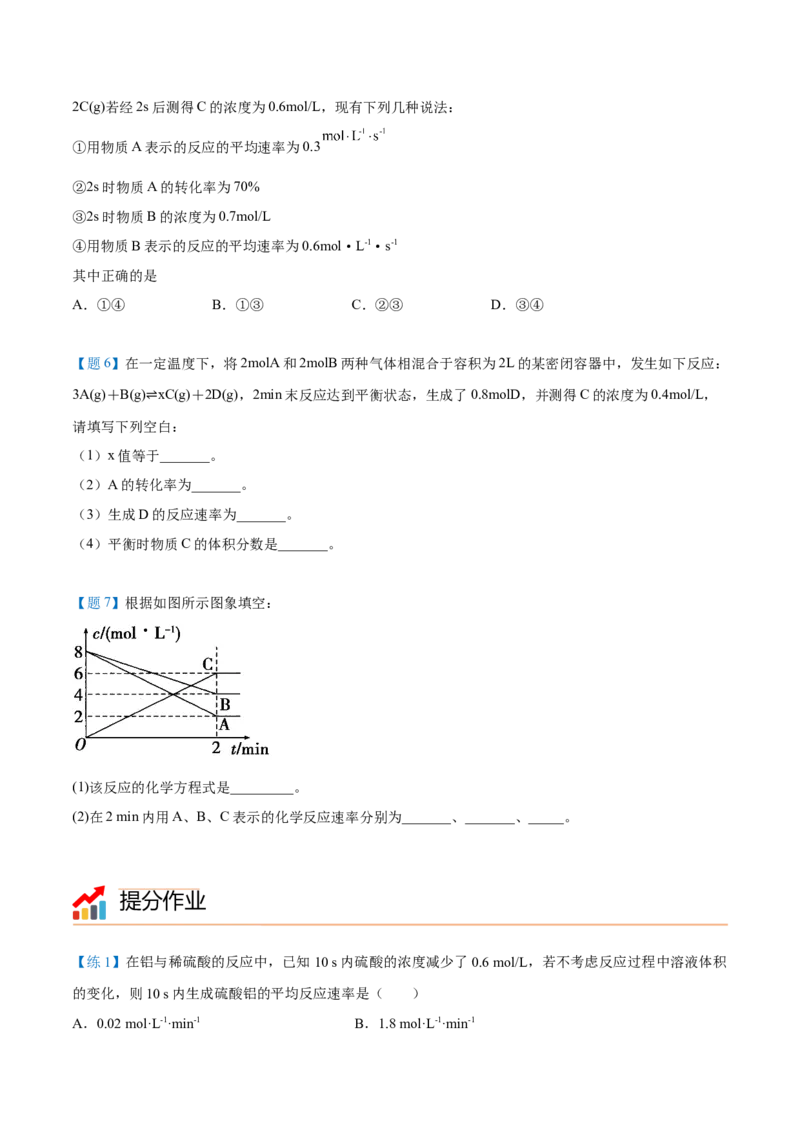
【题7】根据如图所示图象填空:
(1)该反应的化学方程式是_________。
杨sir化学,侵权必究
(2)在2 min内用A、B、C表示的化学反应速率分别为_______、_______、_____。
提分作业
小杨老师 15521324728 侵权必究
【练1】在铝与稀硫酸的反应中,已知10 s内硫酸的浓度减少了0.6 mol/L,若不考虑反应过程中溶液体积
的变化,则10 s内生成硫酸铝的平均反应速率是( )
A.0.02 mol·L-1·min-1 B.1.8 mol·L-1·min-1C.1.2 mol·L-1·min-1 D.0.18 mol·L-1·min-1
【练2】下列关于化学反应速率的说法,不正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率的大小主要取决于反应物的性质
C.化学反应速率可以用单位时间内生成某物质的质量的多少来表示
D.化学反应速率常用单位有mol·L-1·s-1和mol·L-1·min-1
【练3】在mA+nB=pC的反应中,(m、n、p为各物质的化学计量数)现测得C每分钟增加2mol·L-1,B每
分钟减少1.5mol·L-1,A每分钟减少0.5mol·L-1,则m:n:p为
A.1:3:4 B.4:3:1 C.2:3:2 D.2:2:3
杨sir化学,侵权必究
【练4】反应:3A(g)+B(g)=2C(g)+2D(g),在不同条件下,用不同物质表示其反应速率,分别为
①v(A)=0.6mol·L-1·min-1
②v(B)=0.45mol·L-1·min-1
③v(C)=0.15mol·L-1·min-1
④v(D)=0.45mol·L-1·min-1
则此反应在不同条件下进行快慢顺序正确的是
A.①>②>③>④ B.①>②=④>③ C.②>④>③>① D.②>④>①>③
【练5】反应4A(s)+3B(g)=2C(g)+D(g),经2min,B的浓度减少0.6mol·L-1。对此反应速率的表示,正确的
是
A.用A表示的反应速率是0.4mol·(L·min)-1
B.分别用B、C、D表示反应的速率,其比是3:2:1
C.在2min末的反应速率,用B表示是0.3mol·(L·min)-1
D.在这2min内用B和C表示的反应速率的值都是逐渐减小的
杨sir化学,侵权必究
【练6】一定温度下,向2L恒容密闭容器中充入0.4molNH 和0.5molO 发生反应4NH (g)+5O(g) 4NO(g)
3 2 3 2
+6H O(g)。2min后,NO的浓度为0.06mol·L-1。下列有关说法不正确的是 ⇌
2
A.2min末,用NO表示的反应速率为0.06mol·L-1·min-1
B.2min末,NH 的浓度为0.14mol·L-1
3C.0~2min内,生成的水的质量为3.24g
D.0~2min内,O 的物质的量减少了0.15mol
2
【练7】把0.6molX气体和0.6molY气体混合于2L的密闭容器中,使它们发生反应3X(g)+Y(g) nZ(g)
+2W(g),5min末生成0.2molW。若测知以Z的浓度变化表示的平均反应速率为0.01mol·L-1·min-1,则化学
方程式中的n值为
A.1 B.2 C.3 D.4
杨sir化学,侵权必究
【练8】将等物质的量A、B混合于2L的密闭容器中,发生反应: ,经
5min后测得D的浓度为0.5mol/L, ,C的平均反应速率是 。
(1)经5min后A的浓度为_______。
(2)反应开始前充入容器中的B的物质的量为_______。
(3)B的平均反应速率为_______。
(4)x的值为_______。
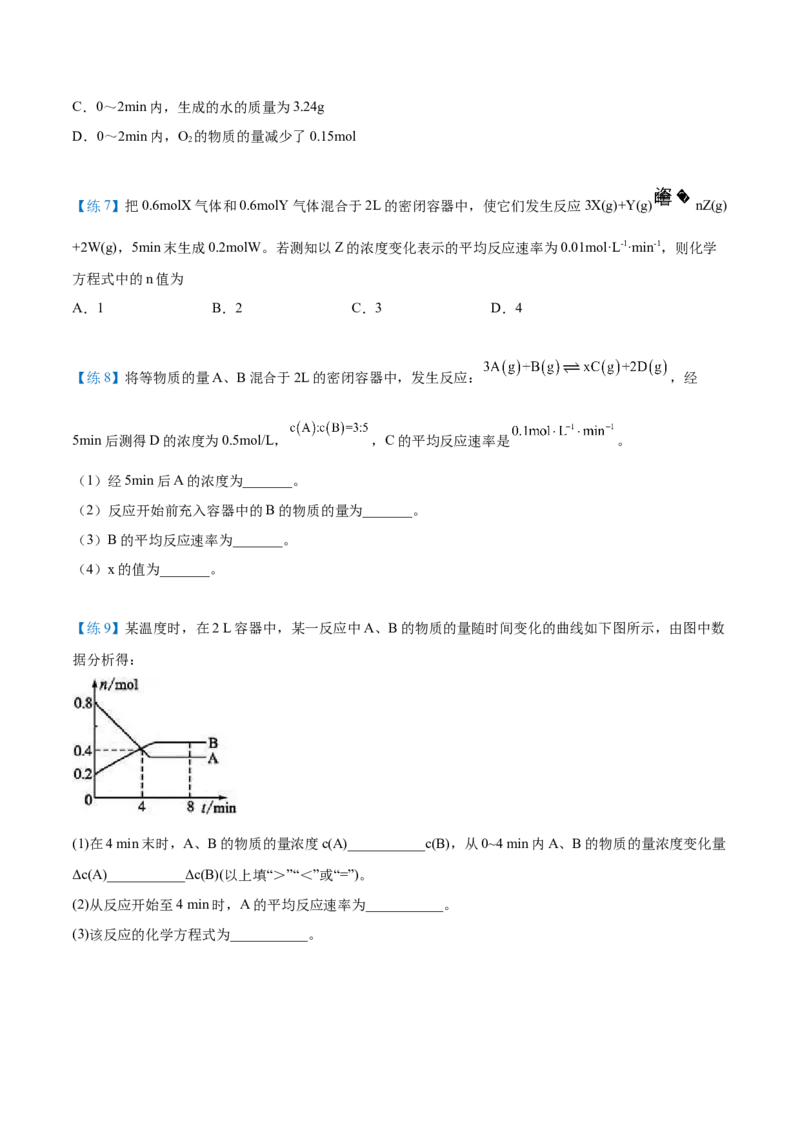
【练9】某温度时,在2 L容器中,某一反应中A、B的物质的量随时间变化的曲线如下图所示,由图中数
据分析得:
(1)在4 min末时,A、B的物质的量浓度c(A)___________c(B),从0~4 min内A、B的物质的量浓度变化量
Δc(A)___________Δc(B)(以上填“>”“<”或“=”)。
杨sir化学,侵权必究
(2)从反应开始至4 min时,A的平均反应速率为___________。
(3)该反应的化学方程式为___________。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育