文档内容
7.进行化学实验时应强化安全意识。下列做法正确的是:
A.金属钠着火时使用泡沫灭火器灭火
B.用试管加热碳酸氢钠固体时使试管口竖直向上
C.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗
D.制备乙烯时向乙醇和浓硫酸的混合液中加入碎瓷片
【答案】D
8.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知YW的原子充
数之和是Z的3倍,下列说法正确的是
A.原子半径:XZ X W
C.Z、W均可与Mg形成离子化合物
D.最高价氧化物对应水化物的酸性:Y>W
【答案】C
【解析】
试题分析:设元素Y的原子序数为y,则y+y+10=3×(y+1),解得y=7,则Y为N元素、X
为Si元素、Z为O元素、W为Cl元素。A、原子半径:Zc(A—)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)= c(A—)+ c(HA)
D.b点所示溶液中c(A—)> c(HA)
【答案】D
【解析】
试题分析:A、a点NaOH与HA恰好完全反应,溶液的pH为8.7,呈碱性,说明HA为弱酸,
NaA发生水解反应,c(Na+)>c(A-)>c(HA)>c(H+),错误;B、a点NaA发生水解反应,促进
了水的电离,所以a点水的电离程度大于b点,错误;C、根据电荷守恒,c(H+)+c(Na+)=c(OH‾)+c(A-),pH=7,则c(H+)=c(OH‾),则c(Na+)= c(A-),错
误;D、b点HA过量,溶液呈酸性,HA的电离程度大于NaA的水解程度,所以c
(A-)>c(HA),正确。
考点:电解质溶液
29.(15分)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧
化物可通过处理钴渣获得。
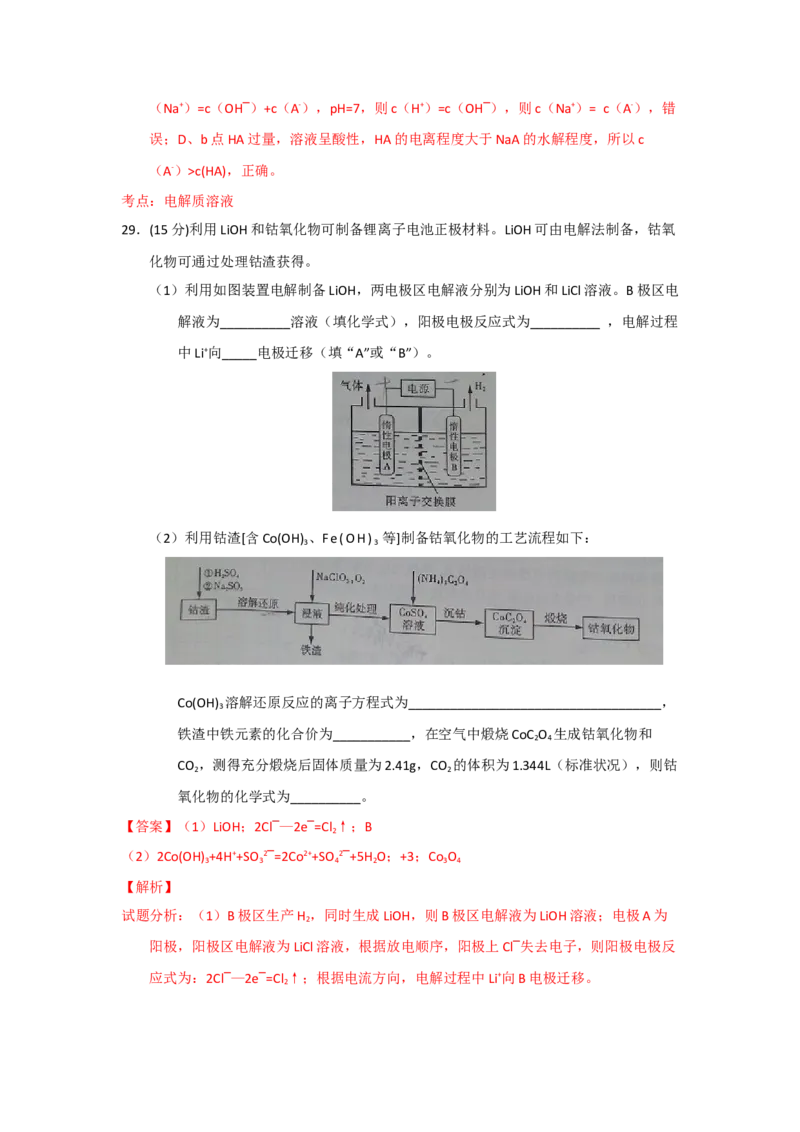
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电
解液为__________溶液(填化学式),阳极电极反应式为__________ ,电解过程
中Li+向_____电极迁移(填“A”或“B”)。
(2)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为____________________________________,
3
铁渣中铁元素的化合价为___________,在空气中煅烧CoC O 生成钴氧化物和
2 4
CO ,测得充分煅烧后固体质量为2.41g,CO 的体积为1.344L(标准状况),则钴
2 2
氧化物的化学式为__________。
【答案】(1)LiOH;2Cl‾—2e‾=Cl ↑;B
2
(2)2Co(OH) +4H++SO 2‾=2Co2++SO 2‾+5H O;+3;Co O
3 3 4 2 3 4
【解析】
试题分析:(1)B极区生产H ,同时生成LiOH,则B极区电解液为LiOH溶液;电极A为
2
阳极,阳极区电解液为LiCl溶液,根据放电顺序,阳极上Cl‾失去电子,则阳极电极反
应式为:2Cl‾—2e‾=Cl ↑;根据电流方向,电解过程中Li+向B电极迁移。
2(2)在酸性条件下,Co(OH) 首先与H+反应生成Co3+,Co3+具有氧化性,把SO 2‾氧化为
3 3
SO 2‾,配平可得离子方程式:2Co(OH) +4H++SO 2‾=2Co2++SO 2‾+5H O;铁渣中铁元素的
4 3 3 4 2
化合价应该为高价,为+3价;CO 的物质的量为:1.344L÷22.4L/mol=0.06mol,根据
2
CoC O 的组成可知Co元素物质的量为0.03mol,设钴氧化物的化学式为CoO,根据元
2 4 x y
素的质量比可得:59x:16y=0.03mol×59g/mol:(2.41g—0.03mol×59g/mol),解得
x:y=3:4,则钴氧化物的化学式为:Co O 。
3 4
考点:电化学、氧化还原反应、工艺流程
30.(19分)合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。
(1)一定温度下,某贮氢合金(M)的贮氢过程如图所示,纵轴为平衡时氢气的压强
(p),横轴表示固相中氢原子与金属原子的个数比(H/M)。
在OA段,氢溶解于M中形成固溶体MH,随着氢气压强的增大,H/M逐惭增大;
x
在AB段,MH 与氢气发生氢化反应生成氢化物MH,氢化反应方程式为:zMH(s)
x y x
+H2(g)==ZMH(s) △H(Ⅰ);在B点,氢化反应结束,进一步增大氢气压强,H/M
y
几乎不变。反应(Ⅰ)中z=_____(用含x和y的代数式表示)。温度为T 时,2g
1
某合金4min内吸收氢气240mL,吸氢速率v=______mL•g-1•min。反应的焓变
△H _____0(填“>”“<”或“=”)。
Ⅰ
(2)η表示单位质量贮氢合金在氢化反应阶段的最大吸氢量占其总吸氢量的比例,
则温度为T1、T2时,η(T )____ η(T )(填“>”“<”或“=”)。当反应
1 2
(Ⅰ)处于图中a点时,保持温度不变,向恒容体系中通入少量氢气,达到平衡
后反应(Ⅰ)可能处于图中的_____点(填“b”“c”或“d”),该贮氢合金可通过
______或_______的方式释放氢气。
(3)贮氢合金ThNi 可催化由CO、H 合成CH 的反应,温度为T时,该反应的热化学
5 2 4
方程式为_________。已知温度为T时:CH (g)+2H O=CO (g)+4H (g)
4 2 2 2
△H=+165KJ•mol
CO(g)+H O(g)=CO (g)+H (g) △H=-41KJ•mol
2 2 2
【答案】(1)2/(y—x);30;<
(2)>;c;加热 减压(3)CO(g)+3H (g)=CH (g)+H O(g) ∆H=—206kJ•mol‾1
2 4 2
【解析】
31.(19分)毒重石的主要成分BaCO (含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒
3
重石制备BaCl ·2H O的流程如下:
2 2
(1)毒重石用盐酸浸取前需充分研磨,目的是 。实验室用37%的盐酸配置15%的
盐酸,除量筒外还需使用下列仪器中的 。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
Ca2+ Mg2+ Fe3+
开始沉淀时的pH 11.9 9.1 1.9
完全沉淀时的pH 13.9 11.1 3.2
加入NH ·H O调节pH=8可除去 (填离子符号),滤渣Ⅱ中含 (填
3 2
化学式)。加入H C O 时应避免过量,原因是 。
2 2 4
已知:Ksp(BaC O )=1.6×10-7,Ksp(CaC O )=2.3×10-9
2 4 2 4
(3)利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO 2—+2H+=Cr O 2—+H 0 Ba2++CrO 2—=BaCrO ↓
4 2 7 2 4 4
步骤Ⅰ 移取xml一定浓度的Na CrO 溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-
2 4
1盐酸标准液滴定至终点,测得滴加盐酸体积为V mL。
0步骤Ⅱ:移取y mLBaCl 溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na CrO 溶
2 2 4
液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,
测得滴加盐酸的体积为V mL。
1
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的 (填“上方”
或“下方”)。BaCl 溶液的浓度为 mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待
2
测液溅出,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
【答案】(1)增大接触面积从而使反应速率加快;ac
(2)Fe3+;Mg(OH) 、Ca(OH) ;H C O 过量会导致生成BaC O 沉淀,产品的产量减少。
2 2 2 2 4 2 4
(3)上方;(V b—V b)/y;偏小。
0 1
【解析】
试题分析:(1)充分研磨可以增大反应物的接触面积,增大反应速率;因为配制的盐酸溶
液浓度为质量分数,可以计算出浓盐酸的体积和水的体积,所以使用烧杯作为容器稀
释,玻璃杯搅拌。
(2)根据流程图和表中数据,加入NH•HO调pH为8,只有Fe3+完全沉淀,故可除去
3 2
Fe3+;加入NaOH调pH=12.5,Mg2+也完全沉淀,Ca2+部分沉淀,所以滤渣Ⅱ中含
Mg(OH) 、Ca(OH) ;根据Ksp(BaC O )=1.6×10-7,H C O 过量时Ba2+转化为BaC O 沉淀,
2 2 2 4 2 2 4 2 4
BaCl ·2H O产品的产量减少。
2 2
(3)“0”刻度位于滴定管的上方;与Ba2+反应的CrO 2‾的物质的量为(V b—V b)/
4 0 1
1000mol,则Ba2+浓度为(V b—V b)/y;根据计算式,若步骤Ⅱ中滴加盐酸时有少量
0 1
待测液溅出,V 减小,则Ba2+浓度测量值将偏大。
1
考点:工艺流程
32.(12分)[化学---化学与技术]
工业上利用氨氧化获得的高浓度NOx气体(含NO、NO )制备NaNO 、NaNO ,工艺流程
2 2 3
如下:已知:Na CO +NO+NO =2NaNO +
2 3 2 2 CO2
(1)中和液所含溶质除NaNO 及少量Na CO 外,还有__________(填化学式)。
2 2 3
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。
蒸发Ⅰ产生的蒸气中含有少量的NaNO 等有毒物质,不能直接排放,将其冷凝后
2
用于流程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO 的目的是_______。母液Ⅱ需回收利用,下列处理
3
方法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作 c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO 、NaNO 两种产品的物质的量之比设为2:1,则生产1.38吨NaNO
2 3 2
时,Na CO 的理论用量为______吨(假定Na CO 恰好完全反应)。
2 3 2 3
【答案】(1)NaNO
3
(2)防止NaNO 的析出;溶碱
2
(3)将NaNO 氧化为NaNO ;c、d;
2 2
(4)1.59
【解析】
试题分析:(1)NO 与碱液反应可生成NaNO 。
2 3
(2)浓度过大时,NaNO 可能会析出;NaNO 有毒,不能直接排放,回收后可用于流程中
2 2
的溶碱。
(3)NaNO 在酸性条件下易被氧化,加入稀硝酸可提供酸性环境;母液Ⅱ的溶质主要是
2
NaNO ,所以回收利用时应转入转化液,或转入结晶Ⅱ操作,故c、d正确。
3
(4)1.38吨NaNO 的物质的量为:1.38×106÷69g/mol=2×104mol,则生成的NaNO 物质
2 3
的量为:1×104mol,故Na CO 的理论用量=1/2×(2×104+1×104)mol×106g/
2 3
mol=1.59×106g=1.59吨。
考点:化学与技术
33.(12分)[化学---物质结构与性质]
氟在自然界中常以CaF 的形式存在。
2
(1)下列关于CaF 的表述正确的是_______。
2
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF 的熔点高于CaCl
2 2
c.阴阳离子比为2:1的物质,均与CaF 晶体构型相同
2
d.CaF 中的化学键为离子键,因此CaF 在熔融状态下能导电
2 2(2)CaF 难溶于水,但可溶于含Al3+的溶液中,原因是________(用离子方程式表示)。
2
已知AlF 3-在溶液中可稳定存在。
6
(3)F 通入稀NaOH溶液中可生成OF ,OF 分子构型为______________,其中氧原子的
2 2 2
杂化方式为_________。
(4)F 与其他卤素单质反应可以形成卤素互化物,例如ClF 、BrF 等。已知反应Cl (g)+
2 3 3 2
3F (g)=2ClF (g) △H=-313kJ·mol-1,F-F键的键能为159kJ·mol-1,Cl-Cl键的键能为
2 3
242kJ·mol-1,则ClF 中Cl-F键的平均键能为______kJ·mol-1。ClF 的熔、沸点比BrF
3 3 3
的________(填“高”或“低”)。
【答案】(1)bd
(2)Al3++3CaF = 3Ca2++AlF 3-
2 6
(3)角形或V形;sp3。
(4)172;低。
【解析】
考点:物质结构与性质
34.(12分)[化学---有机化学基础]
菠萝酯F是一种具有菠萝香味的赋香剂,其合成路线如下:(1)A的结构简式为_________________,A中所含官能团的名称是_________。
(2)由A生成B的反应类型是______________,E的某同分异构体只有一种相同化学环
境的氢,该同分异构体的结构简式为_________________。
(3)写出D和E反应生成F的化学方程式________________________。
(4)结合题给信息,以溴乙烷和环氧乙烷为原料制备1-丁醇,设计合成路线(其他试
剂任选)。
【答案】(1) ,碳碳双键、醛基。
O
(2)加成(或还原)反应;CH C CH ,
3 3
(3) —(CH ) COOH+CH =CHCH OH —(CH ) COO CH CH= CH +H O
2 2 2 2 2 2 2 2 2
(4)CH3CH2Br CH3CH2MgBr CH3CH2CH2CH2OH
【解析】
试题分析:(1)根据题目所给信息,1,3-丁二烯与丙烯醛反应生成 ,根
据结构简式可知该有机物含有碳碳双键和醛基。(2)A中碳碳双键和醛基与H 发生加成反应;根据有机合成路线E为CH =CHCH OH,
2 2 2
E的某同分异构体只有一种相同化学环境的氢,该同分异构体的结构简式为:CH
3
O
C CH 。
3
(3)D和E反应生成F为酯化反应,化学方程式为:
—(CH ) COOH+CH =CHCH OH —(CH ) COO CH CH= CH +H O
2 2 2 2 2 2 2 2 2
(4)根据题目所给信息,溴乙烷与Mg在干醚条件下反应生成CH CH MgBr,
3 2
条件下反应即可生成1-丁醇,合成路线为:
CH CH MgBr与环氧乙烷在H+
3 2
CH3CH2Br CH3CH2MgBr CH3CH2CH2CH2OH。
考点:有机推断与有机合成