文档内容
2019 年天津市高考化学试卷解析版 D 氧化亚铁溶于稀硝酸 FeO+2H+═Fe2++H O
2
A.A B.B C.C D.D
参考答案与试题解析
【考点】49:离子方程式的书写.
一、选择题(共6小题,每小题6分,满分36分)
菁优网版权所有
【分析】A.NH +水解导致溶液呈酸性,Mg(OH) 能溶于酸;
1.(6分)化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( ) 4 2
B.得到的是胶体,胶体不是沉淀;
A.利用废弃的秸秆生产生物质燃料乙醇
C.转移电子不守恒;
B.利用石油生产塑料、化纤等高分子材料
D.亚铁离子易被氧化生成铁离子。
C.利用基本的化学原料生产化学合成药物
【解答】解:A.NH +水解导致溶液呈酸性,Mg(OH) 能溶于酸,离子方程式为 Mg(OH) +2NH +═
D.利用反渗透膜从海水中分离出淡水 4 2 2 4
Mg2++2NH •H O,故A正确;
【考点】18:物理变化与化学变化的区别与联系. 3 2
菁优网版权所有
B.得到的是胶体,胶体不是沉淀,所以不能写沉淀符号,离子方程式为Fe3++3H O═Fe(OH) (胶体)
【分析】A.秸秆通过发酵生成乙醇; 2 3
+3H+,故B错误;
B.石油生产塑料、化纤,裂化生成小分子,小分子发生加聚反应生成高分子;
C.二者发生氧化还原反应生成锰离子、硫酸,转移电子不守恒,离子方程式为 5SO +2MnO ﹣+2H O═
C.基本的化学原料生产化学合成药物,发生有机反应生成新物质; 2 4 2
5SO 2﹣+2Mn2++4H+,故C错误;
D.利用反渗透膜从海水中分离出淡水,无新物质生成。 4
D.亚铁离子易被氧化生成铁离子,离子方程式为3FeO+10H++NO ﹣═3Fe3++NO↑+5H O,故D错误;
【解答】解:A.秸秆通过发酵生成乙醇,为化学变化,故A不选; 3 2
故选:A。
B.石油生产塑料、化纤,裂化生成小分子,小分子发生加聚反应生成高分子,为化学变化,故B不选;
【点评】本题考查离子方程式正误判断,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的
C.基本的化学原料生产化学合成药物,发生有机反应生成新物质,为化学变化,故C不选;
关键,侧重复分解反应、氧化还原反应的考查,注意电子、电荷守恒的应用,选项BD为解答的易错点,题
D.利用反渗透膜从海水中分离出淡水,无新物质生成,是物理变化,故D选;
目难度不大。
故选:D。
3.(6分)下列有关金属及其化合物的应用不合理的是( )
【点评】本题考查化学变化与物理变化,为基础性习题,把握物质的性质、发生的反应为解答的关键,侧重
A.将废铁屑加入FeCl 溶液中,可用于除去工业废气中的Cl
分析与应用能力的考查,注意新物质的判断,题目难度不大。 2 2
B.铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
2.(6分)下列离子方程式能用来解释相应实验现象的是( )
C.盐碱地(含较多Na CO 等)不利于作物生长,可施加熟石灰进行改良
实验现象 离子方程式 2 3
D.无水CoCl 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
2
A 向氢氧化镁悬浊液中滴加氯化铵溶 Mg(OH) +2NH +═Mg2++2NH •H O
2 4 3 2
【考点】GR:常见金属元素的单质及其化合物的综合应用.
液,沉淀溶解 菁优网版权所有
【分析】A.氯气具有强氧化性,能氧化亚铁离子生成铁离子,铁离子能氧化Fe生成亚铁离子;
B 向沸水中滴加饱和氯化铁溶液得到红 Fe3++3H O═Fe(OH) ↓+3H+
2 3
B.Li﹣Al合金密度较小且硬度及强度大;
褐色液体
C.熟石灰成分为氢氧化钙,具有碱性;
C 二氧化硫使酸性高锰酸钾溶液褪色 3SO +2MnO ﹣+4H+═3SO 2﹣+2Mn2++2H O
2 4 4 2
D.无水CoCl 呈蓝色,吸水会变为粉红色。
2【解答】解:A.氯气具有强氧化性,能氧化亚铁离子生成铁离子,铁离子能氧化Fe生成亚铁离子,涉及的 误;
反应为2Fe2++Cl =2Fe3++2Cl﹣、2Fe3++Fe=3Fe2+,从而除去氯气,故A正确; D.得到的乙炔中含有硫化氢等气体,硫化氢等气体也能使溴水褪色,应该先将得到的气体通入硫酸铜溶液
2
B.Li﹣Al合金密度较小且硬度及强度大,所以Li﹣Al合金可以用于航空工业,故B正确; 除去杂质,然后将得到的气体通入溴水检验乙炔,故D错误;
C.熟石灰成分为氢氧化钙,具有碱性,碳酸钠水解导致其水溶液呈碱性,所以盐碱地中加入熟石灰不能改 故选:B。
良土壤,通过施加适量石膏粉末(主要含有CaSO ,微溶于水)来降低土壤的碱性,故C错误; 【点评】本题考查化学实验方案评价,涉及气体收集、溶液配制、气体检验等知识点,明确化学反应原理、
4
D.无水CoCl 呈蓝色,吸水会变为粉红色,如果变色硅胶中加入CoCl ,可以根据变色硅胶颜色变化判断 元素化合物性质、实验规则是解本题关键,D为解答易错点。
2 2
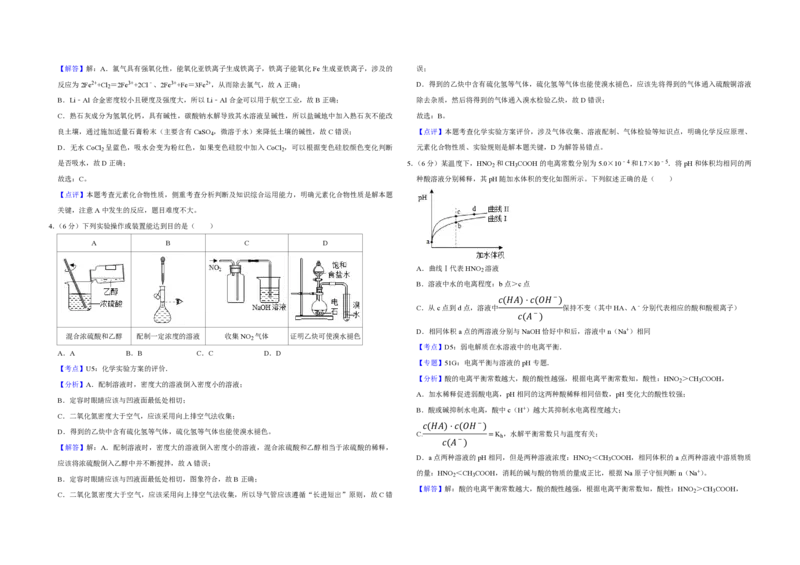
是否吸水,故D正确; 5.(6分)某温度下,HNO 和CH COOH的电离常数分别为5.0×10﹣4和l.7×l0﹣5.将pH和体积均相同的两
2 3
故选:C。 种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
【点评】本题考查元素化合物性质,侧重考查分析判断及知识综合运用能力,明确元素化合物性质是解本题
关键,注意A中发生的反应,题目难度不大。
4.(6分)下列实验操作或装置能达到目的是( )
A B C D
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
‒
𝑐(𝐻𝐴) ⋅ 𝑐(𝑂𝐻 )
C.从c点到d点,溶液中 保持不变(其中HA、A﹣分别代表相应的酸和酸根离子)
‒
𝑐(𝐴 )
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
混合浓硫酸和乙醇 配制一定浓度的溶液 收集NO 气体 证明乙炔可使溴水褪色
2
【考点】D5:弱电解质在水溶液中的电离平衡.
A.A B.B C.C D.D 菁优网版权所有
【专题】51G:电离平衡与溶液的pH专题.
【考点】U5:化学实验方案的评价.
菁优网版权所有
【分析】酸的电离平衡常数越大,酸的酸性越强,根据电离平衡常数知,酸性:HNO >CH COOH,
2 3
【分析】A.配制溶液时,密度大的溶液倒入密度小的溶液;
A.加水稀释促进弱酸电离,pH相同的这两种酸稀释相同倍数,pH变化大的酸性较强;
B.定容时眼睛应该与凹液面最低处相切;
B.酸或碱抑制水电离,酸中c(H+)越大其抑制水电离程度越大;
C.二氧化氮密度大于空气,应该采用向上排空气法收集;
‒
𝑐(𝐻𝐴) ⋅ 𝑐(𝑂𝐻 )
D.得到的乙炔中含有硫化氢等气体,硫化氢等气体也能使溴水褪色。
C. =K ,水解平衡常数只与温度有关;
h
‒
𝑐(𝐴 )
【解答】解:A.配制溶液时,密度大的溶液倒入密度小的溶液,混合浓硫酸和乙醇相当于浓硫酸的稀释,
D.a点两种溶液的pH相同,但是两种溶液浓度:HNO <CH COOH,相同体积的a点两种溶液中溶质物质
2 3
应该将浓硫酸倒入乙醇中并不断搅拌,故A错误;
的量:HNO <CH COOH,消耗的碱与酸的物质的量成正比,根据Na原子守恒判断n(Na+)。
2 3
B.定容时眼睛应该与凹液面最低处相切,图象符合,故B正确;
【解答】解:酸的电离平衡常数越大,酸的酸性越强,根据电离平衡常数知,酸性:HNO >CH COOH,
2 3
C.二氧化氮密度大于空气,应该采用向上排空气法收集,所以导气管应该遵循“长进短出”原则,故C错A.加水稀释促进弱酸电离,pH相同的这两种酸稀释相同倍数,pH变化大的酸性较强,根据图知,pH变化 【考点】BH:原电池和电解池的工作原理.
菁优网版权所有
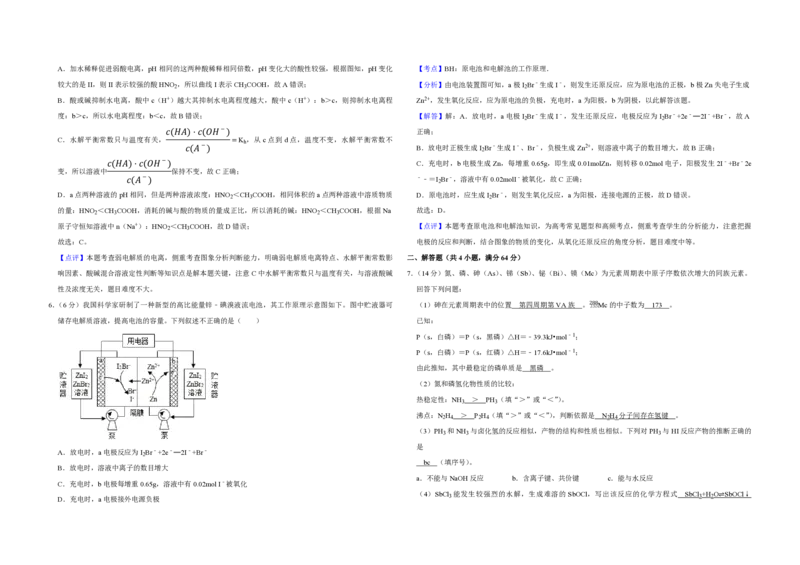
较大的是II,则II表示较强的酸HNO ,所以曲线I表示CH COOH,故A错误; 【分析】由电池装置图可知,a极I Br﹣生成I﹣,则发生还原反应,应为原电池的正极,b极Zn失电子生成
2 3 2
B.酸或碱抑制水电离,酸中c(H+)越大其抑制水电离程度越大,酸中c(H+):b>c,则抑制水电离程 Zn2+,发生氧化反应,应为原电池的负极,充电时,a为阳极,b为阴极,以此解答该题。
度:b>c,所以水电离程度:b<c,故B错误; 【解答】解:A.放电时,a电极I Br﹣生成I﹣,发生还原反应,电极反应为I Br﹣+2e﹣═2I﹣+Br﹣,故A
2 2
‒
𝑐(𝐻𝐴) ⋅ 𝑐(𝑂𝐻 ) 正确;
C.水解平衡常数只与温度有关, =K ,从 c点到 d点,温度不变,水解平衡常数不
h
𝑐(𝐴 ‒ ) B.放电时正极生成I Br﹣生成I﹣、Br﹣,负极生成Zn2+,则溶液中离子的数目增大,故B正确;
2
‒
𝑐(𝐻𝐴) ⋅ 𝑐(𝑂𝐻 ) C.充电时,b电极生成Zn,每增重0.65g,即生成0.01molZn,则转移0.02mol电子,阳极发生2I﹣+Br﹣2e
变,所以溶液中 保持不变,故C正确;
𝑐(𝐴 ‒ ) ﹣﹣=I Br﹣,溶液中有0.02molI﹣被氧化,故C正确;
2
D.a点两种溶液的pH相同,但是两种溶液浓度:HNO <CH COOH,相同体积的a点两种溶液中溶质物质 D.原电池时,应生成I Br﹣,则发生氧化反应,a为阳极,连接电源的正极,故D错误。
2 3 2
的量:HNO <CH COOH,消耗的碱与酸的物质的量成正比,所以消耗的碱:HNO <CH COOH,根据Na 故选:D。
2 3 2 3
原子守恒知溶液中n(Na+):HNO <CH COOH,故D错误; 【点评】本题考查原电池和电解池知识,为高考常见题型和高频考点,侧重考查学生的分析能力,注意把握
2 3
故选:C。 电极的反应和判断,结合图象的物质的变化,从氧化还原反应的角度分析,题目难度中等。
【点评】本题考查弱电解质的电离,侧重考查图象分析判断能力,明确弱电解质电离特点、水解平衡常数影 二、解答题(共4小题,满分64分)
响因素、酸碱混合溶液定性判断等知识点是解本题关键,注意C中水解平衡常数只与温度有关,与溶液酸碱 7.(14分)氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。
性及浓度无关,题目难度不大。 回答下列问题:
6.(6分)我国科学家研制了一种新型的高比能量锌﹣碘溴液流电池,其工作原理示意图如下。图中贮液器可 (1)砷在元素周期表中的位置 第四周期第VA族 。2 15 8 5 8Mc的中子数为 173 。
储存电解质溶液,提高电池的容量。下列叙述不正确的是( ) 已知:
P(s,白磷)=P(s,黑磷)△H=﹣39.3kJ•mol﹣1;
P(s,白磷)=P(s,红磷)△H=﹣17.6kJ•mol﹣1;
由此推知,其中最稳定的磷单质是 黑磷 。
(2)氮和磷氢化物性质的比较:
热稳定性:NH > PH (填“>”或“<”)。
3 3
沸点:N H > P H (填“>”或“<”),判断依据是 N H 分子间存在氢键 。
2 4 2 4 2 4
(3)PH 和NH 与卤化氢的反应相似,产物的结构和性质也相似。下列对PH 与HI反应产物的推断正确的
3 3 3
是
A.放电时,a电极反应为I Br﹣+2e﹣═2I﹣+Br﹣
2
bc (填序号)。
B.放电时,溶液中离子的数目增大
a.不能与NaOH反应 b.含离子键、共价键 c.能与水反应
C.充电时,b电极每增重0.65g,溶液中有0.02mol I﹣被氧化
(4)SbCl 能发生较强烈的水解,生成难溶的 SbOCl,写出该反应的化学方程式 SbCl +H O⇌SbOCl↓
D.充电时,a电极接外电源负极 3 3 2+2HCl ,因此,配制SbCl 溶液应注意 加入盐酸抑制水解 。 能量越低越稳定,
3
(5)在1L真空密闭容器中加入a molPH I固体,t℃时发生如下反应: P(s,白磷)=P(s,黑磷)△H=﹣39.3 kJ•mol﹣1①
4
PH I(S)⇌PH (g)+HI(g) ① P(s,白磷)=P(s,红磷)△H=﹣17.6kJ•mol﹣1②
4 3
4PH (g)⇌P (g)+6H (g) ② 将方程式①﹣②得P(s,红磷)=P(s,黑磷)△H=(﹣39.3+17.6)kJ/mol=﹣21.7kJ/mol,
3 4 2
2HI(g)⇌H (g)+I (g) ③ 则能量:红磷>黑磷,则黑磷稳定,
2 2
达平衡时,体系中 n(HI)=bmol,n(I )=c mol,n(H )=d mol,则t℃时反应①的平衡常数 K值为 故答案为:第四周期第VA族;173;黑磷;
2 2
8𝑐 ‒ 2𝑑 (2)元素的非金属性越强,其氢化物越稳定;
(b + )b (用字母表示)。
3
非金属性N>P,所以热稳定性:NH >PH ;
3 3
【考点】8F:原子结构与元素周期律的关系. N H 能形成分子间氢键、P H 分子间不能形成氢键,所以沸点:N H >P H ,
2 4 2 4 2 4 2 4
菁优网版权所有
【专题】51E:化学平衡专题. 故答案为:>;>;N H 分子间存在氢键;
2 4
【分析】(1)As位于第四周期第VA族,中子数=质量数﹣质子数; 分子晶体熔沸点与分子间作用力和氢键有关,能形成分子间氢键的氢化物熔沸点较高;
能量越低越稳定; (3)PH 和NH 与卤化氢的反应相似,产物的结构和性质也相似,PH 与HI反应产物为PH I,相当于铵
3 3 3 4
(2)元素的非金属性越强,其氢化物越稳定; 盐,具有铵盐结构性质,
分子晶体熔沸点与分子间作用力和氢键有关,能形成分子间氢键的氢化物熔沸点较高; a.铵盐能和NaOH发生复分解反应,所以PH I能与NaOH反应,故错误;
4
(3)PH 和NH 与卤化氢的反应相似,产物的结构和性质也相似,PH 与HI反应产物为PH I,相当于铵 b.铵盐中存在离子键和共价键,所以PH I中含离子键、共价键,故正确;
3 3 3 4 4
盐,具有铵盐结构性质; c.铵盐都易发生水解反应,所以PH I能与水反应,故正确;
4
(4)SbCl 能发生较强烈的水解,生成难溶的SbOCl,根据元素守恒知,还生成HCl;配制SbCl 溶液要防 故答案为:bc;
3 3
止其水解,其水溶液呈酸性,所以酸能抑制水解; (4)SbCl 能发生较强烈的水解,生成难溶的 SbOCl,根据元素守恒知,还生成 HCl,反应方程式为
3
(5)可逆反应2HI(g)⇌H (g)+I (g) ③ SbCl +H O⇌SbOCl↓+2HCl;配制SbCl 溶液要防止其水解,其水溶液呈酸性,所以酸能抑制水解,则配制
2 2 3 2 3
平衡(mol/L)b c c 该溶液时为防止水解应该加入盐酸,
可逆反应4PH (g)⇌P (g)+6H (g) ② 故答案为:SbCl +H O⇌SbOCl↓+HCl;加入盐酸抑制水解;
3 4 2 3 2
2 (5)可逆反应2HI(g)⇌H (g)+I (g) ③
2 2
反应(mol/L) (d﹣c) d﹣c
3
平衡(mol/L)b c c
可逆反应PH I(S)⇌PH (g)+HI(g) ① 可逆反应4PH (g)⇌P (g)+6H (g) ②
4 3 3 4 2
2 2
平衡(mo/L) b+2c (d﹣c) b 反应(mol/L) (d﹣c) d﹣c
-
3 3
则t℃时反应①的平衡常数K值=c(PH )×c(HI)。 可逆反应PH I(S)⇌PH (g)+HI(g) ①
3 4 3
【解答】解:(1)As位于第四周期第VA族,中子数=质量数﹣质子数=288﹣115=173;2 ①分子中含有碳碳三键和乙酯基(﹣COOCH CH )
2 3
平衡(mo/L) b+2c (d﹣c) b
-
3
②分子中有连续四个碳原子在一条直线上
2 8𝑐 ‒ 2𝑑 写 出 其 中 碳 碳 三 键 和 乙 酯 基 直 接 相 连 的 同 分 异 构 体 的 结 构 简 式
则t℃时反应①的平衡常数K值=c(PH )×c(HI)=[b+2c (d﹣c)]×b=(b + )b,
3 -
3 3
8𝑐 ‒ 2𝑑
故答案为:(b + )b。 。
3
(3)C→D的反应类型为 加成反应或还原反应 。
【点评】本题考查较综合,涉及化学平衡常数计算、氢键、铵盐、盐类水解等知识点,侧重考查基础知识再
( 4) D→ E的 化 学 方 程 式 为
现和灵活运用,明确化学反应原理、元素化合物性质是解本题关键,难点是(5)题计算,要计算①中平衡
时各物质浓度,注意①中反应物为固体,为解答易错点,题目难度中等。
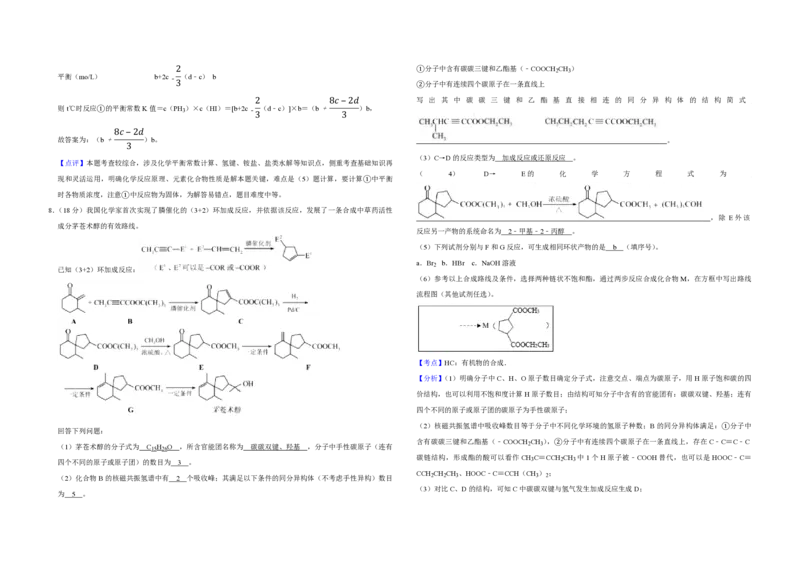
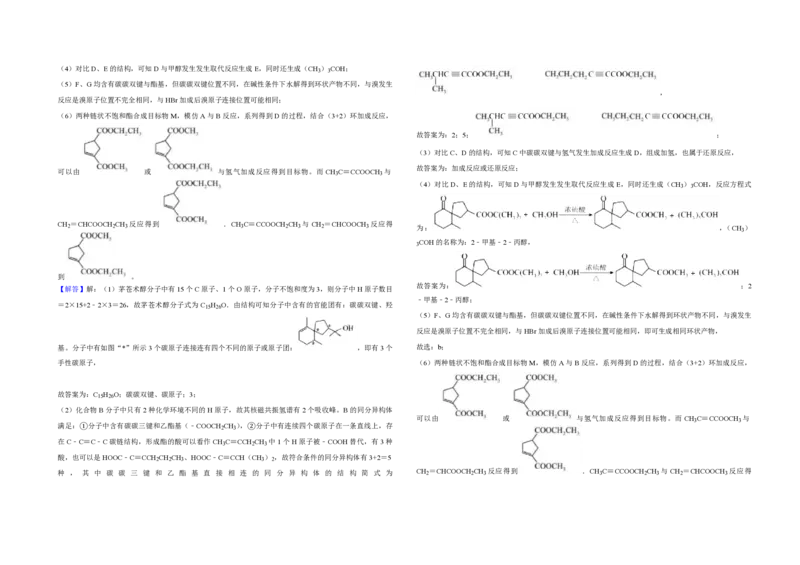
8.(18分)我国化学家首次实现了膦催化的(3+2)环加成反应,并依据该反应,发展了一条合成中草药活性
,除 E外该
成分茅苍术醇的有效路线。
反应另一产物的系统命名为 2﹣甲基﹣2﹣丙醇 。
(5)下列试剂分别与F和G反应,可生成相同环状产物的是 b (填序号)。
a.Br b.HBr c.NaOH溶液
2
已知(3+2)环加成反应:
(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物M,在方框中写出路线
流程图(其他试剂任选)。
【考点】HC:有机物的合成.
菁优网版权所有
【分析】(1)明确分子中C、H、O原子数目确定分子式,注意交点、端点为碳原子,用H原子饱和碳的四
价结构,也可以利用不饱和度计算H原子数目;由结构可知分子中含有的官能团有:碳碳双键、羟基;连有
四个不同的原子或原子团的碳原子为手性碳原子;
(2)核磁共振氢谱中吸收峰数目等于分子中不同化学环境的氢原子种数;B的同分异构体满足:①分子中
回答下列问题:
含有碳碳三键和乙酯基(﹣COOCH CH ),②分子中有连续四个碳原子在一条直线上,存在C﹣C≡C﹣C
2 3
(1)茅苍术醇的分子式为 C H O ,所含官能团名称为 碳碳双键、羟基 ,分子中手性碳原子(连有
15 26
碳链结构,形成酯的酸可以看作 CH C≡CCH CH 中 1个 H原子被﹣COOH替代,也可以是 HOOC﹣C≡
四个不同的原子或原子团)的数目为 3 。 3 2 3
CCH CH CH 、HOOC﹣C≡CCH(CH ) ;
(2)化合物B的核磁共振氢谱中有 2 个吸收峰;其满足以下条件的同分异构体(不考虑手性异构)数目 2 2 3 3 2
(3)对比C、D的结构,可知C中碳碳双键与氢气发生加成反应生成D;
为 5 。(4)对比D、E的结构,可知D与甲醇发生发生取代反应生成E,同时还生成(CH ) COH;
3 3
(5)F、G均含有碳碳双键与酯基,但碳碳双键位置不同,在碱性条件下水解得到环状产物不同,与溴发生
,
反应是溴原子位置不完全相同,与HBr加成后溴原子连接位置可能相同;
(6)两种链状不饱和酯合成目标物M,模仿A与B反应,系列得到D的过程,结合(3+2)环加成反应,
故答案为:2;5; ;
(3)对比C、D的结构,可知C中碳碳双键与氢气发生加成反应生成D,组成加氢,也属于还原反应,
故答案为:加成反应或还原反应;
可以由 或 与氢气加成反应得到目标物。而 CH C≡CCOOCH 与
3 3
(4)对比D、E的结构,可知D与甲醇发生发生取代反应生成E,同时还生成(CH ) COH,反应方程式
3 3
CH =CHCOOCH CH 反应得到 .CH C≡CCOOCH CH 与 CH =CHCOOCH 反应得
2 2 3 3 2 3 2 3 为: ,(CH )
3
COH的名称为:2﹣甲基﹣2﹣丙醇,
3
到 。
故答案为: ;2
【解答】解:(1)茅苍术醇分子中有15个C原子、1个O原子,分子不饱和度为3,则分子中H原子数目
﹣甲基﹣2﹣丙醇;
=2×15+2﹣2×3=26,故茅苍术醇分子式为C H O.由结构可知分子中含有的官能团有:碳碳双键、羟
15 26
(5)F、G均含有碳碳双键与酯基,但碳碳双键位置不同,在碱性条件下水解得到环状产物不同,与溴发生
反应是溴原子位置不完全相同,与HBr加成后溴原子连接位置可能相同,即可生成相同环状产物,
基。分子中有如图“*”所示3个碳原子连接连有四个不同的原子或原子团: ,即有3个 故选:b;
手性碳原子, (6)两种链状不饱和酯合成目标物M,模仿A与B反应,系列得到D的过程,结合(3+2)环加成反应,
故答案为:C H O;碳碳双键、碳原子;3;
15 26
(2)化合物B分子中只有2种化学环境不同的H原子,故其核磁共振氢谱有2个吸收峰。B的同分异构体
可以由 或 与氢气加成反应得到目标物。而 CH C≡CCOOCH 与
3 3
满足:①分子中含有碳碳三键和乙酯基(﹣COOCH CH ),②分子中有连续四个碳原子在一条直线上,存
2 3
在C﹣C≡C﹣C碳链结构,形成酯的酸可以看作CH C≡CCH CH 中1个H原子被﹣COOH替代,有3种
3 2 3
酸,也可以是HOOC﹣C≡CCH CH CH 、HOOC﹣C≡CCH(CH ) ,故符合条件的同分异构体有3+2=5
2 2 3 3 2
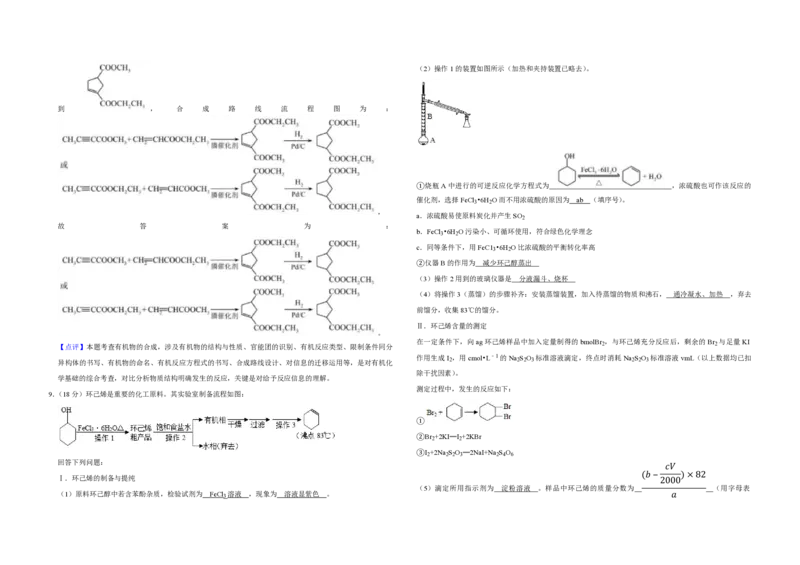
种 , 其 中 碳 碳 三 键 和 乙 酯 基 直 接 相 连 的 同 分 异 构 体 的 结 构 简 式 为 CH 2 =CHCOOCH 2 CH 3 反应得到 .CH 3 C≡CCOOCH 2 CH 3 与 CH 2 =CHCOOCH 3 反应得(2)操作1的装置如图所示(加热和夹持装置已略去)。
到 , 合 成 路 线 流 程 图 为 :
①烧瓶A中进行的可逆反应化学方程式为 ,浓硫酸也可作该反应的
催化剂,选择FeCl •6H O而不用浓硫酸的原因为 ab (填序号)。
3 2
,
a.浓硫酸易使原料炭化并产生SO
2
故 答 案 为 :
b.FeCl •6H O污染小、可循环使用,符合绿色化学理念
3 2
c.同等条件下,用FeC1 •6H O比浓硫酸的平衡转化率高
3 2
②仪器B的作用为 减少环己醇蒸出
(3)操作2用到的玻璃仪器是 分液漏斗、烧杯
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石, 通冷凝水、加热 ,弃去
前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
。
在一定条件下,向ag环己烯样品中加入定量制得的bmolBr ,与环己烯充分反应后,剩余的Br 与足量KI
【点评】本题考查有机物的合成,涉及有机物的结构与性质、官能团的识别、有机反应类型、限制条件同分 2 2
作用生成I ,用cmol•L﹣1的Na S O 标准溶液滴定,终点时消耗Na S O 标准溶液vmL(以上数据均已扣
异构体的书写、有机物的命名、有机反应方程式的书写、合成路线设计、对信息的迁移运用等,是对有机化 2 2 2 3 2 2 3
除干扰因素)。
学基础的综合考查,对比分析物质结构明确发生的反应,关键是对给予反应信息的理解。
测定过程中,发生的反应如下:
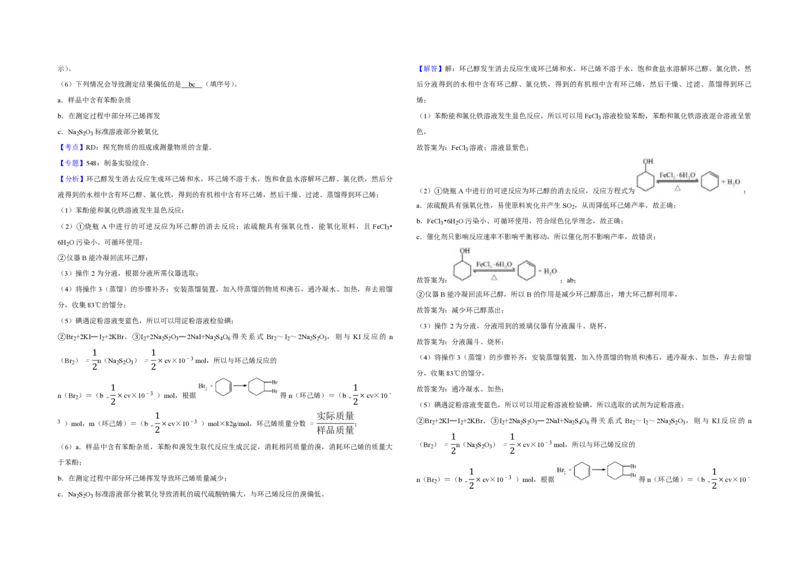
9.(18分)环己烯是重要的化工原料。其实验室制备流程如图:
①
②Br +2KI═I +2KBr
2 2
③I +2Na S O ═2NaI+Na S O
2 2 2 3 2 4 6
回答下列问题:
𝑐𝑉
(𝑏 ‒ ) × 82
Ⅰ.环己烯的制备与提纯 2000
(5)滴定所用指示剂为 淀粉溶液 。样品中环己烯的质量分数为 (用字母表
(1)原料环己醇中若含苯酚杂质,检验试剂为 FeCl 溶液 ,现象为 溶液显紫色 。 𝑎
3示)。 【解答】解:环己醇发生消去反应生成环己烯和水,环己烯不溶于水,饱和食盐水溶解环己醇、氯化铁,然
(6)下列情况会导致测定结果偏低的是 bc (填序号)。 后分液得到的水相中含有环己醇、氯化铁,得到的有机相中含有环己烯,然后干燥、过滤、蒸馏得到环己
a.样品中含有苯酚杂质 烯;
b.在测定过程中部分环己烯挥发 (1)苯酚能和氯化铁溶液发生显色反应,所以可以用FeCl 溶液检验苯酚,苯酚和氯化铁溶液混合溶液呈紫
3
c.Na S O 标准溶液部分被氧化 色,
2 2 3
【考点】RD:探究物质的组成或测量物质的含量. 故答案为:FeCl 溶液;溶液显紫色;
3
菁优网版权所有
【专题】548:制备实验综合.
【分析】环己醇发生消去反应生成环己烯和水,环己烯不溶于水,饱和食盐水溶解环己醇、氯化铁,然后分
(2)①烧瓶A中进行的可逆反应为环己醇的消去反应,反应方程式为 ;
液得到的水相中含有环己醇、氯化铁,得到的有机相中含有环己烯,然后干燥、过滤、蒸馏得到环己烯;
a.浓硫酸具有强氧化性,易使原料炭化并产生SO ,从而降低环己烯产率,故正确;
(1)苯酚能和氯化铁溶液发生显色反应; 2
b.FeCl •6H O污染小、可循环使用,符合绿色化学理念,故正确;
3 2
(2)①烧瓶 A中进行的可逆反应为环己醇的消去反应;浓硫酸具有强氧化性,能氧化原料,且 FeCl •
3
c.催化剂只影响反应速率不影响平衡移动,所以催化剂不影响产率,故错误;
6H O污染小、可循环使用;
2
②仪器B能冷凝回流环己醇;
(3)操作2为分液,根据分液所需仪器选取;
故答案为: ;ab;
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,通冷凝水、加热,弃去前馏
②仪器B能冷凝回流环己醇,所以B的作用是减少环己醇蒸出,增大环己醇利用率,
分,收集83℃的馏分;
故答案为:减少环己醇蒸出;
(5)碘遇淀粉溶液变蓝色,所以可以用淀粉溶液检验碘;
(3)操作2为分液,分液用到的玻璃仪器有分液漏斗、烧杯,
②Br +2KI═I +2KBr、③I +2Na S O ═2NaI+Na S O 得关系式 Br ~I ~2Na S O ,则与 KI反应的 n
2 2 2 2 2 3 2 4 6 2 2 2 2 3 故答案为:分液漏斗、烧杯;
1 1
(Br ) = n(Na S O ) = ×cv×10﹣3 mol,所以与环己烯反应的
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,通冷凝水、加热,弃去前馏
2 2 2 3
2 2
分,收集83℃的馏分,
1 1
故答案为:通冷凝水、加热;
n(Br )=(b ×cv×10﹣3 )mol,根据 得n(环己烯)=(b ×cv×10﹣
2 - -
2 2
(5)碘遇淀粉溶液变蓝色,所以可以用淀粉溶液检验碘,所以选取的试剂为淀粉溶液;
1 实际质量
3 )mol,m(环己烯)=(b ×cv×10﹣3 )mol×82g/mol,环己烯质量分数 = ; ②Br 2 +2KI═I 2 +2KBr、③I 2 +2Na 2 S 2 O 3 ═2NaI+Na 2 S 4 O 6 得关系式 Br 2 ~I 2 ~2Na 2 S 2 O 3 ,则与 KI反应的 n
-
2 样品质量
1 1
(6)a.样品中含有苯酚杂质,苯酚和溴发生取代反应生成沉淀,消耗相同质量的溴,消耗环己烯的质量大 (Br 2 ) = n(Na 2 S 2 O 3 ) = ×cv×10﹣3 mol,所以与环己烯反应的
2 2
于苯酚;
1 1
b.在测定过程中部分环己烯挥发导致环己烯质量减少; n(Br )=(b ×cv×10﹣3 )mol,根据 得n(环己烯)=(b ×cv×10﹣
2 - -
2 2
c.Na S O 标准溶液部分被氧化导致消耗的硫代硫酸钠偏大,与环己烯反应的溴偏低。
2 2 31 Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3
3 ) mol, m( 环 己 烯 ) = ( b ×cv× 10﹣ 3 ) mol× 82g/mol, 环 己 烯 质 量 分 数
-
2
①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g)△H >0
4 2 3 1
1 𝑐𝑉
②3SiCl (g)+2H (g)+Si(s)⇌4SiHCl (g)△H <0
‒3 4 2 3 2
(𝑏 ‒ 𝑐𝑉 × 10 ) × 82𝑔 (𝑏 ‒ ) × 82
实际质量 2 2000
③2SiCl (g)+H (g)+Si(s)+HCl(g)⇌3SiHCl (g) △H
= = = , 4 2 3 3
样品质量 𝑎𝑔 𝑎
(1)氢化过程中所需的高纯度H 可用惰性电极电解KOH溶液制备,写出产生H 的电极名称 阴极 (填
2 2
𝑐𝑉
(𝑏 ‒ ) × 82 “阳极”或“阴极”),该电极反应方程式为 2H O+2e﹣=H ↑+2OH﹣或2H++2e﹣=H ↑ 。
2 2 2
2000
故答案为:淀粉溶液; ;
𝑎
(6)a.样品中含有苯酚杂质,苯酚和溴发生取代反应生成沉淀,消耗相同质量的溴,消耗环己烯的质量大
于苯酚,所以如果含有苯酚导致测定偏高,故错误;
b.在测定过程中部分环己烯挥发导致环己烯质量减少,导致测定结果偏低,故正确;
c.Na S O 标准溶液部分被氧化导致消耗的硫代硫酸钠偏大,与环己烯反应的溴偏低,导致测定结果偏低,
2 2 3
故正确;
故选bc。
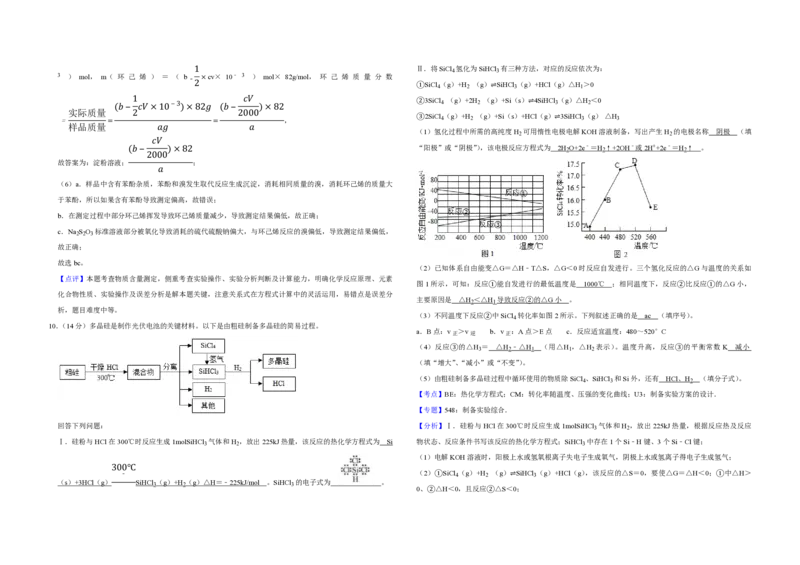
(2)已知体系自由能变△G=△H﹣T△S,△G<0时反应自发进行。三个氢化反应的△G与温度的关系如
【点评】本题考查物质含量测定,侧重考查实验操作、实验分析判断及计算能力,明确化学反应原理、元素
图1所示,可知:反应①能自发进行的最低温度是 1000℃ ;相同温度下,反应②比反应①的△G小,
化合物性质、实验操作及误差分析是解本题关键,注意关系式在方程式计算中的灵活运用,易错点是误差分
主要原因是 △H <△H 导致反应②的△G小 。
2 1
析,题目难度中等。
(3)不同温度下反应②中SiCl 转化率如图2所示。下列叙述正确的是 ac (填序号)。
4
10.(14分)多晶硅是制作光伏电池的关键材料。以下是由粗硅制备多晶硅的简易过程。
a.B点:v
正
>v
逆
b.v
正
:A点>E点 c.反应适宜温度:480~520°C
(4)反应③的△H = △H ﹣△H (用△H ,△H 表示)。温度升高,反应③的平衡常数 K 减小
3 2 1 1 2
(填“增大”、“减小”或“不变”)。
(5)由粗硅制备多晶硅过程中循环使用的物质除SiCl 、SiHCl 和Si外,还有 HCl、H (填分子式)。
4 3 2
【考点】BE:热化学方程式;CM:转化率随温度、压强的变化曲线;U3:制备实验方案的设计.
菁优网版权所有
【专题】548:制备实验综合.
回答下列问题: 【分析】Ⅰ.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H ,放出225kJ热量,根据反应热及反应
3 2
Ⅰ.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H ,放出225kJ热量,该反应的热化学方程式为 Si 物状态、反应条件书写该反应的热化学方程式;SiHCl 中存在1个Si﹣H键、3个Si﹣Cl键;
3 2 3
(1)电解KOH溶液时,阳极上水或氢氧根离子失电子生成氧气,阴极上水或氢离子得电子生成氢气;
300℃
(2)①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g),该反应的△S=0,要使△G=△H<0;①中△H>
¯ 4 2 3
(s)+3HCl(g) SiHCl (g)+H (g)△H=﹣225kJ/mol 。SiHCl 的电子式为 。
3 2 3
0、②△H<0,且反应②△S<0;(3)根据图知,A到D点,随着温度升高,SiCl 转化率增大,说明平衡正向移动且没有达到平衡状态,D (3)根据图知,A到D点,随着温度升高,SiCl 转化率增大,说明平衡正向移动且没有达到平衡状态,D
4 4
点后升高温度SiCl 转化率降低,说明升高温度平衡逆向移动,则D为平衡点, 点后升高温度SiCl 转化率降低,说明升高温度平衡逆向移动,则D为平衡点,
4 4
a.B点平衡正向移动; a.B点平衡正向移动,所以v
正
>v
逆
,故正确;
b.温度越高化学反应速率越快; b.温度越高化学反应速率越快,温度A<E,所以反应速率A<E,故错误;
c.其转化率越大越好且温度不能太高; c.其转化率越大越好且温度不能太高,根据图知,反应适宜温度:480~520°C,故正确;
(4)①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g)△H >0 故选ac;
4 2 3 1
②3SiCl (g)+2H (g)+Si(s)⇌4SiHCl (g)△H <0 (4)①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g)△H >0
4 2 3 2 4 2 3 1
将方程式②﹣①得③2SiCl (g)+H (g)+Si(s)+HCl(g)⇌3SiHCl (g),焓变进行相应的改变; ②3SiCl (g)+2H (g)+Si(s)⇌4SiHCl (g)△H <0
4 2 3 4 2 3 2
升高温度平衡向吸热方向移动; 将方程式②﹣①得③2SiCl (g)+H (g)+Si(s)+HCl(g)⇌3SiHCl (g),△H =△H ﹣△H <0,
4 2 3 3 2 1
(5)根据图知,粗硅和干燥 HCl反应生成混合物,SiHCl 和氢气反应生成 HCl;混合物分离得到氢气, 升高温度平衡向吸热方向移动,该反应的正反应是放热反应,升高温度平衡逆向移动,所以升高温度反应③
3
SiHCl 和氢气反应生成HCl需要氢气。 的平衡常数K减小,
3
【解答】解:Ⅰ.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H ,放出225kJ热量,根据反应热及 故答案为:△H ﹣△H ;减小;
3 2 2 1
300℃ (5)根据图知,粗硅和干燥 HCl反应生成混合物,SiHCl 和氢气反应生成 HCl;混合物分离得到氢气,
3
¯
反应物状态、反应条件书写该反应的热化学方程式为Si(S)+3HCl(g) SiHCl 3 (g)+H 2 (g)△H SiHCl 3 和氢气反应生成HCl需要氢气,所以由粗硅制备多晶硅过程中循环使用的物质除SiCl 4 、SiHCl 3 和Si
外,还有HCl、H ,
2
故答案为:HCl、H 。
2
【点评】本题考查物质制备,涉及盖斯定律、热化学方程式书写、图象分析判断等知识点,明确化学反应原
=﹣225kJ/mol;SiHCl 中存在1个Si﹣H键、3个Si﹣Cl键,其电子式为 ,
3
理及外界条件对化学平衡移动影响因素是解本题关键,易错点是(3)题分析,注意平衡点的判断,题目难
300℃ 度不大。
¯
故答案为:Si(s)+3HCl(g) SiHCl (g)+H (g)△H=﹣225kJ/mol; ;
3 2
(1)电解KOH溶液时,阳极上水或氢氧根离子失电子生成氧气,阴极上水或氢离子得电子生成氢气,电极
反应式为2H O+2e﹣=H ↑+2OH﹣或2H++2e﹣=H ↑,
2 2 2
故答案为:阴极;2H O+2e﹣=H ↑+2OH﹣或2H++2e﹣=H ↑;
2 2 2
(2)①SiCl (g)+H (g)⇌SiHCl (g)+HCl(g),该反应的△S=0,要使△G=△H<0,根据图知,
4 2 3
反应①能自发进行的最低温度是1000℃;①中△H>0、②△H<0,且反应②△S<0,△H <△H 导致反
2 1
应②的△G小,
故答案为:1000℃;△H <△H 导致反应②的△G小;
2 1