文档内容
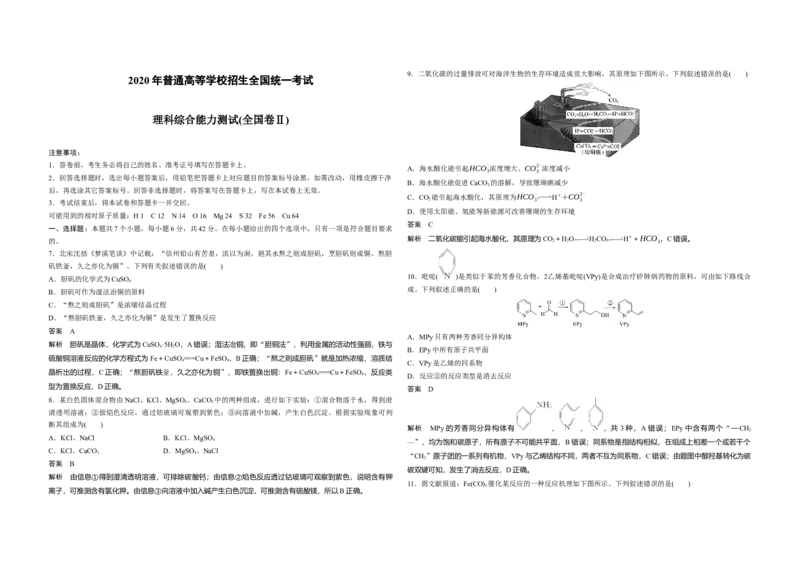
9.二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误的是( )
2020 年普通高等学校招生全国统一考试
理科综合能力测试(全国卷Ⅱ)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。 A.海水酸化能引起HCO- 浓度增大、CO2-
浓度减小
3 3
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
C.CO
能引起海水酸化,其原理为HCO- H++CO2-
3.考试结束后,将本试卷和答题卡一并交回。 2 3 3
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64
答案 C
一、选择题:本题共7个小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求
的。
解析 二氧化碳能引起海水酸化,其原理为CO
2
+H
2
O H
2
CO
3
H++HCO
3
- ,C错误。
7.北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆
矾铁釜,久之亦化为铜”。下列有关叙述错误的是( )
A.胆矾的化学式为CuSO
10.吡啶( )是类似于苯的芳香化合物,2乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如下路线合
4
成。下列叙述正确的是( )
B.胆矾可作为湿法冶铜的原料
C.“熬之则成胆矾”是浓缩结晶过程
D.“熬胆矾铁釜,久之亦化为铜”是发生了置换反应
答案 A
A.MPy只有两种芳香同分异构体
解析 胆矾是晶体,化学式为CuSO ·5H O,A错误;湿法冶铜,即“胆铜法”,利用金属的活动性强弱,铁与
4 2
B.EPy中所有原子共平面
硫酸铜溶液反应的化学方程式为Fe+CuSO ===Cu+FeSO ,B正确;“熬之则成胆矾”就是加热浓缩、溶质结
4 4 C.VPy是乙烯的同系物
晶析出的过程,C正确;“熬胆矾铁釡,久之亦化为铜”,即铁置换出铜:Fe+CuSO ===Cu+FeSO ,反应类
4 4 D.反应②的反应类型是消去反应
型为置换反应,D正确。
答案 D
8.某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进行如下实验:①混合物溶于水,得到澄
4 3
清透明溶液;②做焰色反应,通过钴玻璃可观察到紫色;③向溶液中加碱,产生白色沉淀。根据实验现象可判
断其组成为( )
解析 MPy 的芳香同分异构体有 、 、 ,共 3种,A错误;EPy 中含有两个“—CH
2
A.KCl、NaCl B.KCl、MgSO
4 —”,均为饱和碳原子,所有原子不可能共平面,B错误;同系物是指结构相似,在组成上相差一个或若干个
C.KCl、CaCO D.MgSO 、NaCl
3 4 “CH”原子团的一系列有机物,VPy与乙烯结构不同,两者不互为同系物,C错误;由题图中醇羟基转化为碳
2
答案 B
碳双键可知,发生了消去反应,D正确。
解析 由信息①得到澄清透明溶液,可排除碳酸钙;由信息②焰色反应透过钴玻璃可观察到紫色,说明含有钾
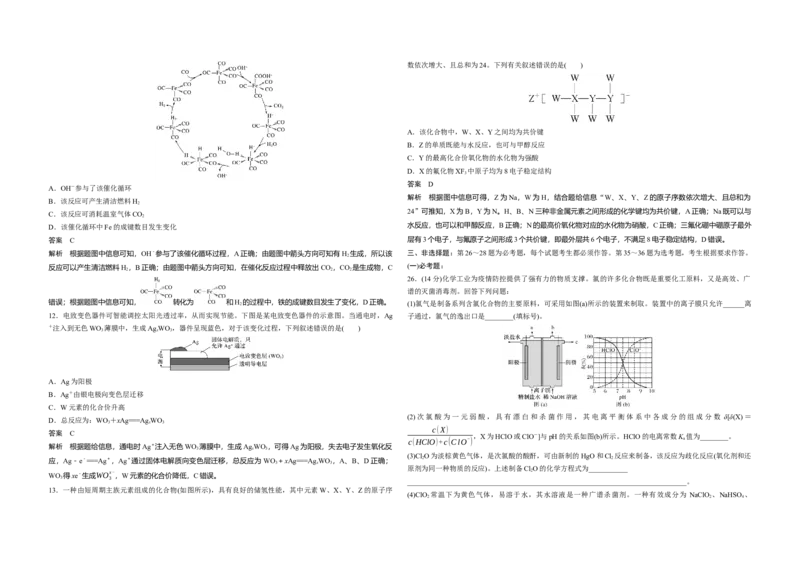
11.据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误的是( )
5
离子,可推测含有氯化钾。由信息③向溶液中加入碱产生白色沉淀,可推测含有硫酸镁,所以B正确。数依次增大、且总和为24。下列有关叙述错误的是( )
A.该化合物中,W、X、Y之间均为共价键
B.Z的单质既能与水反应,也可与甲醇反应
C.Y的最高化合价氧化物的水化物为强酸
D.X的氟化物XF 中原子均为8电子稳定结构
3
答案 D
A.OH-参与了该催化循环
解析 根据图中信息可得,Z为Na,W为H,结合题给信息“W、X、Y、Z的原子序数依次增大、且总和为
B.该反应可产生清洁燃料H
2
24”可推知,X为B,Y为N。H、B、N三种非金属元素之间形成的化学键均为共价键,A正确;Na既可以与
C.该反应可消耗温室气体CO
2
D.该催化循环中Fe的成键数目发生变化 水反应,也可以和甲醇反应,B正确;N的最高价氧化物对应的水化物为硝酸,C正确;三氟化硼中硼原子最外
答案 C 层有3个电子,与氟原子之间形成3个共价键,即最外层共6个电子,不满足8电子稳定结构,D错误。
解析 根据题图中信息可知,OH-参与了该催化循环过程,A正确;由题图中箭头方向可知有H 生成,所以该 三、非选择题:第26~28题为必考题,每个试题考生都必须作答。第35~36题为选考题,考生根据要求作答。
2
反应可以产生清洁燃料H ,B正确;由题图中箭头方向可知,在催化反应过程中释放出CO ,CO 是生成物,C
(一)必考题:
2 2 2
26.(14分)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广
谱的灭菌消毒剂。回答下列问题:
错误;根据题图中信息可知, 转化为 和H 2 的过程中,铁的成键数目发生了变化,D正确。 (1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许______离
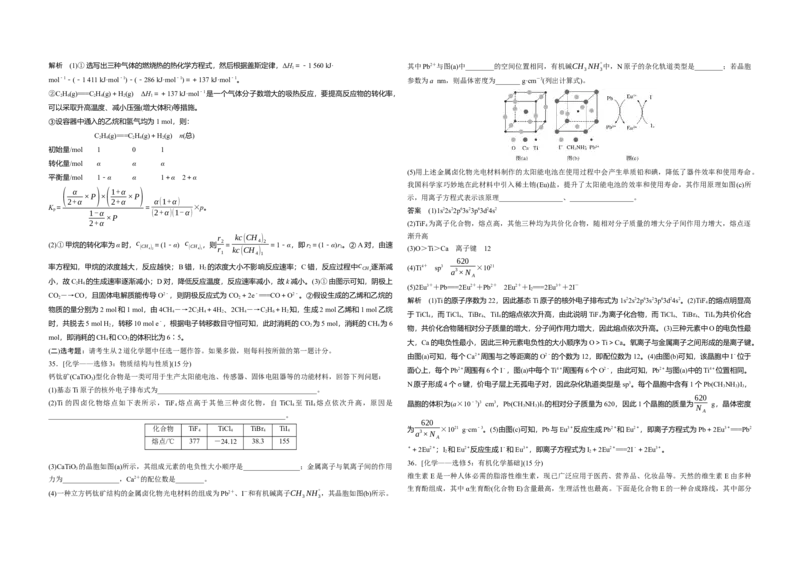
12.电致变色器件可智能调控太阳光透过率,从而实现节能。下图是某电致变色器件的示意图。当通电时,Ag 子通过,氯气的逸出口是________(填标号)。
+注入到无色WO 薄膜中,生成AgWO,器件呈现蓝色,对于该变化过程,下列叙述错误的是( )
3 x 3
A.Ag为阳极
B.Ag+由银电极向变色层迁移
C.W元素的化合价升高
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数 δ[δ(X)=
D.总反应为:WO+xAg===AgWO
3 x 3
c(X)
答案 C
,X为HClO或ClO-]与pH的关系如图(b)所示。HClO的电离常数K 值为________。
c(HClO)+c(ClO-) a
解析 根据题给信息,通电时Ag+注入无色WO 薄膜中,生成AgWO,可得Ag为阳极,失去电子发生氧化反
3 x 3
(3)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反应(氧化剂和还
应,Ag-e-===Ag+,Ag+通过固体电解质向变色层迁移,总反应为 WO +xAg===AgWO ,A、B、D正确; 2 2
3 x 3
原剂为同一种物质的反应)。上述制备ClO的化学方程式为___________
WO
得xe-生成WOx-
,W元素的化合价降低,C错误。
2
3 3 _______________________________________________________________________________。
13.一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序
(4)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为 NaClO 、NaHSO 、
2 2 4NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,生成ClO 的反 27.(15分)苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
3 2 2
应属于歧化反应,每生成 1 mol ClO 消耗 NaClO 的量为________mol;产生“气泡”的化学方程式为
2 2
_______________________________________。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______________(用离子方程式表示)。
工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则 +KMnO ―→ + MnO
4 2
生产1 000 kg该溶液需消耗氯气的质量为________ kg(保留整数)。
答案 (1)Na+ a
(2)10-7.5
(3)2Cl +HgO===HgCl +ClO +HCl―→ +KCl
2 2 2
(4)1.25 NaHCO +NaHSO===CO↑+NaSO +HO 名称 相对分子质量 熔点/℃ 沸点/℃ 密度/(g·mL-1) 溶解性
3 4 2 2 4 2
(5)ClO-+Cl-+2H+===Cl↑+ HO 203 不溶于水,易
2 2 甲苯 92 -95 110.6 0.867
解析 (1)电解精制盐水的电极反应为阳极:2Cl--2e-===Cl↑,阴极:2HO+2e-===H↑+2OH-,为了防止 溶于乙醇
2 2 2
微溶于冷水,
阴极产生的OH-与阳极产生的Cl 2 反应,中间的离子交换膜应为阳离子交换膜,只允许 Na+通过,Cl 2 在a口逸 122.4(100 ℃左
苯甲酸 122 248 — 易溶于乙醇、
c(ClO-) 右开始升华)
出。(2)由图像知,当pH=7.5时,δ(ClO-)= =50%,可求得该点c(ClO-)=c(HClO),由 热水
c(HClO)+c(ClO-)
c(H+)∙c(ClO-) 10-7.5∙c(ClO-)
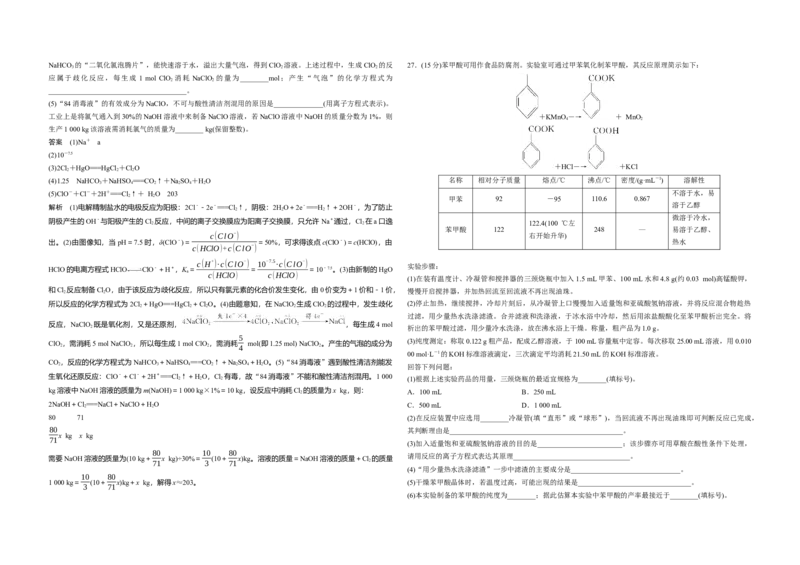
实验步骤:
HClO的电离方程式HClO ClO-+H+,K= = =10-7.5。(3)由新制的HgO
a
c(HClO) c(HClO)
(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,
和Cl 反应制备ClO,由于该反应为歧化反应,所以只有氯元素的化合价发生变化,由0价变为+1价和-1价, 慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
2 2
所以反应的化学方程式为2Cl +HgO===HgCl +ClO。(4)由题意知,在NaClO 生成ClO 的过程中,发生歧化 (2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热
2 2 2 2 2
过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将
反应,NaClO 既是氧化剂,又是还原剂, ,每生成4 mol
2 析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
5
(3)纯度测定:称取0.122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25.00 mL溶液,用0.010
ClO ,需消耗5 mol NaClO ,所以每生成1 mol ClO ,需消耗 mol(即1.25 mol) NaClO 。产生的气泡的成分为
2 2 2 4 2
00 mol·L-1的KOH标准溶液滴定,三次滴定平均消耗21.50 mL的KOH标准溶液。
CO ,反应的化学方程式为NaHCO +NaHSO===CO↑+NaSO +HO。(5)“84消毒液”遇到酸性清洁剂能发
2 3 4 2 2 4 2 回答下列问题:
生氧化还原反应:ClO-+Cl-+2H+===Cl
2
↑+H
2
O,Cl
2
有毒,故“84消毒液”不能和酸性清洁剂混用。1 000
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为________(填标号)。
kg溶液中NaOH溶液的质量为m(NaOH)=1 000 kg×1%=10 kg,设反应中消耗Cl 2 的质量为x kg,则: A.100 mL B.250 mL
2NaOH+Cl===NaCl+NaClO+HO C.500 mL D.1 000 mL
2 2
80 71 (2)在反应装置中应选用________冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,
80 其判断理由是_________________________________________________。
x kg x kg
71
(3)加入适量饱和亚硫酸氢钠溶液的目的是________________________;该步骤亦可用草酸在酸性条件下处理,
80 10 80
请用反应的离子方程式表达其原理_________________________________。
需要NaOH溶液的质量为(10 kg+ x kg)÷30%= (10+ x)kg。溶液的质量=NaOH溶液的质量+Cl 的质量
71 3 71 2
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______________________________。
10 80
1 000 kg= (10+ x)kg+x kg,解得x≈203。 (5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是________________________________。
3 71
(6)本实验制备的苯甲酸的纯度为________;据此估算本实验中苯甲酸的产率最接近于________(填标号)。A.70% B.60% 苯甲酸的理论产量m≈1.72 g
C.50% D.40% 1.0 g×86.0%
苯甲酸的产率为 ×100%=50%。
(7)若要得到纯度更高的苯甲酸,可通过在水中________的方法提纯。 1.72 g
答案 (1)B (7)根据苯甲酸的水溶性可知,若要得到纯度更高的苯甲酸,需要利用重结晶的方法进行提纯。
(2)球形 无油珠说明不溶于水的甲苯已经被完全氧化 28.(14分)天然气的主要成分为CH,一般还含有C H 等烃类,是重要的燃料和化工原料。
4 2 6
(3)除去过量的高锰酸钾,避免在用盐酸酸化时,产生氯气 (1)乙烷在一定条件可发生如下反应:C H(g)===C H(g)+H(g) ΔH,相关物质的燃烧热数据如下表所示:
2 6 2 4 2 1
2MnO- 4 +5H 2 C 2 O 4 +6H+===2Mn2++10CO 2 ↑+8H 2 O 物质 C 2 H 6 (g) C 2 H 4 (g) H 2 (g)
燃烧热ΔH/( kJ·mol-1) -1 560 -1 411 -286
(4)MnO
2
(5)苯甲酸升华而损失
(6)86.0% C
①ΔH
1
=________ kJ·mol-1。
(7)重结晶
②提高该反应平衡转化率的方法有________________、________________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数
解析 (1)该反应需要向三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g高锰酸钾,所以三颈烧瓶的最适宜规格
K =________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
为250 mL。(2)反应中应选用球形冷凝管,球形冷凝管散热面积大,冷凝效果好;回流液中不再出现油珠,说明 p
(2)高温下,甲烷生成乙烷的反应如下:2CH 高温 C H +H 。反应在初期阶段的速率方程为:r=k×c ,其中
不溶于水的甲苯(油状液体)已经被KMnO 完全氧化。(3)加入适量饱和亚硫酸氢钠溶液的目的:NaHSO 与 4 2 6 2 CH
4 3 → 4
KMnO (H+)发生氧化还原反应除去过量的 KMnO (H+),防止用盐酸酸化时,KMnO 把盐酸中的Cl-氧化为 k为反应速率常数。
4 4 4
Cl ;该过程也可用草酸在酸性条件下与KMnO 反应除去KMnO
,反应的离子方程式为2MnO-
+5HC O +6H
①设反应开始时的反应速率为r
1
,甲烷的转化率为α时的反应速率为r
2
,则r
2
=________ r
1
。
2 4 4 4 2 2 4
②对于处于初期阶段的该反应,下列说法正确的是________。
A.增加甲烷浓度,r增大
+===2Mn2++10CO↑+8HO。(4)用少量热水洗涤滤渣的目的是使生成的 尽可能溶于水,故滤
2 2 B.增加H 浓度,r增大
2
渣的主要成分是KMnO
4
在中性条件下的还原产物MnO
2
。(5)苯甲酸在100 ℃左右开始升华,干燥苯甲酸晶体时,
C.乙烷的生成速率逐渐增大
D.降低反应温度,k减小
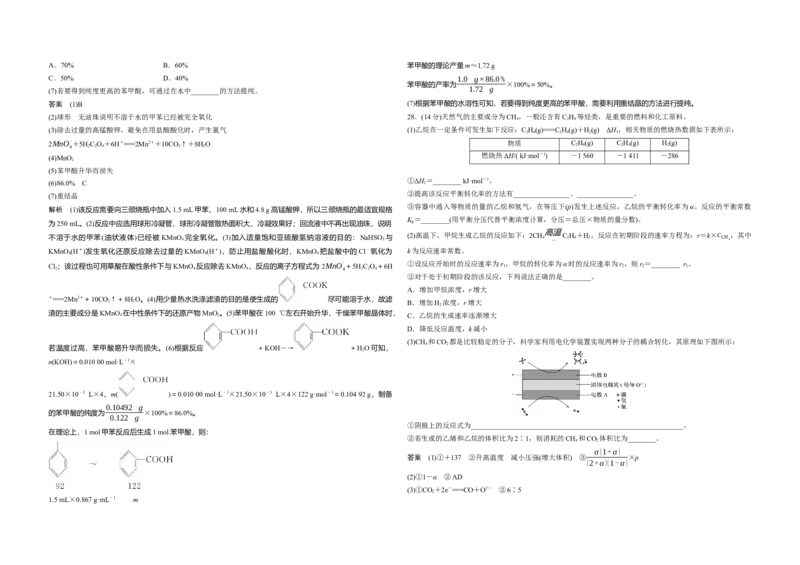
(3)CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
4 2
若温度过高,苯甲酸易升华而损失。(6)根据反应 +KOH―→ +HO可知,
2
n(KOH)=0.010 00 mol·L-1×
21.50×10-3 L×4,m( )=0.010 00 mol·L-1×21.50×10-3 L×4×122 g·mol-1=0.104 92 g,制备
0.10492 g
的苯甲酸的纯度为 ×100%=86.0%。
0.122 g
①阴极上的反应式为____________________________________________________________。
在理论上,1 mol甲苯反应后生成1 mol苯甲酸,则:
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为________。
4 2
α(1+α)
答案 (1)①+137 ②升高温度 减小压强(增大体积) ③ ×p
(2+α)(1-α)
(2)①1-α ②AD
(3)①CO+2e-===CO+O2- ②6∶5
2
1.5 mL×0.867 g·mL-1 m解析 (1)①选写出三种气体的燃烧热的热化学方程式,然后根据盖斯定律,ΔH=-1 560 kJ· 其中Pb2+与图(a)中________的空间位置相同,有机碱CH NH+ 中,N原子的杂化轨道类型是________;若晶胞
1 3 3
mol-1-(-1 411 kJ·mol-1)-(-286 kJ·mol-1)=+137 kJ·mol-1。 参数为a nm,则晶体密度为_______ g·cm-3(列出计算式)。
②C H(g)===C H(g)+H(g) ΔH =+137 kJ·mol-1是一个气体分子数增大的吸热反应,要提高反应物的转化率,
2 6 2 4 2 1
可以采取升高温度、减小压强(增大体积)等措施。
③设容器中通入的乙烷和氢气均为1 mol,则:
C H(g)===C H(g)+H(g) n(总)
2 6 2 4 2
初始量/mol 1 0 1
转化量/mol α α α
(5)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了器件效率和使用寿命。
平衡量/mol 1-α α 1+α 2+α
我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电池的效率和使用寿命,其作用原理如图(c)所
( α ) (1+α )
×P × ×P 示,用离子方程式表示该原理__________________、__________________。
2+α 2+α α(1+α)
K = = ×p。
p 1-α (2+α)(1-α) 答案 (1)1s22s22p63s23p63d24s2
×P
2+α (2)TiF 为离子化合物,熔点高,其他三种均为共价化合物,随相对分子质量的增大分子间作用力增大,熔点逐
4
r kc(CH ) 渐升高
(2)①甲烷的转化率为α时, c =(1-α) c ,则 2 = 4 2 =1-α,即r =(1-α)r 。②A对,由速
(CH 4 ) 2 (CH 4 ) 1 r kc(CH ) 2 1 (3)O>Ti>Ca 离子键 12
1 4 1
620
率方程知,甲烷的浓度越大,反应越快;B错,H
2
的浓度大小不影响反应速率;C错,反应过程中 c
CH 4
逐渐减 (4)Ti4+ sp3
a3×N
×1021
A
小,故C H 的生成速率逐渐减小;D对,降低反应温度,反应速率减小,故k减小。(3)①由图示可知,阴极上
2 6 (5)2Eu3++Pb===2Eu2++Pb2+ 2Eu2++I===2Eu3++2I-
2
CO―→CO,且固体电解质能传导O2-,则阴极反应式为CO +2e-===CO+O2-。②假设生成的乙烯和乙烷的
2 2 解析 (1)Ti的原子序数为22,因此基态Ti原子的核外电子排布式为1s22s22p63s23p63d24s2。(2)TiF 的熔点明显高
4
物质的量分别为2 mol和1 mol,由4CH―→2C H +4H 、2CH―→C H +H 知,生成2 mol乙烯和1 mol乙烷
4 2 4 2 4 2 6 2
于TiCl ,而TiCl 、TiBr 、TiI 的熔点依次升高,由此说明TiF 为离子化合物,而TiCl 、TiBr 、TiI 为共价化合
4 4 4 4 4 4 4 4
时,共脱去5 mol H ,转移10 mol e-,根据电子转移数目守恒可知,此时消耗的CO 为5 mol,消耗的CH 为6
2 2 4
物,共价化合物随相对分子质量的增大,分子间作用力增大,因此熔点依次升高。(3)三种元素中O的电负性最
mol,即消耗的CH 和CO 的体积比为6∶5。
4 2
大,Ca的电负性最小,因此三种元素电负性的大小顺序为O>Ti>Ca。氧离子与金属离子之间形成的是离子键。
(二)选考题:请考生从2道化学题中任选一题作答。如果多做,则每科按所做的第一题计分。
由图(a)可知,每个Ca2+周围与之等距离的O2-的个数为12,即配位数为12。(4)由图(b)可知,该晶胞中I-位于
35.[化学——选修3:物质结构与性质](15分)
面心上,每个Pb2+周围有6个I-,图(a)中每个Ti4+周围有6个O2-,由此可知,Pb2+与图(a)中的Ti4+位置相同。
钙钛矿(CaTiO )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
3
N原子形成4个σ键,价电子层上无孤电子对,因此杂化轨道类型是sp3。每个晶胞中含有1个Pb(CH NH )I ,
3 3 3
(1)基态Ti原子的核外电子排布式为_____________________________________________。
620
(2)Ti 的四卤化物熔点如下表所示,TiF 4 熔点高于其他三种卤化物,自 TiCl 4 至TiI 4 熔点依次升高,原因是 晶胞的体积为(a×10-7)3 cm3,Pb(CH 3 NH 3 )I 3 的相对分子质量为620,因此1个晶胞的质量为 N g,晶体密度
A
___________________________________________________________________。
620
化合物 TiF 4 TiCl 4 TiBr 4 TiI 4 为 a3×N ×1021 g·cm-3。(5)由图(c)可知,Pb与Eu3+反应生成Pb2+和Eu2+,即离子方程式为Pb+2Eu3+===Pb2
A
熔点/℃ 377 -24.12 38.3 155
++2Eu2+;I 和Eu2+反应生成I-和Eu3+,即离子方程式为I+2Eu2+===2I-+2Eu3+。
2 2
36.[化学——选修5:有机化学基础](15分)
(3)CaTiO 的晶胞如图(a)所示,其组成元素的电负性大小顺序是________________;金属离子与氧离子间的作用
3
维生素E是一种人体必需的脂溶性维生素,现已广泛应用于医药、营养品、化妆品等。天然的维生素E由多种
力为________________,Ca2+的配位数是________。
(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH NH+ ,其晶胞如图(b)所示。
生育酚组成,其中α生育酚(化合物E)含量最高,生理活性也最高。下面是化合物E的一种合成路线,其中部分
3 3反应略去。
(5)
(6)c
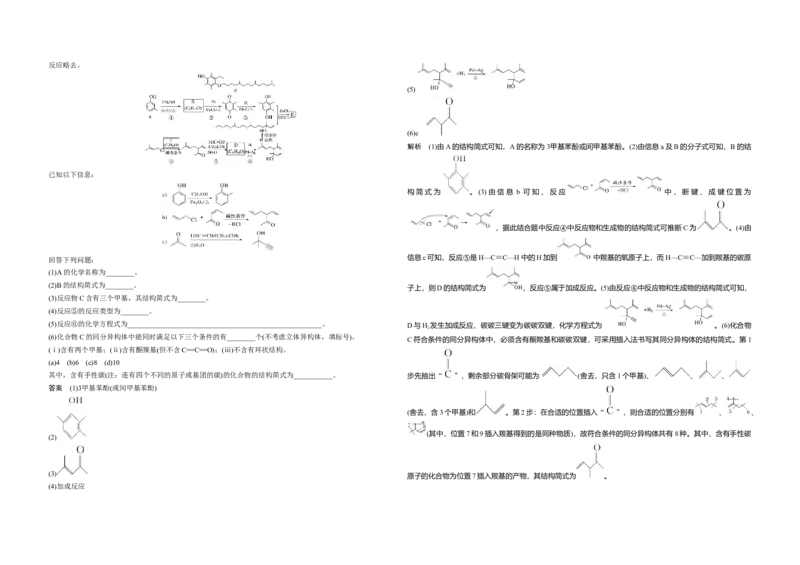
解析 (1)由A的结构简式可知,A的名称为3甲基苯酚或间甲基苯酚。(2)由信息a及B的分子式可知,B的结
已知以下信息:
构简式为 。(3)由信息 b 可知,反应 中,断键、成键位置为
,据此结合题中反应④中反应物和生成物的结构简式可推断C为 。(4)由
回答下列问题:
信息c可知,反应⑤是H—C≡C—H中的H加到 中羰基的氧原子上,而H—C≡C—加到羰基的碳原
(1)A的化学名称为________。
(2)B的结构简式为________。
子上,则D的结构简式为 ,反应⑤属于加成反应。(5)由反应⑥中反应物和生成物的结构简式可知,
(3)反应物C含有三个甲基,其结构简式为________。
(4)反应⑤的反应类型为________。
(5)反应⑥的化学方程式为_______________________________________________________。 D与H 发生加成反应,碳碳三键变为碳碳双键,化学方程式为 。(6)化合物
2
(6)化合物C的同分异构体中能同时满足以下三个条件的有________个(不考虑立体异构体,填标号)。
C符合条件的同分异构体中,必须含有酮羰基和碳碳双键,可采用插入法书写其同分异构体的结构简式。第1
(ⅰ)含有两个甲基;(ⅱ)含有酮羰基(但不含C==C==O);(ⅲ)不含有环状结构。
(a)4 (b)6 (c)8 (d)10
其中,含有手性碳(注:连有四个不同的原子或基团的碳)的化合物的结构简式为___________。 步先抽出“ ”,剩余部分碳骨架可能为 (舍去,只含1个甲基)、 、 、
答案 (1)3甲基苯酚(或间甲基苯酚)
(舍去,含3个甲基)和 。第2步:在合适的位置插入“ ”,则合适的位置分别有 、 、
(其中,位置7和9插入羰基得到的是同种物质),故符合条件的同分异构体共有8种。其中,含有手性碳
(2)
(3)
原子的化合物为位置7插入羰基的产物,其结构简式为 。
(4)加成反应