文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 12 化学计算
【题型一】有关化学式的计算
[例题1] (2024•旺苍县模拟)生姜中含有的姜油酮(C H O )有辛辣刺激的味道,可
11 14 3
溶于乙醇,具有镇痛、解热等作用。下列关于姜油酮的说法正确的是( )
A.姜油酮属于氧化物
B.姜油酮中碳、氢原子个数比为14:11
C.姜油酮中碳元素的质量分数为24.7%
D.姜油酮中碳、氢、氧的质量比为66:7:24
[例题2] (2023•商水县二模)14g由乙炔(C H )、乙烯(C H )、乙烷(C H )组成
2 2 2 4 2 6
的混合物在足量的氧气中燃烧,生成18gH O和一定质量的CO ,混合物中乙炔、乙烯、乙烷
2 2
的分子个数比可能为( )
A.1:2:3 B.3:2:3 C.6:3:2 D.3:2:1
[例题3] (2023•虞城县三模)在医疗上葡萄糖(C H O )常用于病人输液。测得某种葡
6 12 6
萄糖水溶液中氢元素的质量分数为10%,则该溶液中葡萄糖的质量分数为( )
A.10% B.25% C.40% D.55%
[例题4] (2023•秦淮区一模)某气体可能由CO、H 、CH 中的一种或几种组成,一定量
2 4
该气体在足量 O 中充分燃烧,生成 CO 与 H O 的质量比为 22:9,下列说法正确的是
2 2 2
( )
A.该气体中一定含有CO
B.该气体中一定含有H
2
C.该气体中一定含有CH
4
D.该气体不可能同时含有CO、H 、CH
2 4
[例题5] (2023•郑州二模)向一定质量的某碳酸钠溶液中加入足量的氯化钙溶液,充分
反应后过滤,所得沉淀的质量恰好等于原碳酸钠溶液质量的 1/5。则原碳酸钠溶液中溶质的质
量分数约为( )
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.11% B.21% C.31% D.41%
[例题6] (多选)(2023•济阳区一模)现有18.6gNaOH与Na CO 的固体混合物,在室
2 3
温下,将该混合物与100g稀盐酸混合,恰好完全反应,所得不饱和溶液的质量为 114.2g,则
下列有关说法正确的是( )
A.所用稀盐酸的溶质质量分数为14.6%
B.反应中有气体生成,质量为4.4g
C.恰好完全反应后,所得溶液中溶质的质量为11.7g
D.固体混合物中Na CO 的质量为10.6g
2 3
以化合物AaBb为例,可推导出下列计算公式
(1)相对分子质量:相对分子质量=A的相对原子质量×a+B的相对原子质量×b;
(2)A、B原子个数比==
(3)A、B元素质量比==
(4)A元素的质量分数=A元素的质量分数=×100%
(5)A元素的质量=化合物(AaBb)质量×A元素的质量分数
【题型二】有关溶液的计算
[例题7] (2023•长春一模)研究溶液对生产、生活有重要的意义。如表是 NaCl和KNO
3
在不同温度下的溶解度。
温度℃ 0 20 40 60 80
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4
KNO 13.3 31.6 63.9 110 169
3
(1)20℃时,NaCl的溶解度为 g。
(2)NaCl的饱和溶液中含有少量KNO ,提纯NaCl,采用的方法是 (选填“蒸
3
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
发结晶”或“降温结晶”)。
(3)根据图示实验和溶解度表,下列说法不正确的是 。
A.若a是NaCl,则③中的溶液是不饱和溶液
B.若a是NaCl,则④中溶质的质量分数约为27.2%
C.若a是KNO ,则③到④溶液由不饱和转化为饱和
3
D.实验证明溶液是否饱和与温度、溶质的量和溶剂种类有关
[例题8] (2024•西城区模拟)用780g硫化钠(Na S)溶液恰好能吸收64gSO ,反应的
2 2
化学方程式为2Na S+5SO +2H O═4NaHSO +3S↓。假设烟气中的其他成分不与Na S反应,
2 2 2 3 2
求:
(1)理论上消耗Na S的质量;
2
(2)使用的Na S溶液溶质的质量分数。
2
(1)溶解度的计算: 或 (溶液具有均一性)
(2)溶液质量=溶质质量+溶剂质量
溶质质量分数=×100% 变形后为:溶质质量=溶液质量×溶质质量分数
(3)溶液稀释计算主要是根据稀释前后溶质质量相等列式:若浓溶液的质量为m ,质量分数为
浓
a%,加m 稀释后质量分数为b%,则可列式为:(m +m )b%=m a%
水 浓 水 浓
(4)溶液稀混合计算主要是根据混合前后溶质质量相等列式:若浓溶液的质量为m ,质量分数
浓
为a%,稀溶液的质量为m ,质量分数为b%,
稀
则混合后的质量分数(m +m )c%=m a%+m b%
浓 稀 浓 稀
(5)化学方程式反映的是纯净物间的质量关系,涉及到的一般都是溶液中的溶质的质量,常要
用到的公式:m =m ×a%,然后把得到的溶质的质量代入方程式计算。
溶质 溶液
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【题型三】有关化学方程式的计算
[例题9] (2024•召陵区校级一模)复分解反应是初中化学中常见的一种基本反应类型。
(1)下列复分解相关的说法错误的是 。
A.复分解反应中的物质都是化合物
B.复分解反应一定具有明显的现象
C.酸碱盐之间不一定发生复分解反应
D.复分解反应中一定有盐生成
(2)中和反应是典型的复分解反应。如图是盐酸和氢氧化钠溶液反应时溶液pH的变化曲线。
该图对应操作是将 溶液滴入另一种溶液中,该反应的化学方程式是
。向反应后溶液中滴加紫色石蕊溶液,溶液变红,则对应图中 点。
复分解反应在物质检验、除杂、分离提纯、物质制取等方面均有广泛的应用。
(3)为除去氯化钠中的CaCl 、MgCl 、Na SO 杂质,某化学兴趣小组的同学设计了如图实验
2 2 2 4
流程。
①溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是 。
②写出加入BaCl
2
溶液时发生反应的化学方程式 。
③设计实验验证过滤后加入盐酸前,溶液中含有的杂质 。
(4)利用复分解反应,工业上常用熟石灰与碳酸钠反应制备氢氧化钠。现有 7.4t熟石灰,若完
全参与反应,则能制得氢氧化钠的质量是多少?
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
[例题10](2024•泌阳县一模)酸、碱、盐在生产、生活中有重要用途。
(1)酸、碱、盐之间能发生复分解反应的条件是有沉淀析出,或有气体放出,或有
生成。
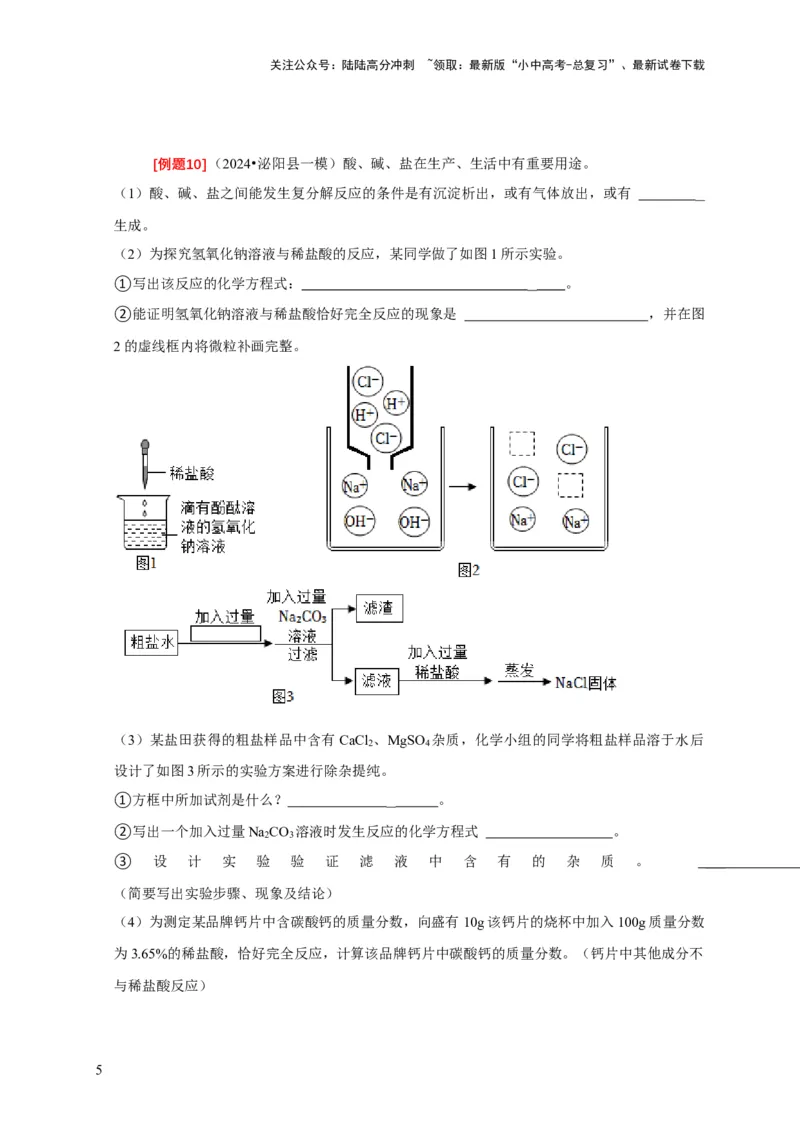
(2)为探究氢氧化钠溶液与稀盐酸的反应,某同学做了如图1所示实验。
①写出该反应的化学方程式: 。
②能证明氢氧化钠溶液与稀盐酸恰好完全反应的现象是 ,并在图
2的虚线框内将微粒补画完整。
(3)某盐田获得的粗盐样品中含有CaCl 、MgSO 杂质,化学小组的同学将粗盐样品溶于水后
2 4
设计了如图3所示的实验方案进行除杂提纯。
①方框中所加试剂是什么? 。
②写出一个加入过量Na CO 溶液时发生反应的化学方程式 。
2 3
③ 设 计 实 验 验 证 滤 液 中 含 有 的 杂 质 。
(简要写出实验步骤、现象及结论)
(4)为测定某品牌钙片中含碳酸钙的质量分数,向盛有10g该钙片的烧杯中加入100g质量分数
为3.65%的稀盐酸,恰好完全反应,计算该品牌钙片中碳酸钙的质量分数。(钙片中其他成分不
与稀盐酸反应)
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化学方程式进行纯净物质间的计算
(1)知道反应物(或生成物)的质量求生成物(或反应物)的质量。
(2)根据质量守恒定律的化学方程式的计算
此内容是本课时的拓展,一类习题可根据质量守恒定律的定义或实质,利用反应物前后物质或
元素质量守恒进行计算。另一类习题还可根据反应前后物质质量之差,算出气体或沉淀物的质量,
再进行化学方程式的计算。
解题步骤:
1)设未知量,用x、y等字母表示(不带单位);
2)正确写出有关的化学方程式(注意配平);
3)找出相关物质间的质量关系,写在对应化学式的下面;
4)列出比例式,求出未知量;
5)简明写出答案。
含一定杂质的化学方程式的计算
1.有关混合物的计算(混合物中杂质不参加反应或混合物中只有一种物质参加反应)。
2.原理:将不纯物质的质量转化为纯净物质的质量代入化学方程式进行计算,一般不纯物质
有:样品、合金、矿石、溶液等。
3.公式
(1)纯净物的质量=混合物的质量×纯度(或质量分数)
(2)纯度=×100%
(3)纯净物的质量分数=1-杂质的质量分数
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1. (2023•南山区二模)春夏季节是流感的高发季,板蓝根中主要成分之一靛玉红
(C H N O )对预防流感有一定的作用。下列说法正确的是( )
16 10 2 2
A.靛玉红属于有机小分子物质
B.1个靛玉红分子中含有1个N 分子和1个O 分子
2 2
C.靛玉红中C、H、N、O三种元素的质量比为16:10:2:2
D.靛玉红由碳、氢、氮、氧四个元素组成
2. (2023•兰考县一模)将24gCO和CO 的混合气体通过足量灼热的CuO,充分反应后,
2
得到CO 的总质量为36g,则原混合气体中CO的质量分数为( )
2
A.17.5% B.21% C.66.7% D.87.5%
3. (2023•双流区校级模拟)氢能是一种极具发展潜力的清洁能源,以太阳能为热源,
热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示,下列说法中不
正确的是( )
A.该流程可实现太阳能向氢能的转化
B.制得H 中氢元素最初来源于水
2
C.反应Ⅱ中,每消耗98g硫酸就能产生16gO
2
D.所有涉及的反应中,化合价升高的元素有4种
4. (2023•淮阳区三模)现有两种金属的混合物2.4 g,与100 g质量分数为9.8%的硫酸
恰好完全反应。则该混合物的组成可能为( )
A.Mg、Cu B.Mg、Al C.Al、Fe D.Fe、Zn
5. (2023•东港区校级三模)布洛芬(化学式为C H O )具有解热镇痛作用,常规剂
13 18 2
量使用时,不良反应发生率低,是国内外包括世界卫生组织公认的用于小儿发热的经典解热镇
痛药。下列有关布洛芬的说法正确的是( )
A.布洛芬是氧化物
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
B.布洛芬分子中碳元素、氢元素、氧元素的质量之比是13:18:2
C.一个布洛芬分子中含有1个氧分子
D.布洛芬的相对分子质量为206
6. (2023•滑县校级一模)某锌的样品中含有Fe、Mg、Al、Cu等金属杂质中的2种,
6.5g该样品与足量的稀硫酸反应,可得到0.2g氢气,对该样品中含有金属杂质的组成有如下猜
测:①Mg和Al;②Mg和Fe;③Mg和Cu;④Al和Fe;⑤Al和Cu;⑥Fe和Cu。其
中合理的个数为( )
A.3个 B.4个 C.5个 D.6个
7. (2023•林州市三模)有Mg、Al、Zn、Fe的混合物共5.4g,与足量盐酸反应,生成
H 的质量可能是( )
2
A.0.8g B.0.6g C.0.3g D.0.1g
8. (2023•台江区校级三模)Alq 是用于制作有机发光二极管的新材料,其化学式为
3
C H AlN O ,可应用于柔性智能手机显示屏。下列关于Alq 的说法正确的是( )
27 18 3 3 3
A.Alq 由五种原子构成
3
B.碳元素与氢元素质量比为27:18
C.Alq 中含有一个臭氧分子
3
D.Alq 中碳元素的质量分数最大
3
9. (2023•盐城一模)Cu一Zn合金中加入200gCuSO 溶液,恰好完全反应,得到溶液
4
200.1g和固体19.9g。合金中Cu的质量分数是( )
A.32.5% B.43.0% C.67.5% D.75%
10. (2023•遂平县模拟)往一定质量Fe O 和Al O 的混合物中加入100g溶质质量分数
2 3 2 3
为9.8%的稀硫酸,恰好完全反应后,测得溶液质量增加了12g,把反应后的溶液完全蒸干,所
得固体质量为( )
A.12g B.20g C.21.6g D.21.8g
△
11. (2023•龙华区校级二模)硝酸铵与熟石灰混合可发生2NH NO +Ca(OH) Ca
4 3 2
¯
❑
(NO ) +2NH ↑+2H O反应。若准确称取某硝酸铵氮肥样品8.5g,与足量的熟石灰混合充分
3 2 3 2
反应后,最多生成1.7g氨气(NH ),确定该氮肥样品中硝酸铵的纯度。
3
12. (2023•合肥三模)AgNO 溶液是实验室中的常用试剂。AgNO 的化学性质不稳定。
3 3
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
光照
在温度稍高或光照条件下可以发生反应:2AgNO 2Ag↓+2NO ↑+O ↑(假设气体全部
3 2 2
¯
❑
逸出)。现有一瓶100g10%的AgNO 溶液,久置后(不考虑水分挥发),将瓶内物质过滤,
3
得到固体1.08g和若干滤液。试计算:
(1)AgNO 中N和O的质量比为 。
3
(2)滤液中AgNO 的质量分数(结果精确到0.1%)。
3
(3)若要将滤液的AgNO 恢复到原来的质量分数,并把溶液质量增加到200g。应在滤液中加
3
入一定量水和AgNO 固体,计算加入AgNO 的质量。
3 3
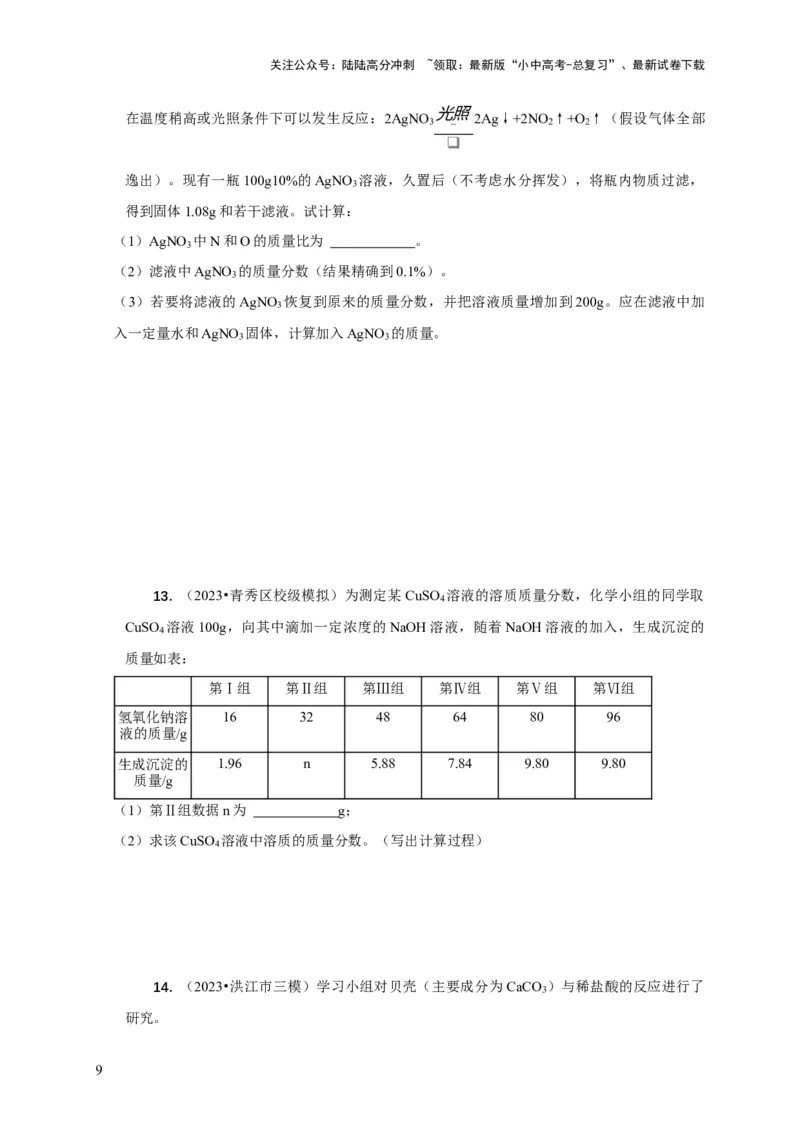
13. (2023•青秀区校级模拟)为测定某CuSO 溶液的溶质质量分数,化学小组的同学取
4
CuSO 溶液100g,向其中滴加一定浓度的NaOH溶液,随着NaOH溶液的加入,生成沉淀的
4
质量如表:
第Ⅰ组 第Ⅱ组 第Ⅲ组 第Ⅳ组 第Ⅴ组 第Ⅵ组
氢氧化钠溶 16 32 48 64 80 96
液的质量/g
生成沉淀的 1.96 n 5.88 7.84 9.80 9.80
质量/g
(1)第Ⅱ组数据n为 g;
(2)求该CuSO 溶液中溶质的质量分数。(写出计算过程)
4
14. (2023•洪江市三模)学习小组对贝壳(主要成分为CaCO )与稀盐酸的反应进行了
3
研究。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
I.研究贝壳的状态对反应速率的影响
取等纯度、等质量的块状和粉末状贝壳,分别加入足量等浓度的稀盐酸,实验过程中生成气体
的体积随时间变化的情况如图所示(贝壳中的杂质不与稀盐酸反应)。
(1)结合实验分析图中曲线,可得出结论: 。
Ⅱ.测定贝壳中碳酸钙的质量分数
小组取10g贝壳,按照如图所示过程进行实验。实验过程中测得不同时刻装置和药品总质量随时
间变化的数据见如表。请计算:
时刻 t t t t
0 1 2 3
装置和药品总质量/g 240.00 237.00 236.48 236.48
(2)实验中共产生二氧化碳 g。
(3)该贝壳中碳酸钙的质量分数(写出计算过程)。
15. (2023•巴南区模拟)甲醛(HCHO)是一种防腐剂,同时也是一种有毒物质。为了
测定溶液中甲醛的含量。某同学取含甲醛的溶液10.0g,滴加过量酸性KMnO 溶液11.1g,
4
(反应的方程式为:4KMnO +5HCHO+6H SO ═2K SO +4MnSO +5CO ↑+11H O );整个过
4 2 4 2 4 4 2 2
程中无沉淀产生。将产生的气体用40.0g10%NaOH溶液恰好完全吸收,吸收后溶液的总质量为
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
41.1g;试计算。(已知MnSO 的相对分子质量为151)
4
(1)甲醛中碳、氢元素的质量比 。
(2)若用20%的溶液配制40.0g10%的NaOH,需要加入水的质量。
(3)所得溶液中MnSO 的质量分数。
4
11