文档内容
2025 年重庆市普通高中学业水平选择性考试
9 月调研测试卷 化学参考答案
1~5 CBCAA 6~10 BBDBA 11~14CAAD
1.C
【解析】
A.精制食盐的有效成分为NaCl,A正确;
B.味精的有效成分为谷氨酸钠,B正确;
C.白砂糖有效成分应为C H O ,C错误;
12 22 11
D.食用白醋的有效成分为CH COOH,D正确。
3
2.B
【解析】
A.H+和ClO-生成弱电解质HClO而不能大量共存;
B.选项中所给离子相互都不反应,可以大量共存;
C.Ca2+和OH-、SO2-反应生成沉淀而不能大量共存;
4
D.HCO-和Fe3+发生双水解生成沉淀和气体,不能大量共存。
3
3.C
【解析】
A.CO 的球棍模型为 ,是直线型,A错误;
2
B.LiH为离子化合物,电子式为Li+[∶H]-,B错误;
C.用于考古的碳原子为14 C,C正确;
6
D.顺-2-丁烯的结构中两个甲基在双键的同一侧,其结构简式为 ,D错误。
4.A
【解析】
A.加热条件下,浓盐酸可与MnO 反应制Cl ,A正确;
2 2
B.中和热的测定实验中,温度计应该插入溶液中以测量溶液的温度,B错误;
C.NaHCO 固体分解时会生成水,故试管口应向下倾斜,C错误;
3
D.FeSO 溶液中Fe2+加热时会被氧化,故不能蒸干FeSO 溶液获得FeSO ·7H O,D错误。
4 4 4 2
5.A
【解析】
A.1个CHCl 分子中含有3个C-Cl键,故1 mol CHCl 含C-Cl键的数目为3N ,A正确;
3 3 A
B.Fe与S加热反应只能生成FeS,故转移的电子数目为2N ,B错误;
A
C.未告知溶液体积,无法计算,C错误;
D.未提到具体的温度、压强(如标况下),无法计算11.2 L NO与11.2 L O 混合后的分子数目,D错误。
2
6.B
9月调研测试卷(化学)参考答案 第1页 共5页
{#{QQABJYaQggCgAJBAABhCUwF4CEEQkAGAAagOwEAIMAAAwQNABAA=}#}【解析】
A.一氯代物有3种(不含立体异构),A错误;
B.分子中含4个手性碳原子,B正确;
C.碳原子均采用sp3杂化,C错误;
D.不能发生加成反应,D错误。
7.B
【解析】
A.As的电负性小于Se,A错误;
B.Mn元素位于周期表ⅦB族,B正确;
C.Se的第一电离能大于Fe,C错误;
D.基态Fe原子有4个单电子,基态Cu原子有1个单电子,未成对电子数不相同,D错误。
8.D
【解析】经推断A、B、C、D依次为H、C、O、S。
A.简单离子半径:S2->O2-,A错误;
B.单质的沸点C>H ,B错误;
2
C.未指明是最高价含氧酸的酸性,无法比较,C错误;
D.简单氢化物稳定性H O>CH ,D正确。
2 4
9.B
【解析】
A.M分子中-CH -的C所连接的四个原子构成四面体,则所有原子不可能共平面,A错误;
2
B.由有机物M、N的结构简式可知,M含有碳碳双键和醚键,N含有碳碳双键和酚羟基,红外光谱图中
可以反映不同官能团或化学键的吸收峰,故依据红外光谱可确证M、N存在不同的官能团,B正确;
C.化合物M、N中官能团和NaHCO 溶液均不反应,不能进行鉴别,C错误;
3
D.酚羟基的邻位和对位、碳碳双键均能与Br 发生反应,则1mol N最多能与3molBr 发生反应,D错误。
2 2
10.A
【解析】
A.pH=7时,加入NaOH溶液体积应小于20mL,A错误;
B.a点溶液中溶质为CH COOH和CH COONa,溶液pH=4,则水电离出c(OH-)和c(H+)约为10-10 mol/L,
3 3
B正确;
C.b点溶液中存在元素守恒,C正确;
D.酸碱中和滴定可以选择酚酞作指示剂,D正确。
11.C
【解析】
A.石油裂解气中含有乙烯、丙烯等烯烃,溴的CCl 褪色不能证明一定是乙烯,A错误;
4
B.向2mL 0.1mol/L(NH ) Fe(SO ) 溶液中滴加几滴0.1mol/L NaOH溶液,NaOH会与Fe2+反应被消耗,
4 2 4 2
且反应过程中未加热,不会有氨气生成,B错误;
9月调研测试卷(化学)参考答案 第2页 共5页
{#{QQABJYaQggCgAJBAABhCUwF4CEEQkAGAAagOwEAIMAAAwQNABAA=}#}C.将SO 通入酸性KMnO 溶液中,发生氧化还原反应,溶液褪色,C正确;
2 4
D.向黑色PbS悬浊液中加入H O 会被氧化成白色的PbSO ,但不能证明K (PbS)>K (PbSO ),D错误。
2 2 4 sp sp 4
12.A
【解析】
A.Ca2+与F-的配位数之比为2∶1,A错误;
B.A位置原子坐标为(0.25,0.75,0.75),B正确;
C.Ca2+与F-的最短距离是体对角线的四分之一,为 3 bnm,C正确;
4
478 312
D.该晶体的密度为 1021g/cm3,D正确。
N (b107)3 b3N
A A
13.A
【解析】
A.Li为负极,失电子发生氧化反应,A错误;
B.电池工作时Li+向正极即石墨电极移动,B正确;
C.锂是活泼金属,易与水反应,SOCl 易与氧气反应,C正确;
2
D.电池总反应为:4Li+2SOCl =4LiCl+S+SO ↑,D正确。
2 2
14.D
【解析】
A.随温度升高CO 含量先减小后增大,因此该反应的△H<0,A错误;
2
B.容器甲中反应速率v(H )=0.12/t mol/(L·min),B错误;
2
C.容器乙当前状态下无法判断是否已经达到平衡,因此v 和v 大小无法判断,C错误;
正 逆
D.容器丙中反应过程中物质的量变化如下:
CO (g)+3H (g) CH OH(g)+H O(g)
2 2 3 2
起始/mol 1 8.6
转化/mol 0.8 2.4 0.8 0.8
t分钟/mol 0.2 6.2 0.8 0.8
故甲醇的体积分数为10%,D正确。
15.(14分,每空2分)
(1)3d54s1 正四面体形
(2)5H++3HSO-+Cr O2-=3SO2-+2Cr3++4H O
3 2 7 4 2
(3)5.6≤pH<7.1 4.0×10-9或10-8.4
(4)H O 受热易分解,所以氧化Cr(OH) 的H O 减少,故导致Na CrO 的产率反而降低
2 2 3 2 2 2 4
(5)CrO
2
【解析】
(2)酸浸后,溶液中有大量H+,因此离子方程式为5H++3HSO-+Cr O2-=3SO2-+2Cr3++4H O;
3 2 7 4 2
(3)加入氢氧化钠溶液调pH,若使Cr3+完全沉淀而Ni2+不沉淀,则调pH范围应该为5.6≤pH<7.1,
当Cr3+的浓度为1.0×10-5 mol/L时,可认为Cr3+沉淀完全,将1.0×10-5 mol/L 代入K 计算公式,
sp
可得c(OH-)=4.0×10-9 mol/L,也可通过pH进行计算。
9月调研测试卷(化学)参考答案 第3页 共5页
{#{QQABJYaQggCgAJBAABhCUwF4CEEQkAGAAagOwEAIMAAAwQNABAA=}#}(5)Cr(OH) 相对分子质量为103,失重率为18.45%,设剩余氧化物化学式为CrO ,计算可得氧化物的
3 x
相对分子质量约为103×(1-18.45%)=84,故化学式为CrO 。
2
16.(15分,除标注外均2分)
(1)+148
(2)B(1分)
(3)X>Y>Z 4
(4)①温度高于500℃后,随温度升高,两个反应正向进行程度都增大,但副反应增大程度更高,故丁烯
转化率增大,但丙烯产率降低
②MgO
(5)①2H O-4e-=O ↑+4H+
2 2
②11.2
【解析】
(1)H =2049×2-1411-2539=+148kJ/mol
(3)假设充入C H (g)和C H (g)各1mol,转化的C H (g)为x mol,则有如下转化:
4 8 2 4 4 8
C H (g)+C H (g) 2C H (g)
4 8 2 4 3 6
起始/mol 1 1
转化/mol x x 2x
平衡/mol 1-x 1-x 2x
12
C H 的体积分数为2x/2=50%,x=0.5,则K 4。
3 6
0.50.5
(4)②据图可知,MgO作催化剂助剂时C H 转化率和C H 产率都最大,故选MgO。
4 8 3 6
(5)阳极反应式为2H O-4e-=O ↑+4H+,阴极反应式为3CO +18H++18e-=C H +6H O,故转移
2 2 2 3 6 2
9mol电子时生成0.5mol C H ,在标况下体积为11.2L。
3 6
17.(14分,每空2分)
(1)球形冷凝管 下口进水,上口出水
(2)排尽装置内的空气,避免空气中氧气与原料反应影响实验
70℃
(3)Fe2++2NH++CH CSNH +5OH-====FeS↓+CH COO-+3NH ↑+3H O
4 3 2 3 3 2
(4)热NaOH溶液(或CS )
2
(5)①滴入最后半滴K Cr O 溶液,溶液由无色变为紫红色,且半分钟内不变色。
2 2 7
②80%
【解析】
(3)控制混合液pH约为9,则溶液呈碱性,当加热温度为70℃时,反应生成CH COO-和NH ,制备FeS
3 3
70℃
的离子方程式为Fe2++2NH++CH CSNH +5OH-====FeS↓+CH COO-+3NH ↑+3H O。
4 3 2 3 3 2
(5)①二苯胺磺酸钠滴入含Fe2+的溶液时为还原态,到达滴定终点时变为氧化态,故变成紫红色。
②根据物质之间的转化关系,6Fe2+~K Cr O ,n(FeS)=0.1×2.5×6=1.5mol,可计算出FeS的质量
2 2 7
为132g,因此质量分数为132/165×100%=80%。
9月调研测试卷(化学)参考答案 第4页 共5页
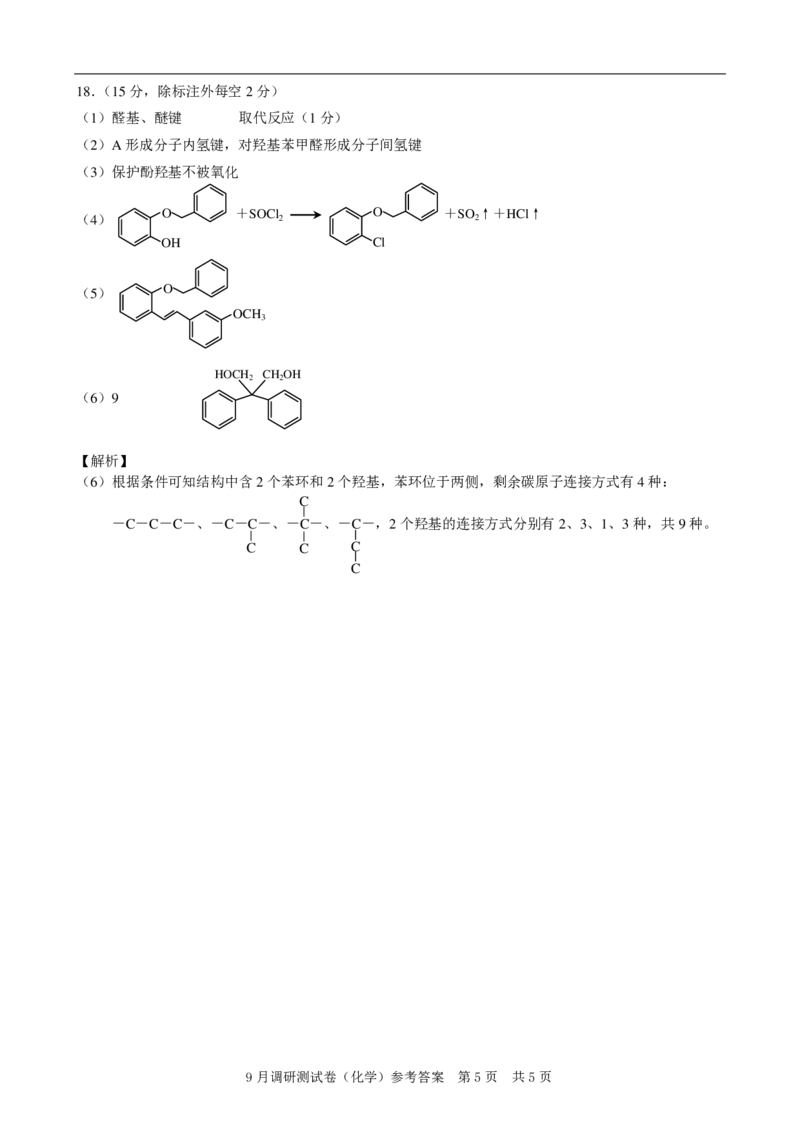
{#{QQABJYaQggCgAJBAABhCUwF4CEEQkAGAAagOwEAIMAAAwQNABAA=}#}18.(15分,除标注外每空2分)
(1)醛基、醚键 取代反应(1分)
(2)A形成分子内氢键,对羟基苯甲醛形成分子间氢键
(3)保护酚羟基不被氧化
O +SOCl O +SO ↑+HCl↑
(4) 2 2
OH Cl
(5) O
OCH
3
HOCH
2
CH
2
OH
(6)9
【解析】
(6)根据条件可知结构中含2个苯环和2个羟基,苯环位于两侧,剩余碳原子连接方式有4种:
C
-C-C-C-、-C-C-、-C-、-C-,2个羟基的连接方式分别有2、3、1、3种,共9种。
C C C
C
9月调研测试卷(化学)参考答案 第5页 共5页
{#{QQABJYaQggCgAJBAABhCUwF4CEEQkAGAAagOwEAIMAAAwQNABAA=}#}