文档内容
2023届高三化学高考备考一轮复习专题训练:工业流程题
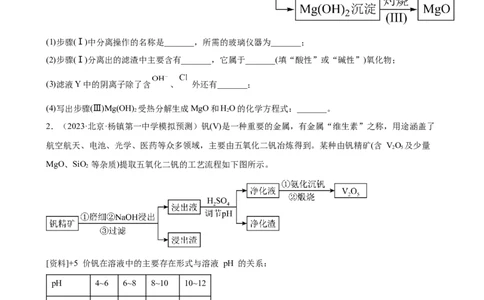
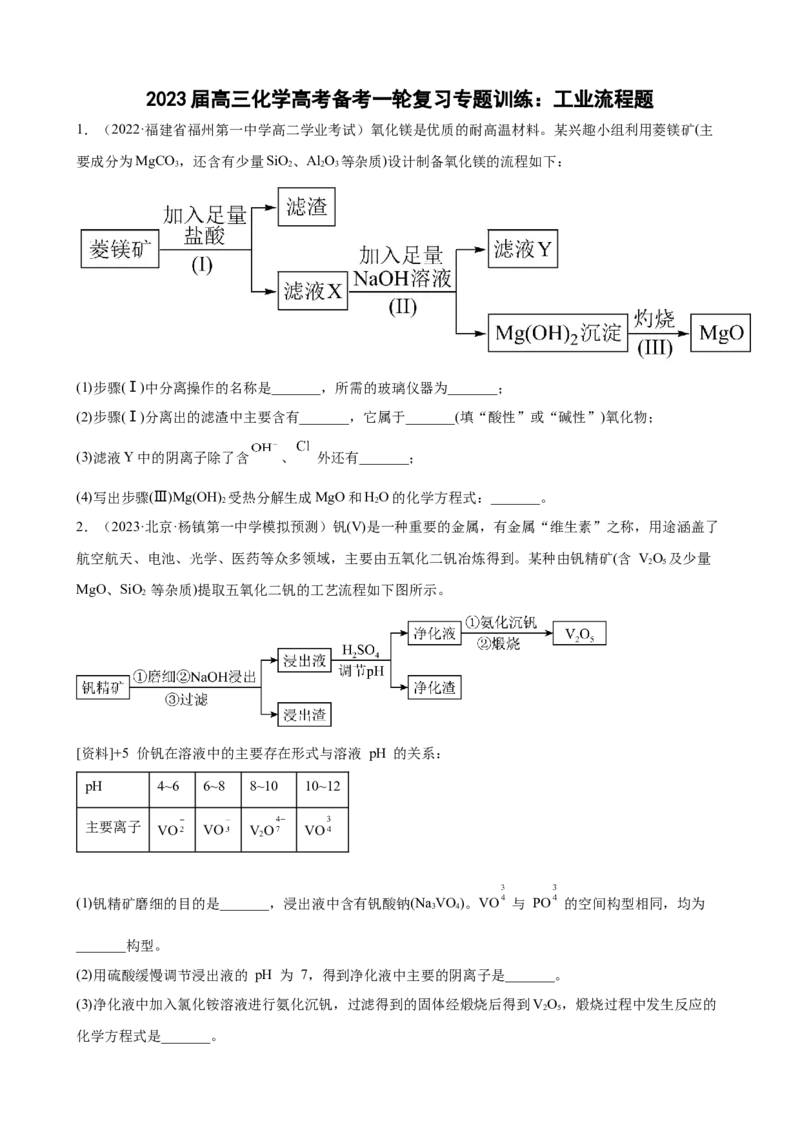
1.(2022·福建省福州第一中学高二学业考试)氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主
要成分为MgCO ,还含有少量SiO、Al O 等杂质)设计制备氧化镁的流程如下:
3 2 2 3
(1)步骤(Ⅰ)中分离操作的名称是_______,所需的玻璃仪器为_______;
(2)步骤(Ⅰ)分离出的滤渣中主要含有_______,它属于_______(填“酸性”或“碱性”)氧化物;
(3)滤液Y中的阴离子除了含 、 外还有_______;
(4)写出步骤(Ⅲ)Mg(OH) 受热分解生成MgO和HO的化学方程式:_______。
2 2
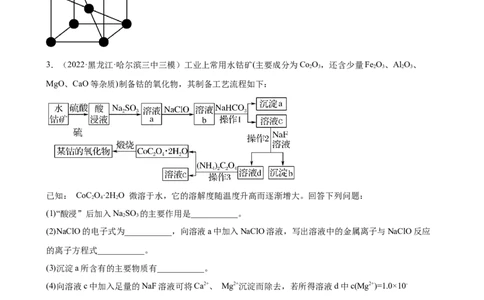
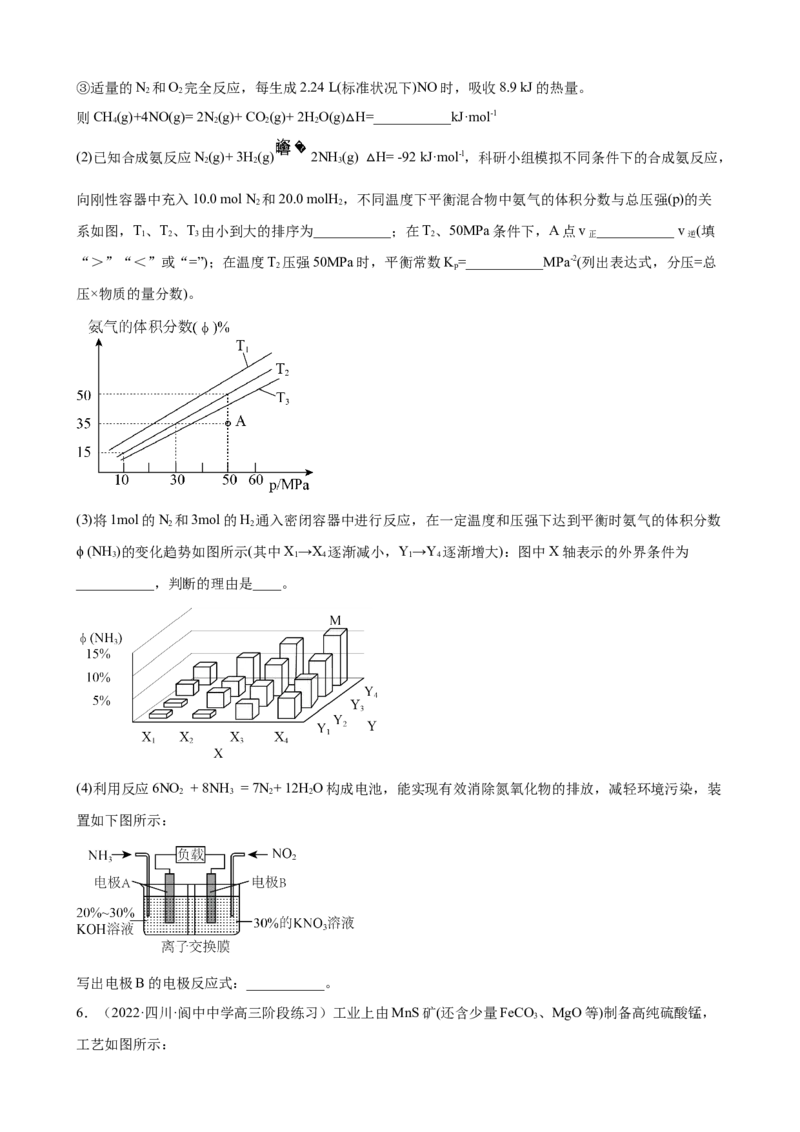
2.(2023·北京·杨镇第一中学模拟预测)钒(V)是一种重要的金属,有金属“维生素”之称,用途涵盖了
航空航天、电池、光学、医药等众多领域,主要由五氧化二钒冶炼得到。某种由钒精矿(含 VO 及少量
2 5
MgO、SiO 等杂质)提取五氧化二钒的工艺流程如下图所示。
2
[资料]+5 价钒在溶液中的主要存在形式与溶液 pH 的关系:
pH 4~6 6~8 8~10 10~12
主要离子
VO VO VO VO
2
(1)钒精矿磨细的目的是_______,浸出液中含有钒酸钠(Na VO )。VO 与 PO 的空间构型相同,均为
3 4
_______构型。
(2)用硫酸缓慢调节浸出液的 pH 为 7,得到净化液中主要的阴离子是_______。
(3)净化液中加入氯化铵溶液进行氨化沉钒,过滤得到的固体经煅烧后得到VO,煅烧过程中发生反应的
2 5
化学方程式是_______。(4)五氧化二钒的结构简式如图所示,该结构中 σ 键与 π 键个数之比是_______。
(5)钒在周期表中的位置是_______,单质钒的晶胞结构如图所示,若晶胞的棱长为 anm,密度为 ρ
g•cm-3,钒的相对原子质量为_______。(设阿伏加德罗常数的值为 N )
A
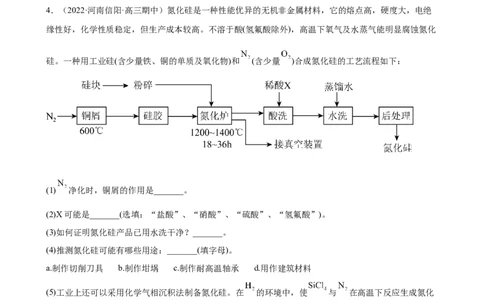
3.(2022·黑龙江·哈尔滨三中三模)工业上常用水钴矿(主要成分为Co O,还含少量Fe O、Al O、
2 3 2 3 2 3
MgO、CaO等杂质)制备钴的氧化物,其制备工艺流程如下:
已知: CoC O·2H O 微溶于水,它的溶解度随温度升高而逐渐增大。回答下列问题:
2 4 2
(1)“酸浸”后加入NaSO 的主要作用是___________。
2 3
(2)NaClO的电子式为___________,向溶液a中加入NaClO溶液,写出溶液中的金属离子与NaClO反应
的离子方程式___________。
(3)沉淀a所含有的主要物质有___________。
(4)向溶液c中加入足量的NaF溶液可将Ca2+、 Mg2+沉淀而除去,若所得溶液d中c(Mg2+)=1.0×10-
5mol/L,则溶液d中c(Ca2+)为___________。 [已知该温度下K (CaF ) =3.4 ×10-11,K (MgF )=7.1 ×10-11]
sp 2 sp 2
(5)草酸钴是制备各种钴氧化物和钴粉的重要原料,广泛应用于磁性材料、电极材料及超硬材料等领域。
草酸钴在惰性气氛中的热重分析图谱表明,350-420°C之间的失重率达59.9%,则该温度范围内草酸钴分
解的化学方程式为___________。
(6)“沉钴”过程中,加入(NH )C O 使得n( ):n(Co2+)初始比值为1.15,沉淀反应时间为10min,沉
4 2 2 4
淀反应的温度与钴的沉淀率关系如图所示。该过程需控制温度在46°C -50°C的原因是___________。
4.(2022·河南信阳·高三期中)氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝
缘性好,化学性质稳定,但生产成本较高。不溶于酸(氢氟酸除外),高温下氧气及水蒸气能明显腐蚀氮化
硅。一种用工业硅(含少量铁、铜的单质及氧化物)和 (含少量 )合成氮化硅的工艺流程如下:
(1) 净化时,铜屑的作用是_______。
(2)X可能是_______(选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)如何证明氮化硅产品已用水洗干净?_______。
(4)推测氮化硅可能有哪些用途:_______(填字母)。
a.制作切削刀具 b.制作坩埚 c.制作耐高温轴承 d.用作建筑材料
(5)工业上还可以采用化学气相沉积法制备氮化硅。在 的环境中,使 与 在高温下反应生成氮化
硅沉积在石墨表面,该反应的化学方程式为_______。
5.(2022·宁夏六盘山高级中学三模)氮及其化合物的研究对于生态环境保护和工农业生产发展非常重要。
请回答下列问题:
(1)煤燃烧产生的烟气中含有氮的氧化物NO ,用CH 催化还原NO 可消除氮氧化物的污染。
x 4 x
已知:
①CH(g)+ 2NO (g)= N (g)+CO (g)+ 2H O(g) H=-865.0 kJ·mol-l
4 2 2 2 2
②2NO(g)+O
2
(g)= 2NO
2
(g) H=-112.5 kJ·mol-△1
△③适量的N 和O 完全反应,每生成2.24 L(标准状况下)NO时,吸收8.9 kJ的热量。
2 2
则CH(g)+4NO(g)= 2N (g)+ CO (g)+ 2H O(g) H=___________kJ·mol-1
4 2 2 2
△
(2)已知合成氨反应N(g)+ 3H (g) 2NH (g) H= -92 kJ·mol-l,科研小组模拟不同条件下的合成氨反应,
2 2 3
△
向刚性容器中充入10.0 mol N 和20.0 molH ,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关
2 2
系如图,T、T、T 由小到大的排序为___________;在T、50MPa条件下,A点v ___________ v (填
1 2 3 2 正 逆
“>”“<”或“=”);在温度T 压强50MPa时,平衡常数K=___________MPa-2(列出表达式,分压=总
2 p
压×物质的量分数)。
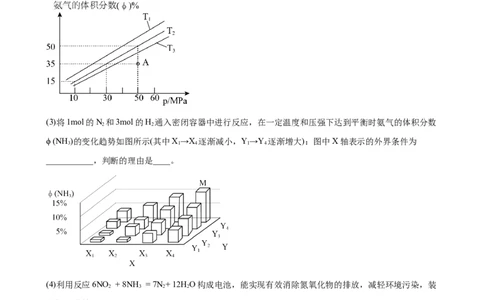
(3)将1mol的N 和3mol的H 通入密闭容器中进行反应,在一定温度和压强下达到平衡时氨气的体积分数
2 2
ϕ (NH )的变化趋势如图所示(其中X→X 逐渐减小,Y→Y 逐渐增大):图中X轴表示的外界条件为
3 1 4 1 4
___________,判断的理由是____。
(4)利用反应6NO + 8NH = 7N + 12H O构成电池,能实现有效消除氮氧化物的排放,减轻环境污染,装
2 3 2 2
置如下图所示:
写出电极B的电极反应式:___________。
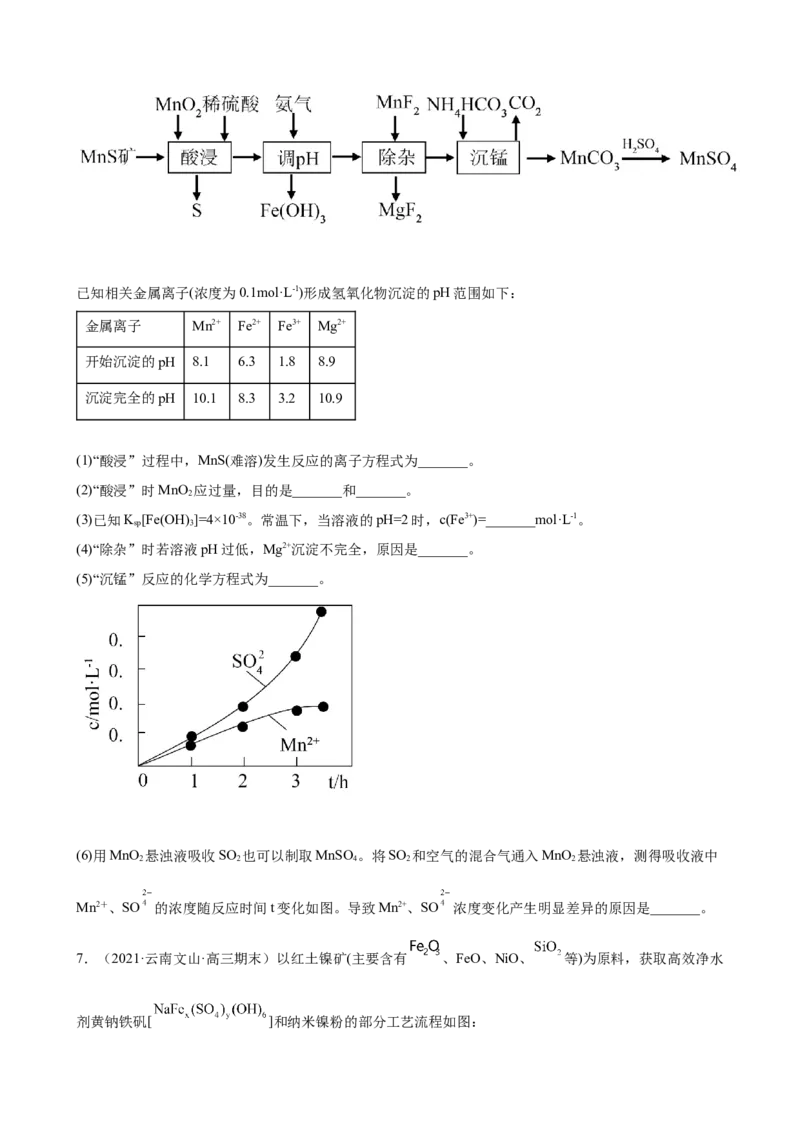
6.(2022·四川·阆中中学高三阶段练习)工业上由MnS矿(还含少量FeCO、MgO等)制备高纯硫酸锰,
3
工艺如图所示:已知相关金属离子(浓度为0.1mol·L-1)形成氢氧化物沉淀的pH范围如下:
金属离子 Mn2+ Fe2+ Fe3+ Mg2+
开始沉淀的pH 8.1 6.3 1.8 8.9
沉淀完全的pH 10.1 8.3 3.2 10.9
(1)“酸浸”过程中,MnS(难溶)发生反应的离子方程式为_______。
(2)“酸浸”时MnO 应过量,目的是_______和_______。
2
(3)已知K [Fe(OH) ]=4×10-38。常温下,当溶液的pH=2时,c(Fe3+)=_______mol·L-1。
sp 3
(4)“除杂”时若溶液pH过低,Mg2+沉淀不完全,原因是_______。
(5)“沉锰”反应的化学方程式为_______。
(6)用MnO 悬浊液吸收SO 也可以制取MnSO 。将SO 和空气的混合气通入MnO 悬浊液,测得吸收液中
2 2 4 2 2
Mn2+、SO 的浓度随反应时间t变化如图。导致Mn2+、SO 浓度变化产生明显差异的原因是_______。
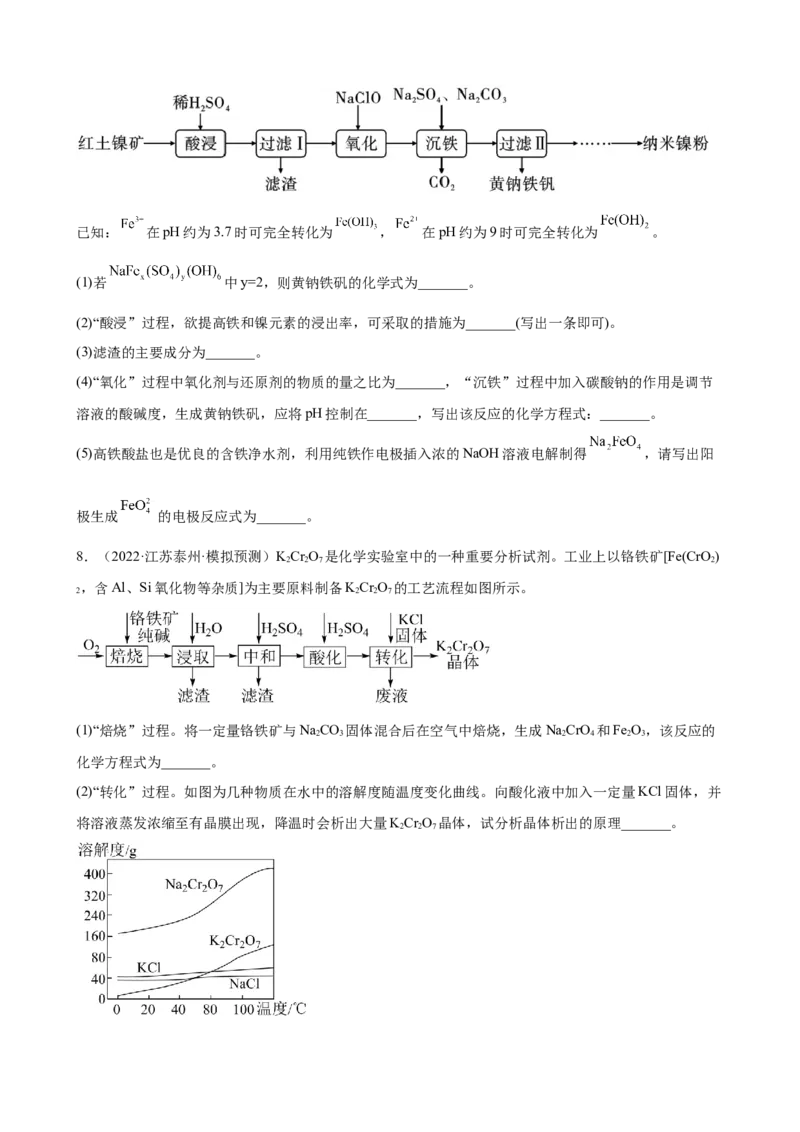
7.(2021·云南文山·高三期末)以红土镍矿(主要含有 、FeO、NiO、 等)为原料,获取高效净水
剂黄钠铁矾[ ]和纳米镍粉的部分工艺流程如图:已知: 在pH约为3.7时可完全转化为 , 在pH约为9时可完全转化为 。
(1)若 中y=2,则黄钠铁矾的化学式为_______。
(2)“酸浸”过程,欲提高铁和镍元素的浸出率,可采取的措施为_______(写出一条即可)。
(3)滤渣的主要成分为_______。
(4)“氧化”过程中氧化剂与还原剂的物质的量之比为_______,“沉铁”过程中加入碳酸钠的作用是调节
溶液的酸碱度,生成黄钠铁矾,应将pH控制在_______,写出该反应的化学方程式:_______。
(5)高铁酸盐也是优良的含铁净水剂,利用纯铁作电极插入浓的NaOH溶液电解制得 ,请写出阳
极生成 的电极反应式为_______。
8.(2022·江苏泰州·模拟预测)KCr O 是化学实验室中的一种重要分析试剂。工业上以铬铁矿[Fe(CrO )
2 2 7 2
,含Al、Si氧化物等杂质]为主要原料制备KCr O 的工艺流程如图所示。
2 2 2 7
(1)“焙烧”过程。将一定量铬铁矿与NaCO 固体混合后在空气中焙烧,生成NaCrO 和Fe O,该反应的
2 3 2 4 2 3
化学方程式为_______。
(2)“转化”过程。如图为几种物质在水中的溶解度随温度变化曲线。向酸化液中加入一定量KCl固体,并
将溶液蒸发浓缩至有晶膜出现,降温时会析出大量KCr O 晶体,试分析晶体析出的原理_______。
2 2 7(3)生产过程中产生的KCr O 酸性废液可通过以下方法处理。
2 2 7
①钡盐沉淀法。先将KCr O 酸性废液碱化处理,再加入BaCl 废液需进行碱化处理的目的是_______。
2 2 7 2.
[已知:BaCrO(s) Ba2+(aq)+ CrO (aq) ΔH>0;K (BaCrO)=1.2×10-10]
4 sp 4
②FeS还原法。在KCr O 酸性废液中加入纳米FeS后,测得Cr(Ⅵ)和总铬去除率随时间的变化关系如图
2 2 7
所示,反应过程中还检测到Cr S 沉淀。10 min后,Cr(Ⅵ)和总铬的去除率升高幅度变小的可能原因是
2 3
_______。
(4)测定KCr O 产品纯度。称取产品2.500 g配成500 mL溶液,取25.00 mL于锥形瓶中,加10 mL 2
2 2 7
mol·L-1HSO 和足量KI,放于暗处5 min ( +I-→I+Cr3+)。然后加入100 mL水,加入3 mL淀粉溶液,
2 4 2
用0.1200 mol·L-1NaSO 标准溶液滴定(I+ →I-+ ),消耗20.00 mLNa SO 标准溶液,则该样品的
2 2 3 2 2 2 3
纯度为_______。(写出计算过程)
9.(2022·河南开封·模拟预测)一种从钼镍废催化剂(主要含MoS 、NiS、Al O、SiO 以及C)中回收镍
2 2 3 2
和钼的工艺流程如下:
回答下列问题:(1)写出“培烧”时产生的CO 的电子式:_______。
2
(2)“焙烧”时,MoS 首先转化为MoO ,写出该反应的化学方程式:_______。
2 3
(3)写出滤液中溶质的一种工业用途:_______ ;“净化2”时,发生反应的离子方程式为_______。
(4)已知常温下,K (CaMoO )=1.46×10-8;K (CaCO)=3.36×10-9,由CaMoO 制备NaMoO 的方法是
sp 4 sp 3 4 2 4
_______。
(5)已知NiO是不溶于水的碱性氧化物,由浸渣“除铝”所用的试剂是_______ ;“酸溶”得到的溶液制
备NiSO ·7H O的操作方法是_______、过滤、洗涤、干燥。
4 2
(6)若废催化剂中含160 g MoS ,上,述工艺中获得CaMoO 的质量为190 g,则CaMoO 的产率为_______。
2 4 4
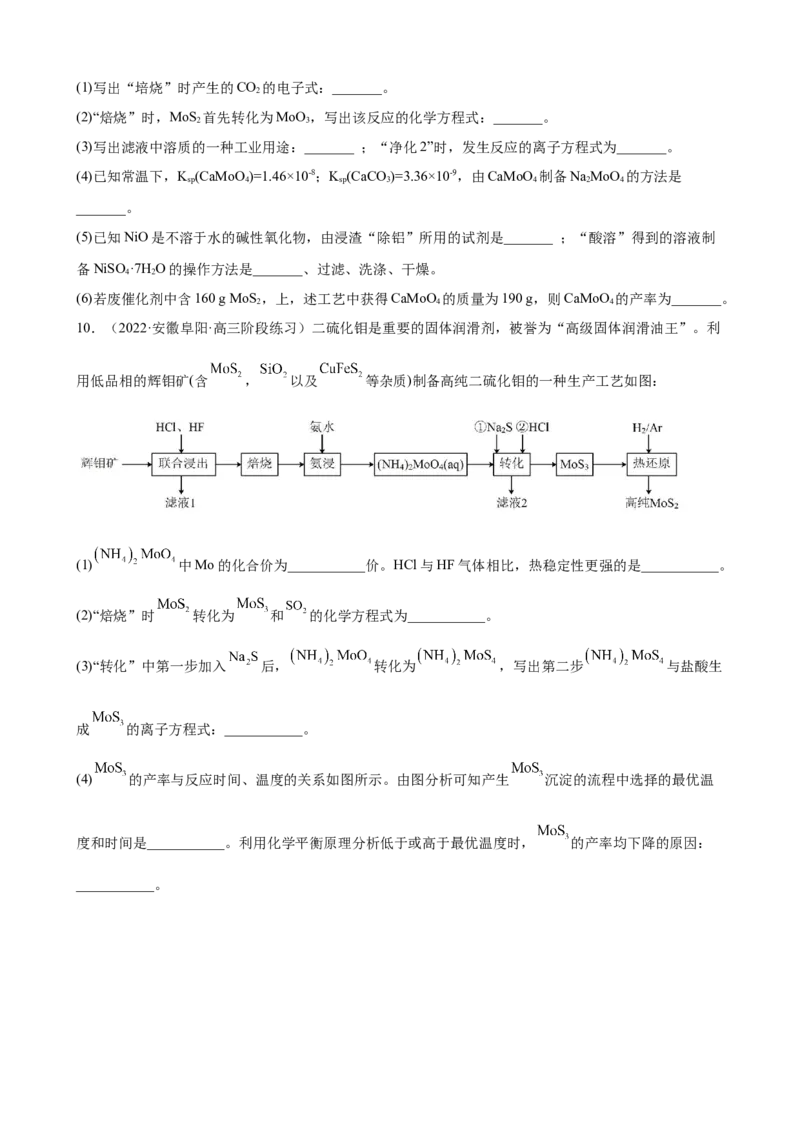
10.(2022·安徽阜阳·高三阶段练习)二硫化钼是重要的固体润滑剂,被誉为“高级固体润滑油王”。利
用低品相的辉钼矿(含 , 以及 等杂质)制备高纯二硫化钼的一种生产工艺如图:
(1) 中Mo的化合价为___________价。HCl与HF气体相比,热稳定性更强的是___________。
(2)“焙烧”时 转化为 和 的化学方程式为___________。
(3)“转化”中第一步加入 后, 转化为 ,写出第二步 与盐酸生
成 的离子方程式:___________。
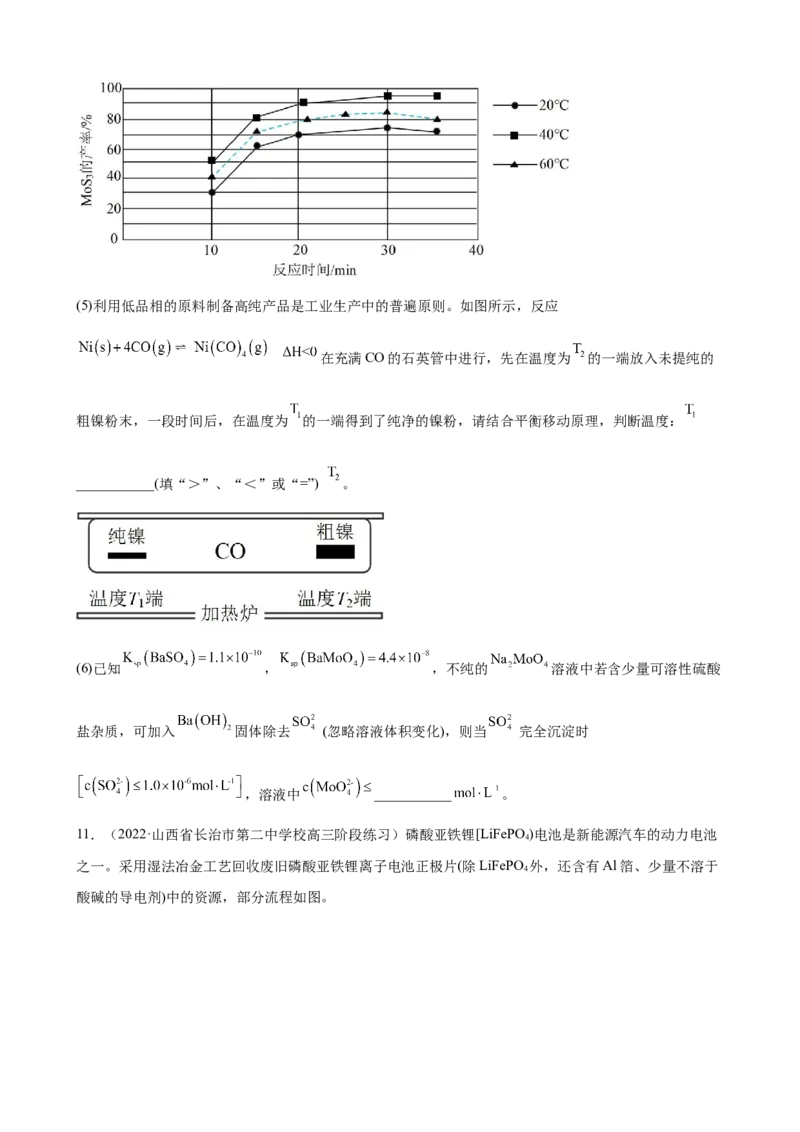
(4) 的产率与反应时间、温度的关系如图所示。由图分析可知产生 沉淀的流程中选择的最优温
度和时间是___________。利用化学平衡原理分析低于或高于最优温度时, 的产率均下降的原因:
___________。(5)利用低品相的原料制备高纯产品是工业生产中的普遍原则。如图所示,反应
在充满CO的石英管中进行,先在温度为 的一端放入未提纯的
粗镍粉末,一段时间后,在温度为 的一端得到了纯净的镍粉,请结合平衡移动原理,判断温度:
___________(填“>”、“<”或“=”) 。
(6)已知 , ,不纯的 溶液中若含少量可溶性硫酸
盐杂质,可加入 固体除去 (忽略溶液体积变化),则当 完全沉淀时
,溶液中 ___________ 。
11.(2022·山西省长治市第二中学校高三阶段练习)磷酸亚铁锂[LiFePO )电池是新能源汽车的动力电池
4
之一。采用湿法冶金工艺回收废旧磷酸亚铁锂离子电池正极片(除LiFePO 外,还含有Al箔、少量不溶于
4
酸碱的导电剂)中的资源,部分流程如图。已知:LiCO 为无色晶体,在水中的溶解度随温度升高而减小。
2 3
(1)LiFePO 中铁元素的化合价为 ___________。
4
(2)“正极碱浸”时,Al箔溶解的离子方程式为 ___________。为提高“正极碱浸”速率,除适当升高温度
外,还可采取的措施有 ___________。
(3)“氧化浸出”时,一般选用HO 作为氧化剂,该步操作加热温度不宜过高的原因是 ___________。
2 2
(4)最后一步“一系列操作”包括趁热过滤、洗涤、干燥。检验LiCO 沉淀是否洗干净的方法是
2 3
___________。
(5)工业上将回收的LiCO、FePO ,粉碎与过量炭黑混合高温灼烧再生制备LiFePO ,写出反应的化学方
2 3 4 4
程式:___________。
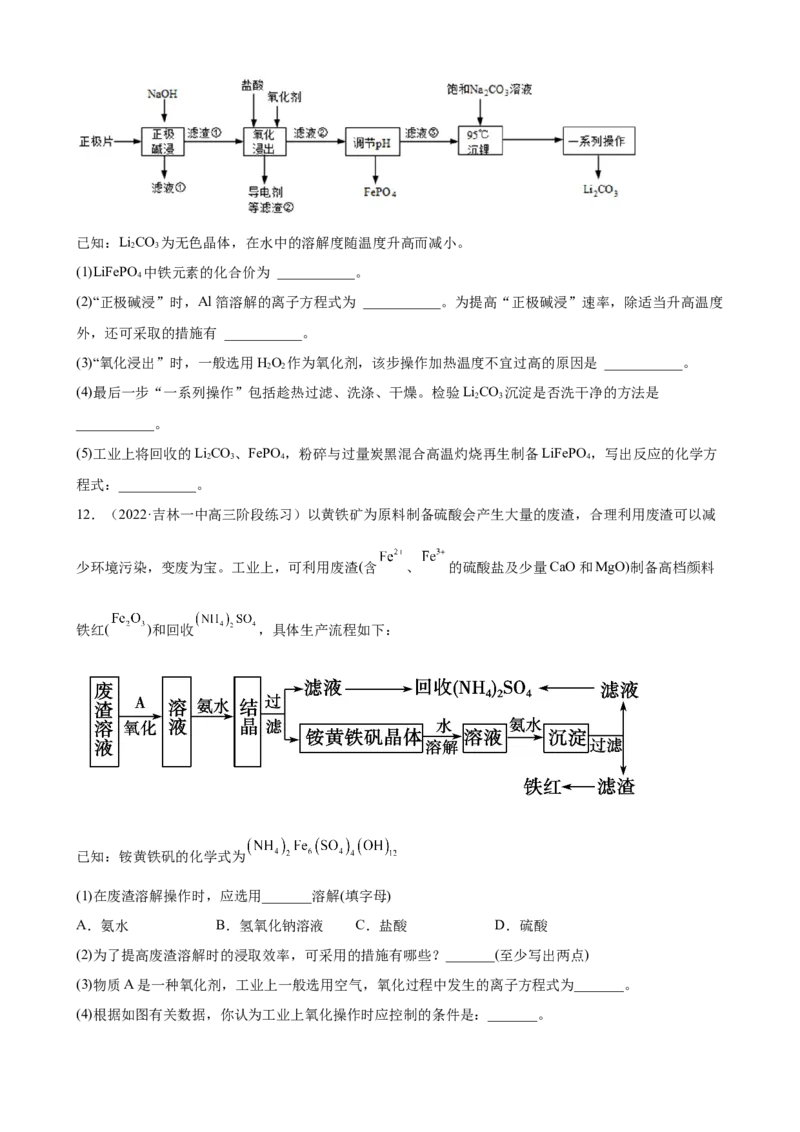
12.(2022·吉林一中高三阶段练习)以黄铁矿为原料制备硫酸会产生大量的废渣,合理利用废渣可以减
少环境污染,变废为宝。工业上,可利用废渣(含 、 的硫酸盐及少量CaO和MgO)制备高档颜料
铁红( )和回收 ,具体生产流程如下:
已知:铵黄铁矾的化学式为
(1)在废渣溶解操作时,应选用_______溶解(填字母)
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2)为了提高废渣溶解时的浸取效率,可采用的措施有哪些?_______(至少写出两点)
(3)物质A是一种氧化剂,工业上一般选用空气,氧化过程中发生的离子方程式为_______。
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件是:_______。(5)铵黄铁矾中铁为_______价,可能混有的杂质有 、 、_______。铵黄铁矾与氨水反应
的离子方程式为_______。
13.(2022·广东·高考真题)稀土( )包括镧、钇等元素,是高科技发展的关键支撑。我国南方特有的
稀土矿可用离子交换法处理,一种从该类矿(含铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属离
子沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位有效
数字)。
(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为
_______。
14.(2022·江西·模拟预测)硫酸亚铁可用于治疗缺铁性贫血。利用黄铜矿(CuFeS)制备硫酸亚铁并回收
2
铜的工艺流程如图所示:
(1)①焙烧生成的SO 可用柠檬酸-柠檬酸钠溶液进行吸收,该过程采用逆流接触法进行吸收的原因是
2
_______。
②还可用电化学氧化法处理SO ,同时生成HSO ,写出SO 参与反应的电极反应式:_______。
2 2 4 2
(2)还原过程中加入的X为_____(填化学式),该过程发生反应的离子方程式是_______。
(3)滤渣的主要成分是_______(填化学式)。
(4)①向滤液中加入稀硫酸后经蒸发浓缩、冷却结晶、过滤可得绿矾晶体,加入稀硫酸的目的是_______。
②为测定产品FeSO ·xH O中结晶水的数量,称取14g产品配制成250mL待测液,准确量取25.00mL待测
4 2
液于锥形瓶中加稀硫酸酸化,用0.0500mol·L-1KMnO 标准溶液滴定至终点,重复三次,平均消耗KMnO
4 4
溶液的体积为20.00mL,则x=_______。
15.(2022·安徽·合肥市第八中学模拟预测)2022北京冬奥会期间的交通服务用车中,氢燃料电车占了绝
大多数。氢氧燃料电池中,贵金属Pt作为催化剂起到关键作用。下列是从某阳极泥中回收铂、金的工艺
流程图,请仔细阅读信息后作答:(1)“酸浸氧化”中无气体排出,此时通入氧气的目的是____,“滤液”中的金属阳离子有____。
(2)若“酸溶”得到的[PtCl ]2-和[AuCl ]-的物质的量均为1mol,则消耗的氯气至少为___________mol。
6 4
(3)沉金过程中的离子反应方程式为___________。
(4)“沉铂”中,生成(NH )PtCl 的沉淀率随温度升高而呈升高趋势,请结合化学反应方程式解释升高温度,
4 2 6
(NH )PtCl 沉淀率升高的主要原因___________。
4 2 6
(5)滤渣氯铂酸铵[(NH )PtCl ]表面有大量氯化铵等可溶性的盐,需要洗涤除去,洗涤沉淀的方法是
4 2 6
___________。
(6)写出(NH )PtCl 灼烧时的化学反应方程式___________。
4 2 6
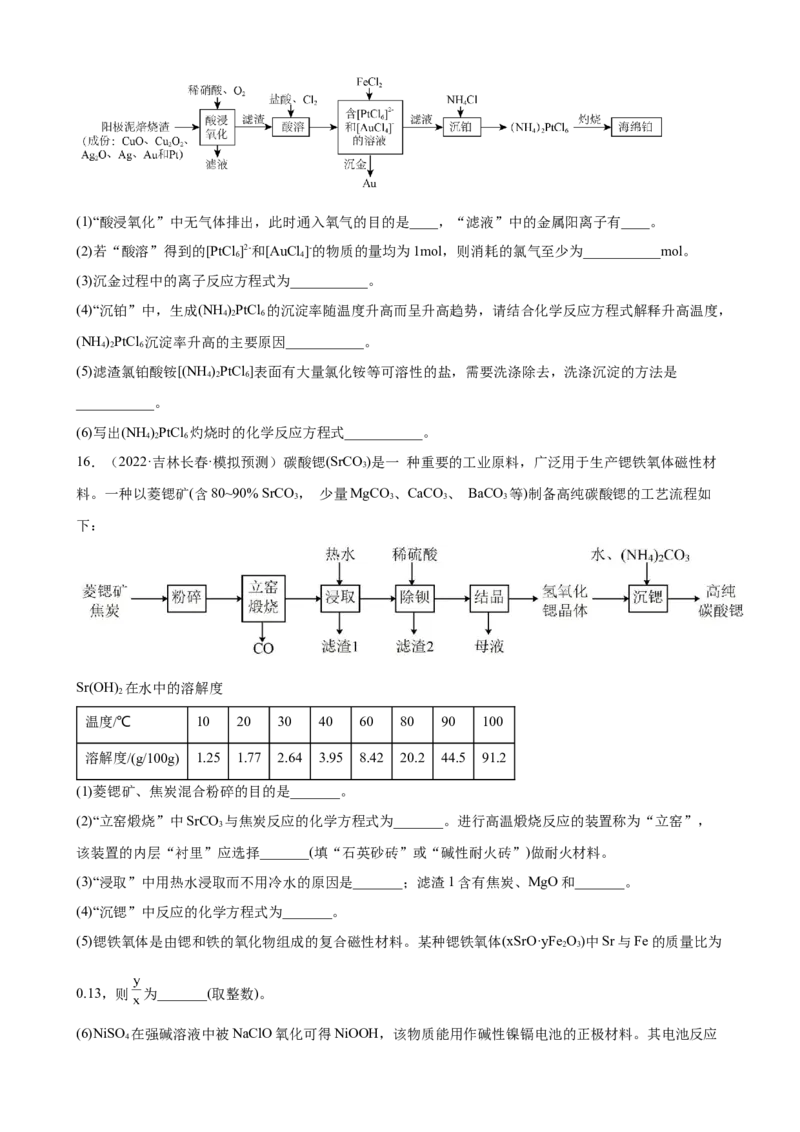
16.(2022·吉林长春·模拟预测)碳酸锶(SrCO )是一 种重要的工业原料,广泛用于生产锶铁氧体磁性材
3
料。一种以菱锶矿(含80~90% SrCO , 少量MgCO 、CaCO 、 BaCO 等)制备高纯碳酸锶的工艺流程如
3 3 3 3
下:
Sr(OH) 在水中的溶解度
2
温度/℃ 10 20 30 40 60 80 90 100
溶解度/(g/100g) 1.25 1.77 2.64 3.95 8.42 20.2 44.5 91.2
(1)菱锶矿、焦炭混合粉碎的目的是_______。
(2)“立窑煅烧”中SrCO 与焦炭反应的化学方程式为_______。进行高温煅烧反应的装置称为“立窑”,
3
该装置的内层“衬里”应选择_______(填“石英砂砖”或“碱性耐火砖”)做耐火材料。
(3)“浸取”中用热水浸取而不用冷水的原因是_______;滤渣1含有焦炭、MgO和_______。
(4)“沉锶”中反应的化学方程式为_______。
(5)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe O)中Sr与Fe的质量比为
2 3
0.13,则 为_______(取整数)。
(6)NiSO 在强碱溶液中被NaClO氧化可得NiOOH,该物质能用作碱性镍镉电池的正极材料。其电池反应
4式:Cd (s) +2NiOOH(s) +2H O (1) Cd (OH) (s) +2Ni (OH) (s)
2 2 2
①放电一段时间后,溶液的pH将_______(填 “增大”“减小”或“不变”)。
②充电时,阳极发生的电极反应式为_______。
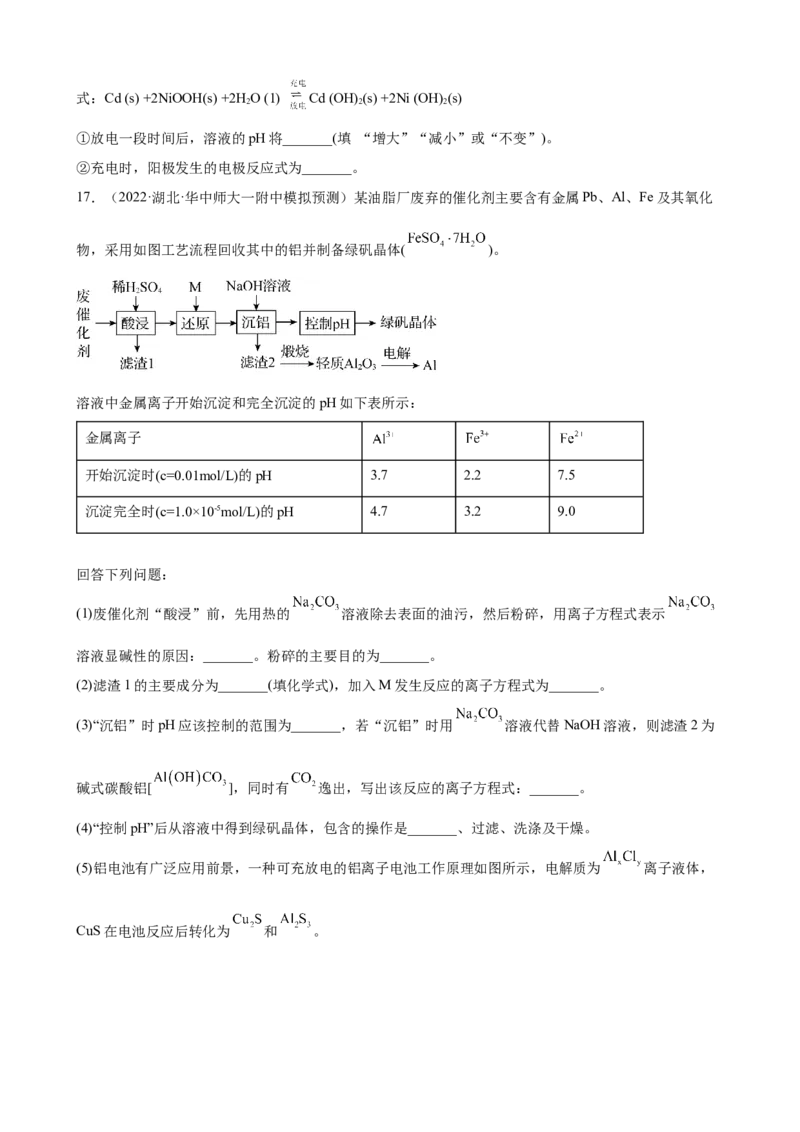
17.(2022·湖北·华中师大一附中模拟预测)某油脂厂废弃的催化剂主要含有金属Pb、Al、Fe及其氧化
物,采用如图工艺流程回收其中的铝并制备绿矾晶体( )。
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子
开始沉淀时(c=0.01mol/L)的pH 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5mol/L)的pH 4.7 3.2 9.0
回答下列问题:
(1)废催化剂“酸浸”前,先用热的 溶液除去表面的油污,然后粉碎,用离子方程式表示
溶液显碱性的原因:_______。粉碎的主要目的为_______。
(2)滤渣1的主要成分为_______(填化学式),加入M发生反应的离子方程式为_______。
(3)“沉铝”时pH应该控制的范围为_______,若“沉铝”时用 溶液代替NaOH溶液,则滤渣2为
碱式碳酸铝[ ],同时有 逸出,写出该反应的离子方程式:_______。
(4)“控制pH”后从溶液中得到绿矾晶体,包含的操作是_______、过滤、洗涤及干燥。
(5)铝电池有广泛应用前景,一种可充放电的铝离子电池工作原理如图所示,电解质为 离子液体,
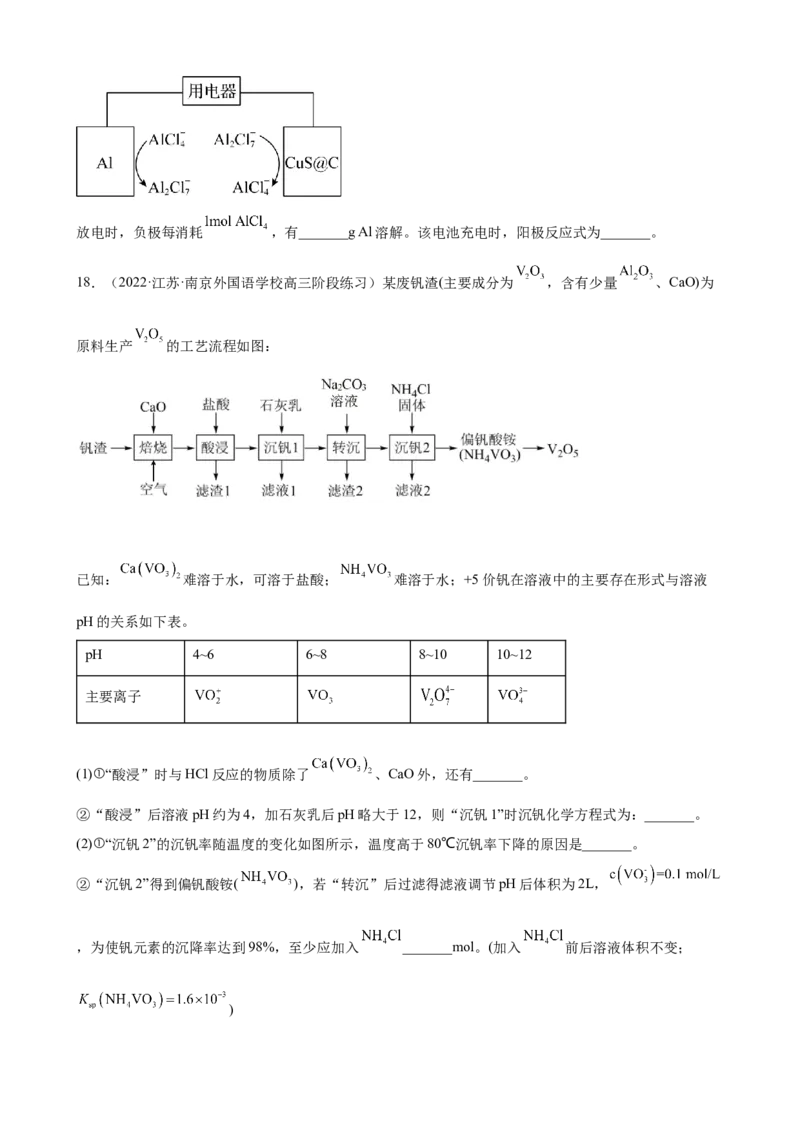
CuS在电池反应后转化为 和 。放电时,负极每消耗 ,有_______g Al溶解。该电池充电时,阳极反应式为_______。
18.(2022·江苏·南京外国语学校高三阶段练习)某废钒渣(主要成分为 ,含有少量 、CaO)为
原料生产 的工艺流程如图:
已知: 难溶于水,可溶于盐酸; 难溶于水;+5价钒在溶液中的主要存在形式与溶液
pH的关系如下表。
pH 4~6 6~8 8~10 10~12
主要离子
(1)①“酸浸”时与HCl反应的物质除了 、CaO外,还有_______。
②“酸浸”后溶液pH约为4,加石灰乳后pH略大于12,则“沉钒1”时沉钒化学方程式为:_______。
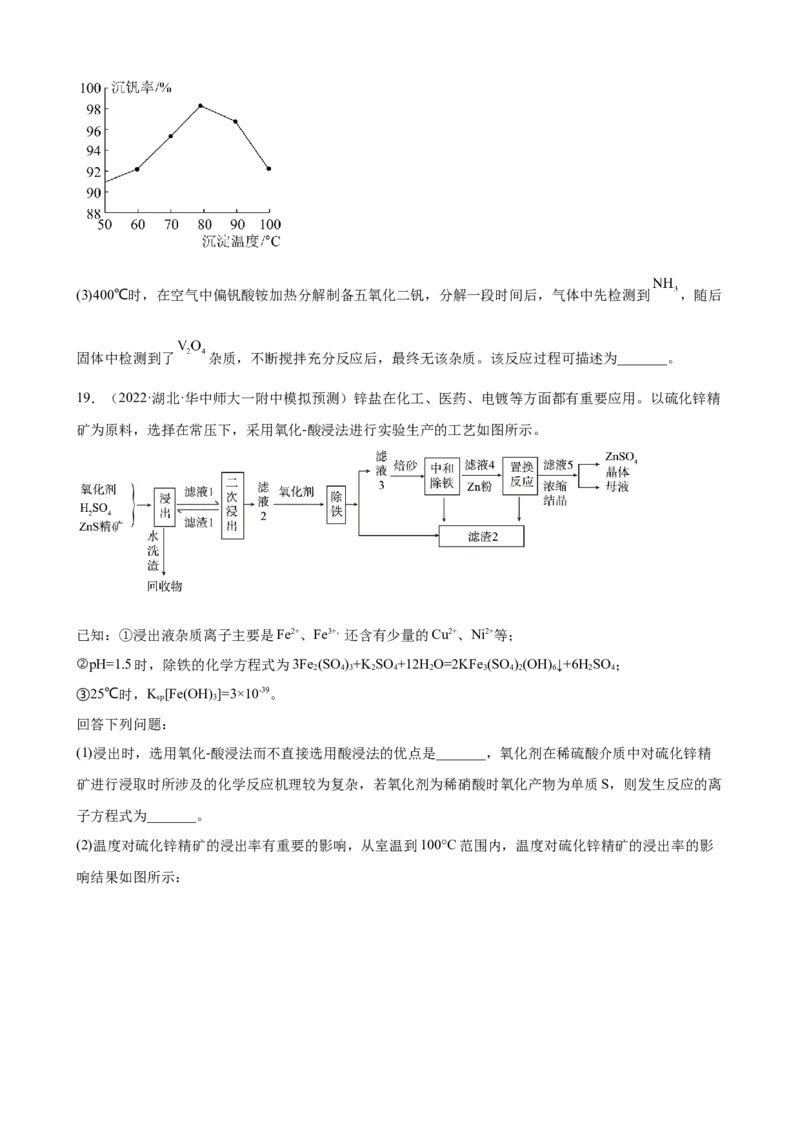
(2)①“沉钒2”的沉钒率随温度的变化如图所示,温度高于80℃沉钒率下降的原因是_______。
②“沉钒2”得到偏钒酸铵( ),若“转沉”后过滤得滤液调节pH后体积为2L,
,为使钒元素的沉降率达到98%,至少应加入 _______mol。(加入 前后溶液体积不变;
)(3)400℃时,在空气中偏钒酸铵加热分解制备五氧化二钒,分解一段时间后,气体中先检测到 ,随后
固体中检测到了 杂质,不断搅拌充分反应后,最终无该杂质。该反应过程可描述为_______。
19.(2022·湖北·华中师大一附中模拟预测)锌盐在化工、医药、电镀等方面都有重要应用。以硫化锌精
矿为原料,选择在常压下,采用氧化-酸浸法进行实验生产的工艺如图所示。
已知:①浸出液杂质离子主要是Fe2+、Fe3+,还含有少量的Cu2+、Ni2+等;
②pH=1.5时,除铁的化学方程式为3Fe (SO )+K SO +12H O=2KFe (SO )(OH) ↓+6H SO ;
2 4 3 2 4 2 3 4 2 6 2 4
③25℃时,K [Fe(OH) ]=3×10-39。
sp 3
回答下列问题:
(1)浸出时,选用氧化-酸浸法而不直接选用酸浸法的优点是_______,氧化剂在稀硫酸介质中对硫化锌精
矿进行浸取时所涉及的化学反应机理较为复杂,若氧化剂为稀硝酸时氧化产物为单质S,则发生反应的离
子方程式为_______。
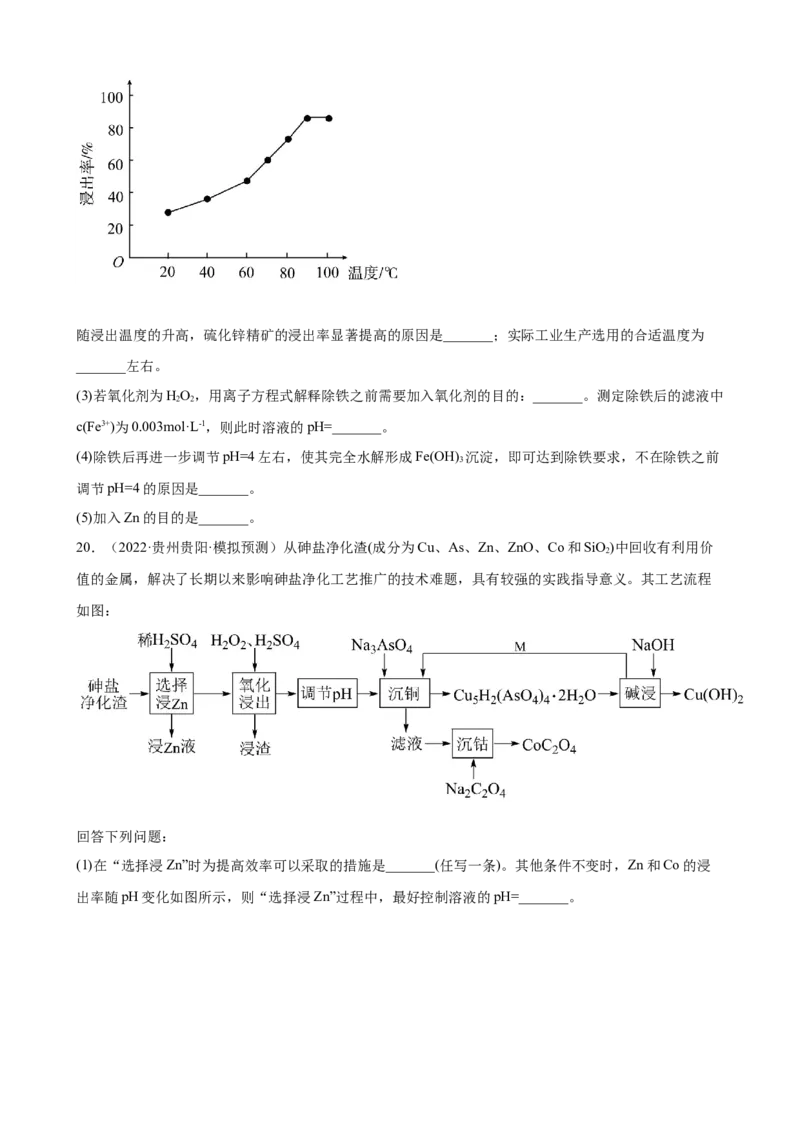
(2)温度对硫化锌精矿的浸出率有重要的影响,从室温到100°C范围内,温度对硫化锌精矿的浸出率的影
响结果如图所示:随浸出温度的升高,硫化锌精矿的浸出率显著提高的原因是_______;实际工业生产选用的合适温度为
_______左右。
(3)若氧化剂为HO,用离子方程式解释除铁之前需要加入氧化剂的目的:_______。测定除铁后的滤液中
2 2
c(Fe3+)为0.003mol·L-1,则此时溶液的pH=_______。
(4)除铁后再进一步调节pH=4左右,使其完全水解形成Fe(OH) 沉淀,即可达到除铁要求,不在除铁之前
3
调节pH=4的原因是_______。
(5)加入Zn的目的是_______。
20.(2022·贵州贵阳·模拟预测)从砷盐净化渣(成分为Cu、As、Zn、ZnO、Co和SiO)中回收有利用价
2
值的金属,解决了长期以来影响砷盐净化工艺推广的技术难题,具有较强的实践指导意义。其工艺流程
如图:
回答下列问题:
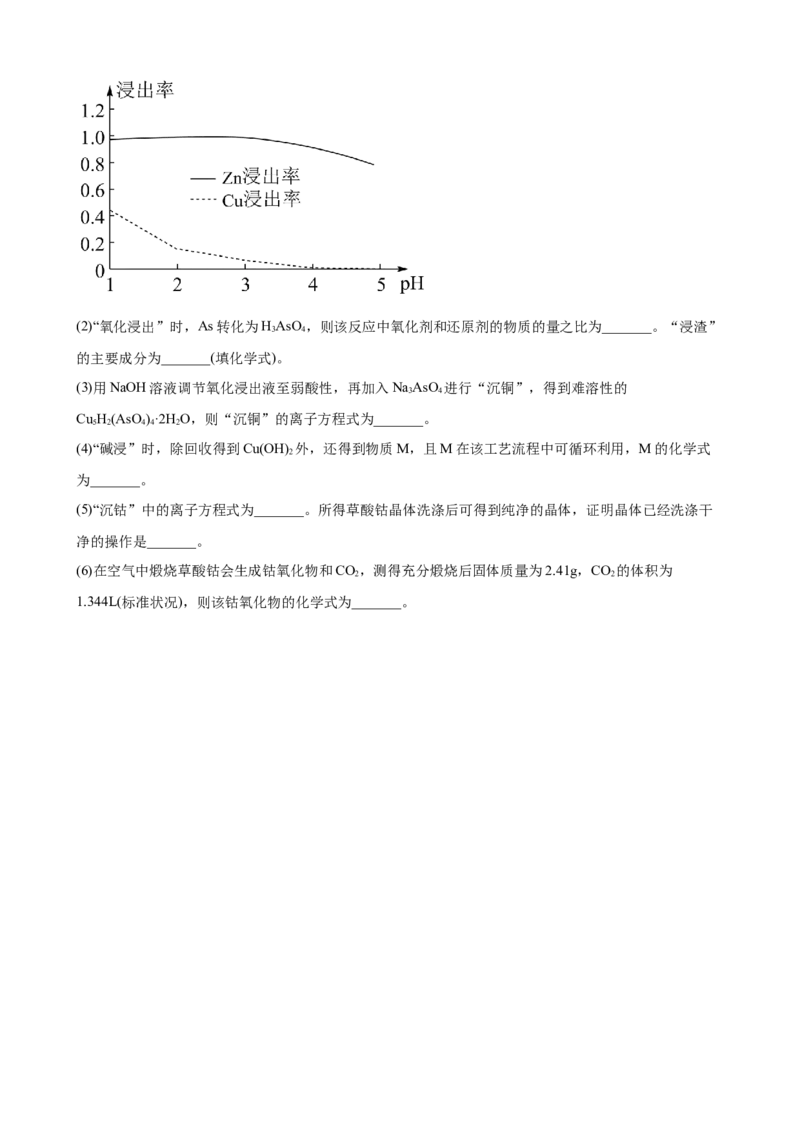
(1)在“选择浸Zn”时为提高效率可以采取的措施是_______(任写一条)。其他条件不变时,Zn和Co的浸
出率随pH变化如图所示,则“选择浸Zn”过程中,最好控制溶液的pH=_______。(2)“氧化浸出”时,As转化为HAsO ,则该反应中氧化剂和还原剂的物质的量之比为_______。“浸渣”
3 4
的主要成分为_______(填化学式)。
(3)用NaOH溶液调节氧化浸出液至弱酸性,再加入NaAsO 进行“沉铜”,得到难溶性的
3 4
Cu H(AsO)·2H O,则“沉铜”的离子方程式为_______。
5 2 4 4 2
(4)“碱浸”时,除回收得到Cu(OH) 外,还得到物质M,且M在该工艺流程中可循环利用,M的化学式
2
为_______。
(5)“沉钴”中的离子方程式为_______。所得草酸钴晶体洗涤后可得到纯净的晶体,证明晶体已经洗涤干
净的操作是_______。
(6)在空气中煅烧草酸钴会生成钴氧化物和CO,测得充分煅烧后固体质量为2.41g,CO 的体积为
2 2
1.344L(标准状况),则该钴氧化物的化学式为_______。参考答案:
1.(1) 过滤 漏斗、烧杯、玻璃棒
(2) SiO 酸性
2
(3)AlO
(4)Mg(OH) MgO+H O
2 2
2.(1) 增大接触面积,加快反应速率和提高V的浸出率 正四面体
(2) 和
(3)2NH VO VO+2NH↑+H O
4 3 2 5 3 2
(4)3:2
(5) 第四周期第VB族 5ρd3N ×10-22
A
3.(1)将Fe3+、Co3+还原为Fe2+、Co2+
(2)
(3)
(4)
(5) ↑
(6)温度过低沉淀过程反应速率较慢,温度过高, 的溶解度随温度的升高而
增大
4.(1)除去氮气中含有的少量氧气
(2)硝酸
(3)取最后一次洗涤液,测其pH为中性,则说明已水洗干净
(4)abc
(5)
5.(1)-1155.5(2) T <T<T >
1 2 3
(3) 温度 该反应为放热反应,降低温度,平衡向正反应方向移动,ϕ(NH)增大
3
(4)
6.(1)MnS+MnO +4H+=S+2Mn2++2HO
2 2
(2) 提高MnS的转化率 将Fe2+氧化为Fe3+
(3)4×10-2
(4)H+与F-反应生成弱酸HF
(5)2NH HCO +MnSO =MnCO↓+(NH )SO +CO↑+HO
4 3 4 3 4 2 4 2 2
(6)Mn2+催化O 与HSO 反应生成HSO
2 2 3 2 4
7.(1)
(2)适当升温、适当增大硫酸浓度、将原料粉碎(合理答案均可)
(3)
(4)
(5)
8.(1)4Fe(CrO )+7O +8Na CO 8NaCrO +2Fe O +8CO
2 2 2 2 3 2 4 2 3 2
(2)低温下,KCr O 的溶解度小于其它组分;随着温度的降低,KCr O 的溶解度明显减小
2 2 7 2 2 7
(3) 促进 转化为 , 浓度升高,有利于与Ba2+生成沉淀 H+浓度
减小,与FeS反应生成具有强还原性的Fe2+、HS-和HS浓度减小, Cr(Ⅵ)还原成Cr(Ⅲ)的
2
速率减小;生成Cr S 沉淀覆盖在FeS表面,减慢其溶解
2 3
(4)94.08%
9.(1)(2)2MoS +7O 4SO +2MoO
2 2 2 3
(3) 制造氯气、纯碱 +H++H O=Al(OH) ↓
2 3
(4)用浓NaCO 溶液充分浸取CaMoO 固体,过滤
2 3 4
(5) 氢氧化钠溶液 蒸发浓缩、冷却结晶
(6)95%
10.(1) +6 HF
(2)
(3)
(4) 40oC,30min 温度太低,反应 产生的气体不易逸出,
不利于平衡正向移动生成MoS ;温度太高,反应物盐酸易挥发,导致溶液中的氢离子浓度,
3
平衡逆向移动,不利于生成MoS ;
3
(5)>
(6)
11.(1)+2
(2) 2Al+2OH﹣+2H O═2AlO +3H ↑ 将正极片粉碎、反应过程中不断搅拌或适当增大
2 2
NaOH溶液的浓度
(3)防止盐酸挥发和HO 受热分解
2 2
(4)取最后一次洗涤液少量于试管中,加入硝酸酸化的硝酸银溶液,若无明显现象,则沉淀
已洗干净
(5)
12.(1)D
(2)废渣粉碎、升高温度
(3)
(4)80℃、pH=1.5(5) +3
13.(1)Fe2+
(2) 4.7 pH<6.2
(3)4.0 10-4
(4) 加热搅拌可加快反应速率 冷却结晶
(5)MgSO
4
(6) 15 O+4e-+2H O=4OH-
2 2
14.(1) 增大气体和液体的接触面积,提高SO 吸收率 SO -2e-+2H O=
2 2 2
+4H+
(2) Fe Fe+Cu2+=Fe2++Cu、Fe+2Fe3+=3Fe2+
(3)Cu、Fe
(4) 抑制Fe2+水解 7
15.(1) 防止硝酸产生的还原产物NO排放到空气中污染空气 Cu2+、Ag+
(2)3.5
(3)[AuCl ]-+3Fe2+=Au↓+3Fe3++4Cl-
4
(4)存在反应HPtCl +2NHCl (NH )PtCl ↓+2HCl,升高温度有利于HCl挥发,促使反应
2 6 4 4 2 6
正向进行,使(NH )PtCl 沉淀率升高
4 2 6
(5)向过滤器中加水至浸没沉淀,待水自然流下,重复操作2~3次
(6)
16.(1)增大接触面积,加快反应速率,提高原料的转化率
(2) SrCO +2C Sr+3CO↑ 碱性耐火砖
3
(3) 为了增大氢氧化锶的浸取率,减少杂质氢氧化钙的溶解 Ca(OH)
2
(4)Sr(OH) + (NH )CO=SrCO +2NH·H O
2 4 2 3 3 3 2
(5)6
(6) 增大 Ni(OH) +OH--e-=NiOOH+H O
2 2
17.(1) 增大接触面积,加快反应速率,提高浸出率(2)
(3)
(4)蒸发浓缩、冷却结晶
(5)
18.(1) 或
(2) 温度高于80℃时, 水解程度增大, 浓度减小导致钒率下降 1.796
(3)偏钒酸铵加热后分解产生 和 , 将五价钒还原为 ;充分搅拌加热反应
后 被氧气氧化为
19.(1) 用氧化-酸浸法不会产生硫化氢等污染性气体 3ZnS+8H++2 =3Zn2+
+3S+2NO↑+4H O
2
(2) 加快了浸取反应的速率,同时还增大了浸出物质的溶解度 90℃
(3) 2Fe2++H O+2H+=2Fe3++2H O 2
2 2 2
(4)由于溶液中Fe3++量较大,直接调节溶液的pH=4,使Fe3+水解成Fe(OH) 胶体而给过滤带
3
来困难;还因胶体吸附Zn2+造成锌的大量损失
(5)除去Cu2+、Ni2+等杂质离子
20.(1) 适当提高稀硫酸浓度、研磨砷盐净化渣 3
(2) 5:2 SiO
2
(3)
(4)Na AsO
3 4
(5) 取最后一次洗涤液少许于试管中,加入盐酸酸化后无明显
现象,再加入少量氯化钡溶液,若无白色沉淀,则证明洗涤干净
(6)Co O
3 4