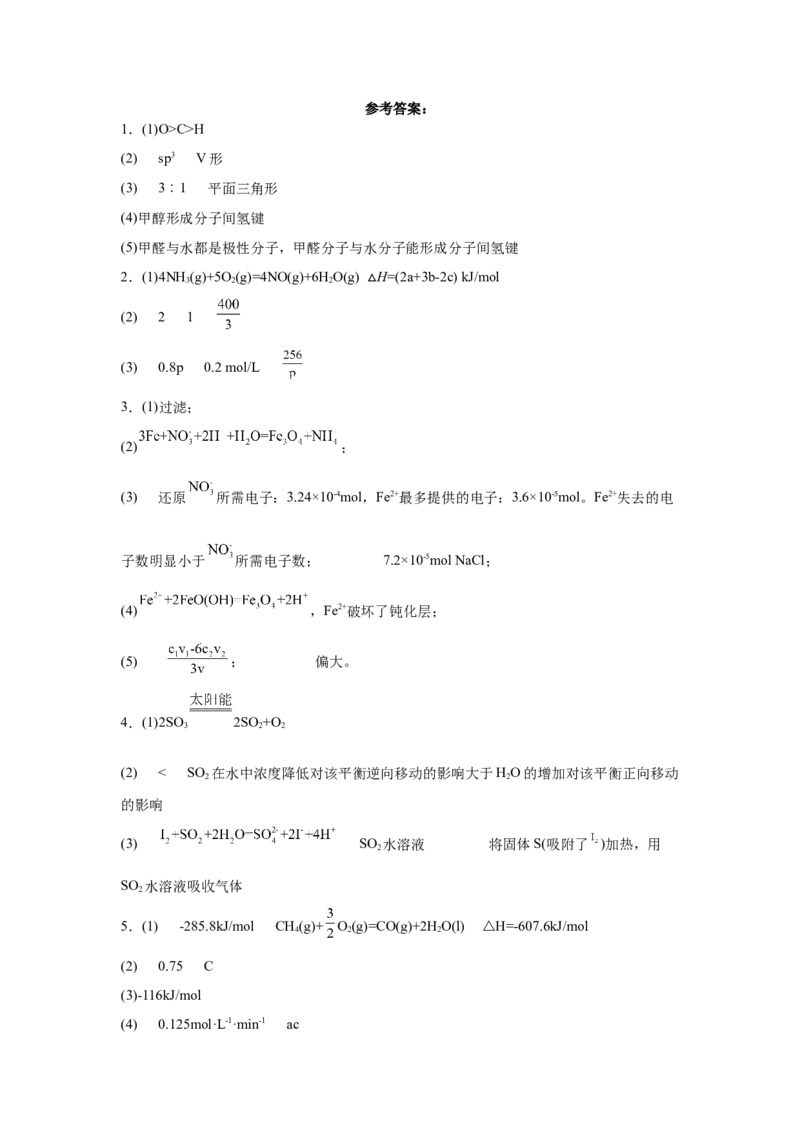文档内容
2023届高考化学一轮备考专题强化训练试题:化学反应原理综合题
1.(2022·北京育才学校高三期末)甲醇(CHOH)空气氧化法是生产工业甲醛(HCHO)的常用方法。发生
3
的反应为2CHOH+O 2 +2H O
3 2 2
(1)C、H、O 三种元素的电负性由大到小的顺序为_______。
(2)H O的氧原子的杂化轨道类型为_______,空间结构为_______。
2
(3)HCHO分子内σ键与π键个数之比为_______,HCHO的空间结构为_______。
(4)相同条件下,CHOH的沸点比O 的高,主要原因为_______。
3 2
(5)工业上利用甲醛易溶于水的性质吸收产品,解释甲醛易溶于水的原因:_______。
2.(2022·河南·高三阶段练习)一氧化氮可用作人造丝的漂白剂及丙烯和二甲醚的安定剂。
(1)工业上在钯或铂催化加热作用下,氨气与氧气制备一氧化氮的反应为4NH (g)+5O(g)=4NO(g)+6H O(g)
3 2 2
H。
△
已知:①
②
③
则 H=_______kJ/mol(用含a、b、c的代数式表示)。
△
(2)1073 K时,在容积不变的密闭容器中发生反应 ,测得反应速率
与NO、H 浓度的变化如下表。
2
实验序
号
1 0.0060 0.0010
2 0.0060 0.0020
3 0.0030 0.0040
4 0.0015 0.0040
该反应的速率方程为 ,则m=_______,n=_______,k=_______(保留两位有效数字)。
(3)T℃时,在2 L恒容密闭容器中充入1 mol NO、1 mol H ,发生反应
2
,起始时体系压强为p MPa,t min时反应达到平衡,此时测得N 的物质的量分数为25%。
2
①平衡时,体系压强p=_______MPa。
②平衡时,c(N )=_______。
2
③T℃时,该反应的压强平衡常数K =_______MPa-1(用含p的代数式表示,K 为以分压表示的平衡常数,
p p
分压=总压×气体的物质的量分数)。
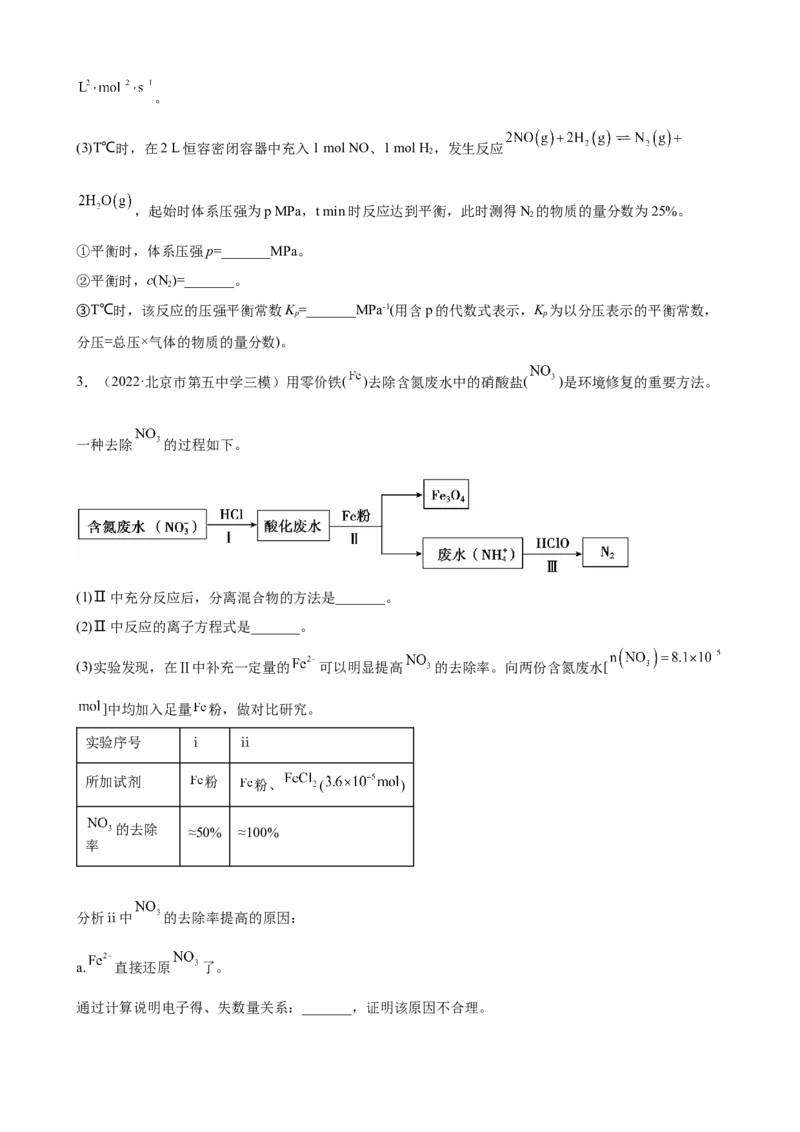
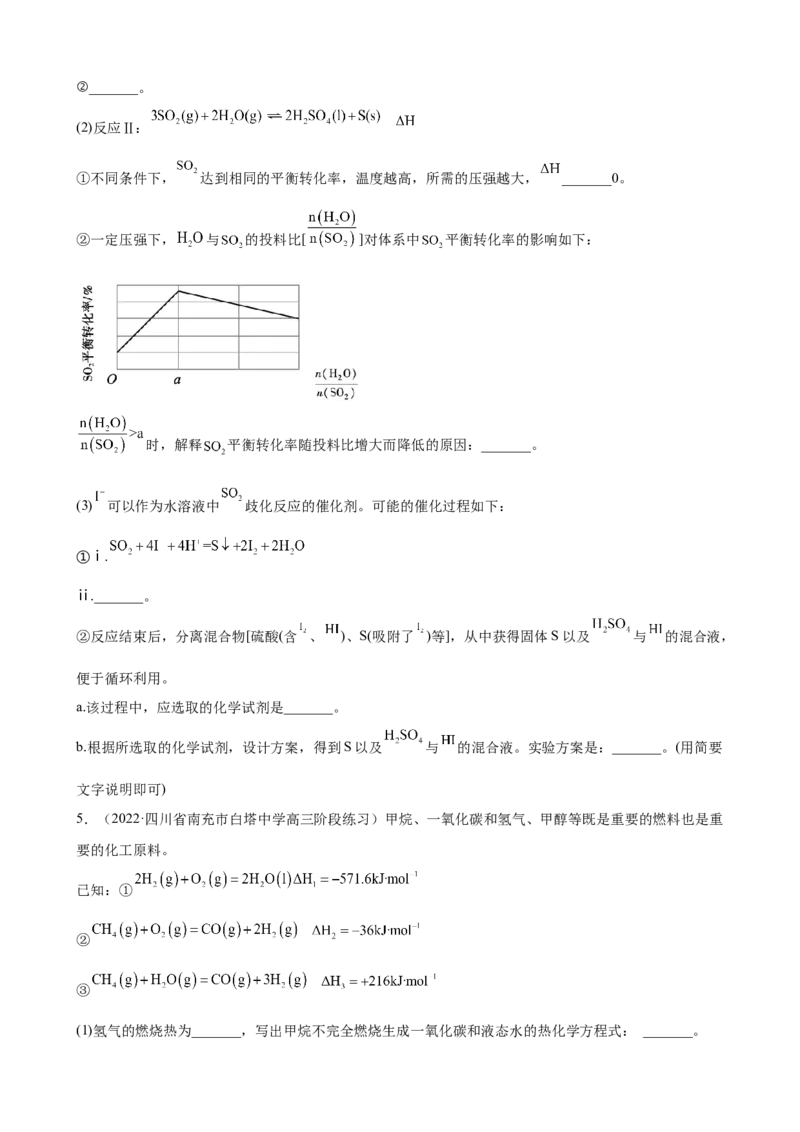
3.(2022·北京市第五中学三模)用零价铁( )去除含氮废水中的硝酸盐( )是环境修复的重要方法。
一种去除 的过程如下。
(1)Ⅱ中充分反应后,分离混合物的方法是_______。
(2)Ⅱ中反应的离子方程式是_______。
(3)实验发现,在Ⅱ中补充一定量的 可以明显提高 的去除率。向两份含氮废水[
]中均加入足量 粉,做对比研究。
实验序号 ⅰ ⅱ
所加试剂 粉 粉、 ( )
的去除 ≈50% ≈100%
率
分析ⅱ中 的去除率提高的原因:
a. 直接还原 了。
通过计算说明电子得、失数量关系:_______,证明该原因不合理。b.研究发现: (导电)覆盖在铁粉表面;随着反应的进行,产生 (不导电),它覆盖在 表
面,形成钝化层,阻碍电子传输。
c. 能与 反应生成 。
用 做同位素示踪实验,证明该原因合理。
d. 破坏钝化层。
将ⅱ中的 替换为_______, 的去除率约为50%,证明该原因不合理。
(4)ⅰ、ⅱ中均能发生 。该反应明显有助于ⅰ中 的去除,结合方程式解释原因:
_______。
(5)测定 含量
步骤1.取v 含氮( )水样,加入催化剂、 标准溶液(过量),再加入稀 。
步骤2.用 标准溶液滴定剩余的 ( 被还原为 ),终点时消耗 。
已知:
①水样中 的含量为_______ 。
②溶液中 影响测定。向步骤1中加入适量 ,产生 驱赶 ,否则会使测定结果_______(填
“偏大”或“偏小”)。
4.(2022·北京市第五中学三模)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存
储。过程如下:
(1)反应Ⅰ由两步反应组成:
① ;②_______。
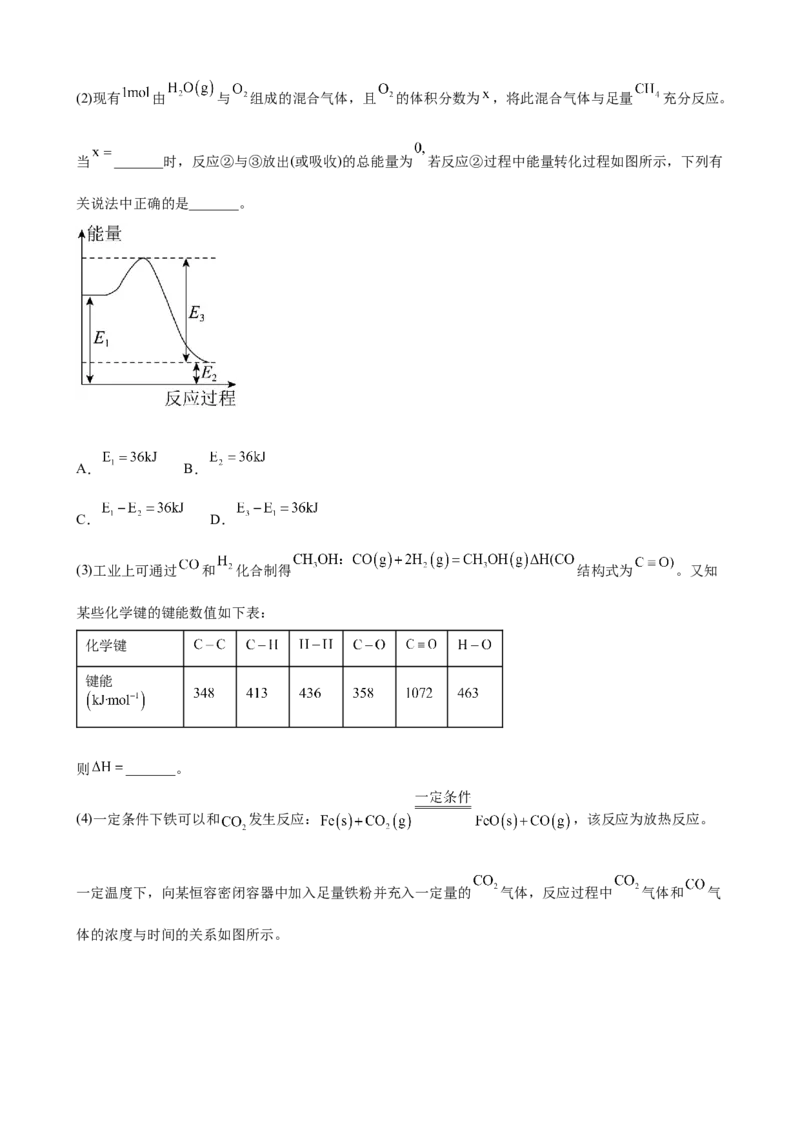
(2)反应Ⅱ:
①不同条件下, 达到相同的平衡转化率,温度越高,所需的压强越大, _______0。
②一定压强下, 与 的投料比[ ]对体系中 平衡转化率的影响如下:
时,解释 平衡转化率随投料比增大而降低的原因:_______。
(3) 可以作为水溶液中 歧化反应的催化剂。可能的催化过程如下:
①ⅰ.
ⅱ._______。
②反应结束后,分离混合物[硫酸(含 、 )、S(吸附了 )等],从中获得固体S以及 与 的混合液,
便于循环利用。
a.该过程中,应选取的化学试剂是_______。
b.根据所选取的化学试剂,设计方案,得到S以及 与 的混合液。实验方案是:_______。(用简要
文字说明即可)
5.(2022·四川省南充市白塔中学高三阶段练习)甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重
要的化工原料。
已知:①
②
③
(1)氢气的燃烧热为_______,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式: _______。(2)现有 由 与 组成的混合气体,且 的体积分数为 ,将此混合气体与足量 充分反应。
当 _______时,反应②与③放出(或吸收)的总能量为 若反应②过程中能量转化过程如图所示,下列有
关说法中正确的是_______。
A. B.
C. D.
(3)工业上可通过 和 化合制得 结构式为 。又知
某些化学键的键能数值如下表:
化学键
键能
则 _______。
(4)一定条件下铁可以和 发生反应: ,该反应为放热反应。
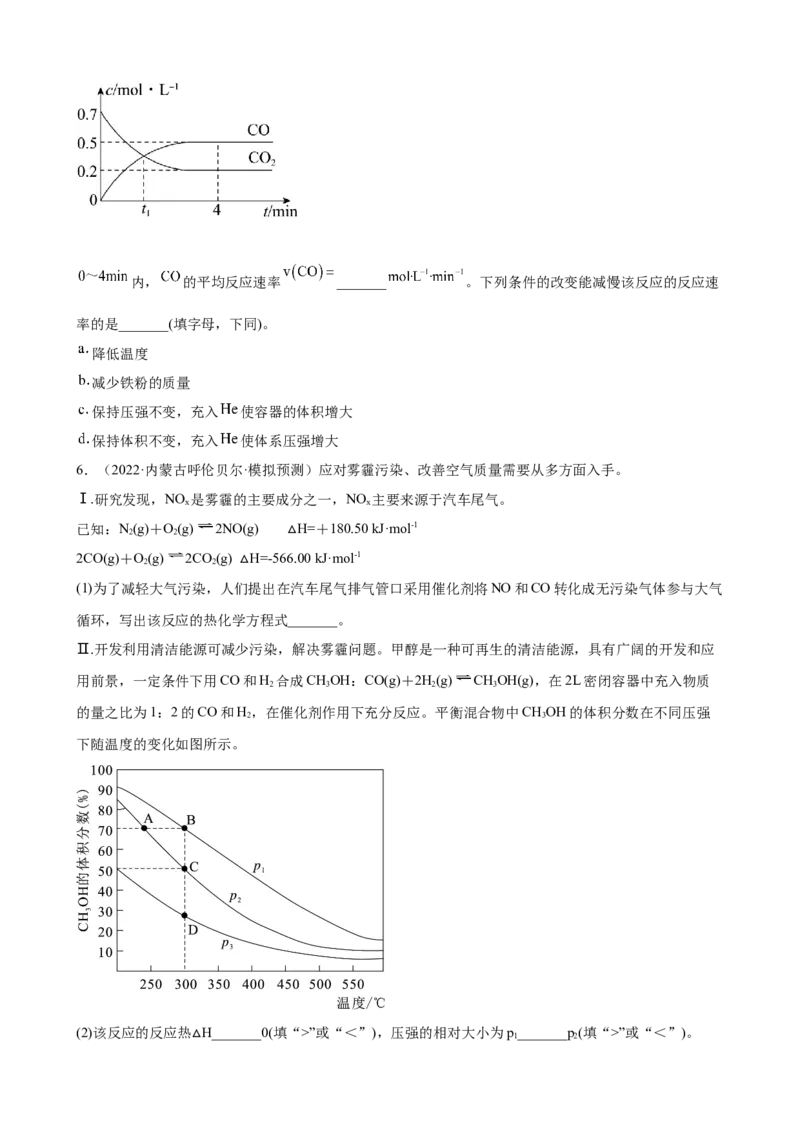
一定温度下,向某恒容密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中 气体和 气
体的浓度与时间的关系如图所示。内, 的平均反应速率 _______ 。下列条件的改变能减慢该反应的反应速
率的是_______(填字母,下同)。
降低温度
减少铁粉的质量
保持压强不变,充入 使容器的体积增大
保持体积不变,充入 使体系压强增大
6.(2022·内蒙古呼伦贝尔·模拟预测)应对雾霾污染、改善空气质量需要从多方面入手。
Ⅰ.研究发现,NO 是雾霾的主要成分之一,NO 主要来源于汽车尾气。
x x
已知:N(g)+O(g) 2NO(g) H=+180.50 kJ·mol-1
2 2
2CO(g)+O
2
(g) 2CO
2
(g) H=-566△.00 kJ·mol-1
(1)为了减轻大气污染,人们△提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气
循环,写出该反应的热化学方程式_______。
Ⅱ.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应
用前景,一定条件下用CO和H 合成CHOH:CO(g)+2H(g) CHOH(g),在2L密闭容器中充入物质
2 3 2 3
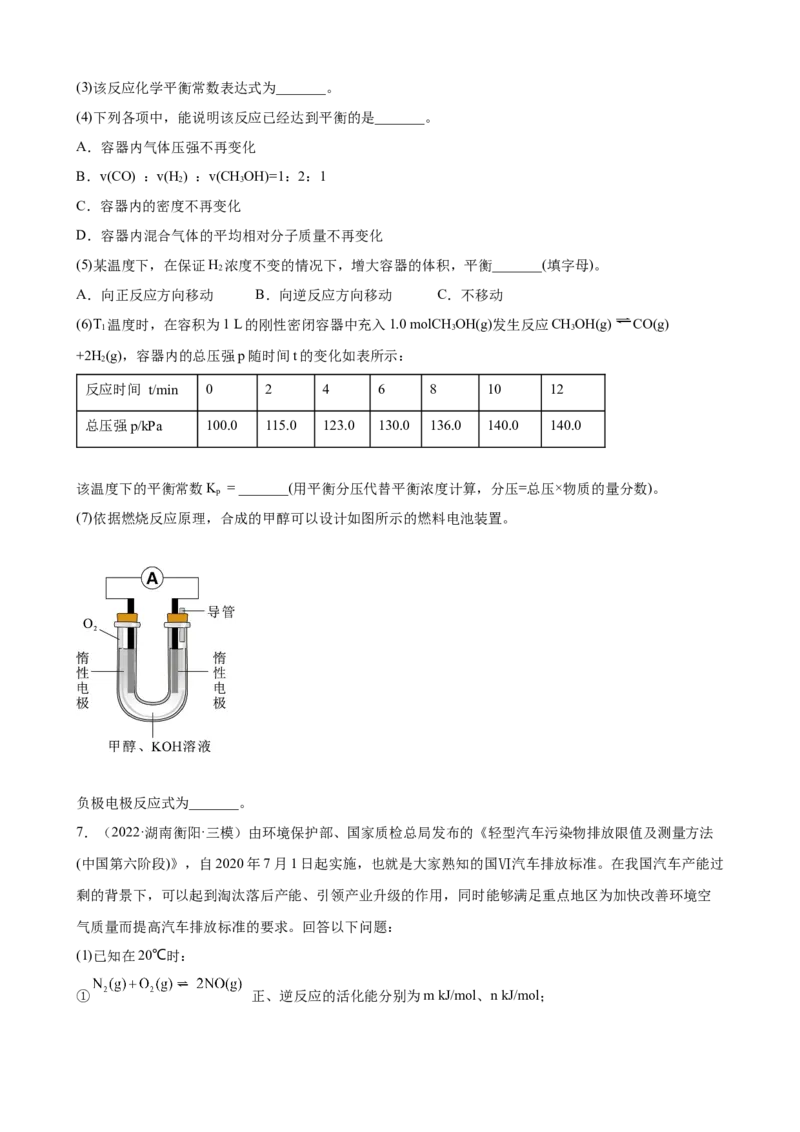
的量之比为1:2的CO和H,在催化剂作用下充分反应。平衡混合物中CHOH的体积分数在不同压强
2 3
下随温度的变化如图所示。
(2)该反应的反应热 H_______0(填“>”或“<”),压强的相对大小为p_______p(填“>”或“<”)。
1 2
△(3)该反应化学平衡常数表达式为_______。
(4)下列各项中,能说明该反应已经达到平衡的是_______。
A.容器内气体压强不再变化
B.v(CO) :v(H ) :v(CHOH)=1:2:1
2 3
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
(5)某温度下,在保证H 浓度不变的情况下,增大容器的体积,平衡_______(填字母)。
2
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(6)T 温度时,在容积为1 L的刚性密闭容器中充入1.0 molCH OH(g)发生反应CHOH(g) CO(g)
1 3 3
+2H (g),容器内的总压强p随时间t的变化如表所示:
2
反应时间 t/min 0 2 4 6 8 10 12
总压强p/kPa 100.0 115.0 123.0 130.0 136.0 140.0 140.0
该温度下的平衡常数K = _______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
(7)依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。
负极电极反应式为_______。
7.(2022·湖南衡阳·三模)由环境保护部、国家质检总局发布的《轻型汽车污染物排放限值及测量方法
(中国第六阶段)》,自2020年7月1日起实施,也就是大家熟知的国Ⅵ汽车排放标准。在我国汽车产能过
剩的背景下,可以起到淘汰落后产能、引领产业升级的作用,同时能够满足重点地区为加快改善环境空
气质量而提高汽车排放标准的要求。回答以下问题:
(1)已知在20℃时:
① 正、逆反应的活化能分别为m kJ/mol、n kJ/mol;② 正、逆反应的活化能分别为p kJ/mol、q kJ/mol。
用NH 处理汽车尾气中的NO的反应为: ,该反应的
3
H=_______。
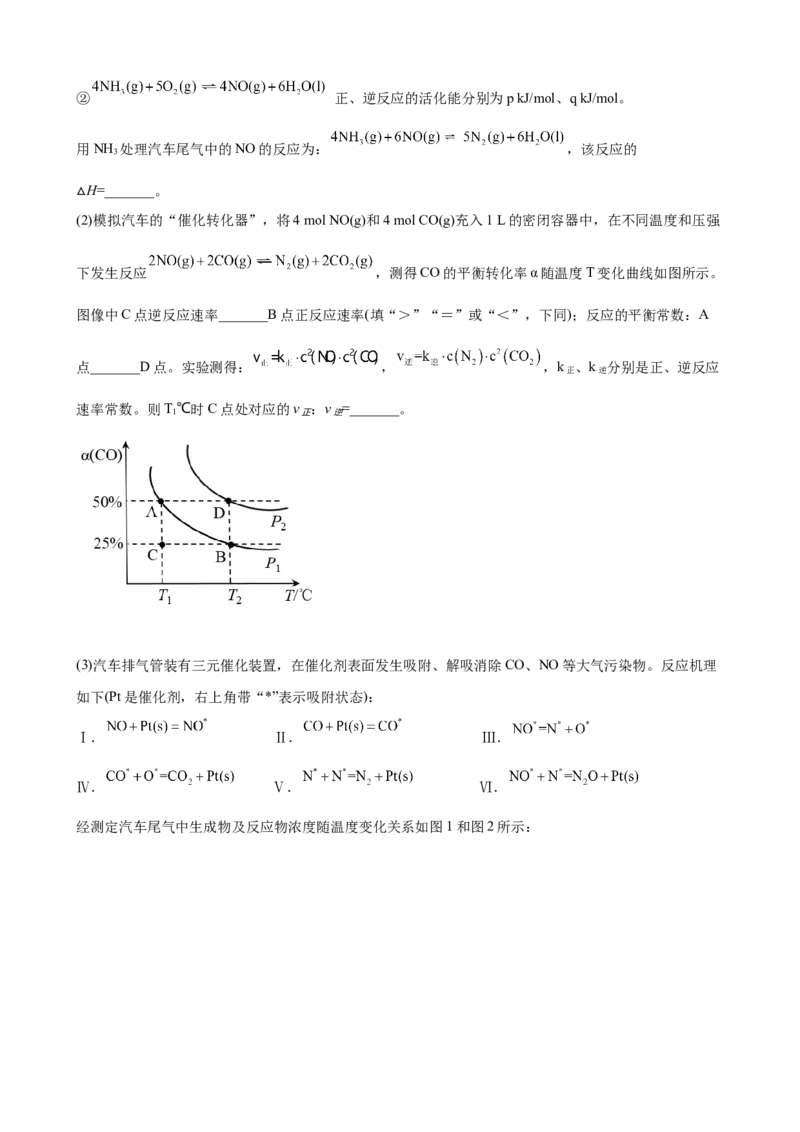
△(2)模拟汽车的“催化转化器”,将4 mol NO(g)和4 mol CO(g)充入1 L的密闭容器中,在不同温度和压强
下发生反应 ,测得CO的平衡转化率α随温度T变化曲线如图所示。
图像中C点逆反应速率_______B点正反应速率(填“>”“=”或“<”,下同);反应的平衡常数:A
点_______D点。实验测得: , ,k 、k 分别是正、逆反应
正 逆
速率常数。则T℃时C点处对应的v :v =_______。
1 正 逆
(3)汽车排气管装有三元催化装置,在催化剂表面发生吸附、解吸消除CO、NO等大气污染物。反应机理
如下(Pt是催化剂,右上角带“*”表示吸附状态):
Ⅰ. Ⅱ. Ⅲ.
Ⅳ. Ⅴ. Ⅵ.
经测定汽车尾气中生成物及反应物浓度随温度变化关系如图1和图2所示:①图1中,温度为330℃时反应V的活化能_______反应VI的活化能(填“<”、“>”或“=”),反应
VI的焓变 H_______0(“<”或“>”)。
②图2中,△温度从T
a
升至T
b
的过程中,反应物浓度急剧减小的主要原因是_______。
8.(2022·江苏徐州·三模)铀(U)可用作核燃料。核废料中+6价的铀[U(VI)]可以通过以下两种方法处
理。
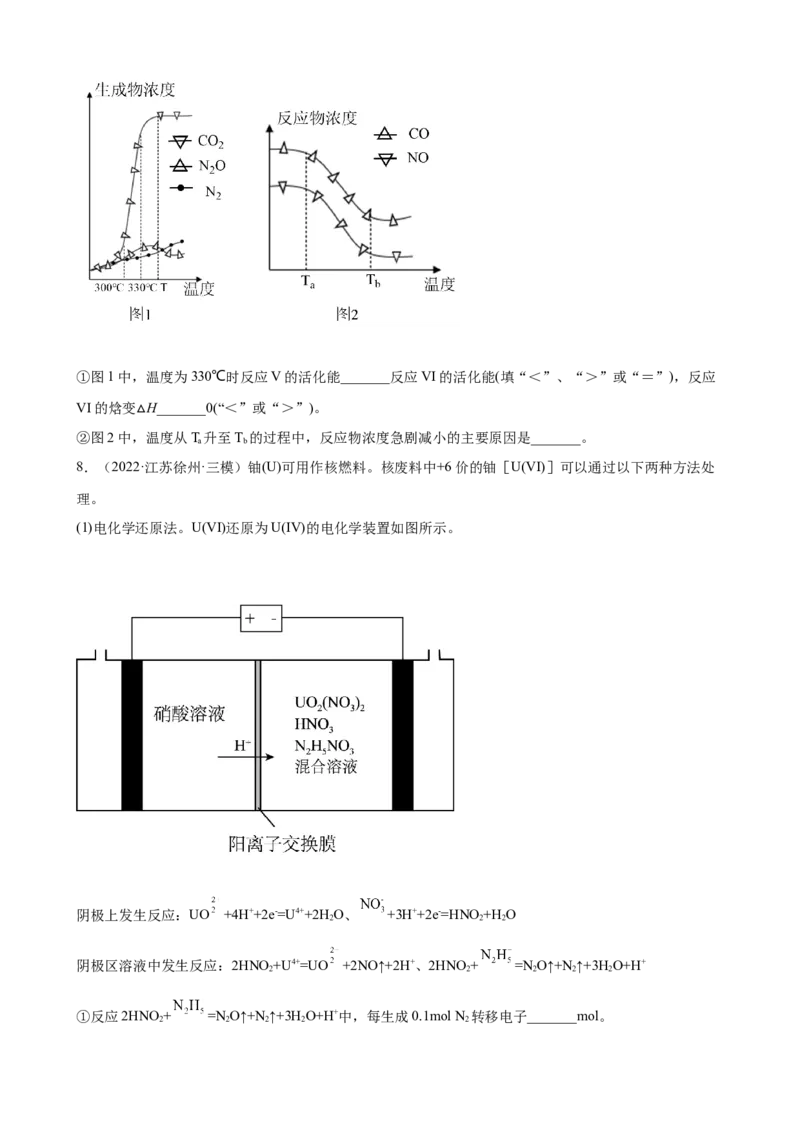
(1)电化学还原法。U(VI)还原为U(IV)的电化学装置如图所示。
阴极上发生反应:UO +4H++2e-=U4++2H O、 +3H++2e-=HNO +H O
2 2 2
阴极区溶液中发生反应:2HNO+U4+=UO +2NO↑+2H+、2HNO+ =N O↑+N↑+3H O+H+
2 2 2 2 2
①反应2HNO+ =N O↑+N↑+3H O+H+中,每生成0.1mol N 转移电子_______mol。
2 2 2 2 2②阴极区溶液中加入NHNO 的目的是_______。
2 5 3
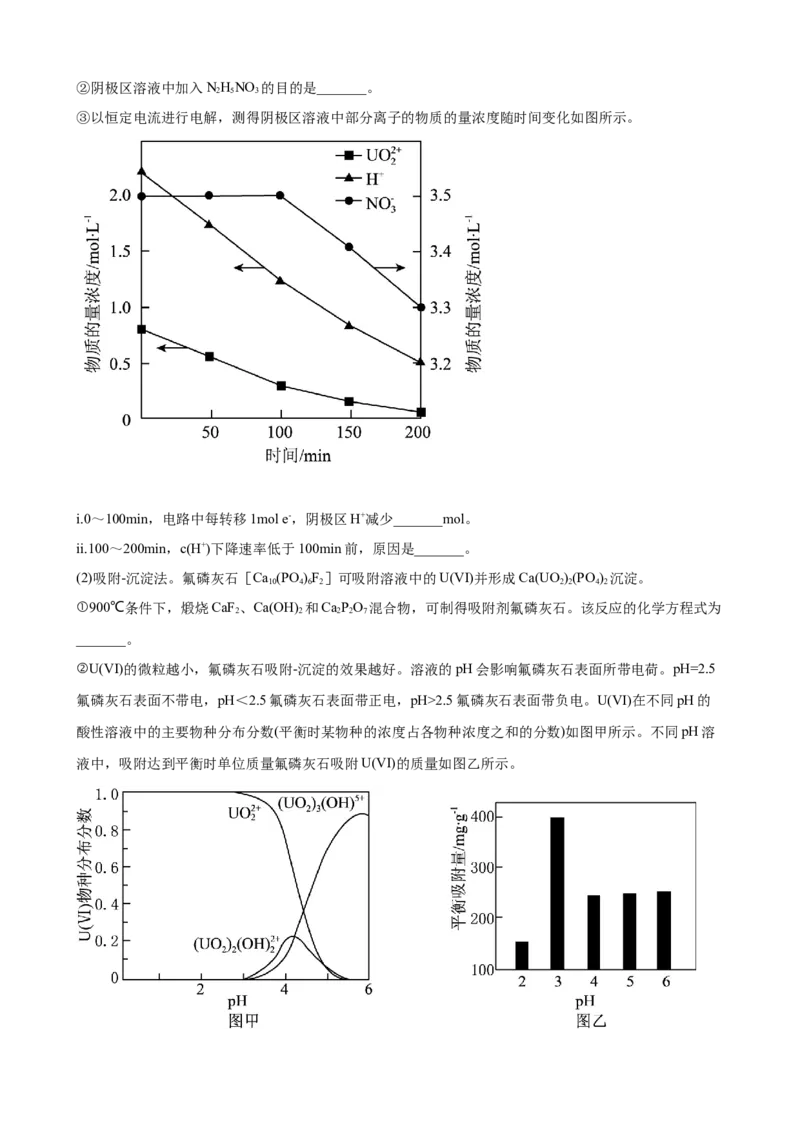
③以恒定电流进行电解,测得阴极区溶液中部分离子的物质的量浓度随时间变化如图所示。
i.0~100min,电路中每转移1mol e-,阴极区H+减少_______mol。
ii.100~200min,c(H+)下降速率低于100min前,原因是_______。
(2)吸附-沉淀法。氟磷灰石[Ca (PO )F]可吸附溶液中的U(VI)并形成Ca(UO )(PO ) 沉淀。
10 4 6 2 2 2 4 2
①900℃条件下,煅烧CaF 、Ca(OH) 和Ca PO 混合物,可制得吸附剂氟磷灰石。该反应的化学方程式为
2 2 2 2 7
_______。
②U(VI)的微粒越小,氟磷灰石吸附-沉淀的效果越好。溶液的pH会影响氟磷灰石表面所带电荷。pH=2.5
氟磷灰石表面不带电,pH<2.5氟磷灰石表面带正电,pH>2.5氟磷灰石表面带负电。U(VI)在不同pH的
酸性溶液中的主要物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)如图甲所示。不同pH溶
液中,吸附达到平衡时单位质量氟磷灰石吸附U(VI)的质量如图乙所示。pH=3时氟磷灰石的平衡吸附量高于pH=2和pH=4时的平衡吸附量,原因分别是_______。
9.(2022·河南郑州·高三专题练习)CO 减排策略主要有三种:减少排放,捕集封存,转化利用。其中
2
CO 转化利用,生产高能燃料和高附加值化学品,有利于实现碳资源的有效循环。由CO 转化制甲醇具有
2 2
重要的经济效益。
(1)高效催化剂对CO 加氢制甲醇的反应速率影响很大。通过计算机分析,CO 加氢制甲醇在不同催化条
2 2
件下存在两种反应路径的势能图如下图所示。
①CO 加氢制甲醇的热化学方程式为CO(g)+3H(g) CHOH(g)+H O(g) ΔH=_______eV/mol(阿伏加德罗常
2 2 2 3 2
数用N 表示); ⇌
A
②_______(填“甲酸盐”或“羧酸”)路径更有利于CO 加氢制甲醇反应,对该路径的反应速率影响最大
2
的一步反应是_______;
③根据势能图,下列说法合理的是_______(填标号)。
A.CO 分压越大,催化剂表面积越大,CO 在催化剂表面的吸附速率越大
2 2
B.不考虑HCOH*,两种路径中产生的含碳中间体种类均有5种
3
C.中间体HCOO*比COOH*更稳定
D.使用高活性催化剂可降低反应焓变,加快反应速率
(2)CO 催化加氢制甲醇反应历程中某一步基元反应的Arthenius经验公式的实验数据如图所示,已知
2
Arrhenius经验公式为 (其中Ea为活化能,k为速率常数,R和C为常数)。①该反应的活化能Ea=________kJ/mol;
②当使用更高效的催化剂时,在图中画出Rlnk与 关系的示意图_______。
(3)在CO 催化加氢制甲醇过程中也存在竞争反应CO(g)+H(g) CO(g)+HO(g) ΔH>0,在恒温密闭容器中,
2 2 2 2
维持压强和投料比不变,将CO 和H 按一定流速通过反应器,⇌CO 转化率和甲醇选择性[x(CH OH)%=
2 2 2 3
]随温度变化关系如下图所示:
CO 转化率和甲醇选择性随温度的变化曲线
2
①若233-251℃时催化剂的活性受温度影响不大,分析235℃后图中曲线下降的原因_______。
②在压强为P的恒温恒压密闭容器中,加入1molCO 和3molH 反应并达到平衡状态,CO 平衡转化率为
2 2 2
20%,甲醇的选择性为50%,计算CO(g)+3H(g) CHOH(g)+H O(g)在该温度下的平衡常数
2 2 3 2
K=_______。(列出计算式) ⇌
p10.(2022·天津红桥·一模)将 和 两种引发温室效应的气体转化为合成气( 和 ),可以实现
能量综合利用,对环境保护具有十分重要的意义。
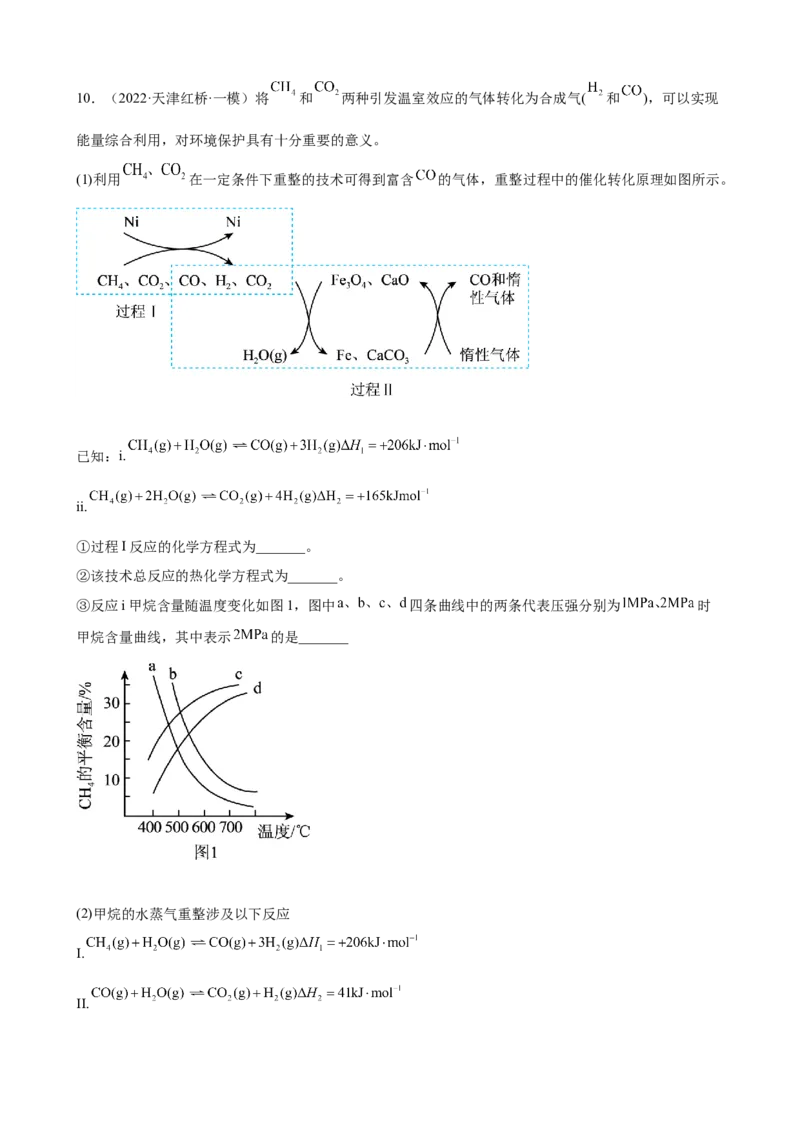
(1)利用 在一定条件下重整的技术可得到富含 的气体,重整过程中的催化转化原理如图所示。
已知:i.
ii.
①过程I反应的化学方程式为_______。
②该技术总反应的热化学方程式为_______。
③反应i甲烷含量随温度变化如图1,图中 四条曲线中的两条代表压强分别为 时
甲烷含量曲线,其中表示 的是_______
(2)甲烷的水蒸气重整涉及以下反应
I.
II.在一密闭体积可变容器中,通入 和 发生甲烷的水蒸气重整反应。
①反应I的平衡常数的表达式为_______。
反应II平衡常数 _______ (填“>”“<”或“=”)。
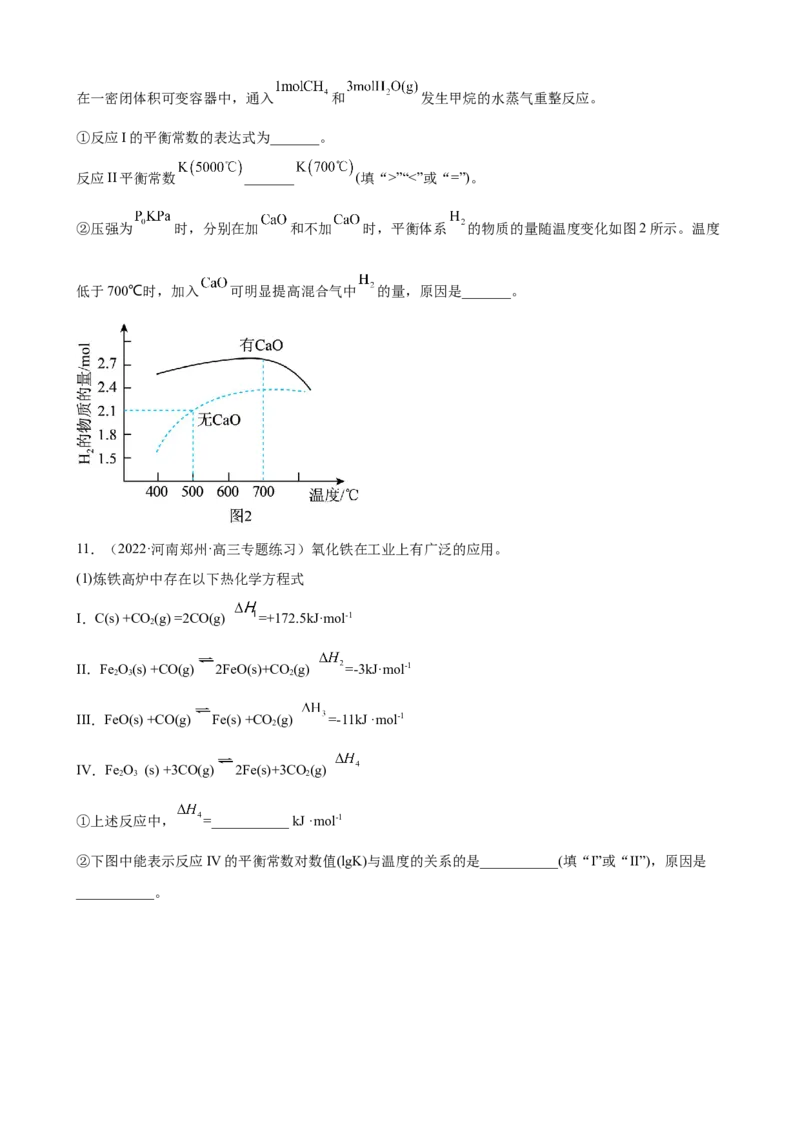
②压强为 时,分别在加 和不加 时,平衡体系 的物质的量随温度变化如图2所示。温度
低于700℃时,加入 可明显提高混合气中 的量,原因是_______。
11.(2022·河南郑州·高三专题练习)氧化铁在工业上有广泛的应用。
(1)炼铁高炉中存在以下热化学方程式
I.C(s) +CO (g) =2CO(g) =+172.5kJ·mol-1
2
II.Fe O(s) +CO(g) 2FeO(s)+CO (g) =-3kJ·mol-1
2 3 2
III.FeO(s) +CO(g) Fe(s) +CO (g) =-11kJ ·mol-1
2
IV.Fe O (s) +3CO(g) 2Fe(s)+3CO (g)
2 3 2
①上述反应中, =___________ kJ ·mol-1
②下图中能表示反应IV的平衡常数对数值(lgK)与温度的关系的是___________(填“I”或“II”),原因是
___________。③1500°C时,在某体积可变的密闭容器中,按物质的量比2:3加入Fe O 和CO发生反应IV ,则达平衡
2 3
时,Fe O 的转化率为___________;下列措施能够提高Fe O 转化率的是___________(填字母序号)。
2 3 2 3
a.对体系加压 b.升高反应体系的温度
c.加入适量的NaO固体 d.增大CO在原料中的物质的量比
2
(2)一定条件下Fe O 可被甲烷还原为“纳米级”的金属铁,其反应为: Fe O(s)+3CH(g) 2Fe(s)+
2 3 2 3 4
3CO(g) +6H (g) ΔH >0
2
①反应在2 L的密闭容器中进行,5 min后达到平衡,测得Fe O 在反应中质量消耗3.2 g,则该段时间内
2 3
用反应物表达的平均反应速率为___________mol·L-1·min-1
②该反应达到平衡时,某物理量(Y)随温度变化如图所示,当温度由T 升高到T 时,平衡常数
1 2
K ___________ K (填“>”“<"或“=”)。纵坐标可以表示的物理量有___________填字 母序号)。
A B
a.H 的逆反应速率 b.CH 的的体积分数
2 4
c.混合气体的平均相对分子质量 d.混合气体的密度
12.(2022·江西南昌·模拟预测)我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的
担当。高效经济性的CO 捕集及利用是有效应对全球气候变化、促进低碳社会构建的重要方法。
2
(1)在催化剂作用下,可用CO 与H 反应制取甲酸。已知:
2 2
共价键 C=O C-O H-H H-O C-H
键能(kJ·mol-1) 799 343 436 463 413
则CO(g)+H(g)=HCOOH(g)的△H=_______kJ/mol。
2 2
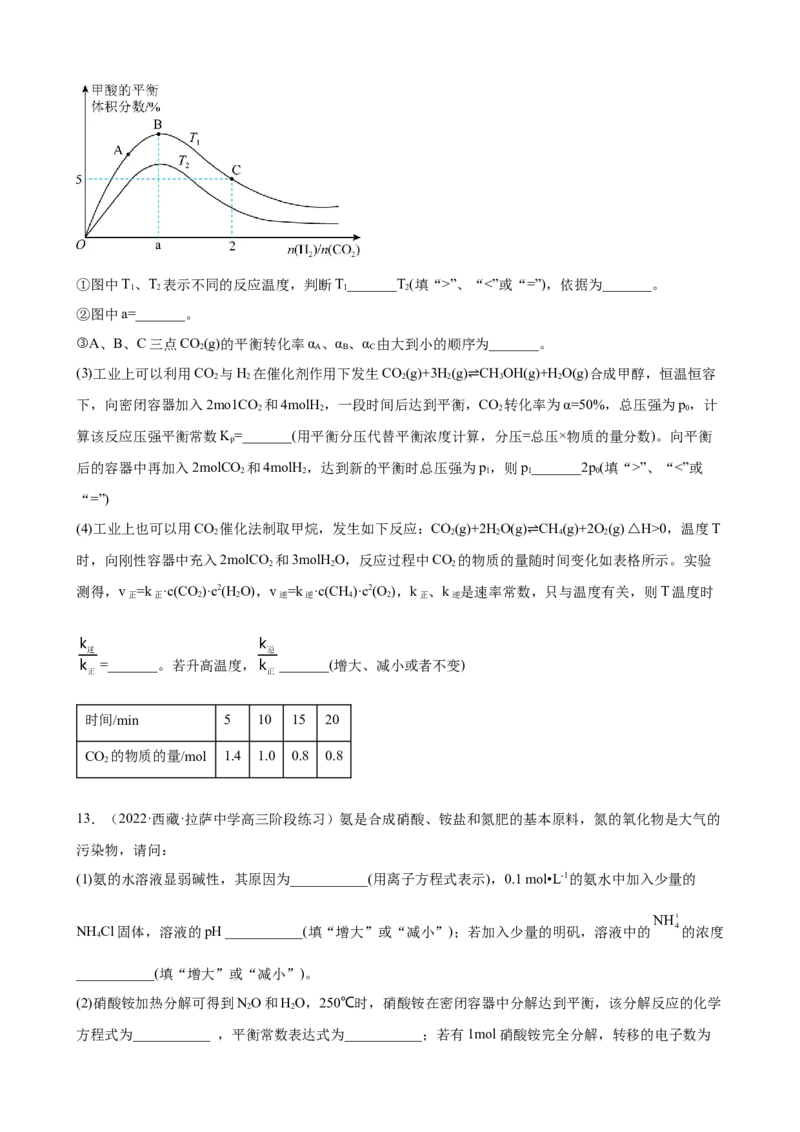
(2)在刚性密闭容器中,HCOOH平衡时的体积分数随投料比[ ]的变化如图所示:①图中T、T 表示不同的反应温度,判断T_______T(填“>”、“<”或“=”),依据为_______。
1 2 1 2
②图中a=_______。
③A、B、C三点CO(g)的平衡转化率α 、α 、α 由大到小的顺序为_______。
2 A B C
(3)工业上可以利用CO 与H 在催化剂作用下发生CO(g)+3H(g) CHOH(g)+H O(g)合成甲醇,恒温恒容
2 2 2 2 3 2
下,向密闭容器加入2mo1CO 和4molH ,一段时间后达到平衡,⇌CO 转化率为α=50%,总压强为p,计
2 2 2 0
算该反应压强平衡常数K=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。向平衡
p
后的容器中再加入2molCO 和4molH ,达到新的平衡时总压强为p,则p_______2p(填“>”、“<”或
2 2 1 1 0
“=”)
(4)工业上也可以用CO 催化法制取甲烷,发生如下反应:CO(g)+2HO(g) CH(g)+2O(g) △H>0,温度T
2 2 2 4 2
时,向刚性容器中充入2molCO 和3molH O,反应过程中CO 的物质的量⇌随时间变化如表格所示。实验
2 2 2
测得,v =k ·c(CO)·c2(H O),v =k ·c(CH)·c2(O ),k 、k 是速率常数,只与温度有关,则T温度时
正 正 2 2 逆 逆 4 2 正 逆
=_______。若升高温度, _______(增大、减小或者不变)
时间/min 5 10 15 20
CO 的物质的量/mol 1.4 1.0 0.8 0.8
2
13.(2022·西藏·拉萨中学高三阶段练习)氨是合成硝酸、铵盐和氮肥的基本原料,氮的氧化物是大气的
污染物,请问:
(1)氨的水溶液显弱碱性,其原因为___________(用离子方程式表示),0.1 mol•L-1的氨水中加入少量的
NH Cl固体,溶液的pH ___________(填“增大”或“减小”);若加入少量的明矾,溶液中的 的浓度
4
___________(填“增大”或“减小”)。
(2)硝酸铵加热分解可得到NO和HO,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学
2 2
方程式为___________ ,平衡常数表达式为___________;若有1mol硝酸铵完全分解,转移的电子数为___________mol。
(3)甲醚(CHOCH )被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气
3 3
体,具有轻微的醚香味,其燃烧热为1455 kJ·mol-1,甲醚可作燃料电池的燃料。已知H(g)和C(s)的燃烧
2
热分别是285.8 kJ·mol-1、393.5 kJ·mol-1;计算反应4C(s)+ 6H (g)+ O (g)=2CH OCH (g)的反应热为
2 2 3 3
___________;
(4)工业上利用H 和CO 合成二甲醚的反应如下:6H(g)+ 2CO (g) CHOCH (g)+ 3H O(g) △H<0
2 2 2 2 3 3 2
①一定温度下,在一个固定体积的密闭容器中进行该反应。下列能判断反应达到化学平衡状态的是
______ (选填编号,注意大小写)
a.c(H )与c(H O)的比值保持不变
2 2
b.单位时间内有2mol H 消耗时,有1mol HO生成
2 2
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CHOCH 的产率将___________(填“变大”、“变
3 3
小”或“不变”)。
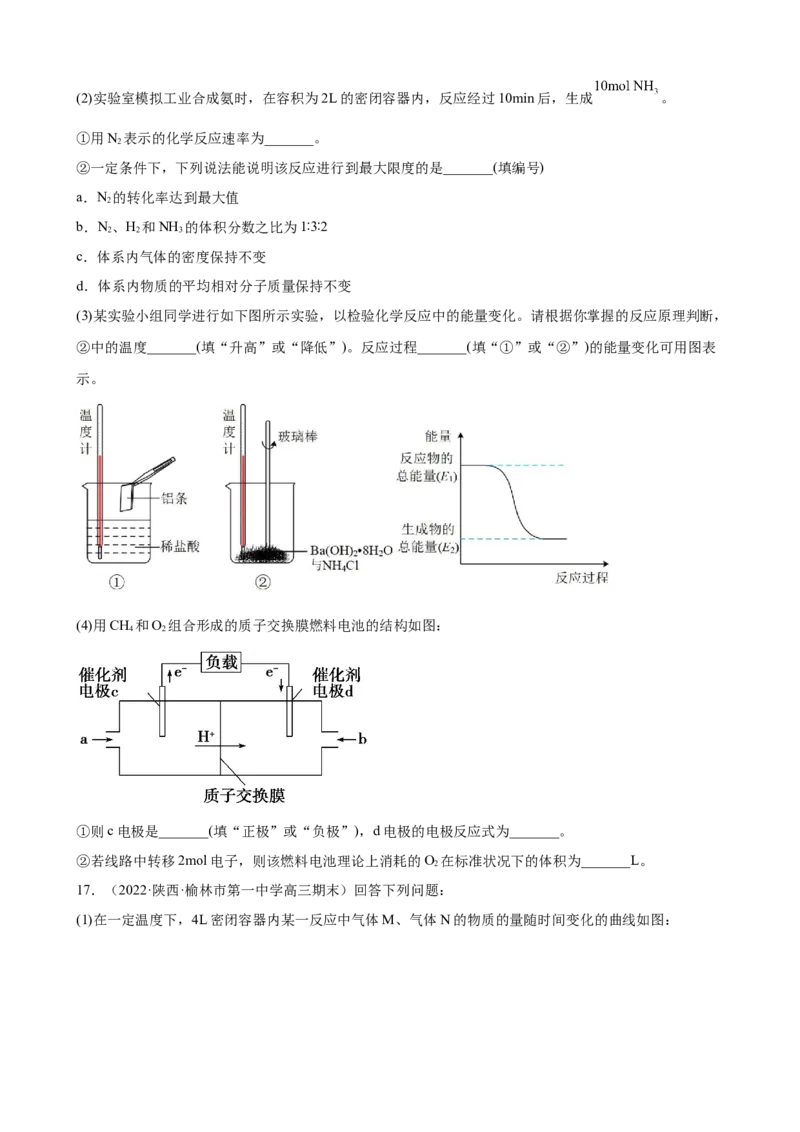
14.(2022·安徽·青阳第一中学高三阶段练习)三氯氢硅SiHCl 是制备硅烷、多晶硅的重要原料。对于反
3
应2SiHCl (g) SiHCl(g)+SiCl (g)采用大孔弱碱性阴离子交换树脂催化剂,在323 K和343 K时SiHCl
3 2 2 4 3
的转化率随时间变化的结果如图所示。
(1)343 K时反应的平衡转化率ɑ=_______%。平衡常数K =_______(保留2位小数)。
343K
(2)在343 K下,要提高SiHCl 转化率,可采取的措施是_______;要缩短反应达到平衡的时间,可采取的
3
措施有_______。
(3)比较a、b处反应速率大小:v_______v(填“大于”“小于”或“等于”)。反应速率v=v −v =k
a b 正 逆 正x2(SiHCl )−k x(SiHCl)x(SiCl ),k 、k 分别为正、逆反应速率常数,x为物质的量分数,计算a处
3 逆 2 2 4 正 逆
=_______(保留1位小数)。
15.(2022·河北保定·高三阶段练习)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望
的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题:
(1)工业催化氧化SO 制备SO 的反应2SO (g)+O(g) 2SO (g)是放热的可逆反应,反应条件是高温、常
2 3 2 2 3
压,并且需要合适的催化剂。已知1molSO (g)完全转化为SO (g)可放出98.3kJ热量。如果将5molSO (g)
2 3 2
和足量O(g)混合,使其充分反应,放出的热量____(填“大于”、“小于”或“等于”)491.5kJ。
2
(2)实验室模拟工业催化氧化SO 制备SO ,在容积为2L的恒容密闭容器内进行,反应经过10min,生成
2 3
8molSO 。
3
①用O 表示的化学反应速率为____。
2
②一定条件下,能说明该反应进行到最大限度的是____(填标号)。
a.SO 的转化率达到最大值
2
b.体系内气体的密度保持不变
c.SO 、O 和SO 的体积分数之比为2:1:2
2 2 3
d.体系内物质的平均相对分子质量保持不变
(3)C、CO、CH 完全燃烧的热化学方程式分别为:
4
C(s)+O(g)=CO (g) H=-393.6kJ·mol-1
2 2
2CO(g)+O
2
(g)=2CO
2
(g)△ H=-565.2kJ·mol-1
CH
4
(g)+2O
2
(g)=CO
2
(g)+2H 2△O(l) H=-889.6kJ·mol-1
完全燃烧等物质的量的上述物质,△放出的热量由大到小的顺序为____。
完全燃烧等质量的上述物质,放出的热量由大到小的顺序为____。
完全燃烧等物质的量的上述物质,需要的空气体积由大到小的顺序为____。
(4)25℃、101kPa时,16gNH(l)在足量的O(g)中充分燃烧生成N(g)和HO(g),放出271.5kJ热量,写出
2 4 2 2 2
NH(l)和O(g)反应的热化学方程式:____。
2 4 2
16.(2022·北京市第一六六中学高三期末)能源是现代文明的原动力,通过化学方法可以使能量按人们
所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)工业合成氨反应: 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化
剂。已知 完全反应生成NH 可放出92kJ热量。如果将 和足量H 混合,使其充分反应,
3 2
放出的热量_______(填“大于”、“小于”或“等于”) 920kJ。(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成 。
①用N 表示的化学反应速率为_______。
2
②一定条件下,下列说法能说明该反应进行到最大限度的是_______(填编号)
a.N 的转化率达到最大值
2
b.N、H 和NH 的体积分数之比为1∶3∶2
2 2 3
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
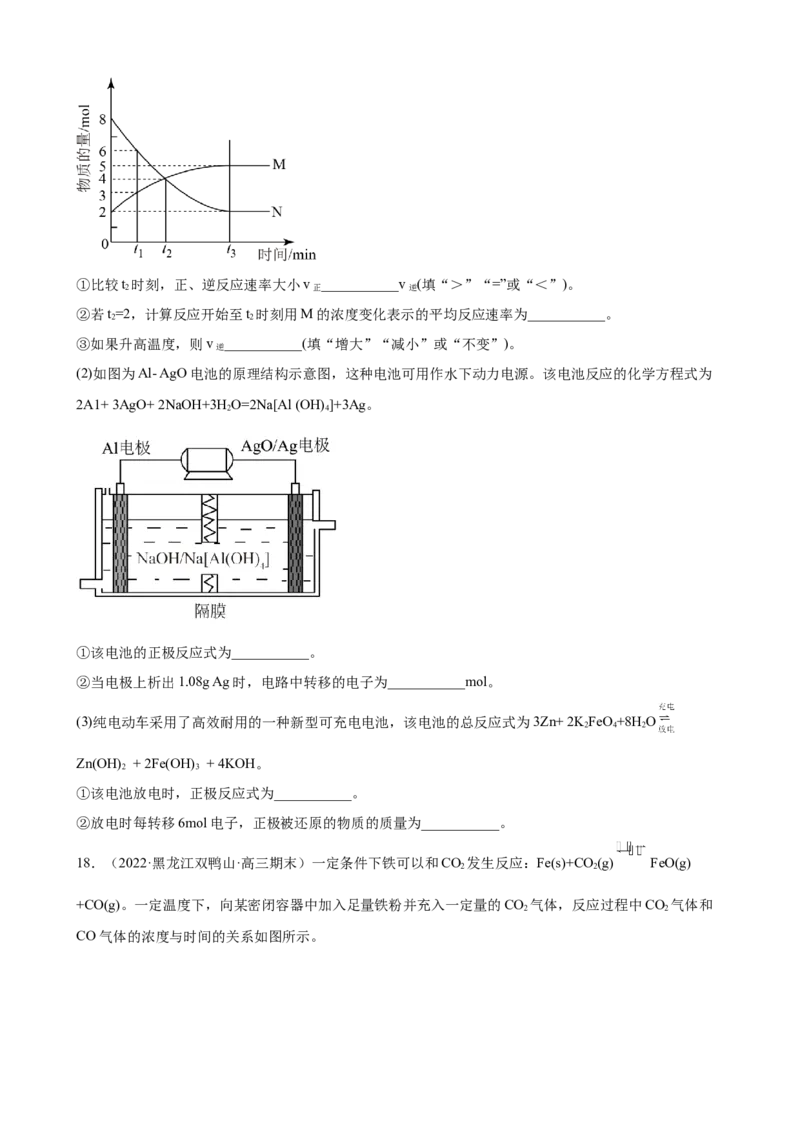
(3)某实验小组同学进行如下图所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,
②中的温度_______(填“升高”或“降低”)。反应过程_______(填“①”或“②”)的能量变化可用图表
示。
(4)用CH 和O 组合形成的质子交换膜燃料电池的结构如图:
4 2
①则c电极是_______(填“正极”或“负极”),d电极的电极反应式为_______。
②若线路中转移2mol电子,则该燃料电池理论上消耗的O 在标准状况下的体积为_______L。
2
17.(2022·陕西·榆林市第一中学高三期末)回答下列问题:
(1)在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图:①比较t 时刻,正、逆反应速率大小v ___________v (填“>”“=”或“<”)。
2 正 逆
②若t=2,计算反应开始至t 时刻用M的浓度变化表示的平均反应速率为___________。
2 2
③如果升高温度,则v ___________(填“增大”“减小”或“不变”)。
逆
(2)如图为Al- AgO电池的原理结构示意图,这种电池可用作水下动力电源。该电池反应的化学方程式为
2A1+ 3AgO+ 2NaOH+3H O=2Na[Al (OH) ]+3Ag。
2 4
①该电池的正极反应式为___________。
②当电极上析出1.08g Ag时,电路中转移的电子为___________mol。
(3)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为3Zn+ 2KFeO+8H O
2 4 2
Zn(OH) + 2Fe(OH) + 4KOH。
2 3
①该电池放电时,正极反应式为___________。
②放电时每转移6mol电子,正极被还原的物质的质量为___________。
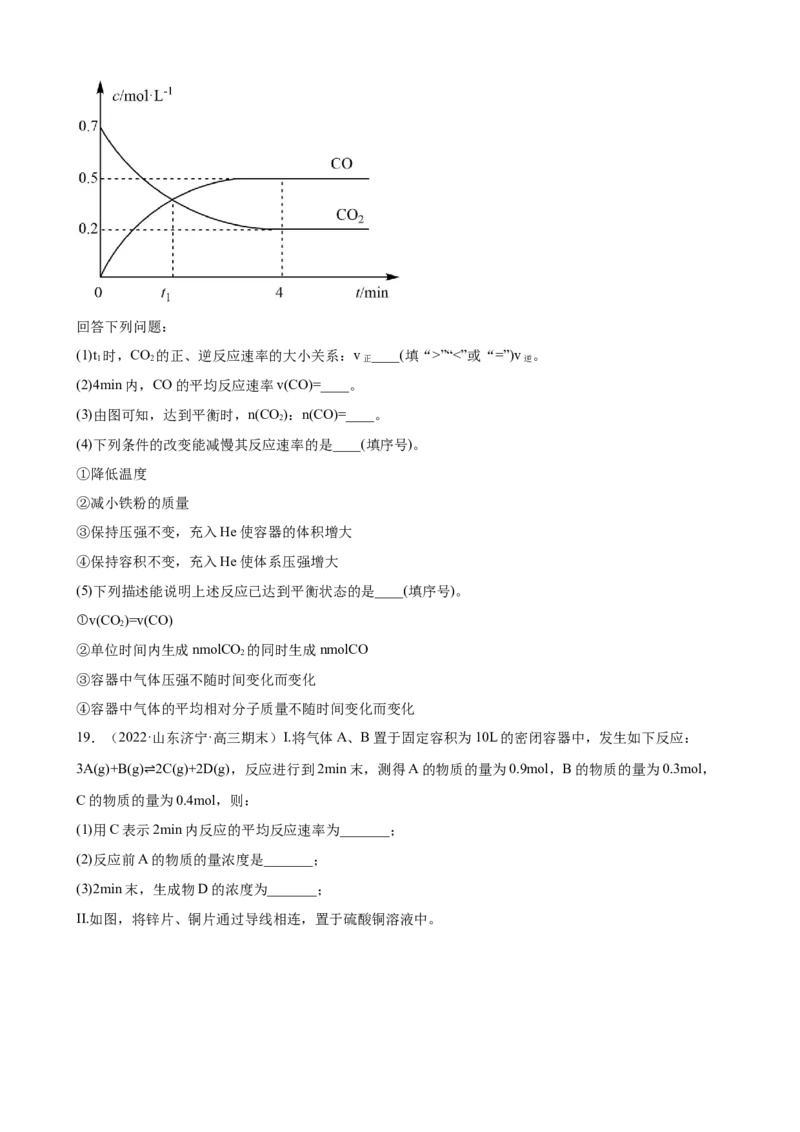
18.(2022·黑龙江双鸭山·高三期末)一定条件下铁可以和CO 发生反应:Fe(s)+CO (g) FeO(g)
2 2
+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO 气体,反应过程中CO 气体和
2 2
CO气体的浓度与时间的关系如图所示。回答下列问题:
(1)t 时,CO 的正、逆反应速率的大小关系:v ____(填“>”“<”或“=”)v 。
1 2 正 逆
(2)4min内,CO的平均反应速率v(CO)=____。
(3)由图可知,达到平衡时,n(CO):n(CO)=____。
2
(4)下列条件的改变能减慢其反应速率的是____(填序号)。
①降低温度
②减小铁粉的质量
③保持压强不变,充入He使容器的体积增大
④保持容积不变,充入He使体系压强增大
(5)下列描述能说明上述反应已达到平衡状态的是____(填序号)。
①v(CO)=v(CO)
2
②单位时间内生成nmolCO 的同时生成nmolCO
2
③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
19.(2022·山东济宁·高三期末)I.将气体A、B置于固定容积为10L的密闭容器中,发生如下反应:
3A(g)+B(g) 2C(g)+2D(g),反应进行到2min末,测得A的物质的量为0.9mol,B的物质的量为0.3mol,
C的物质的⇌量为0.4mol,则:
(1)用C表示2min内反应的平均反应速率为_______;
(2)反应前A的物质的量浓度是_______;
(3)2min末,生成物D的浓度为_______;
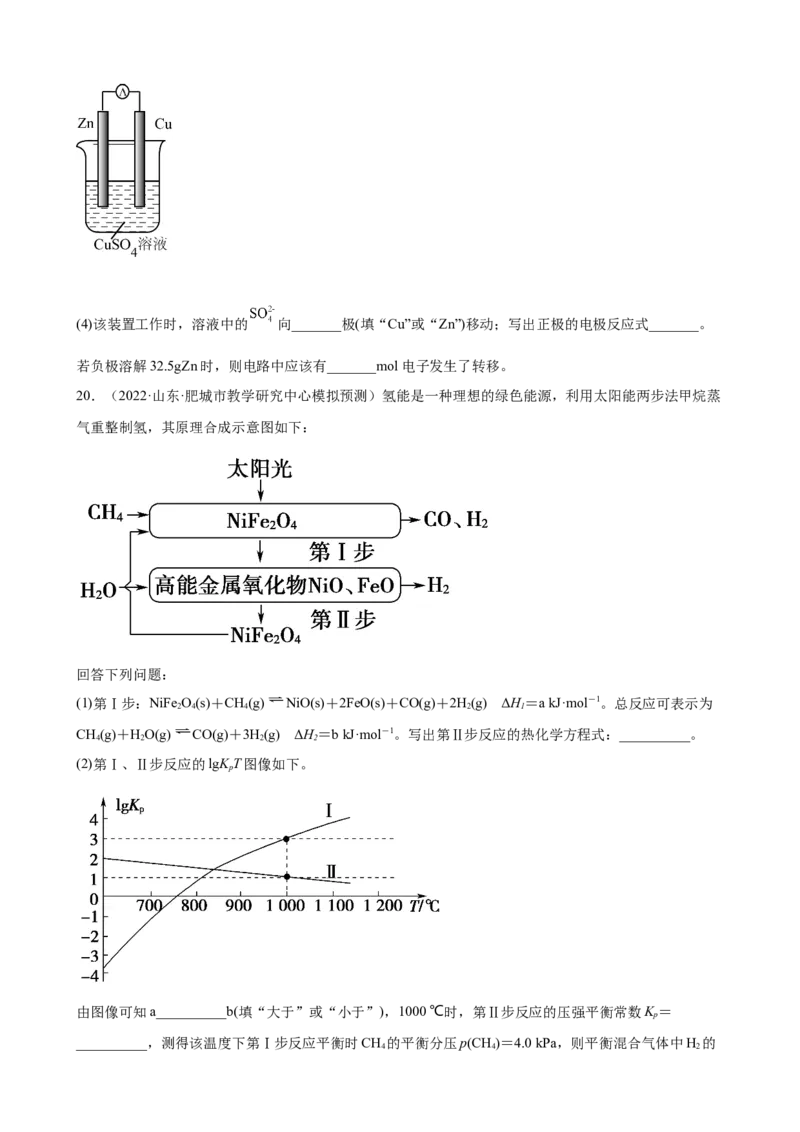
II.如图,将锌片、铜片通过导线相连,置于硫酸铜溶液中。(4)该装置工作时,溶液中的 向_______极(填“Cu”或“Zn”)移动;写出正极的电极反应式_______。
若负极溶解32.5gZn时,则电路中应该有_______mol电子发生了转移。
20.(2022·山东·肥城市教学研究中心模拟预测)氢能是一种理想的绿色能源,利用太阳能两步法甲烷蒸
气重整制氢,其原理合成示意图如下:
回答下列问题:
(1)第Ⅰ步:NiFe O(s)+CH(g) NiO(s)+2FeO(s)+CO(g)+2H(g) ΔH=a kJ·mol-1。总反应可表示为
2 4 4 2 1
CH(g)+HO(g) CO(g)+3H(g) ΔH=b kJ·mol-1。写出第Ⅱ步反应的热化学方程式:__________。
4 2 2 2
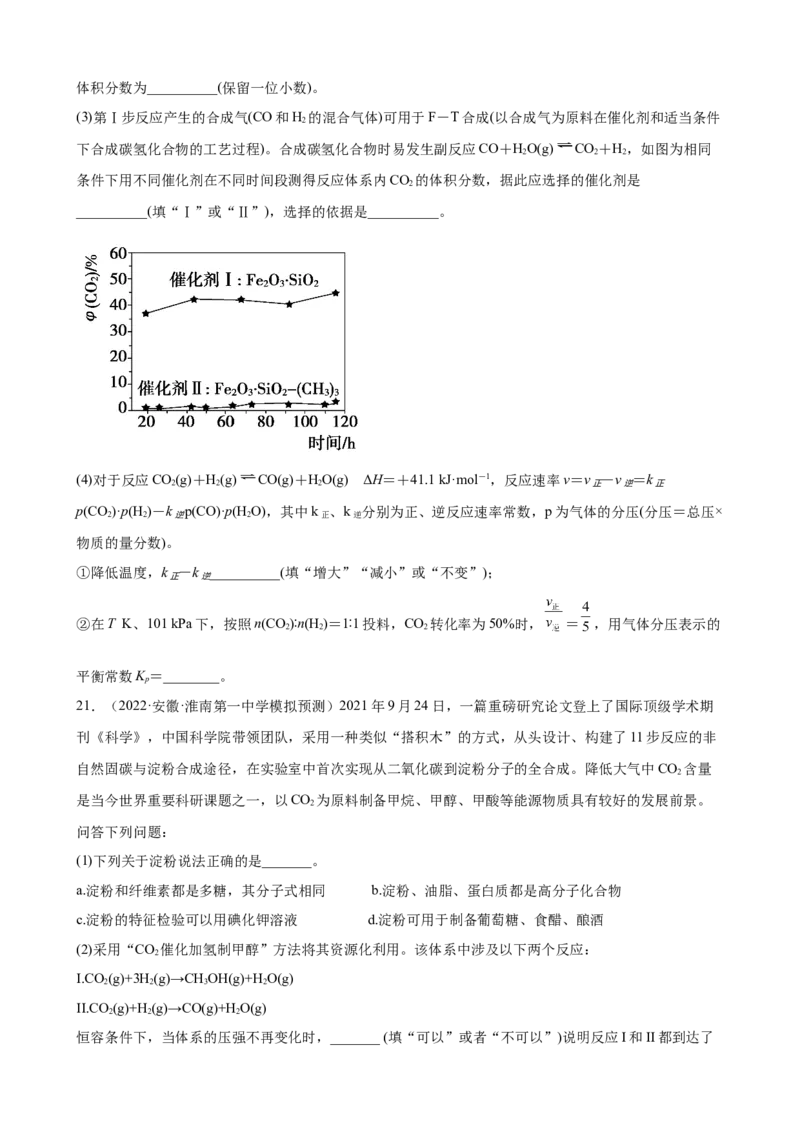
(2)第Ⅰ、Ⅱ步反应的lgK T图像如下。
p
由图像可知a__________b(填“大于”或“小于”),1000 ℃时,第Ⅱ步反应的压强平衡常数K =
p
__________,测得该温度下第Ⅰ步反应平衡时CH 的平衡分压p(CH)=4.0 kPa,则平衡混合气体中H 的
4 4 2体积分数为__________(保留一位小数)。
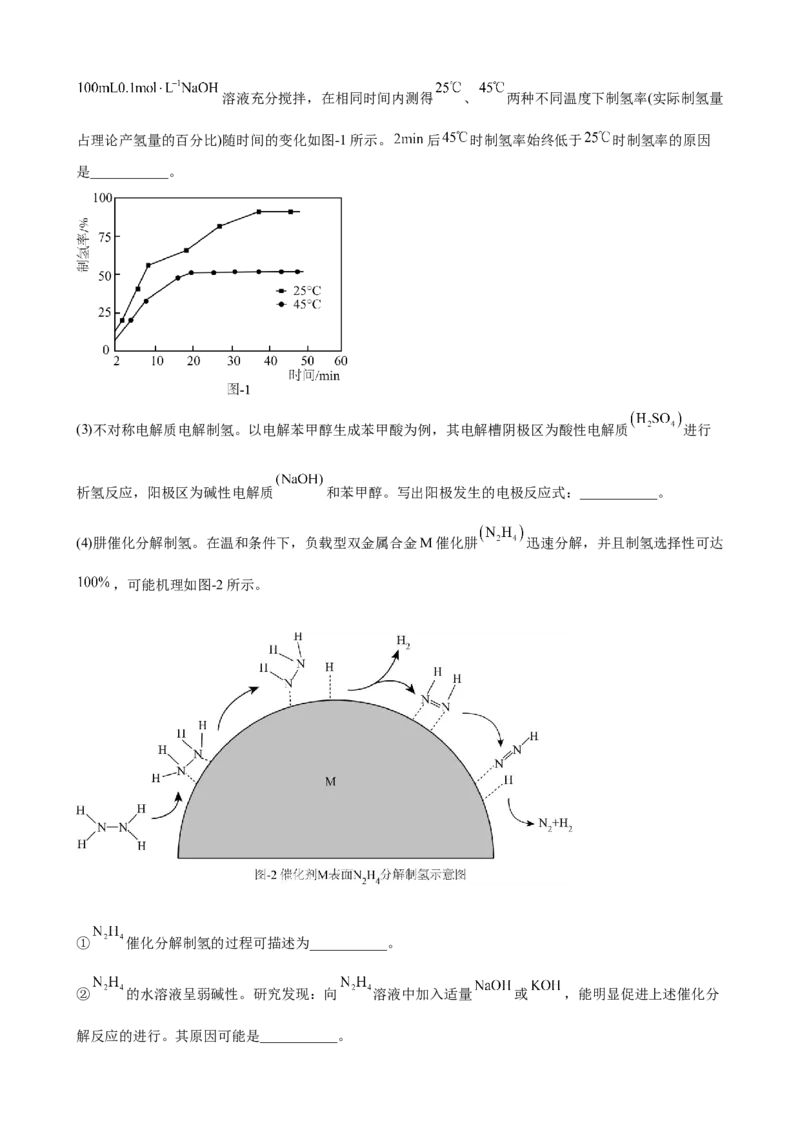
(3)第Ⅰ步反应产生的合成气(CO和H 的混合气体)可用于F-T合成(以合成气为原料在催化剂和适当条件
2
下合成碳氢化合物的工艺过程)。合成碳氢化合物时易发生副反应CO+HO(g) CO+H,如图为相同
2 2 2
条件下用不同催化剂在不同时间段测得反应体系内CO 的体积分数,据此应选择的催化剂是
2
__________(填“Ⅰ”或“Ⅱ”),选择的依据是__________。
(4)对于反应CO(g)+H(g) CO(g)+HO(g) ΔH=+41.1 kJ·mol-1,反应速率v=v -v =k
2 2 2 正 逆 正
p(CO)·p(H )-k p(CO)·p(H O),其中k 、k 分别为正、逆反应速率常数,p为气体的分压(分压=总压×
2 2 逆 2 正 逆
物质的量分数)。
①降低温度,k -k __________(填“增大”“减小”或“不变”);
正 逆
②在T K、101 kPa下,按照n(CO)∶n(H )=1∶1投料,CO 转化率为50%时, = ,用气体分压表示的
2 2 2
平衡常数K =________。
p
21.(2022·安徽·淮南第一中学模拟预测)2021年9月24日,一篇重磅研究论文登上了国际顶级学术期
刊《科学》,中国科学院带领团队,采用一种类似“搭积木”的方式,从头设计、构建了11步反应的非
自然固碳与淀粉合成途径,在实验室中首次实现从二氧化碳到淀粉分子的全合成。降低大气中CO 含量
2
是当今世界重要科研课题之一,以CO 为原料制备甲烷、甲醇、甲酸等能源物质具有较好的发展前景。
2
问答下列问题:
(1)下列关于淀粉说法正确的是_______。
a.淀粉和纤维素都是多糖,其分子式相同 b.淀粉、油脂、蛋白质都是高分子化合物
c.淀粉的特征检验可以用碘化钾溶液 d.淀粉可用于制备葡萄糖、食醋、酿酒
(2)采用“CO 催化加氢制甲醇”方法将其资源化利用。该体系中涉及以下两个反应:
2
I.CO (g)+3H(g)→CH OH(g)+H O(g)
2 2 3 2
II.CO (g)+H(g)→CO(g)+H O(g)
2 2 2
恒容条件下,当体系的压强不再变化时,_______ (填“可以”或者“不可以”)说明反应I和II都到达了化学平衡状态。
(3)CO 在固体催化表面加氢合成甲烷过程中发生以下两个反应:
2
主反应:CO(g)+4H(g)→CH (g)+2HO(g) ΔH K
2 2 4 2 1 1
副反应:CO(g)+H(g)→CO(g)+H O(g) ΔH K
2 2 2 2 2
①已知2H(g)+O(g)→2H O(g) ΔH K
2 2 2 3 3
CH(g)+2O(g)→CO (g)+2HO(g) ΔH K
4 2 2 2 4 4
K=_______(可以用K,K,K 表示)
1 2 3 4
②用物质的量分数表示的平衡常数记为Kx,已知一定温度下,向起始压强为P的2L恒容密闭容器中充入
2 mol CO 和8mol H,10 min时主、副反应都达到平衡状态,测得c(HO)=1.25 mol·L-1,总压变为原来的
2 2 2
4/5,则0~10min内v(CH)= _______mol·L-1min-1,平衡时CH 选择性=_______。(已知CH 的选择性
4 4 4
=n(CH )/[n(CO)+n(CH )]×100%),主反应的K=_______(列出计算式即可,不必化简)
4 4 x
(4)我国科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程
如图甲所示,其中化合物2与HO反应变成化合物3与HCOO-的反应历程如图乙所示,其中TS表示过渡
2
态,I表示中间体。回答下列问题:
①化合物1到化合物2的过程中存在碳氧键的断裂和_______(填“碳氢键”或“碳氧键”)的形成。
②从平衡移动的角度看,_______(填“升高”或“降低”)温度可促进化合物2与HO反应变成化合物3
2
与HCOO-。
③该历程中最大能垒(活化能)E =_______kcal/mol。
正
22.(2022·江苏盐城·三模)氢气是重要的清洁能源,低成本制氢是今后科研攻关的重点课题。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠 在室温下结合 制氢为例, 能将反应中
的部分 还原成碳并放出 ,该反应的化学方程式为___________。
(2)活性金属铝制氢。向两份 活性 合金粉末( 的质量分数为 )中分别加入溶液充分搅拌,在相同时间内测得 、 两种不同温度下制氢率(实际制氢量
占理论产氢量的百分比)随时间的变化如图-1所示。 后 时制氢率始终低于 时制氢率的原因
是___________。
(3)不对称电解质电解制氢。以电解苯甲醇生成苯甲酸为例,其电解槽阴极区为酸性电解质 进行
析氢反应,阳极区为碱性电解质 和苯甲醇。写出阳极发生的电极反应式:___________。
(4)肼催化分解制氢。在温和条件下,负载型双金属合金M催化肼 迅速分解,并且制氢选择性可达
,可能机理如图-2所示。
① 催化分解制氢的过程可描述为___________。
② 的水溶液呈弱碱性。研究发现:向 溶液中加入适量 或 ,能明显促进上述催化分
解反应的进行。其原因可能是___________。参考答案:
1.(1)O>C>H
(2) sp3 V形
(3) 3︰1 平面三角形
(4)甲醇形成分子间氢键
(5)甲醛与水都是极性分子,甲醛分子与水分子能形成分子间氢键
2.(1)4NH (g)+5O(g)=4NO(g)+6H O(g) H=(2a+3b-2c) kJ/mol
3 2 2
△
(2) 2 1
(3) 0.8p 0.2 mol/L
3.(1)过滤;
(2) ;
(3) 还原 所需电子:3.24×10-4mol,Fe2+最多提供的电子:3.6×10-5mol。Fe2+失去的电
子数明显小于 所需电子数; 7.2×10-5mol NaCl;
(4) ,Fe2+破坏了钝化层;
(5) ; 偏大。
4.(1)2SO 2SO +O
3 2 2
(2) < SO 在水中浓度降低对该平衡逆向移动的影响大于HO的增加对该平衡正向移动
2 2
的影响
(3) SO 水溶液 将固体S(吸附了 )加热,用
2
SO 水溶液吸收气体
2
5.(1) -285.8kJ/mol CH(g)+ O(g)=CO(g)+2HO(l) △H=-607.6kJ/mol
4 2 2
(2) 0.75 C
(3)-116kJ/mol
(4) 0.125mol·L-1·min-1 ac6.(1)2CO(g) +2NO(g) N(g)+2CO(g) H=-746.50 kJ·mol-1
2 2
(2) < > ⇌ △
(3)K=
(4)AD
(5)C
(6)400.0 kPa2
(7)CH OH-6e-+8OH-=CO +6HO
3 2
7.(1)(5n+p-5m-q)kJ/mol
(2) < > 40.5
(3) > < 升高温度,催化剂活性增强,反应速率逐渐加快,所以反
应物浓度急剧减小
8.(1) 0.4 消耗反应中生成的HNO,防止HNO 与U4+反应 1 100min后
2 2
参与电极反应,相同时间内,转移等量电子时, 比 消耗的H+更少,且生成
的HNO 与 反应有H+生成
2
(2) CaF +3Ca(OH) +3Ca PO Ca (PO )F+3H O pH=2时,氟磷灰石表面带正电,
2 2 2 2 7 10 4 6 2 2
pH=3时,氟磷灰石表面带负电,带负电氟磷灰石更易吸附溶液中带正电的 ;pH=4时,
溶液中U(VI)以 、 、 三种形式存在,后两种粒子半
径较大,不易被吸附
9.(1) -0.19N 甲酸盐 HCOO*+H*=H COO*(或
A 2
HCOO*+H*+2H =H COO*+2H ) BC
2 2 2(2) 30.0 或
(3) 主反应放热,副反应吸热。升温使主反应平衡逆向移动程度大于副反应平衡正向移
动程度,因而使CO 转化率和甲醇选择性下降
2
10.(1)
b
(2) > 加入 的体系与二氧化碳反应,使反应I、Ⅱ的化学平
衡正向移动,氢气含量增大
11.(1) -25 I 因为该反应正向放热,升高温度,平衡逆向移动,K减小,lgK减
小 25% cd
(2) 0.006 < bc
12.(1)+16
(2) > 该反应为吸热反应,升高温度,平衡正向移动,在相同投料比时,T 温度下产
1
物的体积分数大于T 温度下产物的体积分数,则T>T 1 α >α >α
2 1 2 C B A
(3) <
(4) 减小13.(1) NH ·H O +OH- 减小 增大
3 2
(2) NH NO NO↑ + 2HO↑ K= c(N O)c2(H O) 4
4 3 2 2 2 2
∙
(3)-378.8kJ/mol
(4) a d 变小
14.(1) 22 0.02
(2) 及时移去产物 增大压强(或增大反应物浓度)、改进催化剂(任写一种)
(3) 大于 1.3
15.(1)小于
(2) 0.2mol·L-1·min-1 ad
(3) CH>C>CO CH>C>CO CH>C>CO
4 4 4
(4)N H(l)+O (g)=N(g)+2HO(g) H=-543kJ·mol-1
2 4 2 2 2
16.(1)小于 △
(2) 0.25 mol·L-1·min-1 ad
(3) 降低 ①
(4) 负极 O+4H++4e-=2H O 11.2
2 2
17.(1) > 0.25 mol·L-1·min-1 增大
(2) AgO+2e- +H O= Ag+2OH- 0. 02
2
(3) FeO +3e- +4H O=Fe(OH) +5OH- 396 g
2 3
18.(1)>
(2)0.125 mol∙L-1∙min-1
(3)2:5
(4)ac
(5)bd
19.(1)0.02mol·L-1·min-1
(2)0.15mol·L-1
(3)0.04mol·L-1
(4) Zn Cu2++2e-=Cu 1
20.(1)NiO(s)+2FeO(s)+HO(g) NiFe O(s)+H(g) ΔH=(b-a)kJ·mol-1
2 2 4 2
(2) 大于 10 58.8%
(3) Ⅱ 催化剂Ⅱ对主反应选择性高(或催化剂Ⅱ抑制 CO 生成,减少了副产物)
2(4) 减小 0.8
21.(1)d
(2)可以
(3) 0.05 66.7%
(4) 碳氢键 降低 18.86
22.(1)4NaH+3CO =2Na CO+C+2H
2 2 3 2
(2)45℃较25℃温度高,反应速率更快,较短时间内消耗完NaOH,较多的铝和水反应生成
难溶于水的Al(OH) 覆盖在合金表面,提早阻断了铝与溶液接触,阻止了反应进一步进行;
3
同时温度升高,生成的 水解生成的Al(OH) 增多,覆盖在合金表面,也阻止了反应进
3
一步进行
(3) -4e-+5OH-= +4H O
2
(4) NH 吸附在(催化剂)M表面,连续断裂N-H键、脱H,形成NH、NH、和NH等
2 4 2 3 2 2 2
中间产物,直至H原子全部脱去,生成N,脱去的H两两结合成H 肼是弱碱,
2 2;
在水溶液中存在NH+H O +OH-;加入适量NaOH或KOH后,溶液碱性增强,上
2 4 2
述平衡逆向移动,NH 的浓度增大,肼分解速率加快,同时适宜的偏向碱性的pH有利于
2 4
增强(催化剂)M的活性