文档内容
2023届高考化学一轮练习题:化学能与电能
一、选择题(本大题共15小题)
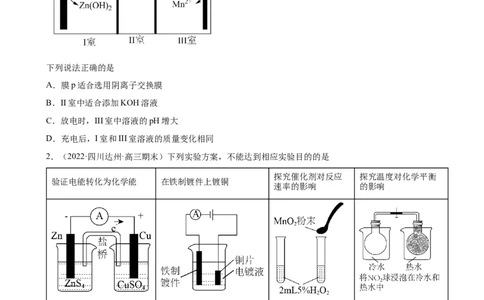
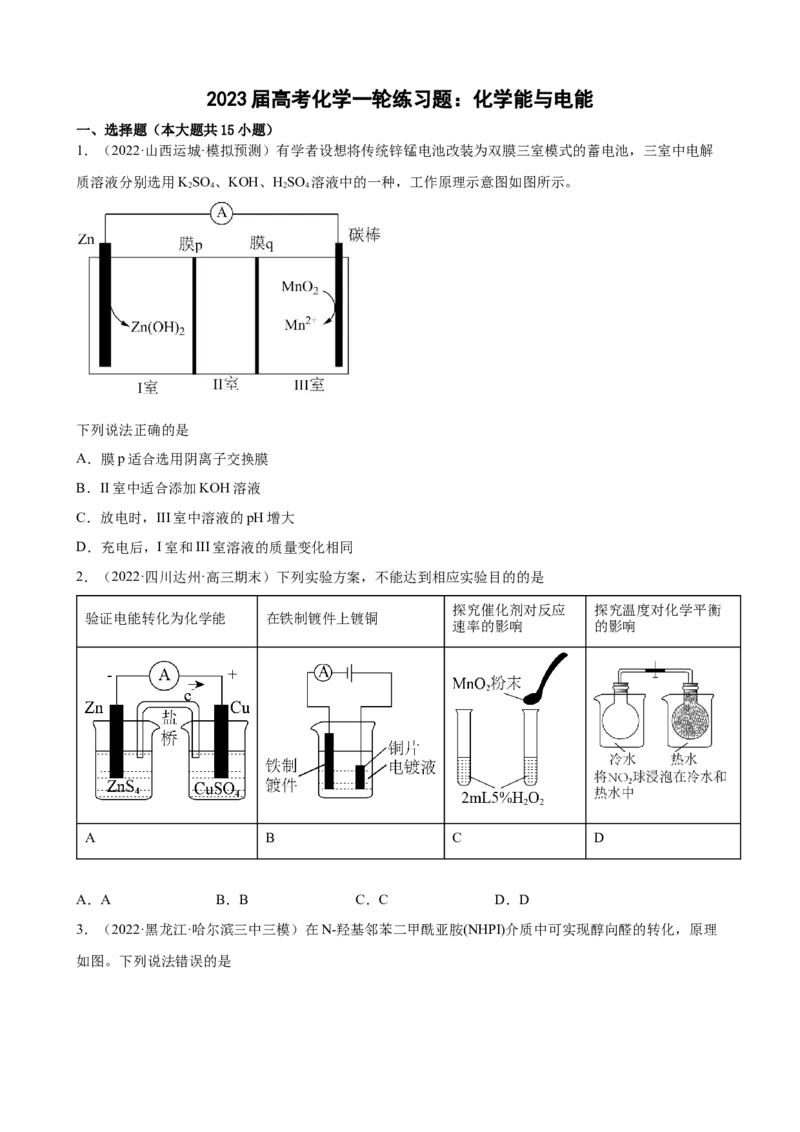
1.(2022·山西运城·模拟预测)有学者设想将传统锌锰电池改装为双膜三室模式的蓄电池,三室中电解
质溶液分别选用KSO 、KOH、HSO 溶液中的一种,工作原理示意图如图所示。
2 4 2 4
下列说法正确的是
A.膜p适合选用阴离子交换膜
B.II室中适合添加KOH溶液
C.放电时,III室中溶液的pH增大
D.充电后,I室和III室溶液的质量变化相同
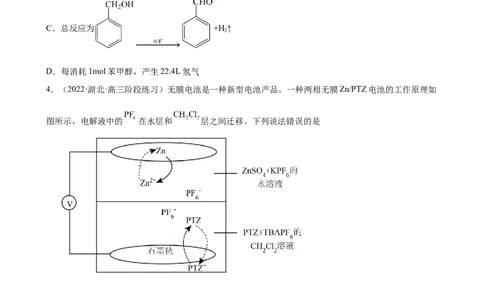
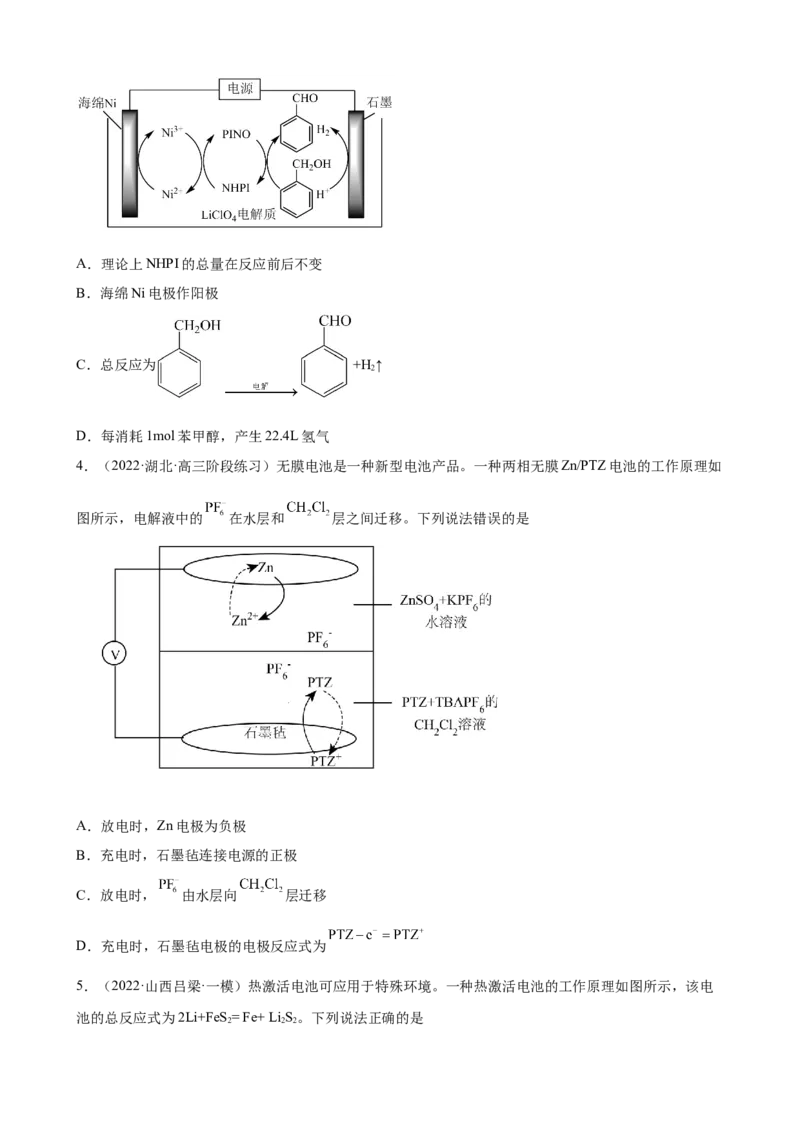
2.(2022·四川达州·高三期末)下列实验方案,不能达到相应实验目的的是
探究催化剂对反应 探究温度对化学平衡
验证电能转化为化学能 在铁制镀件上镀铜
速率的影响 的影响
A B C D
A.A B.B C.C D.D
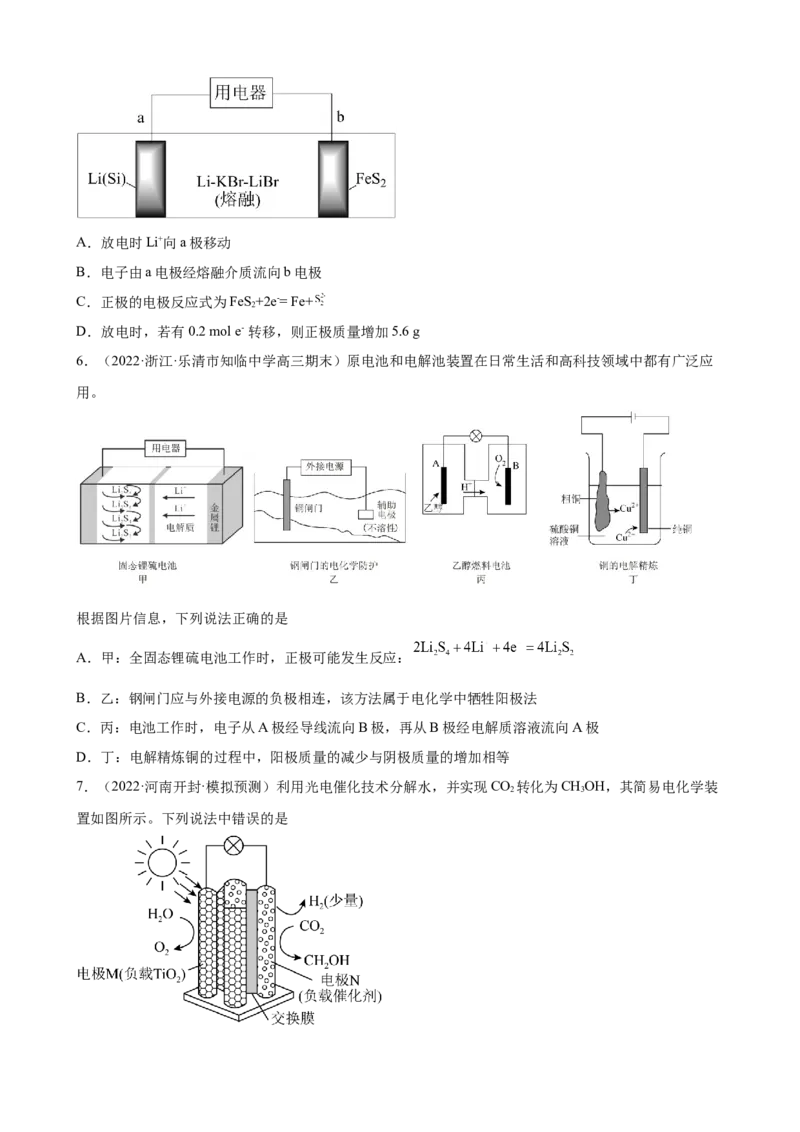
3.(2022·黑龙江·哈尔滨三中三模)在N-羟基邻苯二甲酰亚胺(NHPI)介质中可实现醇向醛的转化,原理
如图。下列说法错误的是A.理论上NHPI的总量在反应前后不变
B.海绵Ni电极作阳极
C.总反应为 +H ↑
2
D.每消耗1mol苯甲醇,产生22.4L氢气
4.(2022·湖北·高三阶段练习)无膜电池是一种新型电池产品。一种两相无膜Zn/PTZ电池的工作原理如
图所示,电解液中的 在水层和 层之间迁移。下列说法错误的是
A.放电时,Zn电极为负极
B.充电时,石墨毡连接电源的正极
C.放电时, 由水层向 层迁移
D.充电时,石墨毡电极的电极反应式为
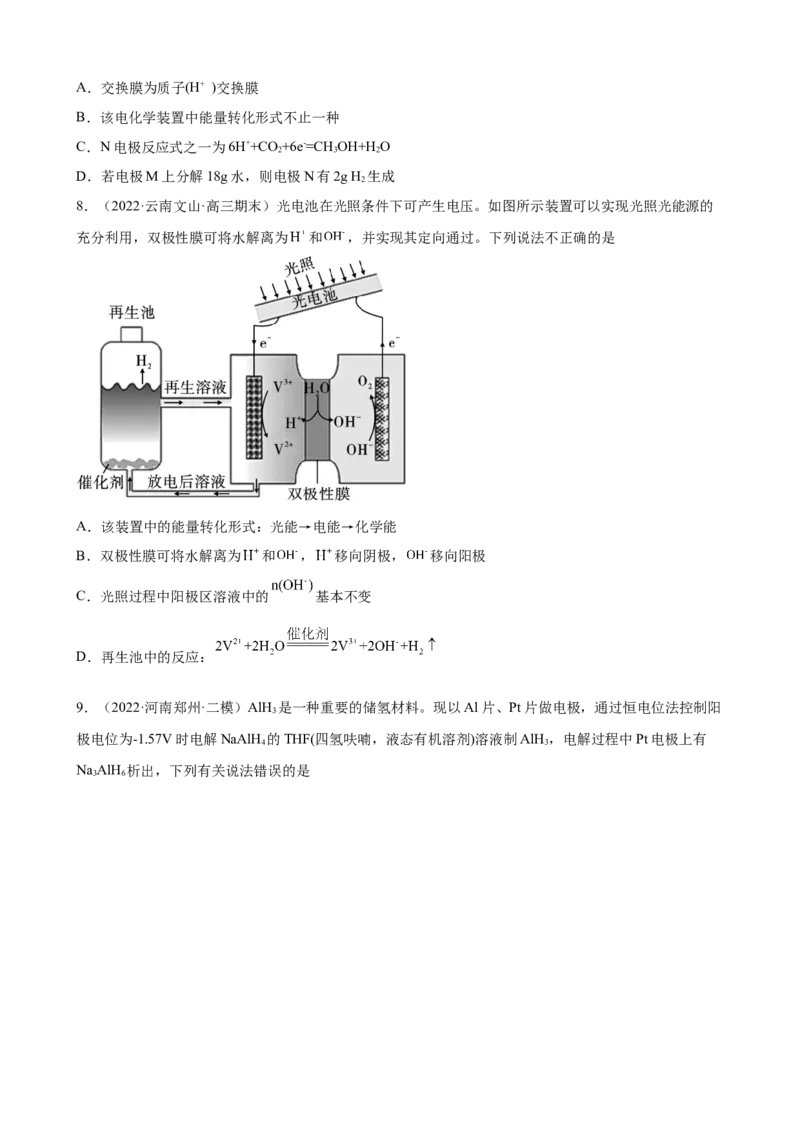
5.(2022·山西吕梁·一模)热激活电池可应用于特殊环境。一种热激活电池的工作原理如图所示,该电
池的总反应式为2Li+FeS= Fe+ Li S。下列说法正确的是
2 2 2A.放电时Li+向a极移动
B.电子由a电极经熔融介质流向b电极
C.正极的电极反应式为FeS+2e-= Fe+
2
D.放电时,若有0.2 mol e- 转移,则正极质量增加5.6 g
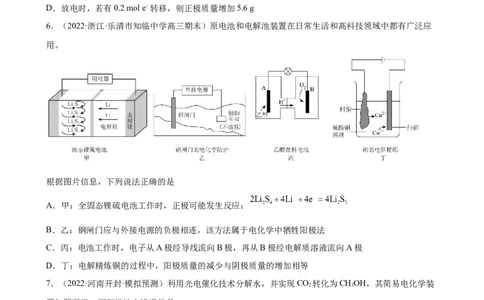
6.(2022·浙江·乐清市知临中学高三期末)原电池和电解池装置在日常生活和高科技领域中都有广泛应
用。
根据图片信息,下列说法正确的是
A.甲:全固态锂硫电池工作时,正极可能发生反应:
B.乙:钢闸门应与外接电源的负极相连,该方法属于电化学中牺牲阳极法
C.丙:电池工作时,电子从A极经导线流向B极,再从B极经电解质溶液流向A极
D.丁:电解精炼铜的过程中,阳极质量的减少与阴极质量的增加相等
7.(2022·河南开封·模拟预测)利用光电催化技术分解水,并实现CO 转化为CHOH,其简易电化学装
2 3
置如图所示。下列说法中错误的是A.交换膜为质子(H+ )交换膜
B.该电化学装置中能量转化形式不止一种
C.N电极反应式之一为6H++CO +6e-=CH OH+H O
2 3 2
D.若电极M上分解18g水,则电极N有2g H 生成
2
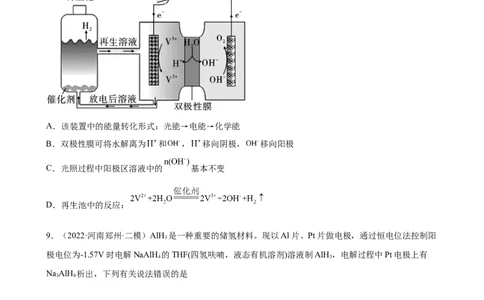
8.(2022·云南文山·高三期末)光电池在光照条件下可产生电压。如图所示装置可以实现光照光能源的
充分利用,双极性膜可将水解离为 和 ,并实现其定向通过。下列说法不正确的是
A.该装置中的能量转化形式:光能→电能→化学能
B.双极性膜可将水解离为 和 , 移向阴极, 移向阳极
C.光照过程中阳极区溶液中的 基本不变
D.再生池中的反应:
9.(2022·河南郑州·二模)AlH 是一种重要的储氢材料。现以Al片、Pt片做电极,通过恒电位法控制阳
3
极电位为-1.57V时电解NaAlH 的THF(四氢呋喃,液态有机溶剂)溶液制AlH,电解过程中Pt电极上有
4 3
NaAlH 析出,下列有关说法错误的是
3 6已知:电位值影响电极放电。
A.Pt片接恒电位仪的负极,NaAlH 在Pt上被还原为NaAlH
4 3 6
B.电解时不能在有水环境中进行
C.Al片接恒电位仪的正极,电极反应为3 +Al-3e-=4AlH
3
D.若阳极电位不是-1.57V,则阳极可能同时生成H
2
10.(2022·山西晋中·二模)近日,一种新型水系可充电无隔膜Zn/MnO 液流电池倍受关注,该电池具有
2
成本低、高离子导电率、高安全性和环境友好性等特点。电池以锌箔、石墨毡为集流体,ZnSO 和
4
MnSO 的混合液作电解质溶液。下列说法错误的是
4
A.过程Ⅰ是充电过程,过程Ⅱ是放电过程
B.充电时锌箔和电源的负极相连
C.充电时阳极反应为Mn2+-2e- +2H O=MnO ↓+4H+
2 2
D.放电时,当外电路转移1 mol e-时,两极板质量变化的差值为22 g
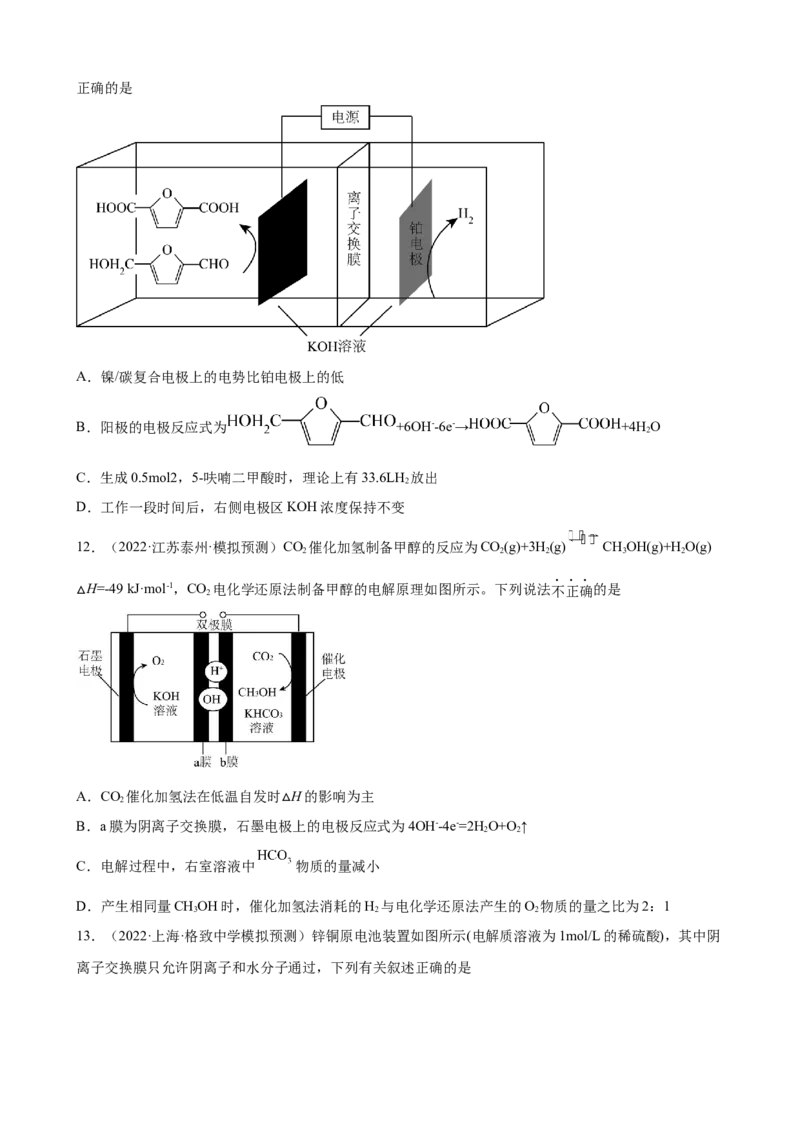
11.(2022·江西南昌·模拟预测)5-羟甲基糠醛可作为原料生产多种高附加值化合物。一种水相碱性体系
中,高选择性电催化5-羟甲基糠醛生成2,5-呋喃二甲酸并耦合高效析氢反应的装置如图所示。下列说法正确的是
A.镍/碳复合电极上的电势比铂电极上的低
B.阳极的电极反应式为 +6OH--6e-→ +4H O
2
C.生成0.5mol2,5-呋喃二甲酸时,理论上有33.6LH 放出
2
D.工作一段时间后,右侧电极区KOH浓度保持不变
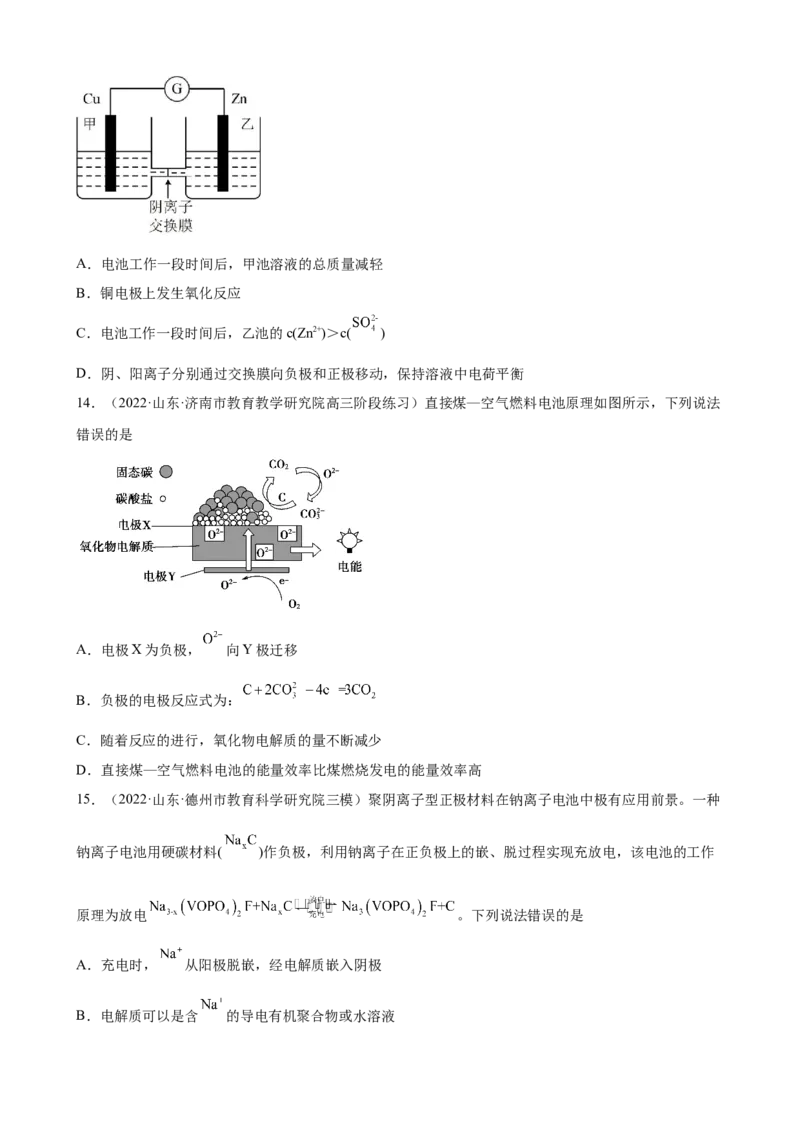
12.(2022·江苏泰州·模拟预测)CO 催化加氢制备甲醇的反应为CO(g)+3H(g) CHOH(g)+H O(g)
2 2 2 3 2
H=-49 kJ·mol-1,CO 电化学还原法制备甲醇的电解原理如图所示。下列说法不正确的是
2
△
A.CO 催化加氢法在低温自发时 H的影响为主
2
B.a膜为阴离子交换膜,石墨电极△上的电极反应式为4OH--4e-=2H
2
O+O
2
↑
C.电解过程中,右室溶液中 物质的量减小
D.产生相同量CHOH时,催化加氢法消耗的H 与电化学还原法产生的O 物质的量之比为2:1
3 2 2
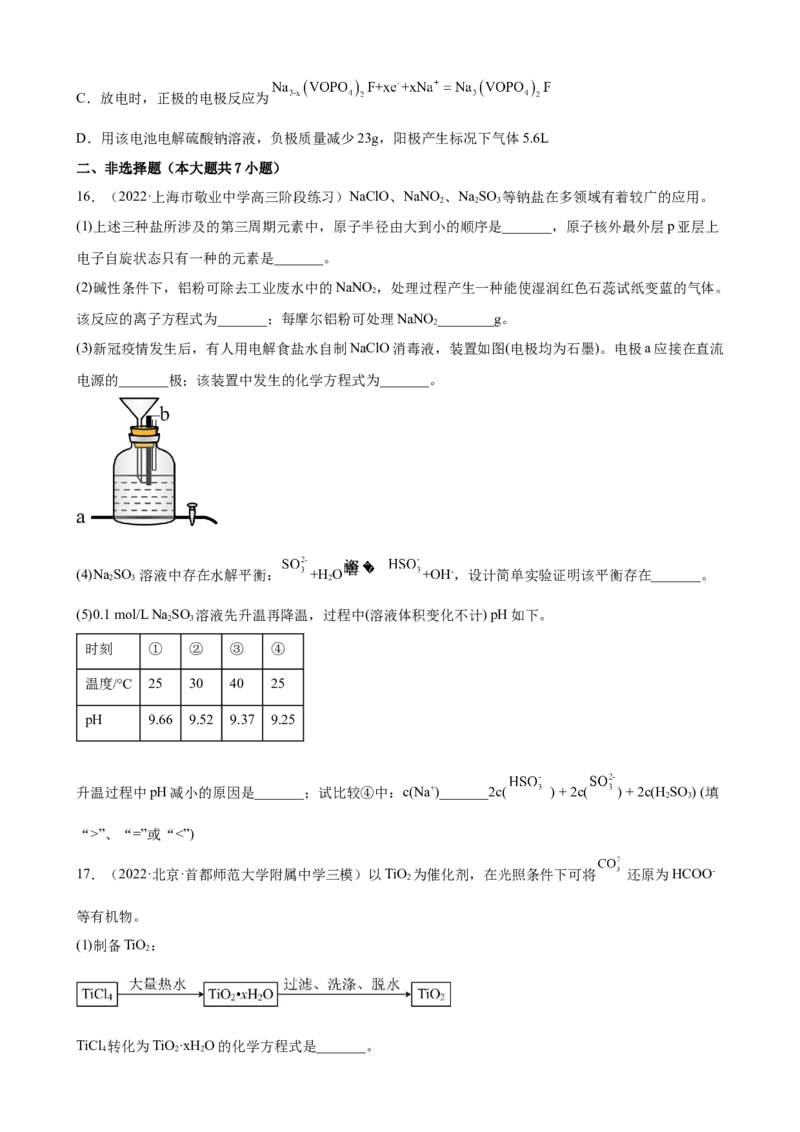
13.(2022·上海·格致中学模拟预测)锌铜原电池装置如图所示(电解质溶液为1mol/L的稀硫酸),其中阴
离子交换膜只允许阴离子和水分子通过,下列有关叙述正确的是A.电池工作一段时间后,甲池溶液的总质量减轻
B.铜电极上发生氧化反应
C.电池工作一段时间后,乙池的c(Zn2+)>c( )
D.阴、阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
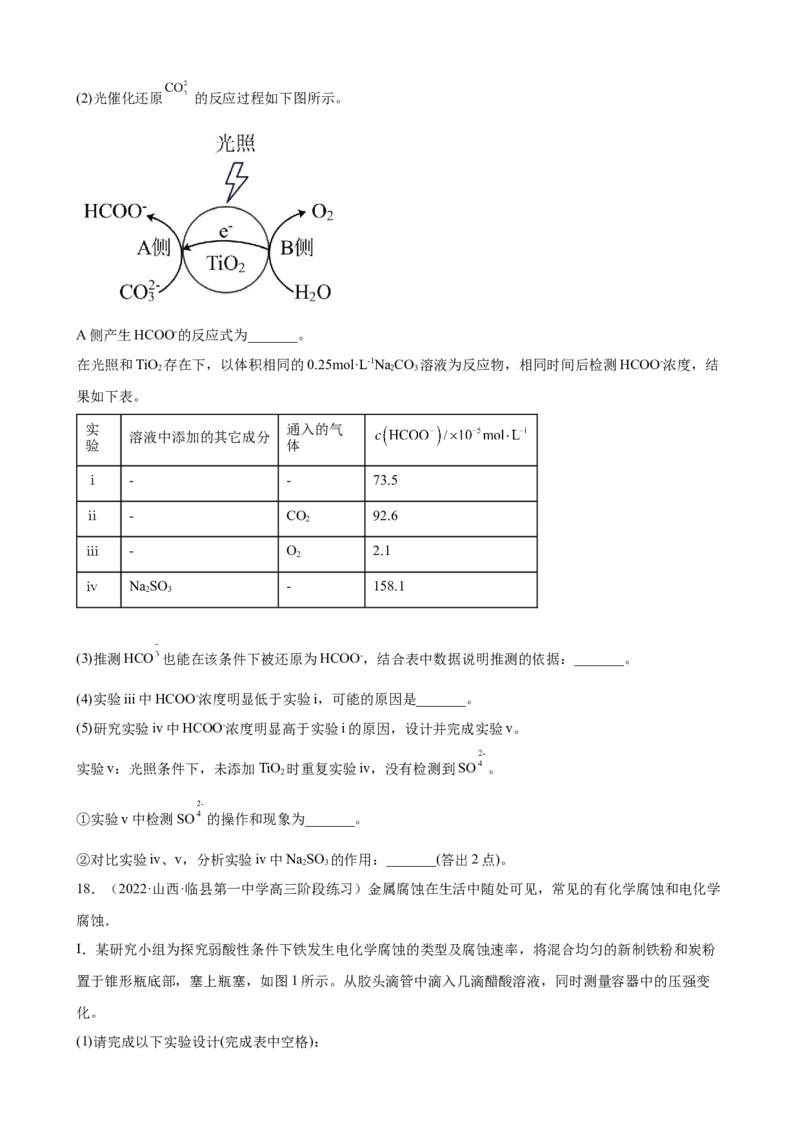
14.(2022·山东·济南市教育教学研究院高三阶段练习)直接煤—空气燃料电池原理如图所示,下列说法
错误的是
A.电极X为负极, 向Y极迁移
B.负极的电极反应式为:
C.随着反应的进行,氧化物电解质的量不断减少
D.直接煤—空气燃料电池的能量效率比煤燃烧发电的能量效率高
15.(2022·山东·德州市教育科学研究院三模)聚阴离子型正极材料在钠离子电池中极有应用前景。一种
钠离子电池用硬碳材料( )作负极,利用钠离子在正负极上的嵌、脱过程实现充放电,该电池的工作
原理为放电 。下列说法错误的是
A.充电时, 从阳极脱嵌,经电解质嵌入阴极
B.电解质可以是含 的导电有机聚合物或水溶液C.放电时,正极的电极反应为
D.用该电池电解硫酸钠溶液,负极质量减少23g,阳极产生标况下气体5.6L
二、非选择题(本大题共7小题)
16.(2022·上海市敬业中学高三阶段练习)NaClO、NaNO 、NaSO 等钠盐在多领域有着较广的应用。
2 2 3
(1)上述三种盐所涉及的第三周期元素中,原子半径由大到小的顺序是_______,原子核外最外层p亚层上
电子自旋状态只有一种的元素是_______。
(2)碱性条件下,铝粉可除去工业废水中的NaNO ,处理过程产生一种能使湿润红色石蕊试纸变蓝的气体。
2
该反应的离子方程式为_______;每摩尔铝粉可处理NaNO ________g。
2
(3)新冠疫情发生后,有人用电解食盐水自制NaClO消毒液,装置如图(电极均为石墨)。电极a应接在直流
电源的_______极;该装置中发生的化学方程式为_______。
(4)Na SO 溶液中存在水解平衡: +H O +OH-,设计简单实验证明该平衡存在_______。
2 3 2
(5)0.1 mol/L Na SO 溶液先升温再降温,过程中(溶液体积变化不计) pH如下。
2 3
时刻 ① ② ③ ④
温度/°C 25 30 40 25
pH 9.66 9.52 9.37 9.25
升温过程中pH减小的原因是_______;试比较④中:c(Na+)_______2c( ) + 2c( ) + 2c(H SO ) (填
2 3
“>”、“=”或“<”)
17.(2022·北京·首都师范大学附属中学三模)以TiO 为催化剂,在光照条件下可将 还原为HCOO-
2
等有机物。
(1)制备TiO:
2
TiCl 转化为TiO·xH O的化学方程式是_______。
4 2 2(2)光催化还原 的反应过程如下图所示。
A侧产生HCOO-的反应式为_______。
在光照和TiO 存在下,以体积相同的0.25mol·L-1NaCO 溶液为反应物,相同时间后检测HCOO-浓度,结
2 2 3
果如下表。
实 通入的气
溶液中添加的其它成分
验 体
ⅰ - - 73.5
ⅱ - CO 92.6
2
ⅲ - O 2.1
2
ⅳ NaSO - 158.1
2 3
(3)推测HCO 也能在该条件下被还原为HCOO-,结合表中数据说明推测的依据:_______。
(4)实验iii中HCOO-浓度明显低于实验i,可能的原因是_______。
(5)研究实验iv中HCOO-浓度明显高于实验i的原因,设计并完成实验v。
实验v:光照条件下,未添加TiO 时重复实验iv,没有检测到SO 。
2
①实验v中检测SO 的操作和现象为_______。
②对比实验iv、v,分析实验iv中NaSO 的作用:_______(答出2点)。
2 3
18.(2022·山西·临县第一中学高三阶段练习)金属腐蚀在生活中随处可见,常见的有化学腐蚀和电化学
腐蚀.
I.某研究小组为探究弱酸性条件下铁发生电化学腐蚀的类型及腐蚀速率,将混合均匀的新制铁粉和炭粉
置于锥形瓶底部,塞上瓶塞,如图1所示。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变
化。
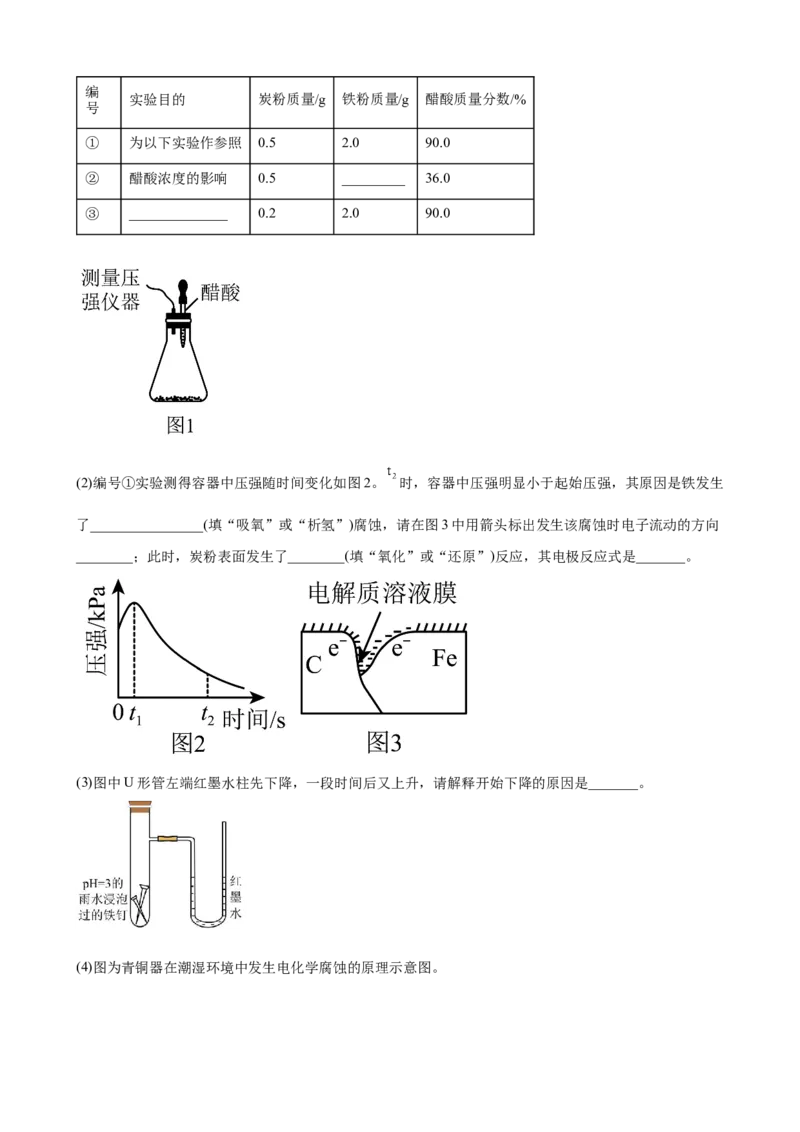
(1)请完成以下实验设计(完成表中空格):编
实验目的 炭粉质量/g 铁粉质量/g 醋酸质量分数/%
号
① 为以下实验作参照 0.5 2.0 90.0
② 醋酸浓度的影响 0.5 _________ 36.0
③ ______________ 0.2 2.0 90.0
(2)编号①实验测得容器中压强随时间变化如图2。 时,容器中压强明显小于起始压强,其原因是铁发生
了________________(填“吸氧”或“析氢”)腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动的方向
________;此时,炭粉表面发生了________(填“氧化”或“还原”)反应,其电极反应式是_______。
(3)图中U形管左端红墨水柱先下降,一段时间后又上升,请解释开始下降的原因是_______。
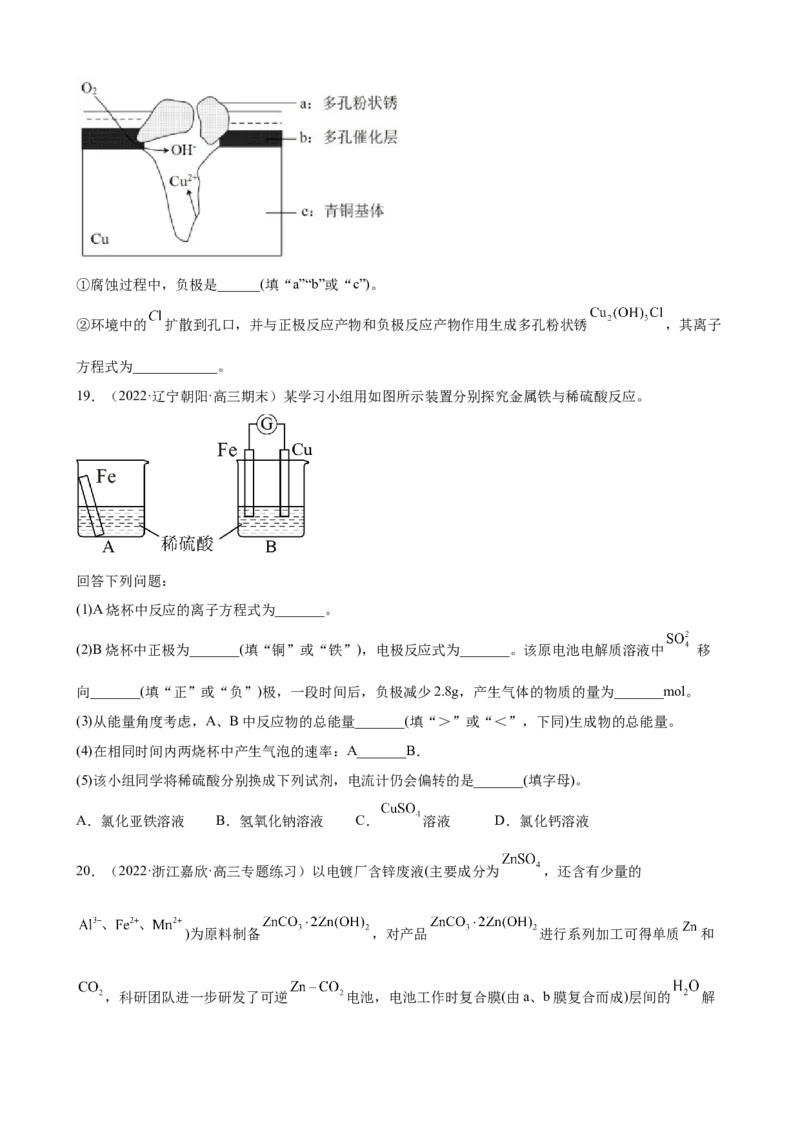
(4)图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。①腐蚀过程中,负极是______(填“a”“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈 ,其离子
方程式为____________。
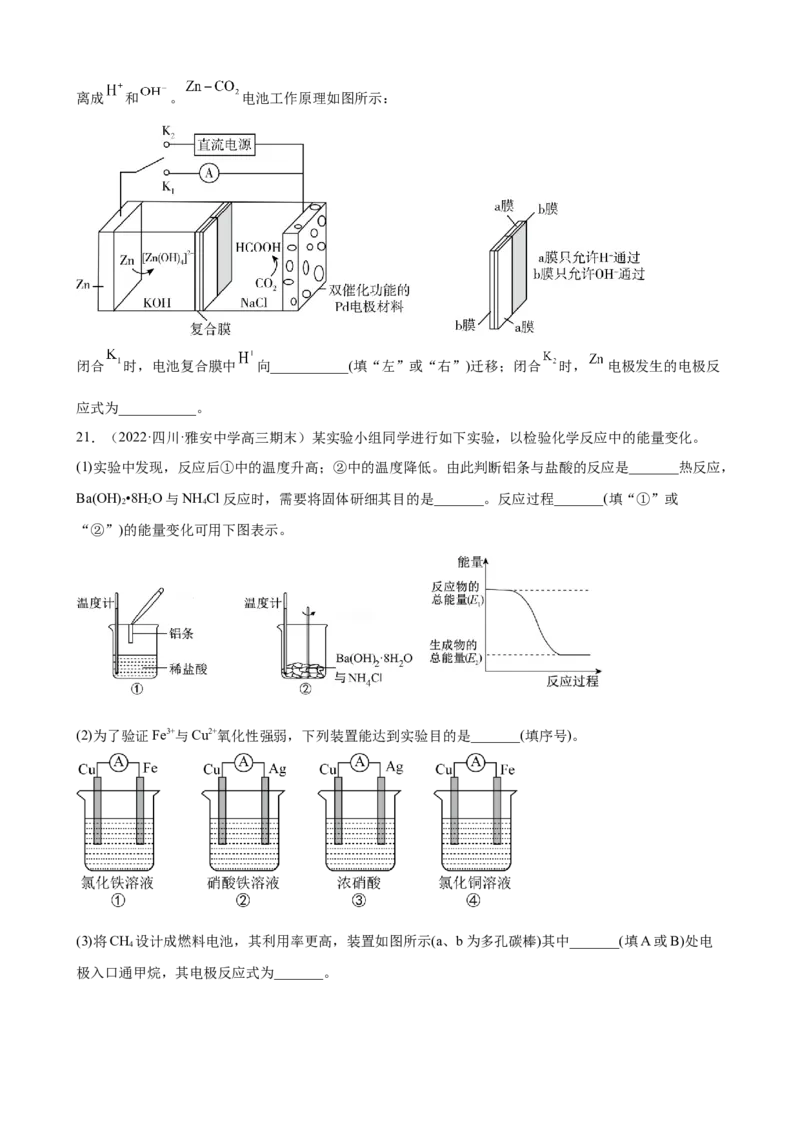
19.(2022·辽宁朝阳·高三期末)某学习小组用如图所示装置分别探究金属铁与稀硫酸反应。
回答下列问题:
(1)A烧杯中反应的离子方程式为_______。
(2)B烧杯中正极为_______(填“铜”或“铁”),电极反应式为_______。该原电池电解质溶液中 移
向_______(填“正”或“负”)极,一段时间后,负极减少2.8g,产生气体的物质的量为_______mol。
(3)从能量角度考虑,A、B中反应物的总能量_______(填“>”或“<”,下同)生成物的总能量。
(4)在相同时间内两烧杯中产生气泡的速率:A_______B.
(5)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_______(填字母)。
A.氯化亚铁溶液 B.氢氧化钠溶液 C. 溶液 D.氯化钙溶液
20.(2022·浙江嘉欣·高三专题练习)以电镀厂含锌废液(主要成分为 ,还含有少量的
)为原料制备 ,对产品 进行系列加工可得单质 和
,科研团队进一步研发了可逆 电池,电池工作时复合膜(由a、b膜复合而成)层间的 解离成 和 。 电池工作原理如图所示:
闭合 时,电池复合膜中 向___________(填“左”或“右”)迁移;闭合 时, 电极发生的电极反
应式为___________。
21.(2022·四川·雅安中学高三期末)某实验小组同学进行如下实验,以检验化学反应中的能量变化。
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是_______热反应,
Ba(OH) •8H O与NH Cl反应时,需要将固体研细其目的是_______。反应过程_______(填“①”或
2 2 4
“②”)的能量变化可用下图表示。
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_______(填序号)。
(3)将CH 设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中_______(填A或B)处电
4
极入口通甲烷,其电极反应式为_______。(4)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸时,写出该原电池正极的电极反应式为_______。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为_______;该原电池
的负极反应式为_______。
22.(2022·江苏省苏州实验中学高三期末)NaClO因其具有强氧化性,在生产及生活中有着广泛的用途。
NaFeO 可通过Fe3+与NaClO在碱性溶液中反应制备。NaFeO 和NaClO均可用于氧化去除高氯(含高浓度
2 4 2 4
Cl-)废水中的有机物。
(1)用NaFeO 处理高氯废水中的有机物时,需在一定条件下使用。
2 4
①pH=5时, 分解放出O 并产生Fe(OH) 沉淀,该反应的离子方程式为_______。
2 3
②酸性溶液中 的氧化性大于Cl 的氧化性。 处理高氯废水中的有机物需在碱性条件下进行,
2
其原因是_______。
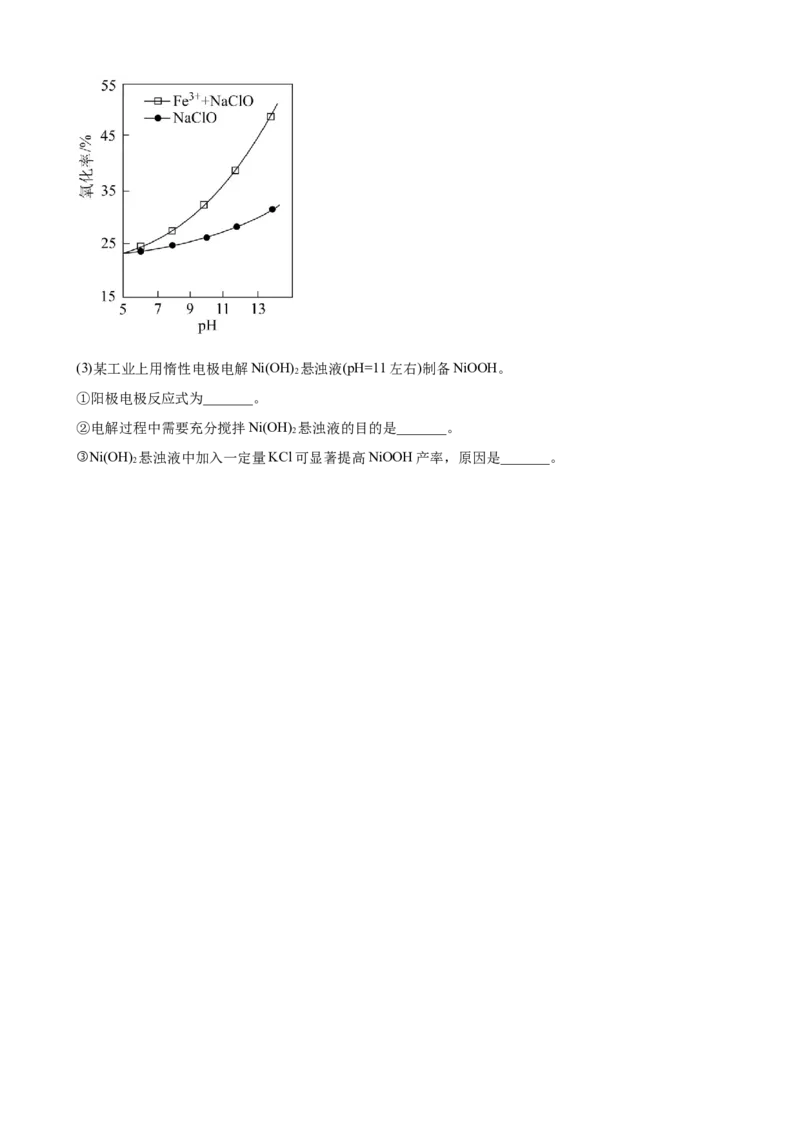
(2)用NaClO处理高氯废水中的有机物时,研究了“NaClO”和“Fe3++NaClO”两种体系对高氯废水中有机
物的氧化率。(废水中被氧化有机物的量占废水中有机物总量的百分率)
①当废水pH<6时,仅使用NaClO处理高氯废水,有机物的氧化率较低,其原因是_______。
②当n(NaClO)相同时,使用“NaClO”与“Fe3++NaClO”处理高氯废水,废水中有机物的氧化率随废水pH
的变化如图所示。与“NaClO”体系相比,“Fe3++NaClO”体系中有机物氧化率随着废水pH升高显著增大
的可能原因是_______。(3)某工业上用惰性电极电解Ni(OH) 悬浊液(pH=11左右)制备NiOOH。
2
①阳极电极反应式为_______。
②电解过程中需要充分搅拌Ni(OH) 悬浊液的目的是_______。
2
③Ni(OH) 悬浊液中加入一定量KCl可显著提高NiOOH产率,原因是_______。
2参考答案:
1.C
2.A
3.D
4.C
5.C
6.A
7.D
8.D
9.A
10.D
11.B
12.C
13.A
14.AC
15.B
16.(1) Na>S>Cl N
(2) 2Al+NO +H O+OH-=NH↑+2AlO 34.5
2 3
(3) 正 2NaCl+2H O 2NaOH+H ↑+Cl↑、Cl+2NaOH=NaCl+NaClO+H O
2 2 2 2 2
(4)取少量NaSO 溶液于小试管中,滴加酚酞试液显红色,微热小试管,溶液红色加深,说
2 3
明该平衡存在
(5) 在加热条件下亚硫酸根离子被氧气氧化为硫酸根离子,使得水解的亚硫酸根浓度减
小,产生的OH-浓度减小,pH减小 >
17.(1)
(2)
(3)实验ⅱ中通入二氧化碳将 转化为HCO , 浓度减小,但HCO 浓度增大
(4)通入氧气,将HCOO-氧化
(5) 取适量的溶液,加入足量的稀盐酸,再加入氯化钡,未出现白色沉淀 亚硫酸钠消耗了氧气,减少了HCOO-的氧化损失;在光照和二氧化钛存在的条件下,亚硫酸根
离子在右侧失去电子,增大了碳酸根离子得电子的机会。
18.(1) 2.0 炭粉含量的影响
(2) 吸氧 还原
(3) 的雨水显酸性,铁发生析氢腐蚀,产生氢气,试管内压强增大
(4) c
19.(1)
(2) 铜 负 0.05
(3)>
(4)<
(5)C
20. 右 [Zn(OH) ]2-+2e-=Zn+4OH-
4
21.(1) 放 扩大接触面积,提高反应速率 ①
(2)②
(3) A CH-8e-+10OH-=CO +7H O
4 2
(4) 2H++2e-═H ↑ Mg Al+4OH-﹣3e-=AlO +2H O
2 2
22.(1) 4 +4H++2H O=3O↑+4Fe(OH) ↓ 防止 水解,防止 把Cl-氧化
2 2 3
为Cl
2
(2) 酸性条件下,ClO-和Cl-反应生成Cl 逸出 随着废水pH的增大,Fe3+和ClO-
2
反应生成的 浓度增大, 氧化废水中有机物的反应速率更大(3) Ni(OH) -e-+OH-=NiOOH+H O 与惰性电极充分接触,防止悬浊液沉降以提高电解
2 2
效率 Cl-在电极上得到电子生成Cl,Cl 与碱反应生成ClO-,ClO-将悬浊液中
2 2
Ni(OH) 氧化成NiOOH
2