文档内容
2023 年邵阳市高三第一次联考试题卷
化 学
本试卷共 页, 个小题。 满分 分。 考试用时 分钟。
6 18 100 75
注意事项:
答卷前,考生务必将自己的姓名、班级、考号填写在答题卡上。 将条形码横贴在答题
1.
卡上“条形码粘贴区”。
作答选择题时,选出每小题答案后,用 铅笔在答题卡上对应题目选项的答案信息
2. 2B
点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案。 答案不能答在试卷上。
非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区
3.
域内相应位置上;如需改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和
涂改液。 不按以上要求作答无效。
保持答题卡的整洁。 考试结束后,只交答题卡,试题卷自行保存。
4.
可能用到的相对原子质量: — — — — — — —
H 1 He 4 Li 7 C 12 O 16 Na 23 P 31
— — — — — —
K 39 Cr 52 Fe 56 Cu 64 Ga 70 As 75
一、选择题:本题共 小题,每小题 分,共 分。 在每小题给出的四个选项中,只有一项
10 3 30
是符合题目要求的。
卡塔尔世界杯上 化学无处不在 下列说法错误的是
1. , ,
的结构酷似足球,故又称足球烯,它与金刚石互为同素异形体
A.
在
C60足球场上,足球裁判随身携带的“任意球喷雾器”能够喷出白色的喷雾,喷剂内含有
B.
的丁烷能使酸性高锰酸钾溶液褪色
中国企业为卡塔尔世界杯建造的阿尔卡萨 兆瓦光伏电站解决了比赛场地用电问
C. 800
题。 制造光伏电池的主要材料是晶体硅
氯乙烷气雾剂俗称足球运动场上的“化学大夫”,用于治疗运动中的急性损伤。 氯乙烷
D.
可以与 水溶液在加热的条件下发生取代反应
NaOH
化学用语是学习化学的重要工具 下列说法正确的是
2. ,
1 、2 、3 互为同位素
A. H2 H2 H2
的电子式为[ ·· ] [ ·· ]
- 2+ -
B.CaO2 ∶·O·∶ Ca ∶·O·∶
基态铜原子的价层电子排布式为
9 2
C. 3d 4s
通过核衰变得到的 的中子数为
45
D. 26Fe 19
用 表示阿伏加德罗常数的值 下列说法正确的是
3. NA 。
16
和
18
中质子数相等,中子数不相等
A. 电 1 m 解 o 精 l D 炼2 铜 O 时, 1 电 m 路 ol 中 H 每2 通 O 过 个电子,阴极析出
B. 常温常压下, 乙烯和丙烯 N 混A合气体含有极性键 3 数 2 为 g Cu
C. 1.4 g 0.3NA
与 溶液完全反应,所得溶液中c( -) c( -)
D.1 mol Cl2 NaOH Cl = ClO
年 月最火爆的药物莫过于布洛芬 它可用于缓解疼痛 也可用于普通流感引起的
4.2022 12 , ,
发热 布洛芬结构简式如右图 下列说法正确的是
。 ,
布洛芬能发生取代反应 O
A.
布洛芬分子式是
B. 布洛芬分子中含有 C1两3H 种16O 含2氧官能团 OH
C.
布洛芬与足量的 反应生成
D.1 mol Na 1 mol H2
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
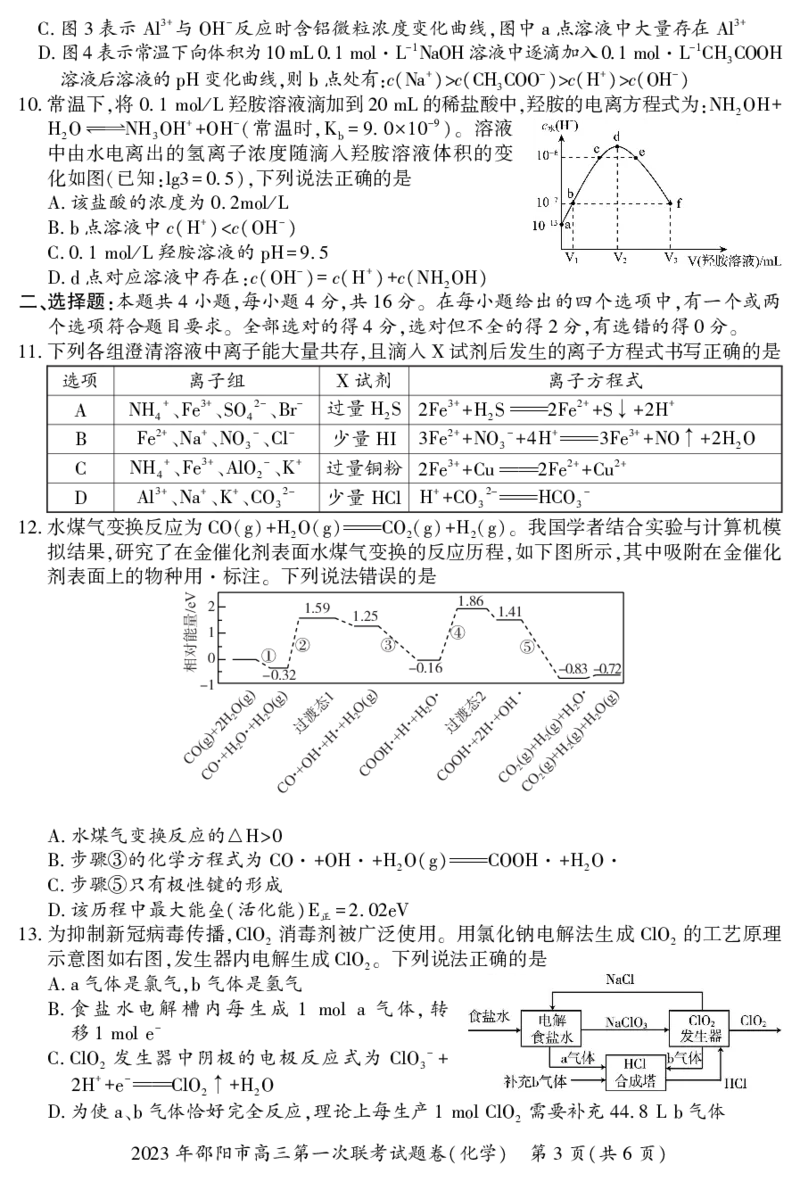
2023 1 6一种用于合成治疗免疫疾病药的物质 结构如右图所示 其中 为 号元
5. , , X、Y、Z、Q、W 1~20
素且原子序数依次增大 与 同主族 和 的简单离子具
,Z Q ,Q W
有相同的电子层结构 下列说法错误的是
。
原子半径:
A. W>Q
的氢化物的熔点低于 的氢化物的熔点
B.Z Q
阴离子 的 模型与其空间结构一致
2-
C. QZ4 VSEPR
溶液与 的最高价氧化物对应的水化物反应有黄色浑浊和无色气体
D.W2Q2Z3 Q
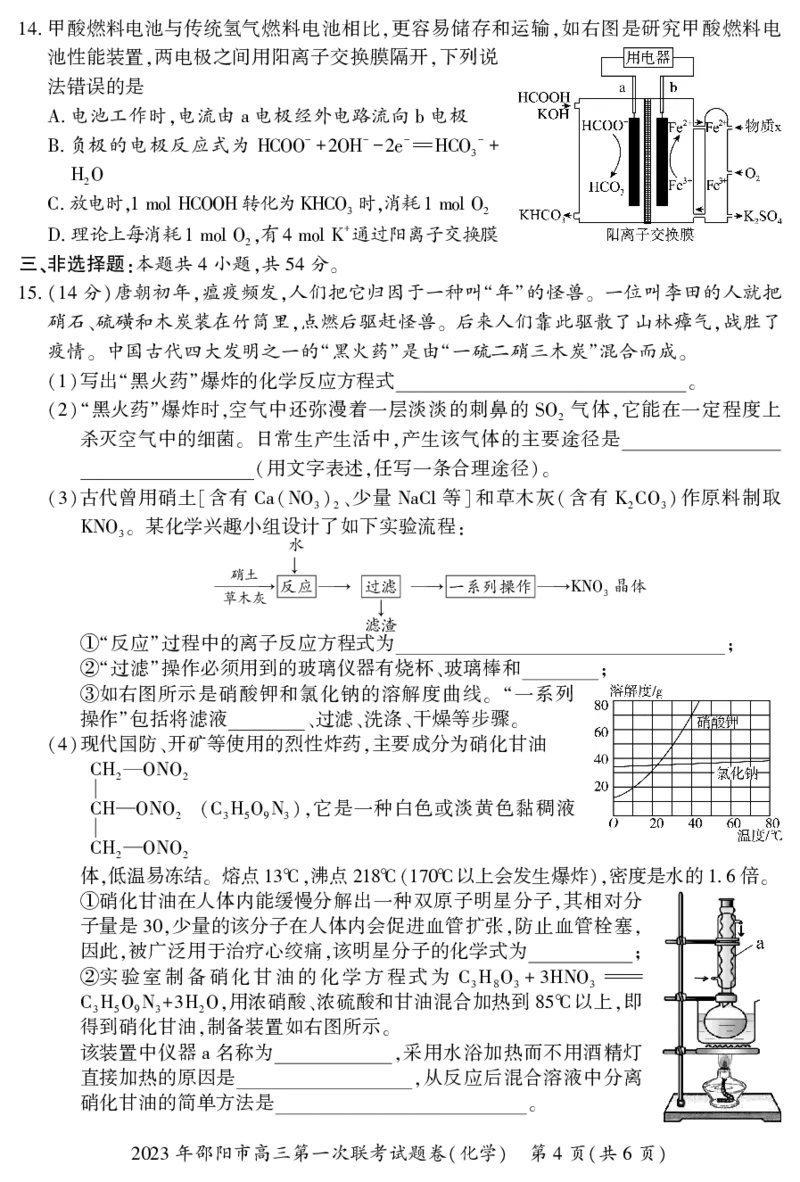
第二代半导体材料的代表物质 其晶胞结构如下图所示 阿伏加德罗常数的值为
6.
晶胞边长为 下列说法正
G
确
a
的
As
是
, , NA,
a pm。
的配位数为
A.As 8
晶体熔点很低
B.GaAs
32
该晶体密度为5.8×10
3
C. g/cm
3
NA×a
核电荷数为 的 的基态原子价电子排布图为
D. 31 Ga
下列设计的实验方案能达到相应实验目的的是
7.
选项 实验目的 实验方案
证明 有漂白性 将 通入酸性高锰酸钾溶液中,溶液褪色
A SO2 SO2
证明碳和浓硫酸共热产生的气 将产生的气体直接通入澄清石灰水中,有白色
B 体中含有 沉淀生成
CO2
用洁净的玻璃棒蘸取氨水点在湿润的 试
C
测定
0.1mol
·
L
-1 氨水的
pH 纸上,与标准比色卡对照读取
pH
pH
证明“ ”消毒液的氧化能力随 将“ ”消毒液(含 )滴入品红溶液中,褪
84 84 NaClO
D 溶液 的减小而增强 色缓慢,若同时加入醋酸,红色很快褪为无色
pH
一种电化学固氮的原理如图所示 已知 的键能为 -1 的键能为
8. , N≡N 946 kJ·mol ,N-N
-1 下列说法正确的是
193 kJ·mol 。
在 电极上, 被氧化
A. b N2
金属 可作为 电极的材料
B. Cu a
电解过程中,固体氧化物电解质中
2-
数目保持不变
C. O
分子中, 键数和 键数为 ,且 键键能小于 键键能
D.N2 π σ 2∶1 π σ
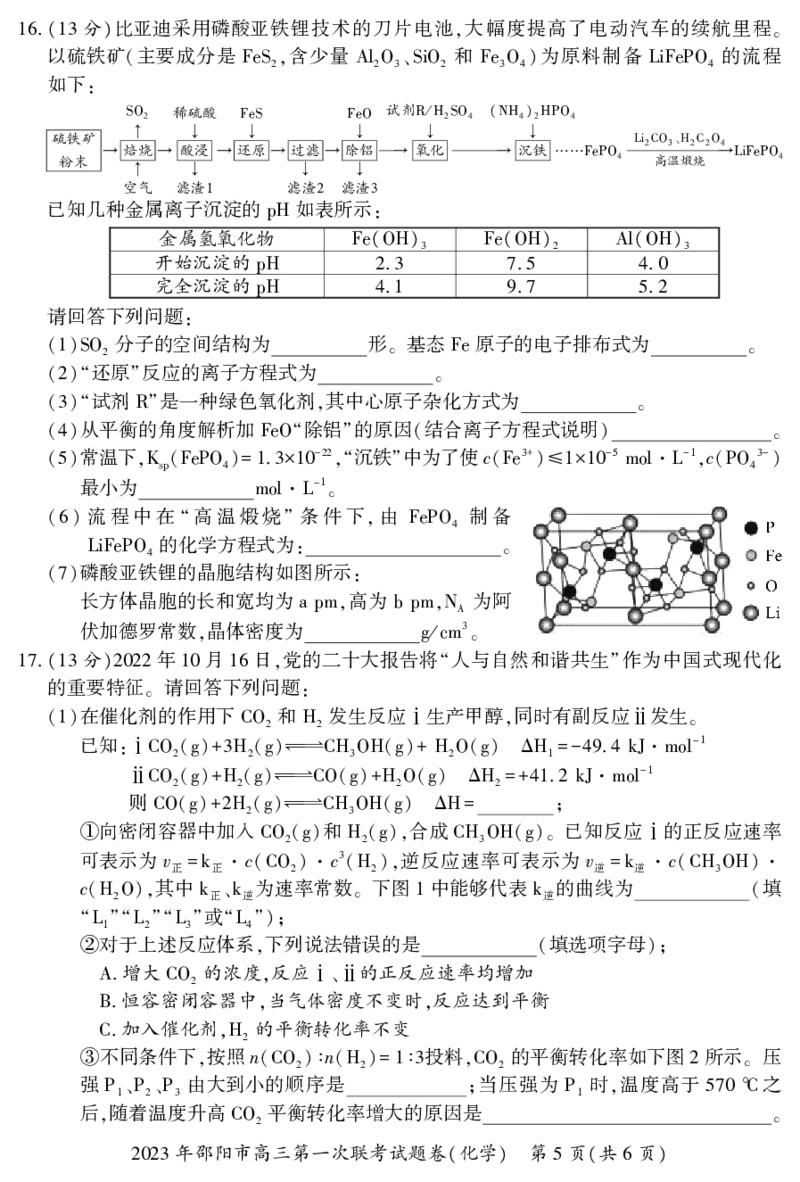
根据下列各图曲线表征的信息 得出的结论正确的是
9. ,
由图 得出若要除去 溶液中的 3+,可采用向溶液中加入适量 ,调节溶液的
A. 1 CuSO4 Fe CuO
至 左右
pH 4
图 表示用水稀释 相同的盐酸和 溶液时,溶液的 变化曲线,其中 表
B. 2 pH CH3COOH pH Ⅰ
示盐酸, 表示 溶液,且溶液导电性:
Ⅱ CH3COOH c>b>a
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
2023 2 6图 表示
3+
与
-
反应时含铝微粒浓度变化曲线,图中 点溶液中大量存在
3+
C. 3 Al OH a Al
图 表示常温下向体积为 · -1 溶液中逐滴加入 · -1
D. 4 10mL0.1mol L NaOH 0.1mol L CH3COOH
溶液后溶液的 变化曲线,则 点处有:c( +) c( -) c( +) c( -)
常温下 将
pH
羟胺溶液滴
b
加到
Na
的稀
>
盐
C
酸
H3
中
CO
羟
O
胺
>
的电
H
离
>
方程
OH
式为
10. , 0.1 mol/L 20 mL , :NH2OH+
+ - 常温时 -9 溶液
H2ONH3OH +OH ( ,Kb=9.0×10 )。
中由水电离出的氢离子浓度随滴入羟胺溶液体积的变
化如图 已知 下列说法正确的是
( :lg3=0.5),
该盐酸的浓度为
A. 0.2mol/L
点溶液中c( +) c( -)
B.b H < OH
羟胺溶液的
C.0.1 mol/L pH=9.5
点对应溶液中存在:c( -) c( +) c( )
二、
D
选
.
择
d
题:本题共 小题,每小
O
题
H =
分,共
H +
分。
NH 在2O
每
H
小题给出的四个选项中,有一个或两
4 4 16
个选项符合题目要求。 全部选对的得 分,选对但不全的得 分,有选错的得 分。
4 2 0
下列各组澄清溶液中离子能大量共存 且滴入 试剂后发生的离子方程式书写正确的是
11. , X
选项 离子组 试剂 离子方程式
X
+、 3+、 2-、 - 过量 3+ 2+ +
A NH4 Fe SO4 Br H2S 2Fe +H2S2Fe +S↓+2H
2+、 +、 -、 - 少量 2+ - + 3+
B Fe Na NO3 Cl HI 3Fe +NO3 +4H 3Fe +NO↑+2H2O
+、 3+、 -、 + 过量铜粉 3+ 2+ 2+
C NH4 Fe AlO2 K 2Fe +Cu2Fe +Cu
3+、 +、 +、 2- 少量 + 2- -
D Al Na K CO3 HCl H +CO3 HCO3
水煤气变换反应为 我国学者结合实验与计算机模
12. CO(g)+H2O(g)CO2(g)+H2(g)。
拟结果 研究了在金催化剂表面水煤气变换的反应历程 如下图所示 其中吸附在金催化
, , ,
剂表面上的物种用 标注 下列说法错误的是
· 。
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
2023 3 6
VeF6,
C O(g C ) O + e 2 + H H O 2 O 2 ( e g) + H O 2 (g
C
) Oe D + O # He + He + H O 2 C (g O ) O He + He + H O 2 e C O D O # He +2 He + O C H O e ( 2 g
C
) O + H ( 2 g ( 2 ) g + ) H + H ( 2 g O 2 ) e + H O 2 (g)
水煤气变换反应的
A. △H>0
步骤 的化学方程式为 · · ( ) · ·
B.
步骤
③
只有极性键的形成
CO +OH +H2O g COOH +H2O
C. ⑤
该历程中最大能垒(活化能)
D. E正=2.02eV
为抑制新冠病毒传播 消毒剂被广泛使用 用氯化钠电解法生成 的工艺原理
13. ,ClO2 。 ClO2
示意图如右图 发生器内电解生成 下列说法正确的是
气体是氯气
,
, 气体是氢气
ClO2。
A.a b
食盐水电解槽内每生成 气体,转
B. 1 mol a
移
-
1 mol e
发生器中阴极的电极反应式为
-
C.ClO2 ClO3 +
+ -
2H +e ClO2↑+H2O
为使 、 气体恰好完全反应,理论上每生产 需要补充 气体
D. a b 1 mol ClO2 44.8 L b甲酸燃料电池与传统氢气燃料电池相比 更容易储存和运输 如右图是研究甲酸燃料电
14. , ,
池性能装置 两电极之间用阳离子交换膜隔开 下列说
, ,
法错误的是
电池工作时,电流由 电极经外电路流向 电极
A. a b
负极的电极反应式为
- - - -
B. HCOO +2OH -2e HCO3 +
H2O
放电时, 转化为 时,消耗
C. 1mol HCOOH KHCO3 1mol O2
理论上每消耗 ,有
+
通过阳离子交换膜
D. 1 mol O2 4 mol K
三、非选择题:本题共 小题,共 分。
4 54
( 分)唐朝初年,瘟疫频发,人们把它归因于一种叫“年”的怪兽。 一位叫李田的人就把
15. 14
硝石、硫磺和木炭装在竹筒里,点燃后驱赶怪兽。 后来人们靠此驱散了山林瘴气,战胜了
疫情。 中国古代四大发明之一的“黑火药”是由“一硫二硝三木炭”混合而成。
写出 黑火药 爆炸的化学反应方程式
(1) “ ” 。
黑火药 爆炸时 空气中还弥漫着一层淡淡的刺鼻的 气体 它能在一定程度上
(2)“ ” , SO2 ,
杀灭空气中的细菌 日常生产生活中 产生该气体的主要途径是
。 ,
用文字表述 任写一条合理途径
( , )。
古代曾用硝土 含有 少量 等 和草木灰 含有 作原料制取
(3) [ Ca(NO3)2、 NaCl ] ( K2CO3)
某化学兴趣小组设计了如下实验流程
KNO3。 水 :
硝土 ↓
反应 过滤 一系列操作 晶体
草木灰→ → → →KNO3
滤↓渣
反应 过程中的离子反应方程式为
①“ ” ;
过滤 操作必须用到的玻璃仪器有烧杯 玻璃棒和
②“ ” 、 ;
如右图所示是硝酸钾和氯化钠的溶解度曲线 一系列
③ 。 “
操作 包括将滤液 过滤 洗涤 干燥等步骤
” 、 、 、 。
现代国防 开矿等使用的烈性炸药 主要成分为硝化甘油
(4) 、 ,
CH2 ONO2
它是一种白色或淡黄色黏稠液
CH ONO2 (C3H5O9N3),
CH2 ONO2
体 低温易冻结 熔点 沸点 以上会发生爆炸 密度是水的 倍
, 。 13℃, 218℃(170℃ ), 1.6 。
硝化甘油在人体内能缓慢分解出一种双原子明星分子 其相对分
① ,
子量是 少量的该分子在人体内会促进血管扩张 防止血管栓塞
30, , ,
因此 被广泛用于治疗心绞痛 该明星分子的化学式为
, , ;
实验室制备硝化甘油的化学方程式为
② C3H8O3 +3HNO3
用浓硝酸 浓硫酸和甘油混合加热到 以上 即
C3H5O9N3+3H2O, 、 85℃ ,
得到硝化甘油 制备装置如右图所示
, 。
该装置中仪器 名称为 采用水浴加热而不用酒精灯
a ,
直接加热的原因是 从反应后混合溶液中分离
,
硝化甘油的简单方法是
。
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
2023 4 6( 分)比亚迪采用磷酸亚铁锂技术的刀片电池 大幅度提高了电动汽车的续航里程
16. 13 , 。
以硫铁矿 主要成分是 含少量 和 为原料制备 的流程
( FeS2, Al2O3、SiO2 Fe3O4) LiFePO4
如下
:
稀硫酸 试剂 ( )
SO2 FeS FeO R/H2SO4 NH4 2HPO4
硫铁矿 焙 ↑ 烧 酸 ↓ 浸 还 ↓ 原 过滤 除 ↓ 铝 氧 ↓ 化 沉 ↓ 铁 …… Li2CO3 、 H2C2O4
粉末 → → → → → → → FePO4 高温煅烧 →LiFePO4
↑ ↓ ↓ ↓
空气 滤渣 滤渣 滤渣
1 2 3
已知几种金属离子沉淀的 如表所示
pH :
金属氢氧化物 ( ) ( ) ( )
开始沉淀的 Fe OH 3 Fe OH 2 Al OH 3
pH 2.3 7.5 4.0
完全沉淀的
pH 4.1 9.7 5.2
请回答下列问题
:
分子的空间结构为 形 基态 原子的电子排布式为
(1)SO2 。 Fe 。
还原 反应的离子方程式为
(2)“ ” 。
试剂 是一种绿色氧化剂 其中心原子杂化方式为
(3)“ R” , 。
从平衡的角度解析加 除铝 的原因 结合离子方程式说明
(4) FeO“ ” ( ) 。
常温下 -22 沉铁 中为了使c 3+ -5 -1 c 3-
(5) ,Ksp(FePO4)=1.3×10 ,“ ” (Fe )≤1×10 mol·L , (PO4 )
最小为 -1
mol·L 。
流程中在 高温煅烧 条件下 由 制备
(6) “ ” , FePO4
的化学方程式为
LiFePO4 : 。
磷酸亚铁锂的晶胞结构如图所示
(7) :
长方体晶胞的长和宽均为 高为 为阿
a pm, b pm,NA
伏加德罗常数 晶体密度为 3
, g/cm 。
( 分) 年 月 日 党的二十大报告将 人与自然和谐共生 作为中国式现代化
17. 13 2022 10 16 , “ ”
的重要特征 请回答下列问题
。 :
在催化剂的作用下 和 发生反应 生产甲醇 同时有副反应 发生
(1) CO2 H2 ⅰ , ⅱ 。
已知 -1
:ⅰCO2(g)+3H2(g)CH3OH(g)+ H2O(g) ΔH1=-49.4 kJ·mol
-1
ⅱCO2(g)+H2(g)CO(g)+H2O(g) ΔH2=+41.2 kJ·mol
则
CO(g)+2H2(g)CH3OH(g) ΔH= ;
向密闭容器中加入 和 合成 已知反应 的正反应速率
① CO2(g) H2(g), CH3OH(g)。 ⅰ
可表示为 v
正=k正·
c
(CO2)·
c3
(H2),
逆反应速率可表示为 v
逆=k逆·
c
(CH3OH)·
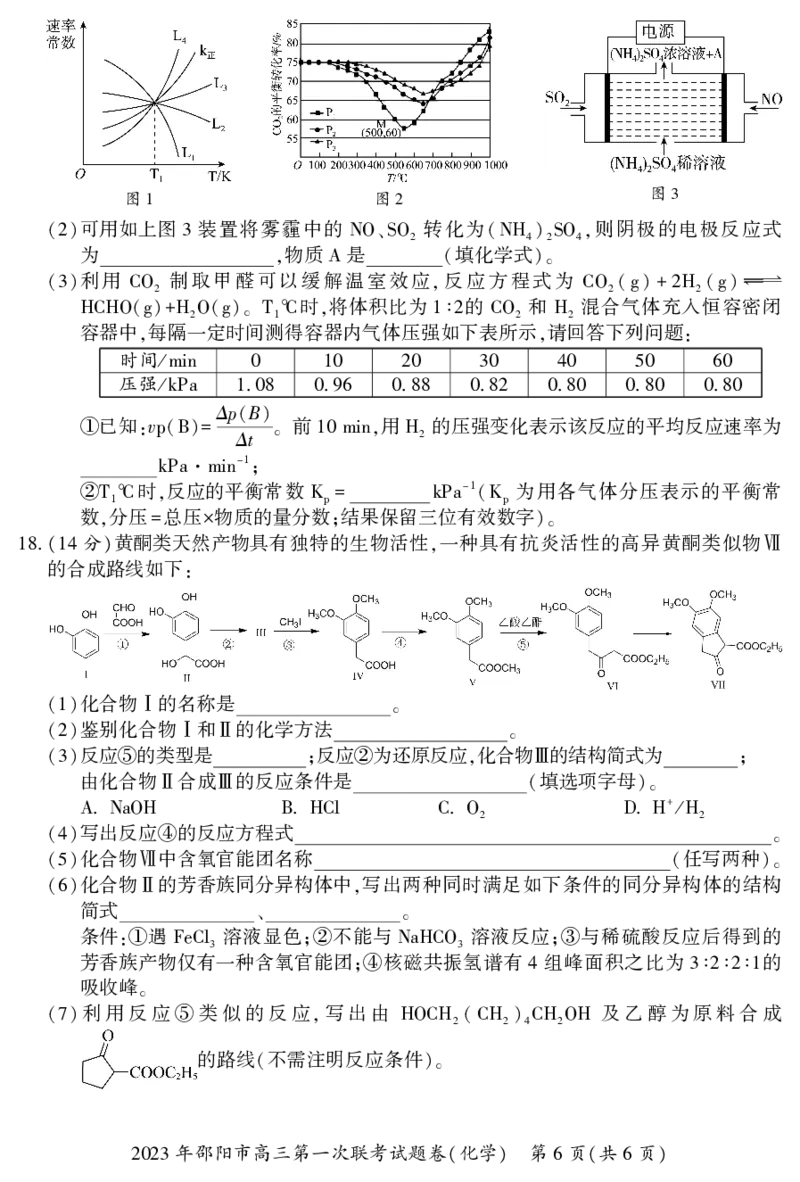
c 其中 为速率常数 下图 中能够代表 的曲线为 填
(H2O), k正、k逆 。 1 k逆 (
或
“L1”“L2”“L3” “L4”);
对于上述反应体系 下列说法错误的是 填选项字母
② , ( );
增大 的浓度,反应 、 的正反应速率均增加
A. CO2 ⅰ ⅱ
恒容密闭容器中,当气体密度不变时,反应达到平衡
B.
加入催化剂, 的平衡转化率不变
C. H2
不同条件下 按照n n 投料 的平衡转化率如下图 所示 压
③ , (CO2)∶ (H2)= 1∶3 ,CO2 2 。
强 由大到小的顺序是 当压强为 时 温度高于 之
P1、P2、P3 ; P1 , 570 ℃
后 随着温度升高 平衡转化率增大的原因是
, CO2 。
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
2023 5 6图 图 图
1 2 3
可用如上图 装置将雾霾中的 转化为 则阴极的电极反应式
(2) 3 NO、SO2 (NH4)2SO4,
为 物质 是 填化学式
, A ( )。
利用 制取甲醛可以缓解温室效应 反应方程式为
(3) CO2 , CO2(g) +2H2(g)
时 将体积比为 的 和 混合气体充入恒容密闭
HCHO(g)+H2O(g)。 T1℃ , 1∶2 CO2 H2
容器中 每隔一定时间测得容器内气体压强如下表所示 请回答下列问题
, , :
时间
/min 0 10 20 30 40 50 60
压强
/kPa 1.08 0.96 0.88 0.82 0.80 0.80 0.80
Δp B
已知 v ( ) 前 用 的压强变化表示该反应的平均反应速率为
① : p(B)= Δt 。 10 min, H2
-1
kPa·min ;
时 反应的平衡常数 -1 为用各气体分压表示的平衡常
②T1℃ , Kp= kPa (Kp
数 分压 总压 物质的量分数 结果保留三位有效数字
, = × ; )。
( 分)黄酮类天然产物具有独特的生物活性 一种具有抗炎活性的高异黄酮类似物
18. 14 , Ⅶ
的合成路线如下
:
化合物 的名称是
(1) Ⅰ 。
鉴别化合物 和 的化学方法
(2) Ⅰ Ⅱ 。
反应 的类型是 反应 为还原反应 化合物 的结构简式为
(3) ⑤ ; ② , Ⅲ ;
由化合物 合成 的反应条件是 填选项字母
Ⅱ Ⅲ ( )。
+
A. NaOH B. HCl C. O2 D. H /H2
写出反应 的反应方程式
(4) ④ 。
化合物 中含氧官能团名称 任写两种
(5) Ⅶ ( )。
化合物 的芳香族同分异构体中 写出两种同时满足如下条件的同分异构体的结构
(6) Ⅱ ,
简式
、 。
条件 遇 溶液显色 不能与 溶液反应 与稀硫酸反应后得到的
:① FeCl3 ;② NaHCO3 ;③
芳香族产物仅有一种含氧官能团 核磁共振氢谱有 组峰面积之比为 的
;④ 4 3∶2∶2∶1
吸收峰
。
利用反应 类似的反应 写出由 及乙醇为原料合成
(7) ⑤ , HOCH2(CH2)4CH2OH
的路线 不需注明反应条件
( )。
年邵阳市高三第一次联考试题卷(化学) 第 页(共 页)
2023 6 62023 年邵阳市高三第一次联考参考答案与评分标准
化 学
一、选择题:本题共 小题,每小题 分,共 分。
10 3 30
题 号
1 2 3 4 5 6 7 8 9 10
答 案
B D B A B C D C A C
二、选择题:本题共 小题,每小题 分,共 分。
4 4 16
题 号
11 12 13 14
答 案
A AC C AC
三、非选择题:本题共 小题,共 分。
4 54
分
15.(14 )
点燃
分
(1)S+2KNO3+3CK2S+N2↑+3CO2↑(2 )
含硫矿物的冶炼 硫酸工业的生产 或其它合理答案 分
(2) 、 ( )(1 )
2+ 2- 分
(3)①Ca +CO3 CaCO3↓(2 )
漏斗 分
② (1 )
蒸发浓缩 冷却结晶 分
③ 、 (1 )
分
(4)①NO(2 )
球形冷凝管 分 如果用酒精灯直接加热 由于混合液沸点较高 可能引发爆炸
② (1 ) , ,
分 冰水冷却 过滤 分
(2 ) , (2 )
分
16.(13 )
分 2 2 6 2 6 6 2 或 6 2 分
(1)V(1 ) 1s 2s 2p 3s 3p 3d 4s [Ar]3d 4s (1 )
3+ 2+ 分
(2)FeS+2Fe 3Fe +S(2 )
3 杂化 分
(3)sp (1 )
由于 3+存在水解平衡 3+ + 加入 发生反应
(4) Al :Al +3H2O Al(OH)3+3H , FeO FeO+
+ 2+ 使得c + 减小 水解正向移动生成 沉淀 分
2H Fe +H2O, (H ) , Al(OH)3 (2 )
-17 分
(5)1.3×10 (2 )
高温
水后面可不打气体符号
(6)2FePO4+Li2CO3+H2C2O4 2LiFePO4+H2O↑+3CO2↑( )
分
(2 )
30 32
4×158×10 或6.32×10 分
(7) (2 )
2 2
a bNA a bNA
分
17.(13 )
分
(1)ΔH=-90.6 kJ/mol(1 )
分 分 分
①L4(1 ) ②B(1 ) ③P3>P2>P1(1 )
反应 是放热反应 反应 是吸热反应 温度高于 之后 反应转化率主要由反
ⅰ , ⅱ , 570℃ ,
应 决定 分
ⅱ (2 )
+ - + 分 分
(2)NO+6H +5e NH4 +H2O(2 ) H2SO4(1 )
年邵阳市高三第一次联考参考答案与评分标准(化学) 第 页(共 页)
2023 1 2分 分
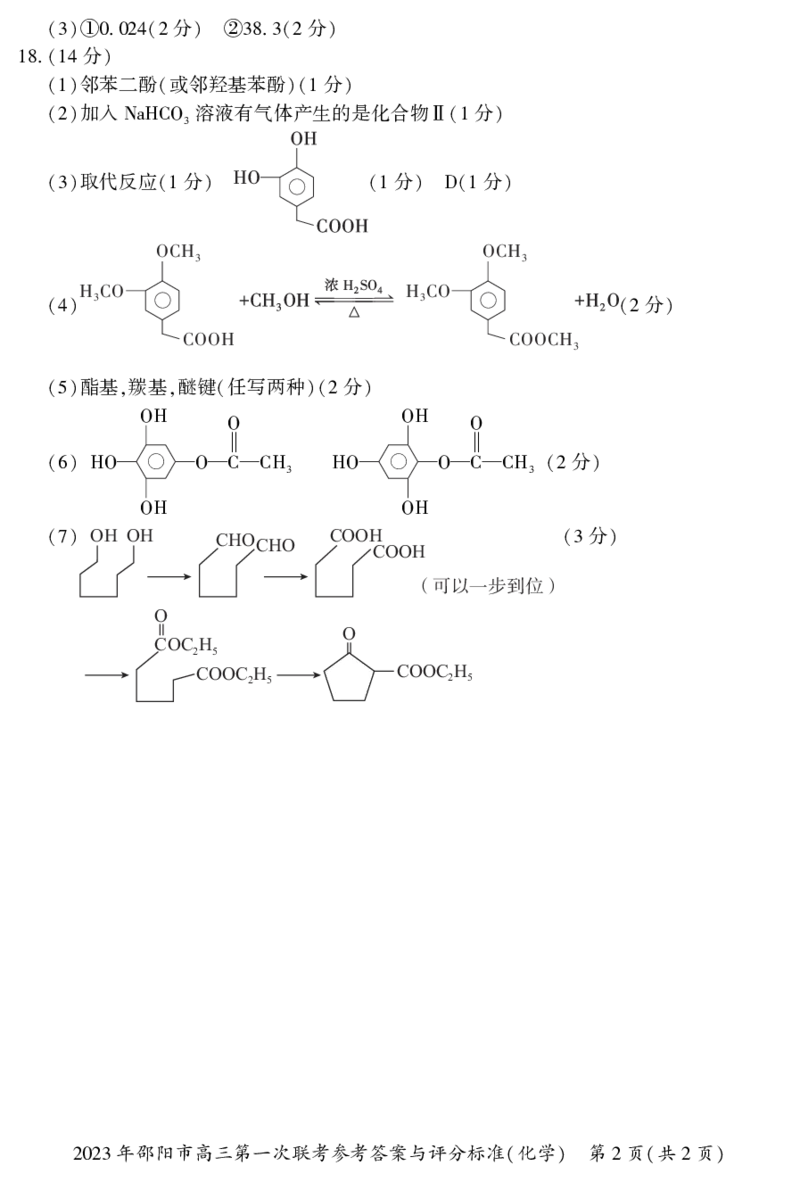
(3)①0.024(2 ) ②38.3(2 )
分
18.(14 )
邻苯二酚 或邻羟基苯酚 分
(1) ( )(1 )
加入 溶液有气体产生的是化合物 分
(2) NaHCO3 Ⅱ(1 )
取代反应 分 分 分
(3) (1 ) (1 ) D(1 )
0$) 0$)
) $0 ) $0
分
(4) (2 )
$00) $00$)
酯基 羰基 醚键 任写两种 分
(5) , , ( )(2 )
OH
O
(6) HO O C
OH
年邵阳市高三第一次联考参考答案与评分标准(化学) 第 页(共 页)
2023 2 2
OH
O
CH3 HO O C
OH
分
CH3 (2 )
OH OH CHO COOH 分
CHO
(7) COOH (3 )
U U
O
O
COCH
2 5
COOCH COOCH
2 5 2 5