文档内容
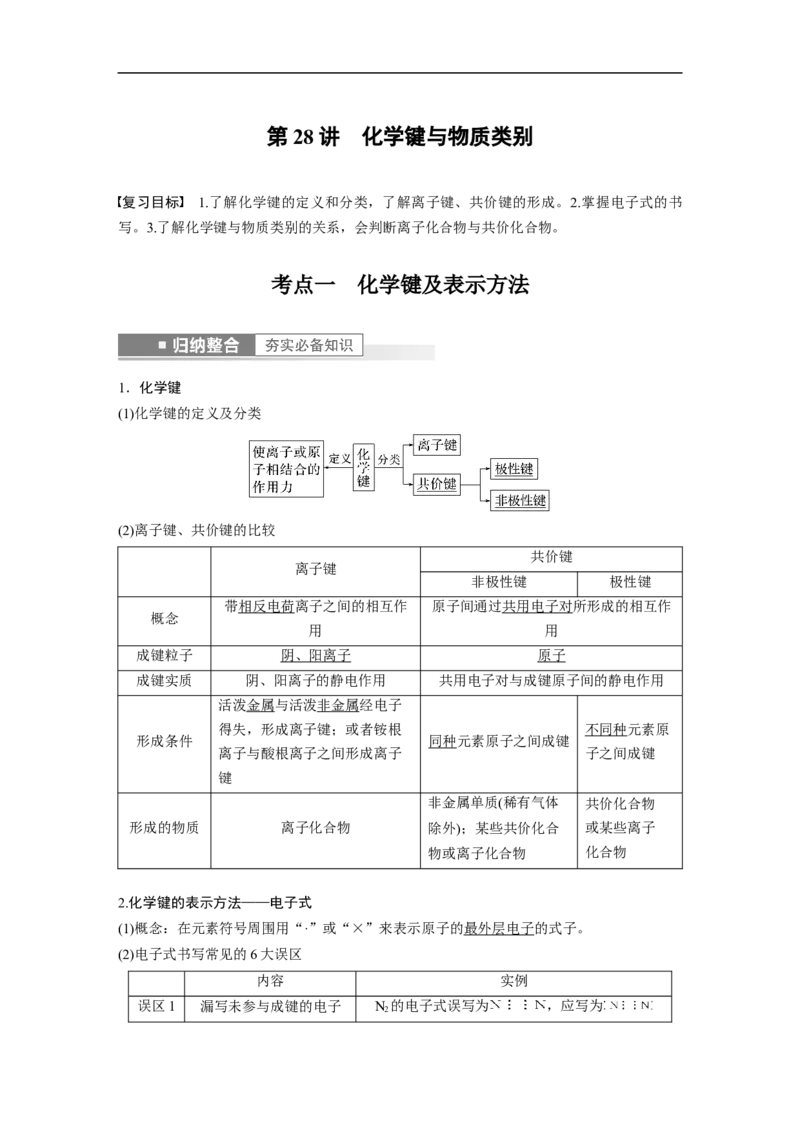
第 28 讲 化学键与物质类别
复习目标 1.了解化学键的定义和分类,了解离子键、共价键的形成。2.掌握电子式的书
写。3.了解化学键与物质类别的关系,会判断离子化合物与共价化合物。
考点一 化学键及表示方法
1.化学键
(1)化学键的定义及分类
(2)离子键、共价键的比较
共价键
离子键
非极性键 极性键
带相反电荷离子之间的相互作 原子间通过共用电子对所形成的相互作
概念
用 用
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子的静电作用 共用电子对与成键原子间的静电作用
活泼金属与活泼非金属经电子
得失,形成离子键;或者铵根 不同种元素原
形成条件 同种元素原子之间成键
离子与酸根离子之间形成离子 子之间成键
键
非金属单质(稀有气体 共价化合物
形成的物质 离子化合物 除外);某些共价化合 或某些离子
物或离子化合物 化合物
2.化学键的表示方法——电子式
(1)概念:在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
(2)电子式书写常见的6大误区
内容 实例
误区1 漏写未参与成键的电子 N 的电子式误写为 ,应写为
2NaCl误写为 ,应写为
化合物类型不清楚,漏写
误区2
或多写[ ]及错写电荷数 ;HF误写为
,应写为
书写不规范,错写共用电 N 的电子式误写为 或 或
2
误区3
子对
HClO的电子式误写为
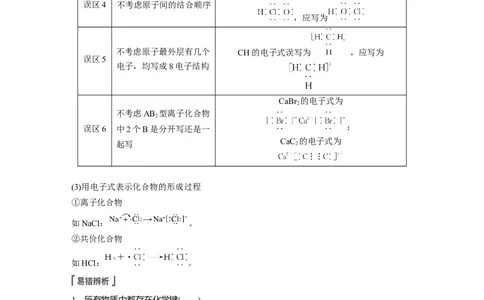
误区4 不考虑原子间的结合顺序
,应写为
不考虑原子最外层有几个 CH的电子式误写为 ,应写为
误区5
电子,均写成8电子结构
CaBr 的电子式为
2
不考虑AB 型离子化合物
2
误区6 中2个B是分开写还是一 ;
起写 CaC 2 的电子式为
(3)用电子式表示化合物的形成过程
①离子化合物
如NaCl: 。
②共价化合物
如HCl: 。
1.所有物质中都存在化学键( )
2.化学键是相邻离子或原子间的一种强作用力,既包括静电吸引力,又包括静电排斥力(
)
3.非金属元素的两个原子之间一定形成共价键,但多个原子间也可能形成离子键( )
4.AsH 的电子式: ( )
3
5.某元素的原子最外层只有一个电子,它跟卤素原子结合时,所形成的化学键一定是离子
键( )
6.某些金属与非金属原子间能形成共价键( )答案 1.× 2.√ 3.√ 4.× 5.× 6.√
一、电子式的书写
1.(1)—OH______________,OH-______________,
HO+______________,NH______________,
3
(2)HClO______________,CCl ______________,
4
CO______________,NH______________,
2 2 4
(3)Na S______________,NaH______________,
2
NaBH ______________,NaO______________。
4 2 2
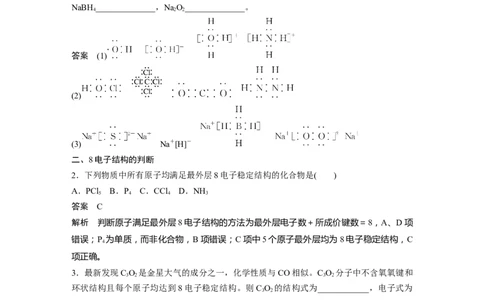
答案 (1)
(2)
(3) Na+[H]-
二、8电子结构的判断
2.下列物质中所有原子均满足最外层8电子稳定结构的化合物是( )
A.PCl B.P C.CCl D.NH
5 4 4 3
答案 C
解析 判断原子满足最外层8电子结构的方法为最外层电子数+所成价键数=8,A、D项
错误;P 为单质,而非化合物,B项错误;C项中5个原子最外层均为8电子稳定结构,C
4
项正确。
3.最新发现C O 是金星大气的成分之一,化学性质与CO相似。C O 分子中不含氧氧键和
3 2 3 2
环状结构且每个原子均达到8电子稳定结构。则C O 的结构式为____________,电子式为
3 2
______________。
答案 O==C==C==C==O
判断分子中各原子是否达到8电子稳定结构的方法
首先,原子序数小于或等于5的元素的原子不能形成8电子稳定结构,然后再根据以下方法
进行判断:
(1)经验规律法凡符合最外层电子数+|化合价|=8的皆为8电子结构。
(2)试写结构法
判断某化合物中的某元素最外层是否达到8电子稳定结构,应从其结构式或电子式结合原子
最外层电子数进行判断。若原子形成的共价键的条数为8-最外层电子数,则该原子即为8
电子稳定结构。
考点二 化学键与物质类别
1.离子化合物与共价化合物
项目 离子化合物 共价化合物
定义 含有离子键的化合物 只含有共价键的化合物
构成微粒 阴、阳离子 原子
化学键类型 一定含有离子键,可能含有共价键 只含有共价键
①含氧酸
①强碱 ②弱碱
②绝大多数盐 ③非金属气态氢化物
物质类别
③金属氧化物 ④非金属氧化物
个例:NaH、CaC 、MgN ⑤极少数盐,如AlCl
2 3 2 3
⑥多数有机物
2.化学键与物质类别的关系
1.氢与硫、氯、钾3种元素均能形成共价化合物( )
2.N和P不能存在于同一离子化合物中( )
3.只含共价键的物质一定是共价化合物( )
4.非极性键只存在于双原子的单质分子中( )
5.非金属元素的原子之间一定形成共价键( )6.含有共价键的化合物一定是共价化合物( )
答案 1.× 2.× 3.× 4.× 5.× 6.×
1.有以下 8 种物质:① Ne ② HCl ③ P ④ HO ⑤ NaS ⑥ NaOH ⑦ NaO
4 2 2 2 2 2
⑧NH Cl
4
(1)不存在化学键的是______(填序号,下同)。
(2)只存在极性共价键的是______。
(3)只存在非极性共价键的是______。
(4)既存在非极性共价键又存在极性共价键的是______。
(5)只存在离子键的是______。
(6)既存在离子键又存在共价键的是______。
答案 (1)① (2)② (3)③ (4)④ (5)⑤ (6)⑥⑦⑧
2.现有下列物质:① NaCl ② NaO ③ NaO ④ NaOH ⑤ AlCl ⑥ HO ⑦ N
2 2 2 3 2 2
⑧NH Cl ⑨CO ○HO
4 2 2 2
(1)只含离子键的物质有________(填序号,下同),只含共价键的物质有__________。
(2)属于离子化合物的有__________,其中含非极性键的离子化合物有__________,含有非
极性键的共价化合物有__________。
答案 (1)①② ⑤⑥⑦⑨○ (2)①②③④⑧ ③ ○
判断离子化合物和共价化合物的三种方法
1.判断正误(正确的打“√”,错误的打“×”)
(1)钠与N、O、Cl分别形成的化合物中只含有离子键(2018·全国卷Ⅱ,10B改编)( × )
(2)1 mol乙烷和1 mol乙烯中,化学键数相同(2018·全国卷Ⅲ,8D)( × )(3)Na O 与ClO 均含有非极性共价键(2018·全国卷Ⅲ,13C改编)( × )
2 2 2
(4)氢元素与其他元素可形成共价化合物或离子化合物(2017·天津,5B)( √ )
(5)甲基的电子式: (2020·浙江7月选考,5D)( √ )
2.下列有关电子式表示正确的是( )
①次氯酸的电子式:
(2019·浙江4月选考,7A)
②甲醛的电子式: (2021·浙江1月选考,5D改编)
③HCl的电子式: (2018·江苏,2B)
④由Na和Cl形成离子键的过程: (2018·北京,8C)
A.①③ B.①④
C.②③ D.②④
答案 D
解析 HClO的电子式应为 ,①错误;HCl的电子式为 ,③错误;Na和Cl
形成离子键时,Na失去1个电子,Cl得到1个电子,且NaCl中存在离子键,④正确。
3.(2019·江苏,2)反应NH Cl+NaNO ===NaCl+N↑+2HO放热且产生气体,可用于冬天
4 2 2 2
石油开采。下列表示反应中相关微粒的化学用语正确的是( )
A.中子数为18的氯原子:Cl
B.N 的结构式:N==N
2
C.Na+的结构示意图:
D.HO的电子式:
2
答案 D
解析 A项,中子数为18的氯原子应表示为Cl,错误;B项,N 分子中N与N之间形成三
2
键,结构式为N≡N,错误;C项,Na+的结构示意图为 ,错误;D项,HO为共价
2
化合物,每个H原子和O原子之间共用一个电子对,正确。
4.(2021·浙江1月选考,1)下列含有共价键的盐是( )
A.CaCl B.HSO
2 2 4C.Ba(OH) D.NaCO
2 2 3
答案 D
解析 CaCl 只含有离子键,不含有共价键,故A错误;HSO 中只含有共价键,属于酸,
2 2 4
不是盐,B错误;Ba(OH) 既含有离子键又含有共价键,属于碱,不是盐,C错误;NaCO
2 2 3
中既含有离子键又含有共价键而且属于盐,D正确。
5.(1)[2020·浙江7月选考,26(2)]CaCN 是离子化合物,各原子均满足8电子稳定结构,
2
CaCN 的电子式是________。
2
(2)[2021·天津,16(1)节选]CH 的电子式为__________________________________________。
4
(3)[2018·海南,13(3)]CO 的电子式为____________。
2
(4)[2017·海南,13(1)]PH 的电子式为_____________________________________________。
3
(5)[2016·全国卷Ⅱ,26(1)节选]联氨(N H)分子的电子式为__________________。
2 4
答案 (1) (2)
(3) (4)
(5)
课时精练
1.在NH 和NH Cl存在的条件下,以活性炭为催化剂,用HO 氧化CoCl 溶液来制备化工
3 4 2 2 2
产品[Co(NH )]Cl ,下列表述正确的是( )
3 6 3
A.中子数为32,质子数为27的钴原子:Co
B.HO 的电子式:
2 2
C.NH 和NH Cl化学键类型相同
3 4
D.[Co(NH )]Cl 中Co的化合价是+3
3 6 3
答案 D
解析 A项,中子数为32,质子数为27的元素,质量数为27+32=59,表示为Co,错误;
B项,HO 为共价化合物,电子式为 ,错误;C项,NH 中只存在共价键,
2 2 3
NH Cl中既存在离子键又存在共价键,二者化学键类型不同,错误;D项,[Co(NH )]Cl 中,
4 3 6 3
NH 整体为0价,Cl为-1价,所以Co的化合价为+3,正确。
3
2.下列关于C 、H、O、N等微粒的叙述错误的是( )
60 3A.碳、氢、氧、氮元素中各含有不同核素
B.H 与H 化学性质相同,互为同位素
3 2
C.C 与N中都含有共价键
60
D.KO 属于含有共价键的离子化合物
2
答案 B
3.下列关于化学键和化合物的说法正确的是( )
A.NaO、NaOH、CaCl 三种化合物含有相同的化学键
2 2 2
B.金属元素和非金属元素形成的化合物一定是离子化合物
C.非金属元素组成的化合物一定是共价化合物
D.HCl、HS溶于水时只破坏了共价键
2
答案 D
4.科学家研制了有望成为高效火箭推进剂的N(NO) ,下列有关N(NO) 分子的说法正确的
2 3 2 3
是( )
A.该物质是只含共价键的共价化合物
B.该物质中既含共价键也含离子键
C.该物质是离子化合物
D.该物质的组成微粒是阴、阳离子
答案 A
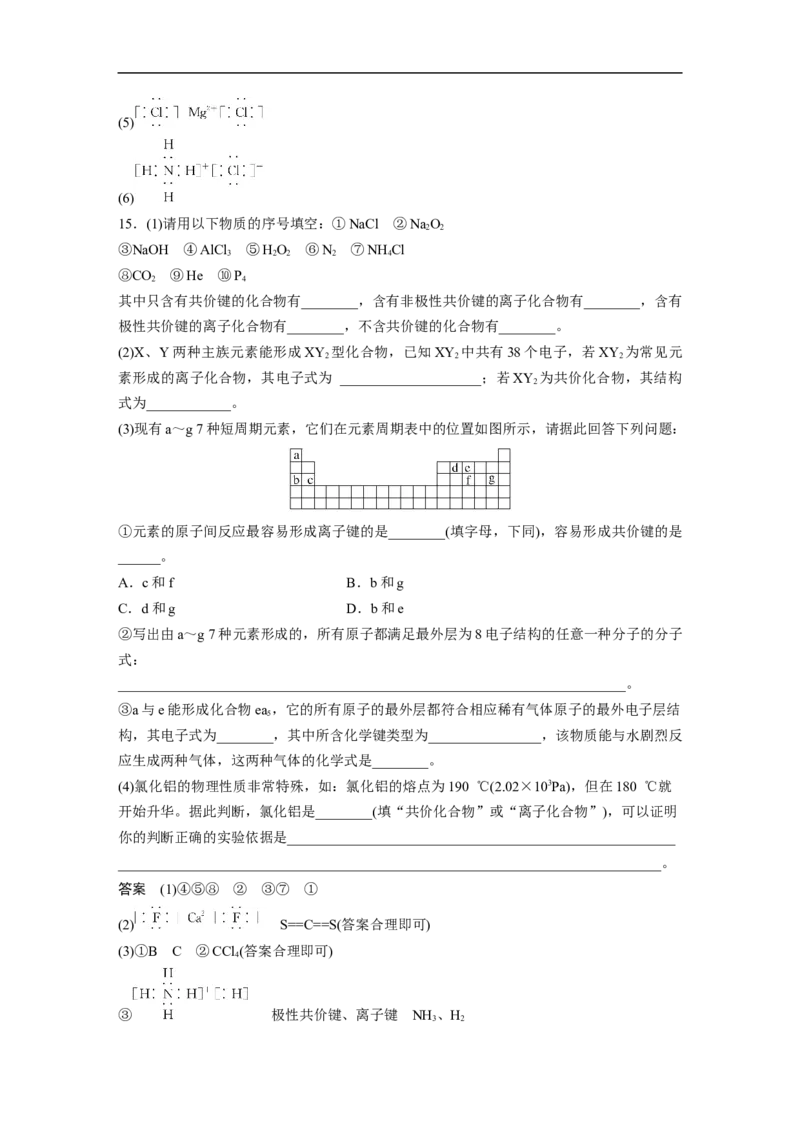
5.X、Y、Z、W均为常见的短周期主族元素,常温下,其最高价氧化物对应的水化物溶液
(浓度均为 0.01 mol·L-1)的pH和原子半径的关系如下图所示。其中,Y为碳元素。下列有
关说法正确的是( )
A.X是硫元素
B.Y的最高价氧化物的电子式为
C.W的最高价氧化物对应的水化物中仅含离子键
D.Z的最高价氧化物对应水化物的化学式为HClO
4
答案 D
解析 X、Z对应的pH为2,高氯酸、硝酸均为一元强酸,原子半径:Z>Y>X,Y为C,则
Z为Cl,X为N,W对应的pH为12,氢氧化钠为一元强碱,则W为Na,以此来解答。
6.下列各组中每种物质都既有离子键又有共价键的是( )
A.NaOH HSO (NH )SO
2 4 4 2 4B.MgO NaSO HNO
2 4 3
C.NaO KOH NaPO
2 2 3 4
D.HCl Al O MgCl
2 3 2
答案 C
解析 HSO 中只含共价键,A错误;MgO中只含离子键,HNO 中只含共价键,B错误。
2 4 3
7.下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.NH NO 晶体中含共价键,是共价化合物
4 3
C.HO、NH 分子中只含有极性共价键
2 2 2 4
D.某化合物熔融状态能导电,可以证明该化合物内一定存在离子键
答案 D
解析 离子键是阴、阳离子间的静电作用,包括引力和斥力,故 A错误;硝酸铵是离子化
合物,含有离子键和共价键,故B错误;HO 的结构式为H—O—O—H,含有极性共价键
2 2
和非极性共价键,NH 中也是含有极性共价键和非极性共价键,故 C错误;离子化合物在
2 4
熔融状态下导电,共价化合物在熔融状态下不导电,故D正确。
8.下列说法错误的是( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中含有的共价键一定是非极性共价键
答案 A
解析 只含有共价键的化合物是共价化合物,离子化合物中也可能含有共价键,如氯化铵,
故A错误,B正确;含有离子键的化合物就是离子化合物,在离子化合物中可以含有共价键,
但共价化合物中不能含有离子键,故C正确;由同一种元素的原子形成的共价键是非极性
共价键,故D正确。
9.全氮类物质具有高密度、超高能量及爆炸产物无污染等优点。中国科学家成功合成全氮
阴离子N,N是制备全氮类物质NN的重要中间体,下列说法不正确的是( )
A.全氮类物质属于绿色能源
B.每个N中含有35个质子
C.每个N中含有35个电子
D.NN结构中含共价键
答案 C
解析 N的质子数为7×5=35,B正确;N含有的电子数为5×7+1=36,C错误;N、N
中均含有5个氮原子,氮原子间以共价键结合,D正确。
10.下列各组物质中化学键的类型完全相同的是( )A.NaCl、MgCl 、NaO B.HO、NaO、SO
2 2 2 2 2 2
C.CaCl 、NaOH、HSO D.NH Cl、NH 、CO
2 2 4 4 3 2
答案 A
解析 NaCl、MgCl 和NaO中均只含离子键,A项正确;NaO 含离子键和共价键,HO和
2 2 2 2 2
SO 只含共价键,B项错误;CaCl 只含离子键,NaOH含离子键和共价键,HSO 只含共价
2 2 2 4
键,C项错误;NH Cl含离子键和共价键,NH 和CO 只含共价键,D项错误。
4 3 2
11.下列反应中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A.NH HCO =====NH ↑+CO↑+HO
4 3 3 2 2
B.NH +HCl===NH Cl
3 4
C.2KOH+Cl===KCl+KClO+HO
2 2
D.2KO+2CO===2KCO+O
2 2 2 2 3 2
答案 D
12.下列分子中所有原子都满足最外层8电子稳定结构的是( )
A.六氟化氙(XeF ) B.次氯酸(HClO)
6
C.二氧化碳(CO) D.三氟化硼(BF)
2 3
答案 C
解析 XeF 中Xe不是8电子稳定结构,A错误;HClO中氢原子为2电子结构,B错误;
6
CO 中所有原子都满足最外层8电子稳定结构,C正确;BF 中硼原子不是8电子稳定结构,
2 3
D错误。
13.一定条件下,氨与氟气发生反应:4NH +3F===NF +3NH F,其中NF 立体构型与
3 2 3 4 3
NH 相似。下列有关说法错误的是( )
3
A.除F 单质外,反应物和生成物均为共价化合物
2
B.NF 中各原子均满足8电子稳定结构
3
C.NF 中只含极性共价键
3
D.NH F中既含有离子键又含有共价键
4
答案 A
解析 NF 为共价化合物,NH F为离子化合物。
3 4
14.写出下列物质的电子式。
(1)NaH:______________;(2)NaCN:________________;
(3)NaBH :____________;(4)H O:______________;
4 2 2
(5)MgCl :____________;(6)NH Cl:_____________。
2 4
答案 (1)Na+[ H]- (2)
(3) (4)(5)
(6)
15.(1)请用以下物质的序号填空:①NaCl ②NaO
2 2
③NaOH ④AlCl ⑤HO ⑥N ⑦NH Cl
3 2 2 2 4
⑧CO ⑨He ⑩P
2 4
其中只含有共价键的化合物有________,含有非极性共价键的离子化合物有________,含有
极性共价键的离子化合物有________,不含共价键的化合物有________。
(2)X、Y两种主族元素能形成XY 型化合物,已知XY 中共有38个电子,若XY 为常见元
2 2 2
素形成的离子化合物,其电子式为 ____________________;若XY 为共价化合物,其结构
2
式为____________。
(3)现有a~g 7种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
①元素的原子间反应最容易形成离子键的是________(填字母,下同),容易形成共价键的是
______。
A.c和f B.b和g
C.d和g D.b和e
②写出由a~g 7种元素形成的,所有原子都满足最外层为8电子结构的任意一种分子的分子
式:
________________________________________________________________________。
③a与e能形成化合物ea,它的所有原子的最外层都符合相应稀有气体原子的最外电子层结
5
构,其电子式为________,其中所含化学键类型为________________,该物质能与水剧烈反
应生成两种气体,这两种气体的化学式是________。
(4)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190 ℃(2.02×103Pa),但在180 ℃就
开始升华。据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明
你的判断正确的实验依据是_______________________________________________________
_____________________________________________________________________________。
答案 (1)④⑤⑧ ② ③⑦ ①
(2) S==C==S(答案合理即可)
(3)①B C ②CCl (答案合理即可)
4
③ 极性共价键、离子键 NH 、H
3 2(4)共价化合物 氯化铝在熔融状态下不导电