文档内容
重点题空热练(二) 综合实验中特殊装置的作用集训
1.过氧化钙(CaO)是水产养殖中广泛使用的一种化学试剂。CaO 微溶于水,可与水缓慢反
2 2
应。实验室用如下方法制备CaO 并测定其纯度。
2
Ⅰ.过氧化钙的制备
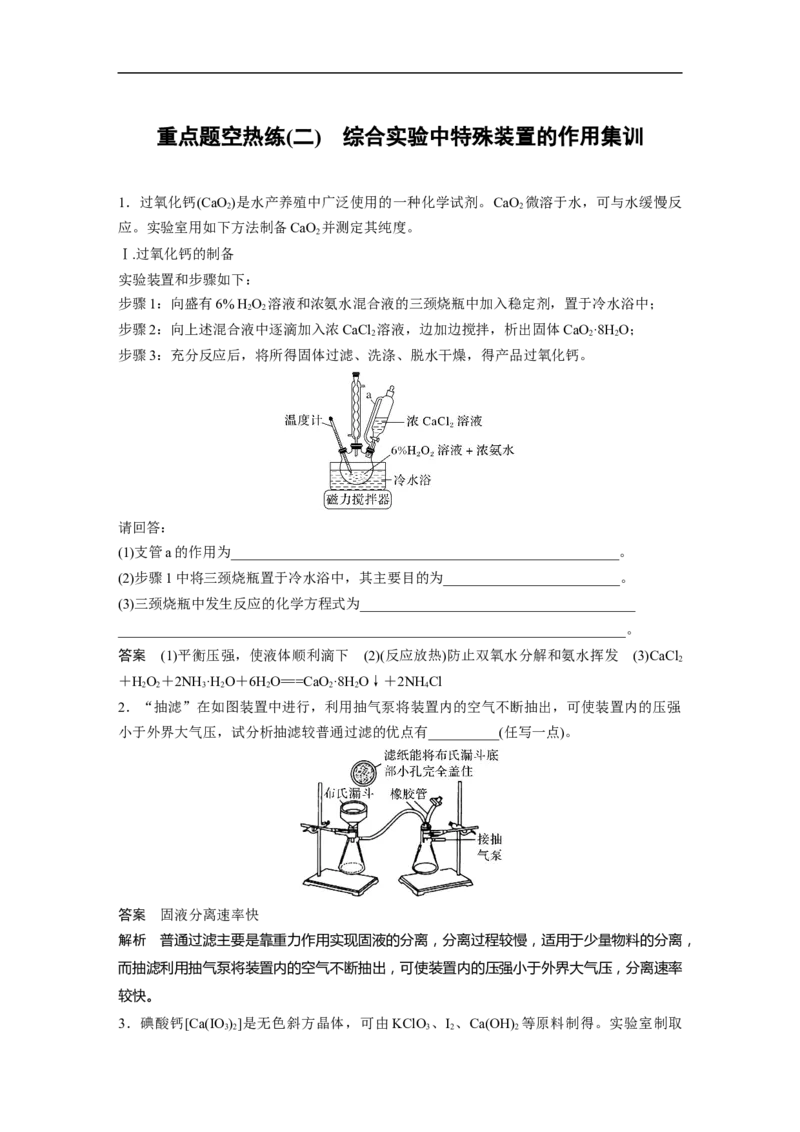
实验装置和步骤如下:
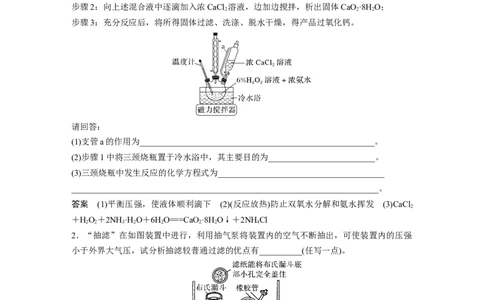
步骤1:向盛有6% H O 溶液和浓氨水混合液的三颈烧瓶中加入稳定剂,置于冷水浴中;
2 2
步骤2:向上述混合液中逐滴加入浓CaCl 溶液,边加边搅拌,析出固体CaO·8H O;
2 2 2
步骤3:充分反应后,将所得固体过滤、洗涤、脱水干燥,得产品过氧化钙。
请回答:
(1)支管a的作用为_______________________________________________________。
(2)步骤1中将三颈烧瓶置于冷水浴中,其主要目的为_________________________。
(3)三颈烧瓶中发生反应的化学方程式为_______________________________________
________________________________________________________________________。
答案 (1)平衡压强,使液体顺利滴下 (2)(反应放热)防止双氧水分解和氨水挥发 (3)CaCl
2
+HO+2NH ·H O+6HO===CaO·8H O↓+2NH Cl
2 2 3 2 2 2 2 4
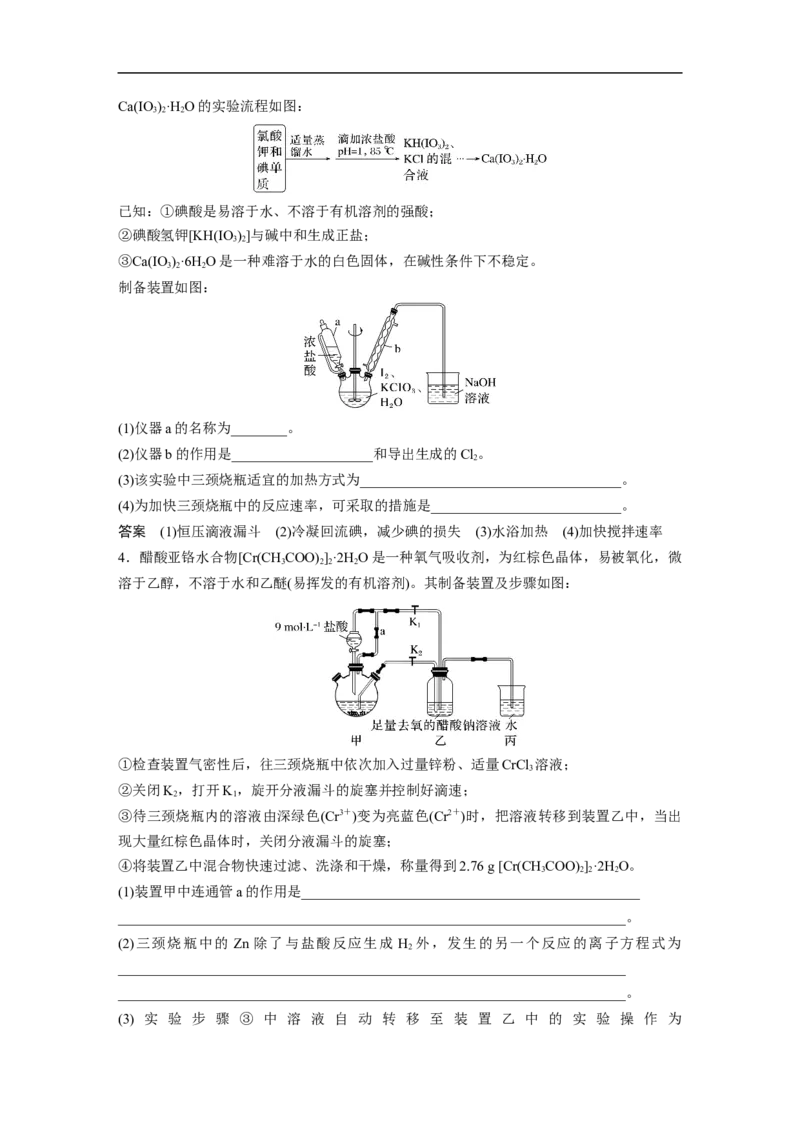
2.“抽滤”在如图装置中进行,利用抽气泵将装置内的空气不断抽出,可使装置内的压强
小于外界大气压,试分析抽滤较普通过滤的优点有__________(任写一点)。
答案 固液分离速率快
解析 普通过滤主要是靠重力作用实现固液的分离,分离过程较慢,适用于少量物料的分离,
而抽滤利用抽气泵将装置内的空气不断抽出,可使装置内的压强小于外界大气压,分离速率
较快。
3.碘酸钙[Ca(IO)]是无色斜方晶体,可由KClO 、I 、Ca(OH) 等原料制得。实验室制取
3 2 3 2 2Ca(IO)·H O的实验流程如图:
3 2 2
已知:①碘酸是易溶于水、不溶于有机溶剂的强酸;
②碘酸氢钾[KH(IO)]与碱中和生成正盐;
3 2
③Ca(IO)·6H O是一种难溶于水的白色固体,在碱性条件下不稳定。
3 2 2
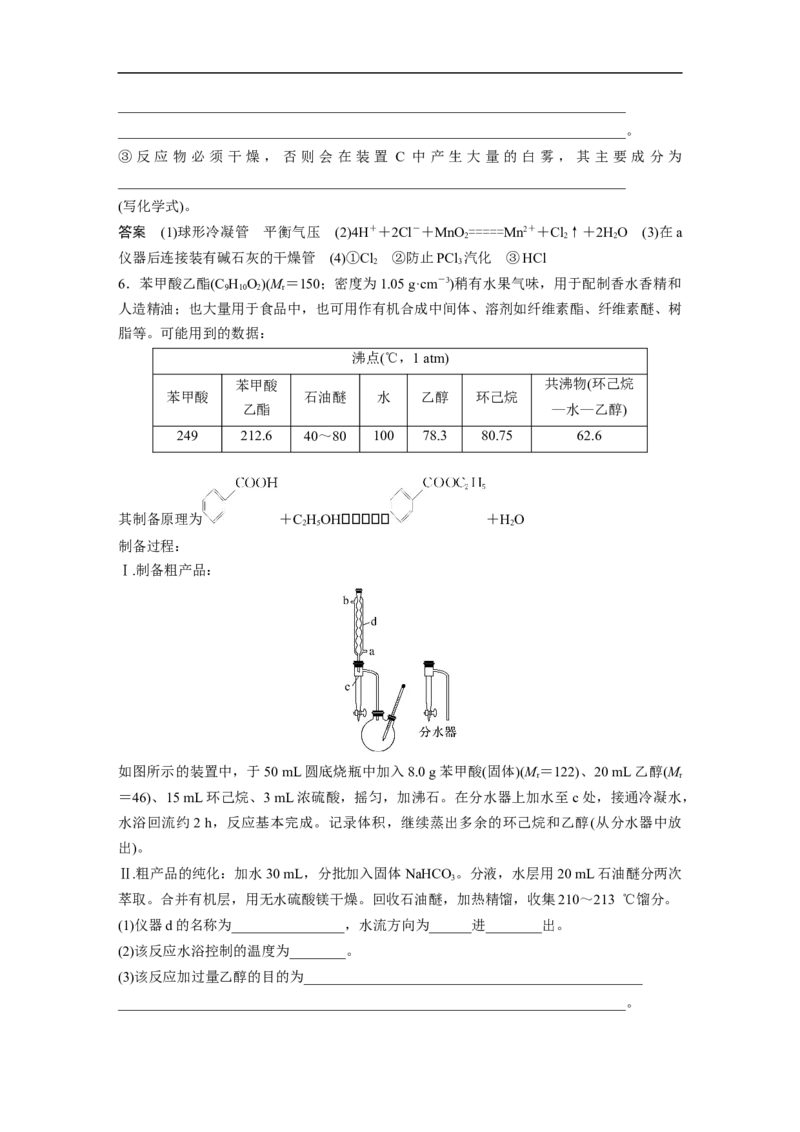
制备装置如图:
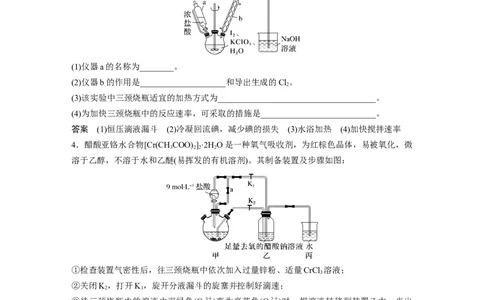
(1)仪器a的名称为________。
(2)仪器b的作用是____________________和导出生成的Cl。
2
(3)该实验中三颈烧瓶适宜的加热方式为_____________________________________。
(4)为加快三颈烧瓶中的反应速率,可采取的措施是___________________________。
答案 (1)恒压滴液漏斗 (2)冷凝回流碘,减少碘的损失 (3)水浴加热 (4)加快搅拌速率
4.醋酸亚铬水合物[Cr(CH COO) ]·2H O是一种氧气吸收剂,为红棕色晶体,易被氧化,微
3 2 2 2
溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如图:
①检查装置气密性后,往三颈烧瓶中依次加入过量锌粉、适量CrCl 溶液;
3
②关闭K,打开K,旋开分液漏斗的旋塞并控制好滴速;
2 1
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,把溶液转移到装置乙中,当出
现大量红棕色晶体时,关闭分液漏斗的旋塞;
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到2.76 g [Cr(CH COO) ]·2H O。
3 2 2 2
(1)装置甲中连通管a的作用是________________________________________________
________________________________________________________________________。
(2)三颈烧瓶中的 Zn 除了与盐酸反应生成 H 外,发生的另一个反应的离子方程式为
2
________________________________________________________________________
________________________________________________________________________。
(3) 实 验 步 骤 ③ 中 溶 液 自 动 转 移 至 装 置 乙 中 的 实 验 操 作 为________________________________________________________________________。
(4)装置丙中导管口水封的目的是____________________________________________。
(5)洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是
______________(填字母)。
a.乙醚 b.去氧冷的蒸馏水 c.无水乙醇
答案 (1)平衡压强,保证分液漏斗中的液体顺利流下
(2)2Cr3++Zn===2Cr2++Zn2+
(3)关闭K,打开K
1 2
(4)防止空气进入装置乙氧化二价铬
(5)bca
5.三氯氧磷(POCl )是一种重要的化工原料,工业上可以直接氧化PCl 制备POCl ,反应原
3 3 3
理为:
P(白磷)+6Cl===4PCl ,2PCl +O===2POCl 。
4 2 3 3 2 3
PCl 、POCl 的部分性质如下:
3 3
物质 熔点/℃ 沸点/℃ 其他
遇水生成
PCl -112 75.5
3
HPO 和HCl
3 3
遇水生成
POCl 2 105.3
3
HPO 和HCl
3 4
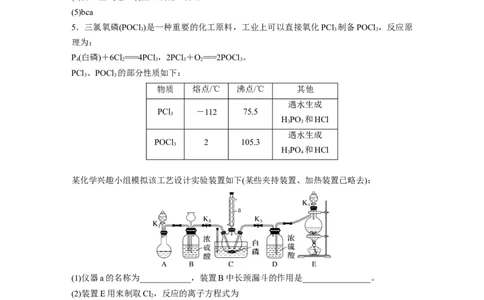
某化学兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):
(1)仪器a的名称为____________,装置B中长颈漏斗的作用是________________。
(2)装置E用来制取Cl,反应的离子方程式为
2
________________________________________________________________________
________________________________________________________________________。
(3)为使实验顺利进行,还需补充的装置为
________________________________________________________________________。
(4)反应时,需严格控制三个条件:
①先制取________,缓慢地通入装置C中,直至装置C中的白磷消失后,再通入另一种气
体。
②C 装置用水浴加热控制温度为 60~65 ℃,除加快反应速率外,另一目的是________________________________________________________________________
________________________________________________________________________。
③ 反 应 物 必 须 干 燥 , 否 则 会 在 装 置 C 中 产 生 大 量 的 白 雾 , 其 主 要 成 分 为
________________________________________________________________________
(写化学式)。
答案 (1)球形冷凝管 平衡气压 (2)4H++2Cl-+MnO =====Mn2++Cl↑+2HO (3)在a
2 2 2
仪器后连接装有碱石灰的干燥管 (4)①Cl ②防止PCl 汽化 ③HCl
2 3
6.苯甲酸乙酯(C H O)(M=150;密度为1.05 g·cm-3)稍有水果气味,用于配制香水香精和
9 10 2 r
人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树
脂等。可能用到的数据:
沸点(℃,1 atm)
苯甲酸 共沸物(环己烷
苯甲酸 石油醚 水 乙醇 环己烷
乙酯 —水—乙醇)
249 212.6 40~80 100 78.3 80.75 62.6
其制备原理为 +C HOH +HO
2 5 2
制备过程:
Ⅰ.制备粗产品:
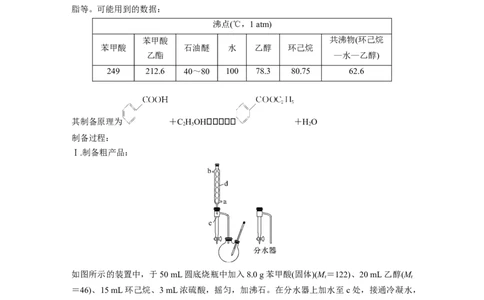
如图所示的装置中,于50 mL圆底烧瓶中加入8.0 g苯甲酸(固体)(M=122)、20 mL乙醇(M
r r
=46)、15 mL环己烷、3 mL浓硫酸,摇匀,加沸石。在分水器上加水至c处,接通冷凝水,
水浴回流约2 h,反应基本完成。记录体积,继续蒸出多余的环己烷和乙醇(从分水器中放
出)。
Ⅱ.粗产品的纯化:加水30 mL,分批加入固体NaHCO 。分液,水层用20 mL石油醚分两次
3
萃取。合并有机层,用无水硫酸镁干燥。回收石油醚,加热精馏,收集210~213 ℃馏分。
(1)仪器d的名称为________________,水流方向为______进________出。
(2)该反应水浴控制的温度为________。
(3)该反应加过量乙醇的目的为________________________________________________
________________________________________________________________________。(4)分水器的作用:__________________________________________________________
________________________________________________________________________,
分水器的检漏方法:________________________________________________________
________________________________________________________________________,
如何利用实验现象判断反应已基本完成:
________________________________________________________________________。
答案 (1)球形冷凝管 a b (2)略高于62.6 ℃
(3)乙醇相对廉价,增大反应物浓度,使平衡向正反应方向移动,提高苯甲酸的转化率,提
高产率;形成共沸物需要添加乙醇 (4)分离产生的水,使平衡向正反应方向移动,提高转
化率 关闭活塞,在分水器中加适量的水,观察是否漏水,若不漏水,旋转活塞180°,若
仍不漏水,说明分水器不漏水 加热回流至分水器中水位不再上升为止