文档内容
特色练 10 化学反应速率与化学平衡
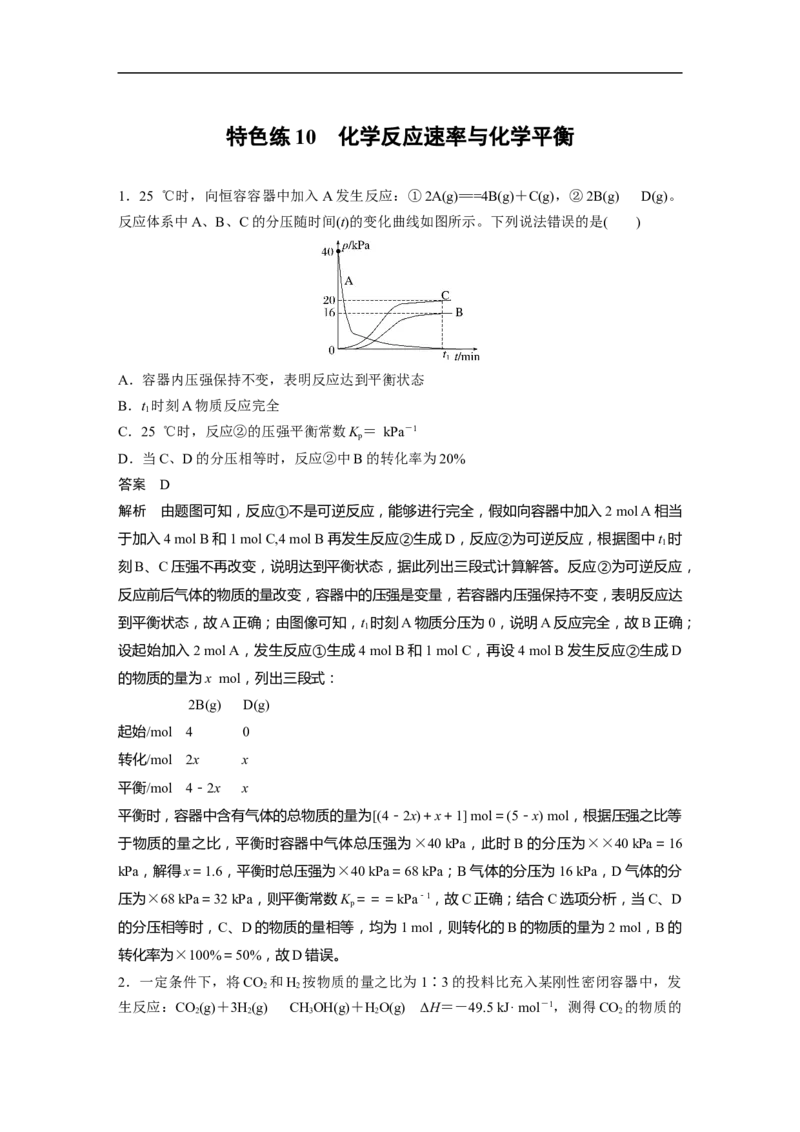
1.25 ℃时,向恒容容器中加入A发生反应:①2A(g)===4B(g)+C(g),②2B(g)D(g)。
反应体系中A、B、C的分压随时间(t)的变化曲线如图所示。下列说法错误的是( )
A.容器内压强保持不变,表明反应达到平衡状态
B.t 时刻A物质反应完全
1
C.25 ℃时,反应②的压强平衡常数K = kPa-1
p
D.当C、D的分压相等时,反应②中B的转化率为20%
答案 D
解析 由题图可知,反应①不是可逆反应,能够进行完全,假如向容器中加入2 mol A相当
于加入4 mol B和1 mol C,4 mol B再发生反应②生成D,反应②为可逆反应,根据图中t 时
1
刻B、C压强不再改变,说明达到平衡状态,据此列出三段式计算解答。反应②为可逆反应,
反应前后气体的物质的量改变,容器中的压强是变量,若容器内压强保持不变,表明反应达
到平衡状态,故A正确;由图像可知,t 时刻A物质分压为0,说明A反应完全,故B正确;
1
设起始加入2 mol A,发生反应①生成4 mol B和1 mol C,再设4 mol B发生反应②生成D
的物质的量为x mol,列出三段式:
2B(g)D(g)
起始/mol 4 0
转化/mol 2x x
平衡/mol 4-2x x
平衡时,容器中含有气体的总物质的量为[(4-2x)+x+1] mol=(5-x) mol,根据压强之比等
于物质的量之比,平衡时容器中气体总压强为×40 kPa,此时B的分压为××40 kPa=16
kPa,解得x=1.6,平衡时总压强为×40 kPa=68 kPa;B气体的分压为16 kPa,D气体的分
压为×68 kPa=32 kPa,则平衡常数K ===kPa-1,故C正确;结合C选项分析,当C、D
p
的分压相等时,C、D的物质的量相等,均为1 mol,则转化的B的物质的量为2 mol,B的
转化率为×100%=50%,故D错误。
2.一定条件下,将CO 和H 按物质的量之比为1∶3的投料比充入某刚性密闭容器中,发
2 2
生反应:CO(g)+3H(g)CHOH(g)+HO(g) ΔH=-49.5 kJ· mol-1,测得CO 的物质的
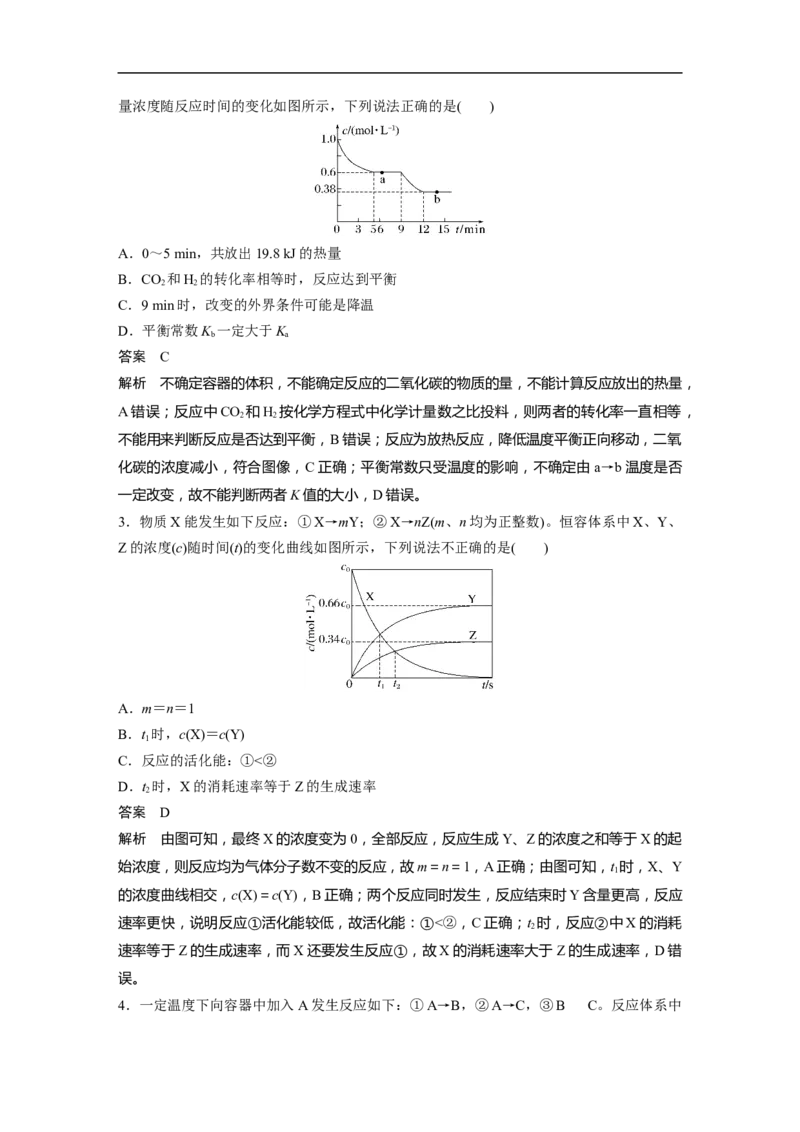
2 2 3 2 2量浓度随反应时间的变化如图所示,下列说法正确的是( )
A.0~5 min,共放出19.8 kJ的热量
B.CO 和H 的转化率相等时,反应达到平衡
2 2
C.9 min时,改变的外界条件可能是降温
D.平衡常数K 一定大于K
b a
答案 C
解析 不确定容器的体积,不能确定反应的二氧化碳的物质的量,不能计算反应放出的热量,
A错误;反应中CO 和H 按化学方程式中化学计量数之比投料,则两者的转化率一直相等,
2 2
不能用来判断反应是否达到平衡,B错误;反应为放热反应,降低温度平衡正向移动,二氧
化碳的浓度减小,符合图像,C正确;平衡常数只受温度的影响,不确定由a→b温度是否
一定改变,故不能判断两者K值的大小,D错误。
3.物质X能发生如下反应:①X→mY;②X→nZ(m、n均为正整数)。恒容体系中X、Y、
Z的浓度(c)随时间(t)的变化曲线如图所示,下列说法不正确的是( )
A.m=n=1
B.t 时,c(X)=c(Y)
1
C.反应的活化能:①<②
D.t 时,X的消耗速率等于Z的生成速率
2
答案 D
解析 由图可知,最终X的浓度变为0,全部反应,反应生成Y、Z的浓度之和等于X的起
始浓度,则反应均为气体分子数不变的反应,故m=n=1,A正确;由图可知,t 时,X、Y
1
的浓度曲线相交,c(X)=c(Y),B正确;两个反应同时发生,反应结束时Y含量更高,反应
速率更快,说明反应①活化能较低,故活化能:①<②,C正确;t 时,反应②中X的消耗
2
速率等于Z的生成速率,而X还要发生反应①,故X的消耗速率大于Z的生成速率,D错
误。
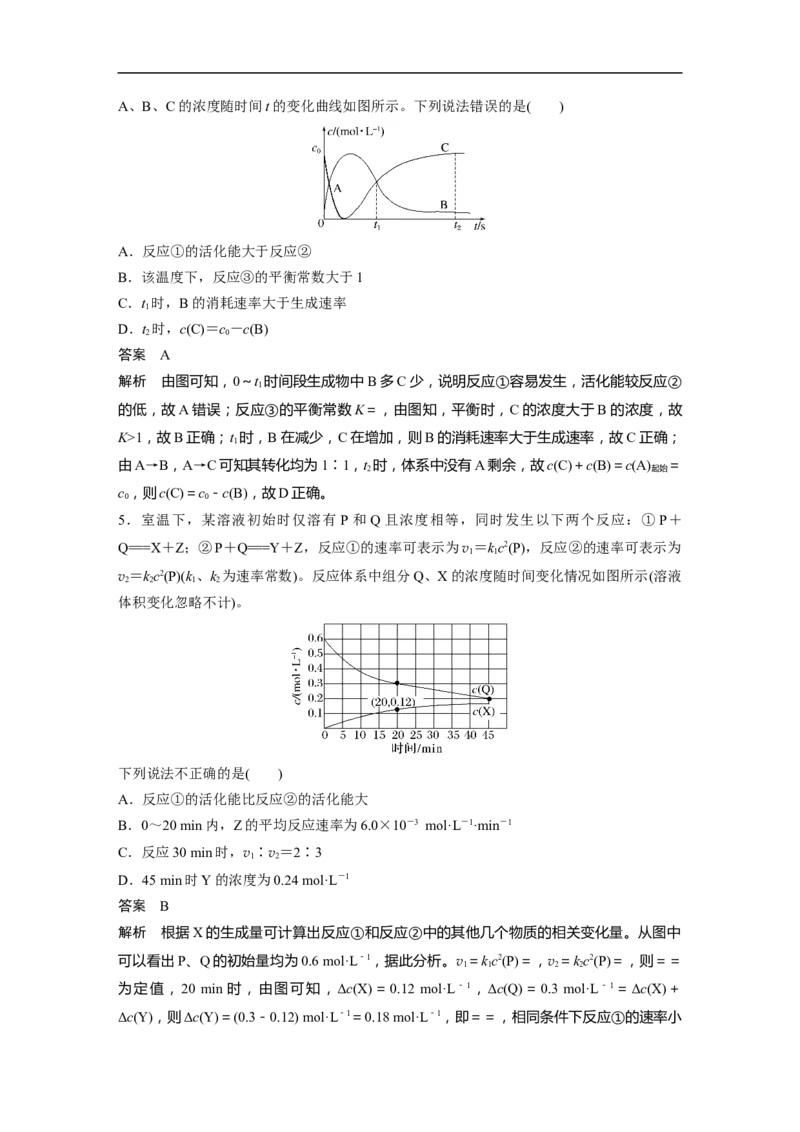
4.一定温度下向容器中加入A发生反应如下:①A→B,②A→C,③BC。反应体系中A、B、C的浓度随时间t的变化曲线如图所示。下列说法错误的是( )
A.反应①的活化能大于反应②
B.该温度下,反应③的平衡常数大于1
C.t 时,B的消耗速率大于生成速率
1
D.t 时,c(C)=c-c(B)
2 0
答案 A
解析 由图可知,0~t 时间段生成物中B多C少,说明反应①容易发生,活化能较反应②
1
的低,故A错误;反应③的平衡常数K=,由图知,平衡时,C的浓度大于B的浓度,故
K>1,故B正确;t 时,B在减少,C在增加,则B的消耗速率大于生成速率,故C正确;
1
由A→B,A→C可知其转化均为1∶1,t 时,体系中没有A剩余,故c(C)+c(B)=c(A) =
2 起始
c,则c(C)=c-c(B),故D正确。
0 0
5.室温下,某溶液初始时仅溶有 P和Q且浓度相等,同时发生以下两个反应:①P+
Q===X+Z;②P+Q===Y+Z,反应①的速率可表示为v =kc2(P),反应②的速率可表示为
1 1
v=kc2(P)(k、k 为速率常数)。反应体系中组分Q、X的浓度随时间变化情况如图所示(溶液
2 2 1 2
体积变化忽略不计)。
下列说法不正确的是( )
A.反应①的活化能比反应②的活化能大
B.0~20 min内,Z的平均反应速率为6.0×10-3 mol·L-1·min-1
C.反应30 min时,v∶v=2∶3
1 2
D.45 min时Y的浓度为0.24 mol·L-1
答案 B
解析 根据X的生成量可计算出反应①和反应②中的其他几个物质的相关变化量。从图中
可以看出P、Q的初始量均为0.6 mol·L-1,据此分析。v =kc2(P)=,v =kc2(P)=,则==
1 1 2 2
为定值,20 min 时,由图可知,Δc(X)=0.12 mol·L-1,Δc(Q)=0.3 mol·L-1=Δc(X)+
Δc(Y),则Δc(Y)=(0.3-0.12) mol·L-1=0.18 mol·L-1,即==,相同条件下反应①的速率小于反应②,所以反应①的活化能大于反应②,故A说法正确;0~20 min内,Z的变化量与
Q的变化量相同,所以Δc(Z)=Δc(Q)=0.3 mol·L-1,Z的平均反应速率为==0.015 mol·L-
1·min-1,故B说法错误;==始终为定值,即=,故C说法正确;45 min时,Q的浓度为
0.2 mol·L-1,Δc(Q)=Δc(X)+Δc(Y)=(0.6-0.2) mol·L-1=0.4 mol·L-1,根据==,可得Y
的浓度为0.24 mol·L-1,故D说法正确。
6.NO和O 混合后可发生反应:①2NO(g)+O(g)===2NO (g)、②2NO (g)NO(g),反
2 2 2 2 2 4
应体系中含氮物质的物质的量浓度(c)随着时间(t)的变化曲线如图。下列说法正确的是( )
A.c为c(NO )随t的变化曲线
2
B.t 时,c(NO)=c(N O)
1 2 4
C.t 时,c(NO)+c(NO )+c(N O)=c
2 2 2 4 0
D.t 后,NO 的消耗速率等于其生成速率
3 2
答案 D
解析 由题干信息可知,NO 和 O 混合后可发生反应:① 2NO(g)+O(g)===2NO (g)、
2 2 2
②2NO (g)NO(g),则随着反应的进行,NO 的浓度先增大后减小,最后达到平衡保持
2 2 4 2
不变,故a为c(NO)、b为c(NO )、c为c(N O)随t的变化曲线,A错误;由以上分析可知,
2 2 4
t 时,c(NO)=c(NO ),B错误;若容器的体积保持不变,则根据 N原子守恒可知,t 时有
1 2 2
c(NO)+c(NO )+2c(N O)=c ,C错误;由图像可知,t 后,NO 、NO 的浓度不再发生改
2 2 4 0 3 2 2 4
变说明反应达到平衡状态,故有NO 的消耗速率等于其生成速率,D正确。
2