文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题07
1.下列物质在熔融状态下不导电且属于电解质是
A. Cu B. AlCl C. CaCl D. SiO
3 2 2
2.下列方程式正确的是
A. 向硫化钠溶液中滴加过量HSO :2S2-+3HSO =3S↓+2SO 3HO
2 3 2 3 + 2
B. 用碳酸钠溶液处理水垢中的硫酸钙:CO CaSO=CaCO +SO
+ 4 3
C. 以铁为电极电解饱和食盐水:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2
D.FeO在空气中受热:4FeO+O===2Fe O
2 2 3
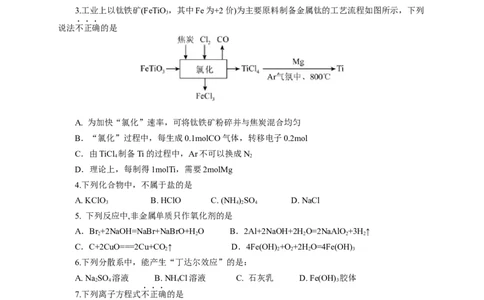
3.工业上以钛铁矿(FeTiO,其中Fe为+2价)为主要原料制备金属钛的工艺流程如图所示,下列
3
说法不正确的是
A. 为加快“氯化”速率,可将钛铁矿粉碎并与焦炭混合均匀
B.“氯化”过程中,每生成0.1molCO气体,转移电子0.2mol
C.由TiCl 制备Ti的过程中,Ar不可以换成N
4 2
D.理论上,每制得1molTi,需要2molMg
4.下列化合物中,不属于盐的是
A. KClO B. HClO C. (NH )SO D. NaCl
3 4 2 4
5. 下列反应中,非金属单质只作氧化剂的是
A.Br +2NaOH=NaBr+NaBrO+HO B.2Al+2NaOH+2H O=2NaAlO +3H ↑
2 2 2 2 2
C.C+2CuO===2Cu+CO ↑ D.4Fe(OH) +O +2H O=4Fe(OH)
2 2 2 2 3
6.下列分散系中,能产生“丁达尔效应”的是:
A. Na SO 溶液 B. NH Cl溶液 C. 石灰乳 D. Fe(OH) 胶体
2 4 4 3
7.下列离子方程式不正确的是
A.Ba(OH) 溶液中滴加NaHSO 至完全沉淀:Ba2++OH-+H++SO=BaSO ↓+H O
2 4 4 2
B.漂白粉的生产原理:2OH-+Cl=Cl-+ClO-+H O
2 2
C.MnO 与浓盐酸加热:MnO +4H++2Cl-===Mn2++Cl↑+2H O
2 2 2 2
D.AlCl 溶液加入过量的氨水:Al3++3NH·H O=Al(OH) ↓+3NH
3 3 2 3
8.关于反应2NaNH +N O=NaN +NaOH+NH ,下列说法正确的是
2 2 3 3
A.NaN 溶液通入CO 可以得到HN (酸性与醋酸相当)
3 2 3
B.氧化剂和还原剂的物质的量之比为2∶1
C.NaN 既是还原产物又是氧化产物
3D.生成1molNaN ,共转移4mol电子
3
9.下列离子方程式书写正确的是
A. 用FeS除去废水中的Hg2+:S2-+Hg2+=HgS↓
B. 向饱和食盐水中加浓盐酸析出固体:Na+(aq)+Cl-(aq) NaCl(s)
C. 在NaS溶液中滴加NaClO溶液:S2-+ClO-+2H+=S↓+Cl-+H O
2 2
D. 向血红色Fe(SCN) 溶液中加入过量铁粉至溶液褪色:2Fe3++Fe=3Fe2+
3
10. 2022年,在卡塔尔举办的世界杯备受全世界瞩目。下列说法错误的是
A. 开幕式的绚丽烟花利用的“焰色试验”是物理变化
B. 运动员需要补充的NaCl溶液是电解质
C. 制作奖杯的材料之一18K 金是合金
D. 足球赛服材料聚酯纤维属于有机高分子材料
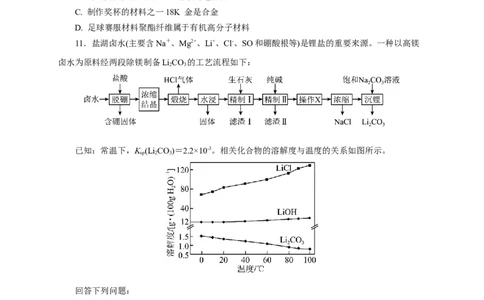
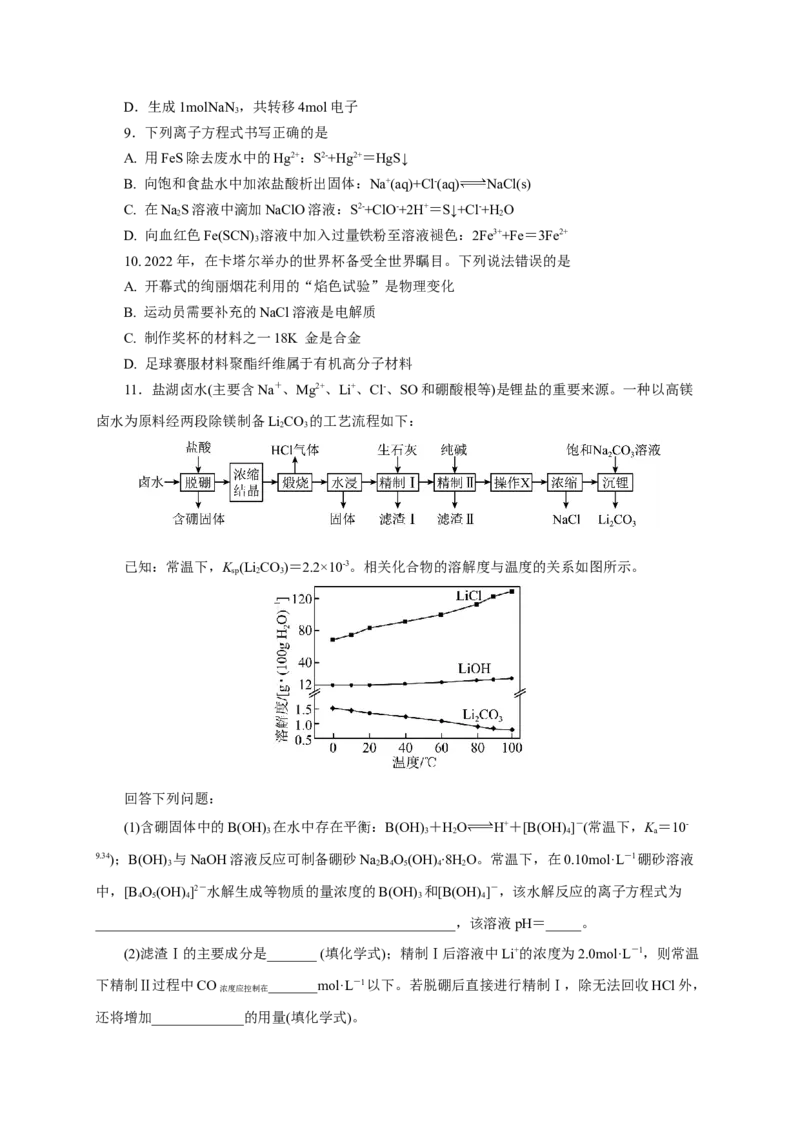
11.盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、SO和硼酸根等)是锂盐的重要来源。一种以高镁
卤水为原料经两段除镁制备LiCO 的工艺流程如下:
2 3
已知:常温下,K (Li CO)=2.2×10-3。相关化合物的溶解度与温度的关系如图所示。
sp 2 3
回答下列问题:
(1)含硼固体中的B(OH) 在水中存在平衡:B(OH) +HO H++[B(OH) ]-(常温下,K=10-
3 3 2 4 a
9.34);B(OH) 与NaOH溶液反应可制备硼砂NaB O(OH) ∙8HO。常温下,在0.10mol·L-1硼砂溶液
3 2 4 5 4 2
中,[B O(OH) ]2-水解生成等物质的量浓度的B(OH) 和[B(OH) ]-,该水解反应的离子方程式为
4 5 4 3 4
___________________________________________________,该溶液pH=_____。
(2)滤渣Ⅰ的主要成分是_______ (填化学式);精制Ⅰ后溶液中Li+的浓度为2.0mol·L-1,则常温
下精制Ⅱ过程中CO _______mol·L-1以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,
浓度应控制在
还将增加_____________的用量(填化学式)。(3)精制Ⅱ的目的是_____________________________;进行操作X时应选择的试剂是_______,
若不进行该操作而直接浓缩,将导致_____________________________。
12.实验室模拟“镁法工业烟气脱硫”并制备MgSO ∙HO,其实验过程可表示为
4 2
(1)在搅拌下向氧化镁浆料中匀速缓慢通入SO 气体,生成MgSO ,反应为Mg(OH) +HSO =
2 3 2 2 3
MgSO +2HO,其平衡常数K与K [Mg(OH) ]、K (MgSO )、K (H SO )、K (H SO )的代数关系式
3 2 sp 2 sp 3 a1 2 3 a2 2 3
为K=___________;下列实验操作一定能提高氧化镁浆料吸收SO 效率的有___________(填序号)。
2
A.水浴加热氧化镁浆料 B.加快搅拌速率
C.降低通入SO 气体的速率 D.通过多孔球泡向氧化镁浆料中通SO
2 2
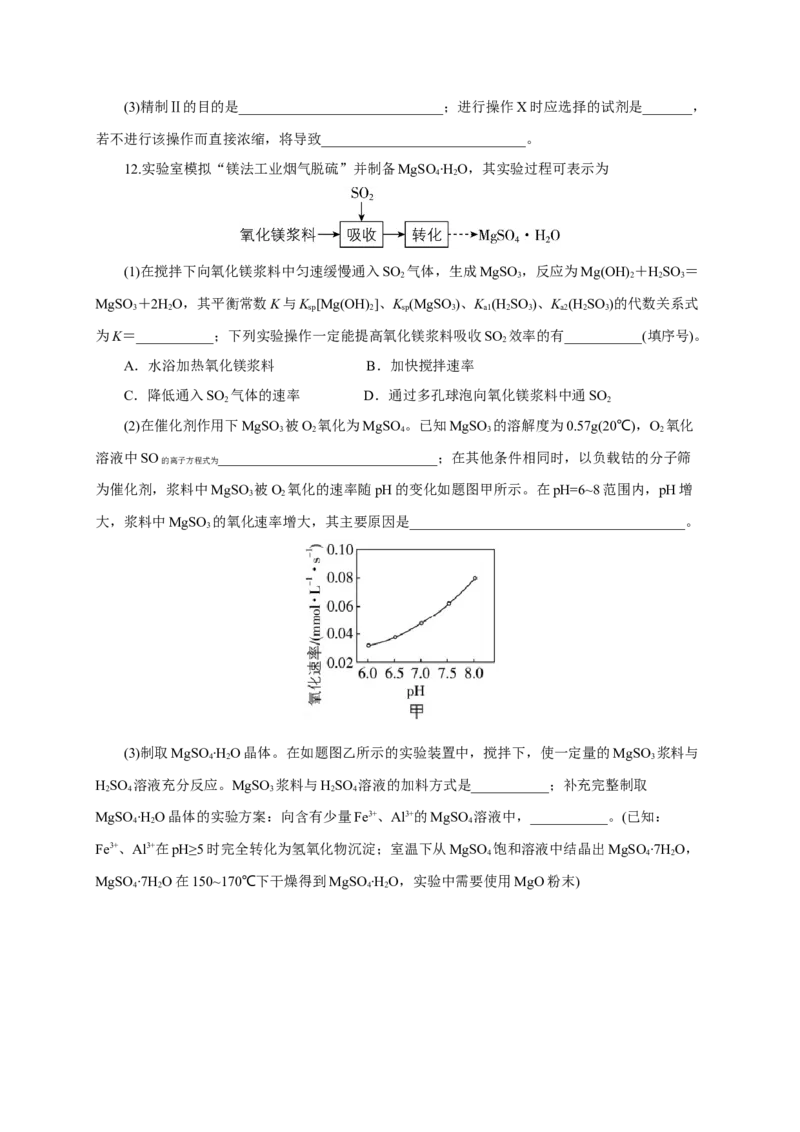
(2)在催化剂作用下MgSO 被O 氧化为MgSO 。已知MgSO 的溶解度为0.57g(20℃),O 氧化
3 2 4 3 2
溶液中SO _______________________________;在其他条件相同时,以负载钴的分子筛
的离子方程式为
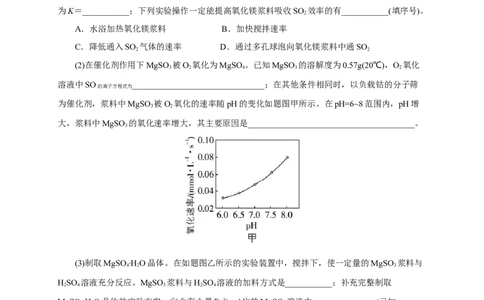
为催化剂,浆料中MgSO 被O 氧化的速率随pH的变化如题图甲所示。在pH=6~8范围内,pH增
3 2
大,浆料中MgSO 的氧化速率增大,其主要原因是_______________________________________。
3
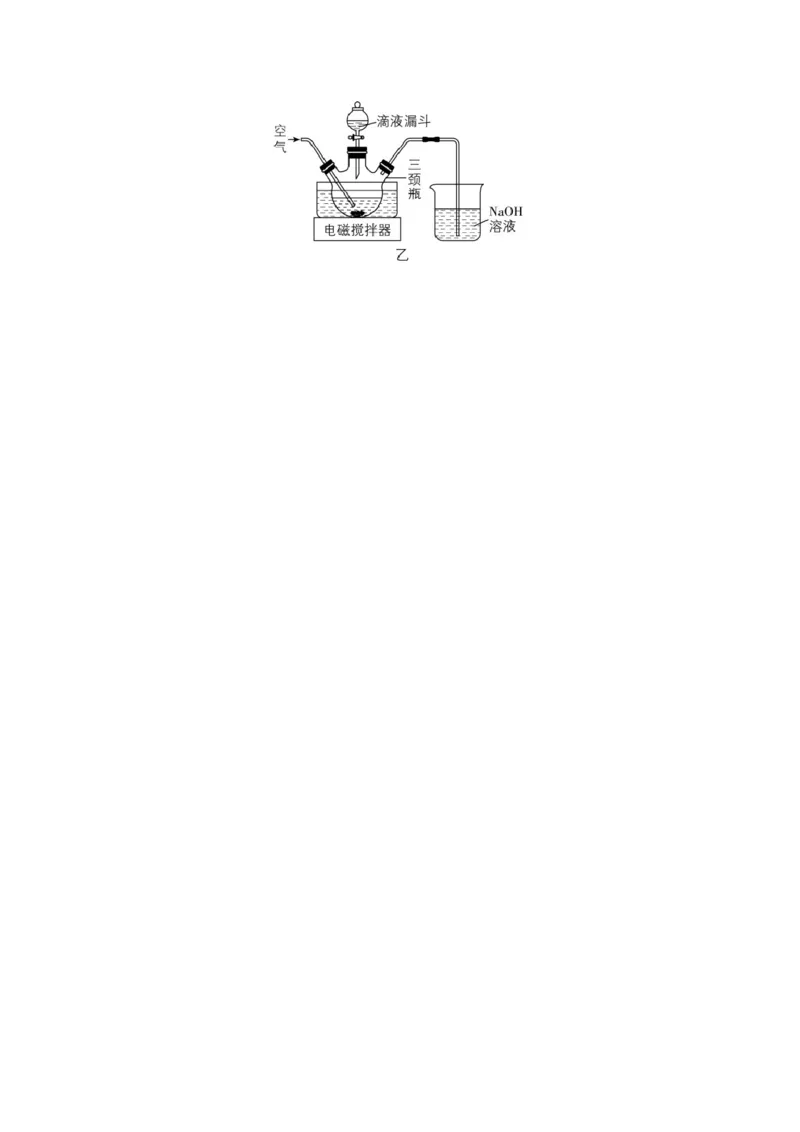
(3)制取MgSO ∙HO晶体。在如题图乙所示的实验装置中,搅拌下,使一定量的MgSO 浆料与
4 2 3
HSO 溶液充分反应。MgSO 浆料与HSO 溶液的加料方式是___________;补充完整制取
2 4 3 2 4
MgSO ∙HO晶体的实验方案:向含有少量Fe3+、Al3+的MgSO 溶液中,___________。(已知:
4 2 4
Fe3+、Al3+在pH≥5时完全转化为氢氧化物沉淀;室温下从MgSO 饱和溶液中结晶出MgSO ∙7HO,
4 4 2
MgSO ∙7HO在150~170℃下干燥得到MgSO ∙HO,实验中需要使用MgO粉末)
4 2 4 2