文档内容
2025届高三化学一轮专题复习讲义(13)
专题三 基本理论
3-6 电离和水解平衡(一)(1课时,共2课时)
【复习目标】
1.了解电离度,学会简单计算,能从定性和定量两个方面理解电离平衡常数。
2.能从图像视角判断强弱电解质在稀释、反应条件下溶液中离子浓度、导电性、电离度、pH变化
等方面的异同。
3.了解水的离子积、溶液的酸碱性、pH等概念。
4.理解盐类水解的概念、条件、本质、特点和规律,认识影响盐类水解的根本因素是内因,理解外
因对盐类水解影响的结果。
【重点突破】
1.了解中和滴定的原理及实验操作、中和滴定曲线的绘制。能用数据、图表、符号等描述实验证
据并据此进行分析推理形成结论;能对实验方案、实验过程和实验结论进行评价,提出进一
步探究的设想。
2.认识盐类的水解平衡在实际生产、生活以及实验中的应用。
【真题再现】
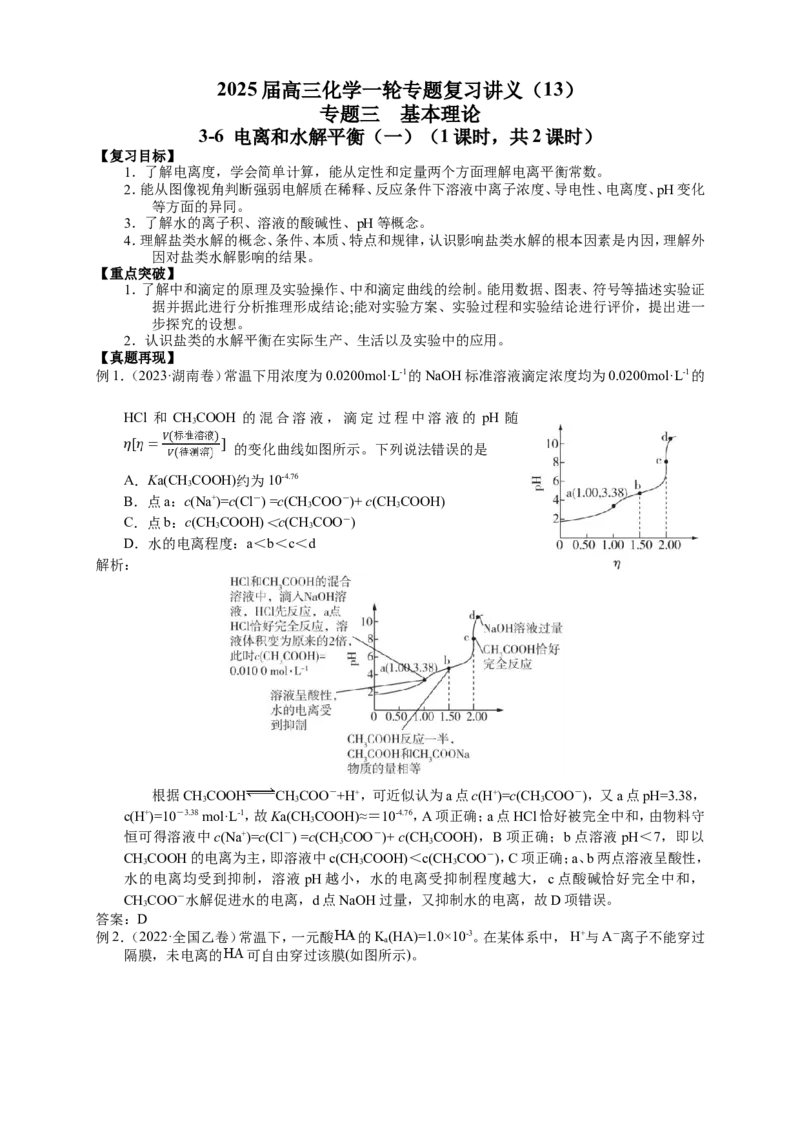
例1.(2023·湖南卷)常温下用浓度为0.0200mol·L-1的NaOH标准溶液滴定浓度均为0.0200mol·L-1的
HCl 和 CHCOOH 的混合溶液,滴定过程中溶液的 pH 随
3
的变化曲线如图所示。下列说法错误的是
A.Ka(CHCOOH)约为10-4.76
3
B.点a:c(Na+)=c(Cl-) =c(CHCOO-)+ c(CHCOOH)
3 3
C.点b:c(CHCOOH)<c(CHCOO-)
3 3
D.水的电离程度:a<b<c<d
解析:
根据CHCOOH CHCOO-+H+,可近似认为a点c(H+)=c(CHCOO-),又a点pH=3.38,
3 3 3
c(H+)=10-3.38 mol·L-1,故Ka(CHCOOH)≈=10-4.76,A项正确;a点HCl恰好被完全中和,由物料守
3
恒可得溶液中c(Na+)=c(Cl-) =c(CHCOO-)+ c(CHCOOH),B项正确;b点溶液pH<7,即以
3 3
CHCOOH的电离为主,即溶液中c(CHCOOH)<c(CHCOO-),C项正确;a、b两点溶液呈酸性,
3 3 3
水的电离均受到抑制,溶液 pH越小,水的电离受抑制程度越大,c点酸碱恰好完全中和,
CHCOO-水解促进水的电离,d点NaOH过量,又抑制水的电离,故D项错误。
3
答案:D
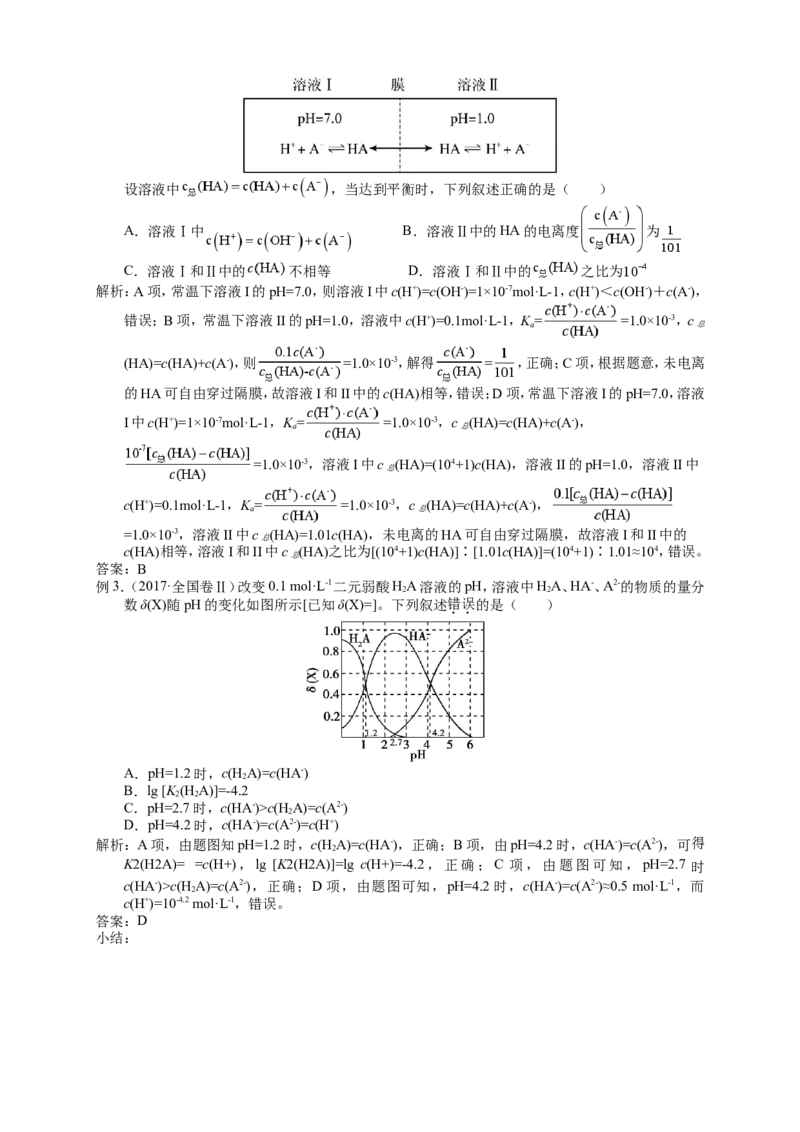
例2.(2022·全国乙卷)常温下,一元酸 的K(HA)=1.0×10-3。在某体系中, H+与A-离子不能穿过
a
隔膜,未电离的 可自由穿过该膜(如图所示)。设溶液中 ,当达到平衡时,下列叙述正确的是( )
A.溶液Ⅰ中 B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等 D.溶液Ⅰ和Ⅱ中的 之比为
解析:A项,常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol·L-1,c(H+)<c(OH-)+c(A-),
错误;B项,常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol·L-1,K = =1.0×10-3,c
a 总
(HA)=c(HA)+c(A-),则 =1.0×10-3,解得 = ,正确;C项,根据题意,未电离
的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,错误;D项,常温下溶液I的pH=7.0,溶液
I中c(H+)=1×10-7mol·L-1,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
=1.0×10-3,溶液I中c (HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中
总
c(H+)=0.1mol·L-1,K = =1.0×10-3,c (HA)=c(HA)+c(A-),
a 总
=1.0×10-3,溶液II中c (HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I和II中的
总
c(HA)相等,溶液I和II中c (HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,错误。
总
答案:B
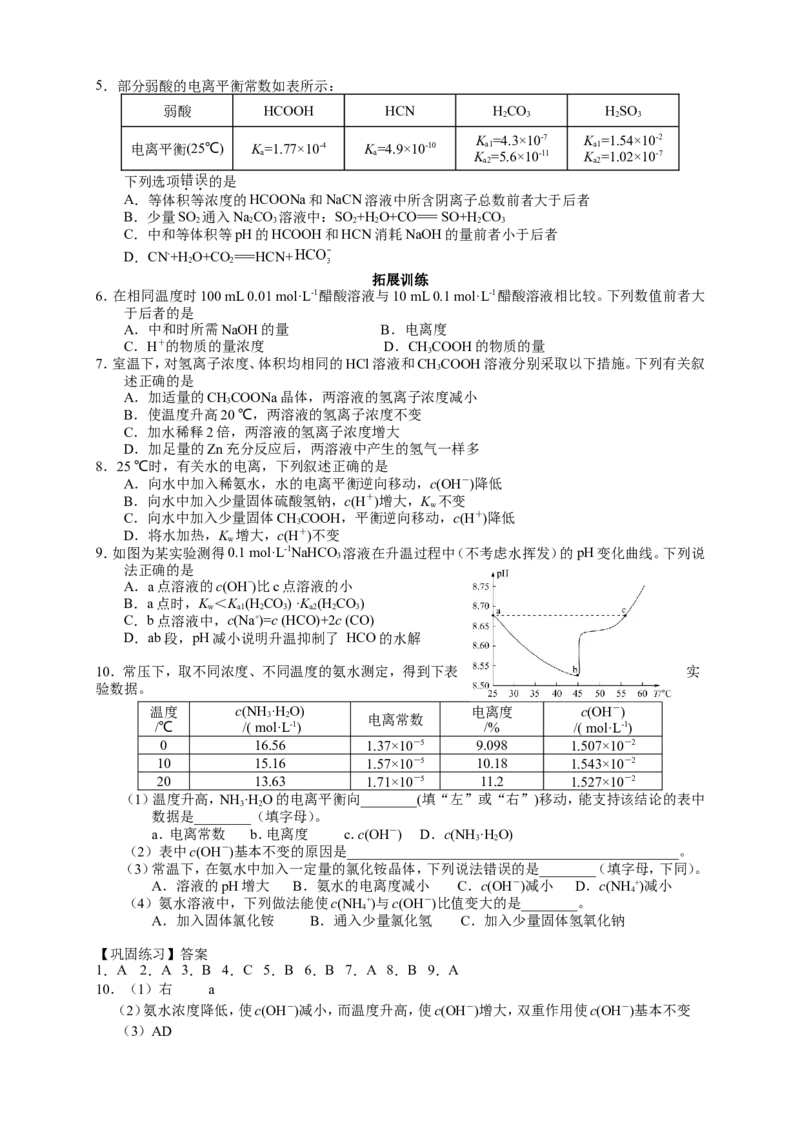
例3.(2017·全国卷Ⅱ)改变0.1 mol·L-1二元弱酸HA溶液的pH,溶液中HA、HA-、A2-的物质的量分
2 2
数δ(X)随pH的变化如图所示[已知δ(X)=]。下列叙述错误的是( )
A.pH=1.2时,c(H A)=c(HA-)
2
B.lg [K (H A)]=-4.2
2 2
C.pH=2.7时,c(HA-)>c(H A)=c(A2-)
2
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
解析:A项,由题图知pH=1.2时,c(H A)=c(HA-),正确;B项,由pH=4.2时,c(HA-)=c(A2-),可得
2
K2(H2A)= =c(H+),lg [K2(H2A)]=lg c(H+)=-4.2,正确;C 项,由题图可知,pH=2.7 时
c(HA-)>c(H A)=c(A2-),正确;D项,由题图可知,pH=4.2时,c(HA-)=c(A2-)≈0.5 mol·L-1,而
2
c(H+)=10-4.2 mol·L-1,错误。
答案:D
小结:【知能整合】
1.电离有关知识的各种判断
应用 举例
判断弱酸酸性(或弱碱碱
K(HF)>K(HClO);同浓度溶液的酸性:HF>HClO
性)的相对强弱
判断酸与盐反应是否能发
K (H CO)>K(HClO);Ca(ClO) +CO+HO===CaCO ↓+2HClO
生(强酸制弱酸) 1 2 3 2 2 2 3
判断溶液中粒子浓度比值 在NH Cl溶液中加水稀释,如何变化?分子分母同时乘以c(OH-),可
4
的变化 得,该比值只与温度有关,温度不变,比值不变
判断盐溶液的酸性(或碱 K(HF)>K(CHCOOH)[盐所对应的酸(或碱)越弱,盐水解的程度越大,盐
3
性)强弱 的碱(或酸)性越强];同浓度盐溶液的碱性:NaFK =
2 3 2 h 2
度的相对大小 4.7×10-11 ,故NaHCO 水解程度大于电离程度
3
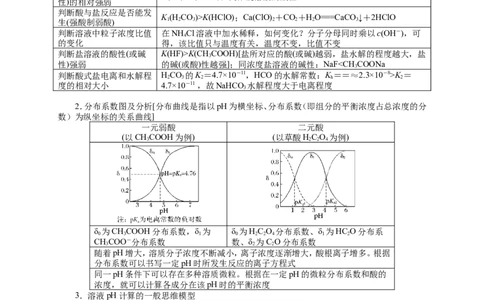
2.分布系数图及分析[分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分
数)为纵坐标的关系曲线]
一元弱酸 二元酸
(以CHCOOH为例) (以草酸HC O 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为 δ 为HC O 分布系数、δ 为HC O分布系
0 3 1 0 2 2 4 1 2
CHCOO-分布系数 数、δ 为C O分布系数
3 2 2
随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多。根据
分布系数可以书写一定pH时所发生反应的离子方程式
同一pH条件下可以存在多种溶质微粒。根据在一定pH的微粒分布系数和酸的
浓度,就可以计算各成分在该pH时的平衡浓度
3.溶液pH计算的一般思维模型4.氧化还原滴定知识与思路
(1)原理:以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴
定一些本身并没有还原性或氧化性,但能与某些还原剂或氧化剂反应的物质。
(2)试剂:常见用于滴定的氧化剂有KMnO 、KCr O 等;常见用于滴定的还原剂有亚铁盐、草酸、
4 2 2 7
维生素C等。
(3)指示剂:氧化还原滴定的指示剂有三类:a氧化还原指示剂。b专用指示剂,如在碘量法滴定
中,可溶性淀粉溶液遇碘标准溶液变蓝。c自身指示剂,如高锰酸钾标准溶液滴定草酸时,滴定终点为
溶液由无色变为浅红色。
5.一元强碱(NaOH)溶液滴定二元弱酸(H A)溶液的图像基本命题点
2
(1)图1:常考K 、K 的计算或求其数量级:根据曲线交点及对应的pH可求K 、K 。
a1 a2 a1 a2
(2)图2:常考M、N哪条线表示lg与pH或lg与pH的关系,K 、K 的计算或数量级:可根据图2
a1 a2
中所示的虚线与直线的交点来求,交点处的c(HA-)=c(H A),c(A2-)=c(HA-),再结合交点对应pH的大
2
小,可知线N表示lg,线M表示lg。利用虚线与直线交点对应的pH也可求出K 、K 或其数量级。
a1 a2
(3)图3:常考哪条线表示-lg与-lgc(HA-)或-lg 与-lg c(A2-)的关系,K 、K 的计算或数量级:可根
a1 a2
据X、Y点对应的横坐标、纵坐标的值相加之后和的大小来求。K (H A) K (H A),则X点为一级电
a1 2 a2 2
离的某一点,设X点横坐标、纵坐标值之和为x,则-lg +[-lg c(HA-)]=x,-lg =x,可得K =10-x。同理Y点
≫ a1
为二级电离的某一点,设Y点横、纵坐标值之和为y,则-lg+[-lg c(A2-)]=y,-lg=y,可得K =10-y。假设成
a2
立。
【体系再构】
【随堂反馈】
基础训练
1.在0.1 mol·L-1的CHCOOH溶液中,要促进醋酸电离且使H+浓度增大,应采取的措施是
3
A.升温 B.降温 C.加入NaOH溶液 D.加入稀盐酸
2.HS水溶液中存在电离平衡:HS H++HS-和HS- H++S2-。若向HS溶液中
2 2 2
A.加水,平衡向右移动,溶液中氢离子浓度减小
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH增大
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
3.下列说法不正确的是
A.pH>7的溶液不一定呈碱性
B.中和pH和体积均相等的氨水、NaOH溶液,所需HCl的物质的量相同
C.相同温度下,pH相等的盐酸、CHCOOH溶液中,c(OH-)相等
3
D.氨水和盐酸反应后的溶液,若溶液呈中性,则c(Cl-)=c(NH +)
4
4.室温下,下列操作可以使0.01 mol·L-1L NH ·H O溶液中c(NH +)增大的是
3 2 4
A.加入少量HO B.加入少量NaOH固体
2
C.通入少量HCl气体 D.降低温度5.部分弱酸的电离平衡常数如表所示:
弱酸 HCOOH HCN HCO HSO
2 3 2 3
K =4.3×10-7 K =1.54×10-2
电离平衡(25℃) K=1.77×10-4 K=4.9×10-10 a1 a1
a a K =5.6×10-11 K =1.02×10-7
a2 a2
下列选项错误的是
A.等体积等浓度的HCOONa和NaCN溶液中所含阴离子总数前者大于后者
B.少量SO 通入NaCO 溶液中:SO +H O+CO=== SO+H CO
2 2 3 2 2 2 3
C.中和等体积等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.CN-+H O+CO===HCN+
2 2
拓展训练
6.在相同温度时100 mL 0.01 mol·L-1醋酸溶液与10 mL 0.1 mol·L-1醋酸溶液相比较。下列数值前者大
于后者的是
A.中和时所需NaOH的量 B.电离度
C.H+的物质的量浓度 D.CHCOOH的物质的量
3
7.室温下,对氢离子浓度、体积均相同的HCl溶液和CHCOOH溶液分别采取以下措施。下列有关叙
3
述正确的是
A.加适量的CHCOONa晶体,两溶液的氢离子浓度减小
3
B.使温度升高20 ℃,两溶液的氢离子浓度不变
C.加水稀释2倍,两溶液的氢离子浓度增大
D.加足量的Zn充分反应后,两溶液中产生的氢气一样多
8.25 ℃时,有关水的电离,下列叙述正确的是
A.向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
w
C.向水中加入少量固体CHCOOH,平衡逆向移动,c(H+)降低
3
D.将水加热,K 增大,c(H+)不变
w
9.如图为某实验测得0.1 mol·L-1NaHCO 溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说
3
法正确的是
A.a点溶液的c(OH-)比c点溶液的小
B.a点时,K <K (H CO) ·K (H CO)
w a1 2 3 a2 2 3
C.b点溶液中,c(Na+)=c (HCO)+2c (CO)
D.ab段,pH减小说明升温抑制了 HCO的水解
10.常压下,取不同浓度、不同温度的氨水测定,得到下表 实
验数据。
温度 c(NH ·H O) 电离度 c(OH-)
3 2 电离常数
/℃ /( mol·L-1) /% /( mol·L-1)
0 16.56 1.37×10-5 9.098 1.507×10-2
10 15.16 1.57×10-5 10.18 1.543×10-2
20 13.63 1.71×10-5 11.2 1.527×10-2
(1)温度升高,NH ·H O的电离平衡向________(填“左”或“右”)移动,能支持该结论的表中
3 2
数据是________(填字母)。
a.电离常数 b.电离度 c.c(OH-) D.c(NH ·H O)
3 2
(2)表中c(OH-)基本不变的原因是_______________________________________________。
(3)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是________(填字母,下同)。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH +)减小
4
(4)氨水溶液中,下列做法能使c(NH +)与c(OH-)比值变大的是________。
4
A.加入固体氯化铵 B.通入少量氯化氢 C.加入少量固体氢氧化钠
【巩固练习】答案
1.A 2.A 3.B 4.C 5.B 6.B 7.A 8.B 9.A
10.(1)右 a
(2)氨水浓度降低,使c(OH-)减小,而温度升高,使c(OH-)增大,双重作用使c(OH-)基本不变
(3)AD(4)AB
【课后作业】
1.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是
A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
2.二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所示。下列叙述错误
的是
A.海水酸化能引起HCO -浓度增大、CO2-浓度减小
3 3
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为HCO - H++CO 2
2 3 3
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
3.醋酸的电离方程式为CHCOOH(aq) H+(aq)+CH COO-(aq)
3 3
ΔH>0,25℃时,0.1mol·L-1醋酸溶液中存在下述关系: ,下列说法
正确的是
A.该温度下0.01mol·L-1醋酸溶液K<1.75×10-5
a
B.升高温度,c(H+)增大,K 变大
a
C.向该溶液中滴加几滴浓盐酸,平衡逆向移动,c(H+)减小
D.向该溶液中加少量CHCOONa固体,平衡正向移动
3
4.室温条件下,现有四种溶液:①pH=2的CHCOOH溶液;②pH=2的HCl溶液;③pH=12的氨水;
3
④pH=12的NaOH溶液;⑤0.5mol·L-1的NH Cl溶液,下列有关说法正确的是
4
A.由水电离出的c(H+):⑤>①=②=③=④
B.将②、③溶液混合后,pH=7,消耗溶液的体积:②<③
C.等体积的①、②、④溶液分别与足量铝粉反应,②生成的H 的物质的量最大
2
D.向溶液中加入100mL水后,溶液的pH:③>④>①>②
5.pH=2的A、B两种酸溶液各取1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系
如图所示。下列说法不正确的是
A.稀释后X溶液的c(H+)比Y溶液小
B.a=5时,X是强酸,Y是弱酸
C.若X、Y都是弱酸,则5>a>2
D.X、Y两种酸溶液物质的量浓度一定相等
6.准确移取 20.00 mL 某待测 NaOH 溶液于锥形瓶中,用 0.1000
mol·L-1盐酸滴定。用酚酞作指示剂,下列说法错误的是
A.常温下,0.100 0 mol·L-1L盐酸pH=1
B.酸式滴定管用蒸馏水洗涤后,再用盐酸润洗
C.随着盐酸的滴入,锥形瓶中溶液pH逐渐变小
D.当滴入最后半滴盐酸时,溶液由无色变为浅红色,且30 s内不褪色,即为滴定终点
7.常温下,以酚酞作指示剂,用0.1 mol·L-1的NaOH溶液滴定20.00 mL mol·L-1的二元酸HA溶液。溶
2
液中pH、分布系数δ随滴加NaOH溶液体积V(NaOH)的变化关系如图所示。[A2−的分布系数为]下列说法正确的是 )
A.当V(NaOH)=0 mL时,c(HA-)+c(A2-)=0.2 mol·L-1
B.当V(NaOH)=20.00 mL时,c(Na+)>c(HA-)+2c(A2-)
C.常温下,A2-的水解常数值为1.0×10-12
D.当V(NaOH)=30.00 mL时,c(HA-)+c(H+)=c(A2-)+c(OH-)
8.已知25 ℃时,向0.100 mol·L-1 H PO 溶液中滴加NaOH溶液,各含磷微粒的物质的量分数随pH变
3 4
化的关系如图所示。
(1)25 ℃,pH=3时溶液中c(H PO )∶c(H PO -)=________。
3 4 2 4
(2)当溶液pH由11到14时,所发生反应的离子方程式为___________________________。
9.用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,根据实验回答问题:
(1)将准确称量好的2.0 g烧碱样品配成100 mL待测液,需要的主要玻璃仪器除量筒、烧杯、玻
璃棒外,还必须用到的仪器有__________、__________。
(2)用碱式滴定管量取10.00 mL待测液,置于锥形瓶中,同时滴加1~2滴指示剂。化学上常选用
的指示剂有酚酞或________。
(3)用0.2010 mol·L-1 标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右
手不停地摇动锥形瓶,两眼注视________________,直到滴定到终点,若选择酚酞作指示剂,
判断滴定终点的标志是________________________________________。
(4)根据下列数据,测得c(NaOH)=__________。烧碱的纯度=________。
滴定 待测液体积 标准盐酸体积/mL
次数 /mL 滴定前读数 滴定后读数
第一次 10.00 0.50 20.40
第二次 10.00 4.00 24.10
第三次 10.00 1.00 24.10
(5)以标准的盐酸溶液滴定未知浓度的氢氧化钠溶液,以下引起待测液浓度偏小的是 ___(填字
母)。
a. 读数时,滴定前平视,滴定后俯视
b. 未用待测液润洗碱式滴定管
c. 用待测液润洗锥形瓶
d. 不小心将标准液滴在锥形瓶外面
e. 滴定接近终点时,用少量蒸馏水冲洗锥形瓶内壁
【课后作业】答案
1.C 2.C 3.B 4.A 5.D 6.D 7.C
8.(1)1∶10(或0.1) (2) HPO 2-+OH-===PO3-+HO
4 4 2
9.(1)100 mL容量瓶 胶头滴管
(2)甲基橙
(3)锥形瓶中溶液颜色的变化 当滴入最后半滴盐酸时,溶液恰好由红色变为无色,且半分钟内不
复原
(4)0.4020 mol·L-1 80.4%
(5)ab