文档内容
2025届高三化学一轮专题复习讲义(17)
专题四 元素及其化合物
4-2 金属及其化合物(二、铁铜及其化合物)(1课时,共2课时)
【复习目标】
1.掌握铁、铜及其重要化合物主要性质及应用;
2.了解铁、铜及其重要化合物的制备方法;
3.掌握铁、铜及其重要化合物的转化关系;
4.理解化工流程及实验室中铁、铜及其化合物的转化原理及条件分析。
【重点突破】
1.掌握铁、铜及其重要化合物的转化关系及应用
2.精准理解铁、铜及其化合物在化工流程及实验室中转化原理和条件分析
【真题再现】
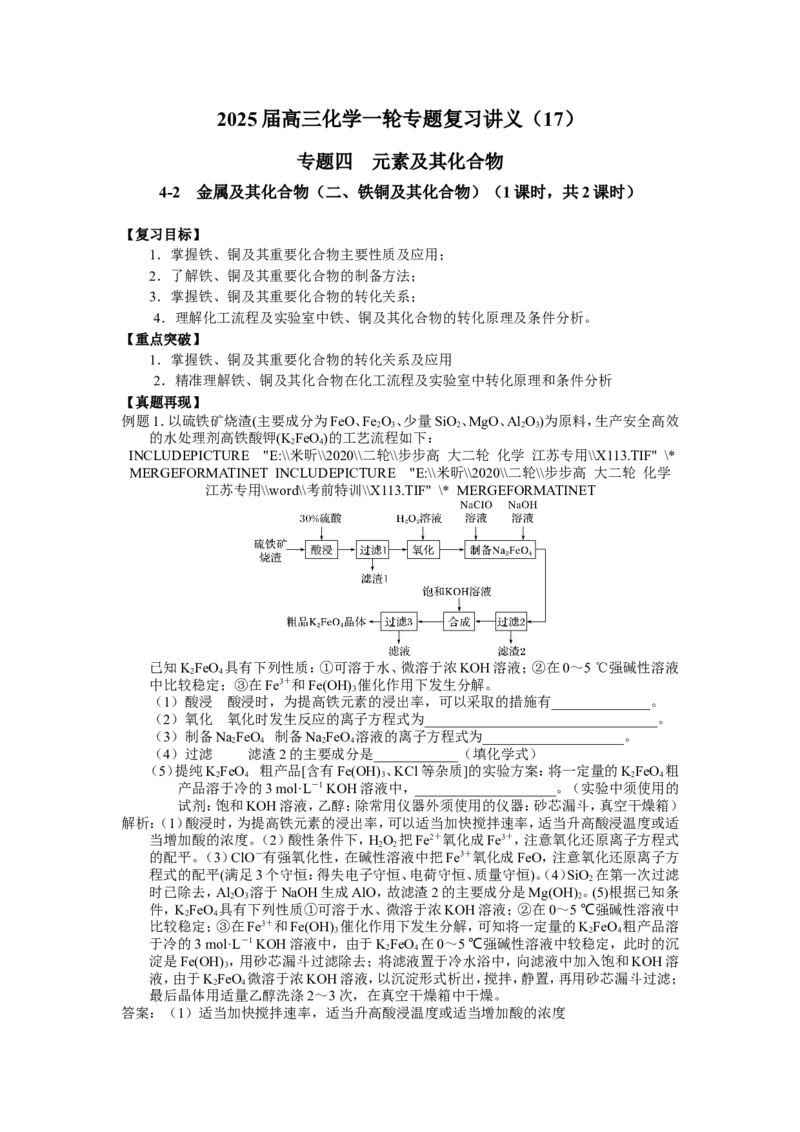
例题1.以硫铁矿烧渣(主要成分为FeO、Fe O、少量SiO、MgO、Al O)为原料,生产安全高效
2 3 2 2 3
的水处理剂高铁酸钾(K FeO)的工艺流程如下:
2 4
INCLUDEPICTURE "E:\\米昕\\2020\\二轮\\步步高 大二轮 化学 江苏专用\\X113.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\米昕\\2020\\二轮\\步步高 大二轮 化学
江苏专用\\word\\考前特训\\X113.TIF" \* MERGEFORMATINET
已知KFeO 具有下列性质:①可溶于水、微溶于浓KOH溶液;②在0~5 ℃强碱性溶液
2 4
中比较稳定;③在Fe3+和Fe(OH) 催化作用下发生分解。
3
(1)酸浸 酸浸时,为提高铁元素的浸出率,可以采取的措施有______________。
(2)氧化 氧化时发生反应的离子方程式为_________________________________。
(3)制备NaFeO 制备NaFeO 溶液的离子方程式为____________________。
2 4 2 4
(4)过滤 滤渣2的主要成分是____________(填化学式)
(5)提纯KFeO 粗产品[含有Fe(OH) 、KCl等杂质]的实验方案:将一定量的KFeO 粗
2 4 3 2 4
产品溶于冷的3 mol·L-1 KOH溶液中,____________________。(实验中须使用的
试剂:饱和KOH溶液,乙醇;除常用仪器外须使用的仪器:砂芯漏斗,真空干燥箱)
解析:(1)酸浸时,为提高铁元素的浸出率,可以适当加快搅拌速率,适当升高酸浸温度或适
当增加酸的浓度。(2)酸性条件下,HO 把Fe2+氧化成Fe3+,注意氧化还原离子方程式
2 2
的配平。(3)ClO-有强氧化性,在碱性溶液中把Fe3+氧化成FeO,注意氧化还原离子方
程式的配平(满足3个守恒:得失电子守恒、电荷守恒、质量守恒)。(4)SiO 在第一次过滤
2
时已除去,Al O 溶于NaOH生成AlO,故滤渣2的主要成分是Mg(OH) 。(5)根据已知条
2 3 2
件,KFeO 具有下列性质①可溶于水、微溶于浓KOH溶液;②在0~5 ℃强碱性溶液中
2 4
比较稳定;③在Fe3+和Fe(OH) 催化作用下发生分解,可知将一定量的KFeO 粗产品溶
3 2 4
于冷的3 mol·L-1 KOH溶液中,由于KFeO 在0~5 ℃强碱性溶液中较稳定,此时的沉
2 4
淀是Fe(OH) ,用砂芯漏斗过滤除去;将滤液置于冷水浴中,向滤液中加入饱和KOH溶
3
液,由于KFeO 微溶于浓KOH溶液,以沉淀形式析出,搅拌,静置,再用砂芯漏斗过滤;
2 4
最后晶体用适量乙醇洗涤2~3次,在真空干燥箱中干燥。
答案:(1)适当加快搅拌速率,适当升高酸浸温度或适当增加酸的浓度(2)2Fe2++2H++HO===2Fe3++2HO
2 2 2
(3)2Fe3++3ClO-+10OH-===2FeO+3Cl-+5HO
2
(4)Mg(OH)
2
(5)用砂芯漏斗过滤,将滤液置于冷水浴中,向滤液中加入饱和KOH溶液,搅拌,静
置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次,在真空干燥箱中干燥
小结:本题以硫铁矿烧渣为原料生产高铁酸钾的流程为载体,考查流程的分析,Fe、Al等元素
及其化合物的性质、获取新信息的能力、指定情境下方程式的书写。
【知能整合】
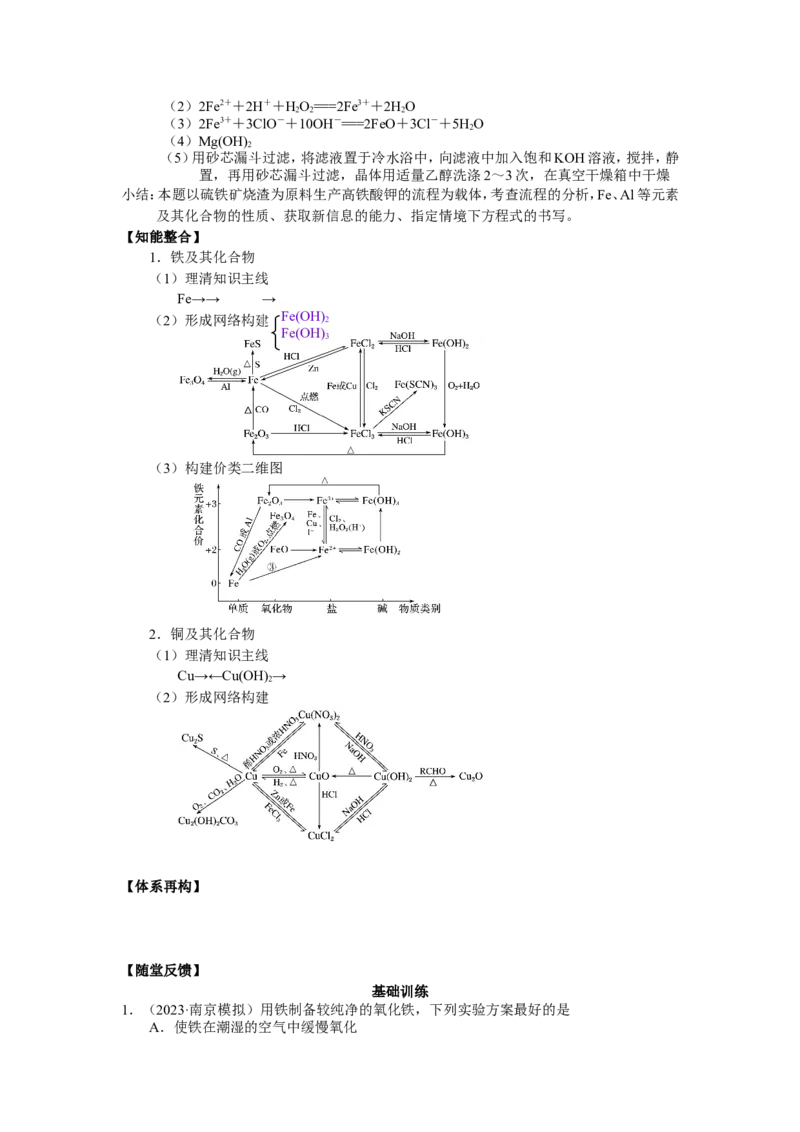
1.铁及其化合物
(1)理清知识主线
Fe→→ →
(2)形成网络构建 Fe(OH) 2
Fe(OH)
3
(3)构建价类二维图
2.铜及其化合物
(1)理清知识主线
Cu→←Cu(OH) →
2
(2)形成网络构建
【体系再构】
【随堂反馈】
基础训练
1.(2023·南京模拟)用铁制备较纯净的氧化铁,下列实验方案最好的是
A.使铁在潮湿的空气中缓慢氧化B.铁在氯气中燃烧,加水溶解,加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
C.使铁溶解于稀硫酸,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
D.使铁与足量稀硝酸反应,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解
2.FeCl 固体易潮解,在300 ℃以上可升华成含二聚三氯化铁( )分子的气体。可
3
用于金属刻蚀、污水处理等。主要有以下制备方法:
方法①:氯化法。以废铁屑和氯气为原料,在立式反应炉里反应,生成的氯化铁蒸气和尾
气由反应炉的顶部排出,进入捕集器冷凝为固体结晶。
方法②:熔融法。将铁屑和干燥氯气在低共熔混合物(如30% KCl与70% FeCl 混合)内
3
进行反应生成氯化铁,升华后收集在冷凝室中,该法制得的氯化铁纯度高。
方法③:复分解法。用氧化铁与盐酸反应后得到氯化铁溶液。
方法④:氯化亚铁合成法。将铁屑溶于盐酸中,然后向其中通入氯气得氯化铁。
下列说法正确的是
A.二聚三氯化铁分子中含有配位键
B.将FeCl 饱和溶液缓慢滴入氢氧化钠溶液中,可制取Fe(OH) 胶体
3 3
C.直接加热蒸干方法③所得的氯化铁溶液制备无水氯化铁
D.向方法④所得的溶液中加入KSCN溶液与氯气,检验该溶液中是否含有Fe2+
3.由铁及其化合物可制得FeSO ·7H O、FeCl 、KFeO 等化工产品,它们在生产、生活中具有
4 2 3 2 4
广泛应用。已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)(H O) ]SO 。高炉炼铁的反
4 2 5 4
应为Fe O(s)+3CO(g)===2Fe(s)+3CO(g) ΔH=-23.5 kJ·mol-1。在给定条件下,下列
2 3 2
选项所示的物质间转化均能实现的是
A.Fe O(s)―――→FeCl (aq)――→Fe(s)
2 3 3
B.FeS――→SO ――→HSO
2 2 2 3
C.Fe O―――→FeCl (aq)――→无水FeCl
2 3 3 3
D.Fe―――→FeCl (aq)――――→Fe(OH) ―――→Fe(OH)
2 2 3
拓展训练
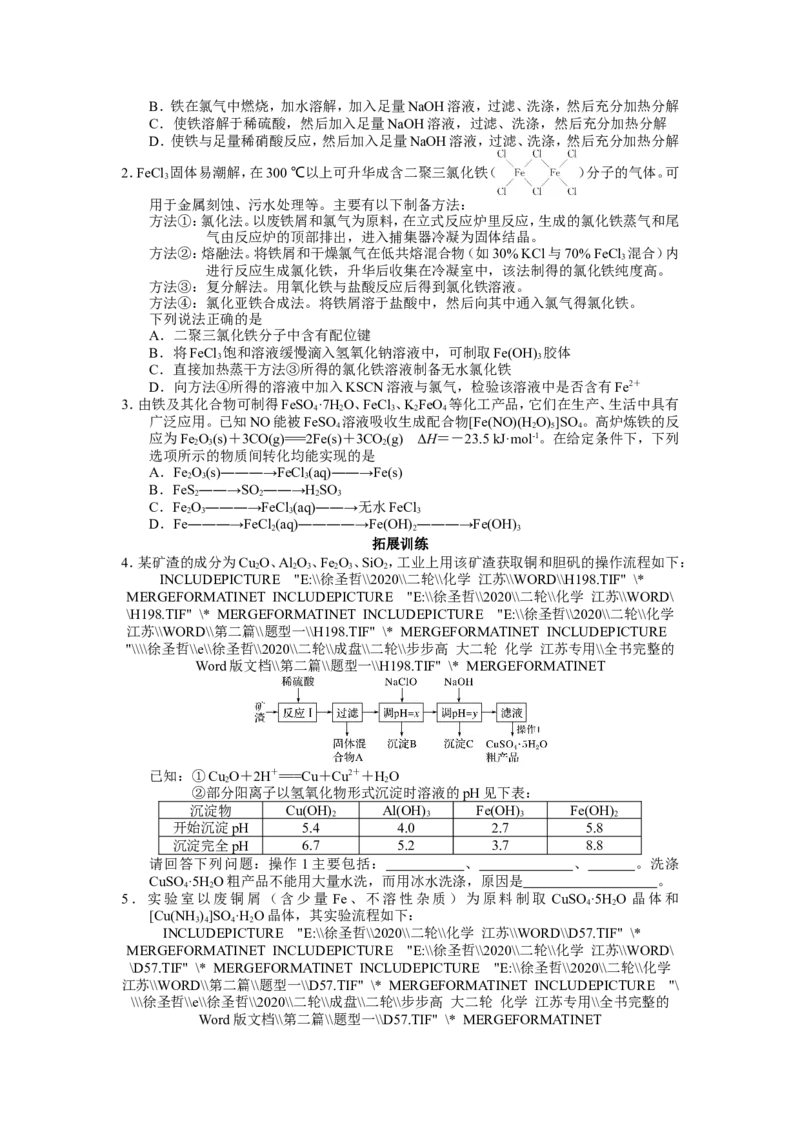
4.某矿渣的成分为Cu O、Al O、Fe O、SiO,工业上用该矿渣获取铜和胆矾的操作流程如下:
2 2 3 2 3 2
INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\H198.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\
\H198.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学
江苏\\WORD\\第二篇\\题型一\\H198.TIF" \* MERGEFORMATINET INCLUDEPICTURE
"\\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化学 江苏专用\\全书完整的
Word版文档\\第二篇\\题型一\\H198.TIF" \* MERGEFORMATINET
已知:①Cu O+2H+===Cu+Cu2++HO
2 2
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Cu(OH) Al(OH) Fe(OH) Fe(OH)
2 3 3 2
开始沉淀pH 5.4 4.0 2.7 5.8
沉淀完全pH 6.7 5.2 3.7 8.8
请回答下列问题:操作1主要包括: 、 、 。洗涤
CuSO ·5H O粗产品不能用大量水洗,而用冰水洗涤,原因是 。
4 2
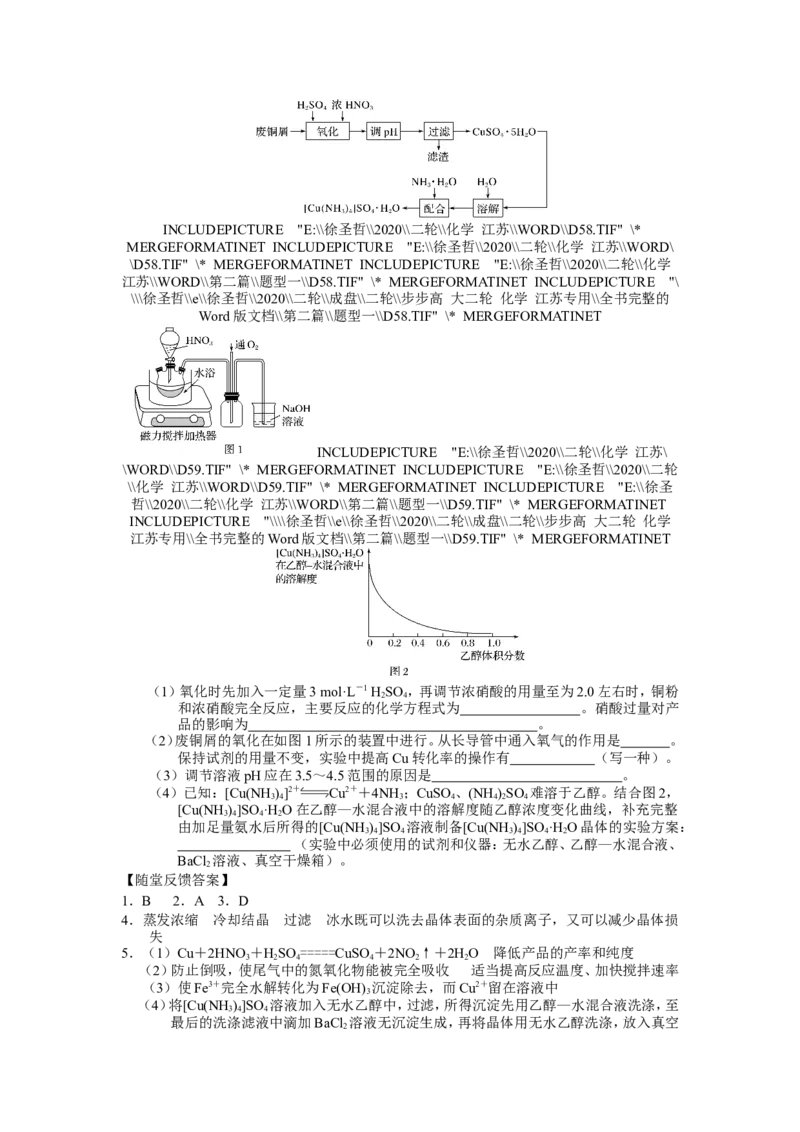
5.实验室以废铜屑(含少量 Fe、不溶性杂质)为原料制取 CuSO ·5H O 晶体和
4 2
[Cu(NH )]SO ·H O晶体,其实验流程如下:
3 4 4 2
INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\D57.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\
\D57.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学
江苏\\WORD\\第二篇\\题型一\\D57.TIF" \* MERGEFORMATINET INCLUDEPICTURE "\
\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化学 江苏专用\\全书完整的
Word版文档\\第二篇\\题型一\\D57.TIF" \* MERGEFORMATINETINCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\D58.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\
\D58.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学
江苏\\WORD\\第二篇\\题型一\\D58.TIF" \* MERGEFORMATINET INCLUDEPICTURE "\
\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化学 江苏专用\\全书完整的
Word版文档\\第二篇\\题型一\\D58.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\
\WORD\\D59.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮
\\化学 江苏\\WORD\\D59.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣
哲\\2020\\二轮\\化学 江苏\\WORD\\第二篇\\题型一\\D59.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "\\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化学
江苏专用\\全书完整的Word版文档\\第二篇\\题型一\\D59.TIF" \* MERGEFORMATINET
(1)氧化时先加入一定量3 mol·L-1 H SO ,再调节浓硝酸的用量至为2.0左右时,铜粉
2 4
和浓硝酸完全反应,主要反应的化学方程式为 。硝酸过量对产
品的影响为 。
(2)废铜屑的氧化在如图1所示的装置中进行。从长导管中通入氧气的作用是 。
保持试剂的用量不变,实验中提高Cu转化率的操作有 (写一种)。
(3)调节溶液pH应在3.5~4.5范围的原因是 。
(4)已知:[Cu(NH )]2+ Cu2++4NH ;CuSO 、(NH )SO 难溶于乙醇。结合图2,
3 4 3 4 4 2 4
[Cu(NH )]SO ·H O在乙醇—水混合液中的溶解度随乙醇浓度变化曲线,补充完整
3 4 4 2
由加足量氨水后所得的[Cu(NH )]SO 溶液制备[Cu(NH )]SO ·H O晶体的实验方案:
3 4 4 3 4 4 2
(实验中必须使用的试剂和仪器:无水乙醇、乙醇—水混合液、
BaCl 溶液、真空干燥箱)。
2
【随堂反馈答案】
1.B 2.A 3.D
4.蒸发浓缩 冷却结晶 过滤 冰水既可以洗去晶体表面的杂质离子,又可以减少晶体损
失
5.(1)Cu+2HNO+HSO =====CuSO +2NO ↑+2HO 降低产品的产率和纯度
3 2 4 4 2 2
(2)防止倒吸,使尾气中的氮氧化物能被完全吸收 适当提高反应温度、加快搅拌速率
(3)使Fe3+完全水解转化为Fe(OH) 沉淀除去,而Cu2+留在溶液中
3
(4)将[Cu(NH )]SO 溶液加入无水乙醇中,过滤,所得沉淀先用乙醇—水混合液洗涤,至
3 4 4
最后的洗涤滤液中滴加BaCl 溶液无沉淀生成,再将晶体用无水乙醇洗涤,放入真空
2干燥箱中干燥
【课后作业】
为
1.氯化亚铜,化学式CuCl或Cu Cl。 白色立方结晶或白色粉末,微溶于水,溶于浓盐酸生
2 2
成氯化亚铜酸(HCuCl 强酸),溶于氨水生成氯化二氨合亚铜,不溶于乙醇。
2
实验室制备氯化亚铜:
方法1:CuCl 溶于浓盐酸,加入铜屑并加热,生成HCuCl 溶液,加水稀释可得CuCl沉淀;
2 2
方法2:向含有铜丝、氯化铵、盐酸的溶液中加入硝酸作催化剂,通入氧气并加热,将反
应得到的NH [CuCl ]用大量的水稀释可得CuCl沉淀。
4 2
工业制法:向CuSO 和NaCl的混合溶液中加入Fe粉或通入SO ,充分反应后再用大量
4 2
的水稀释,过滤、酒精洗涤、真空干燥。
下列说法不正确的是
A.方法2中生成NH [CuCl ],1mol[CuCl ]-含σ键数2mol
4 2 2
B.方法2中制备1molCuCl,参加反应氧气的体积为5.6L
C.[CuCl ]-(aq) CuCl(s)+Cl-(aq),加水稀释,有利于CuCl沉淀生成
2
D.用酒精洗涤CuCl沉淀,真空干燥可有效防止CuCl被空气中氧气氧化
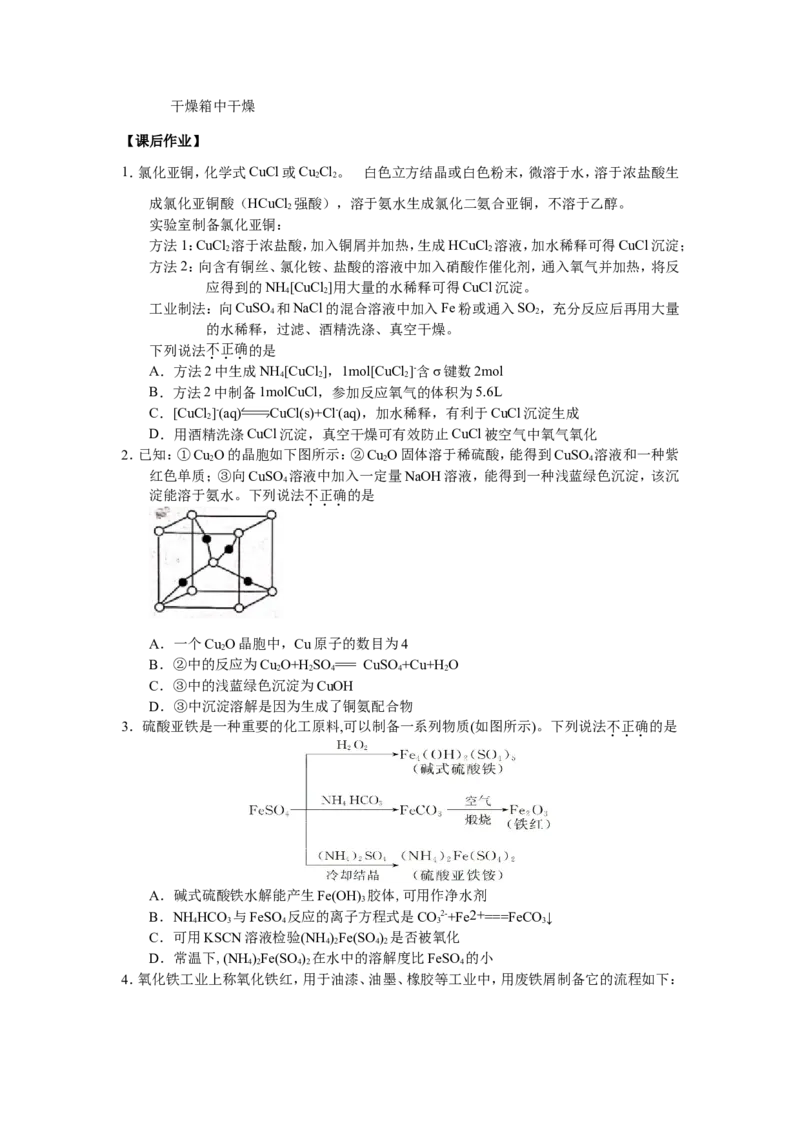
2.已知:①CuO的晶胞如下图所示:②CuO固体溶于稀硫酸,能得到CuSO 溶液和一种紫
2 2 4
红色单质;③向CuSO 溶液中加入一定量NaOH溶液,能得到一种浅蓝绿色沉淀,该沉
4
淀能溶于氨水。下列说法不正确的是
A.一个CuO晶胞中,Cu原子的数目为4
2
B.②中的反应为CuO+HSO === CuSO +Cu+H O
2 2 4 4 2
C.③中的浅蓝绿色沉淀为CuOH
D.③中沉淀溶解是因为生成了铜氨配合物
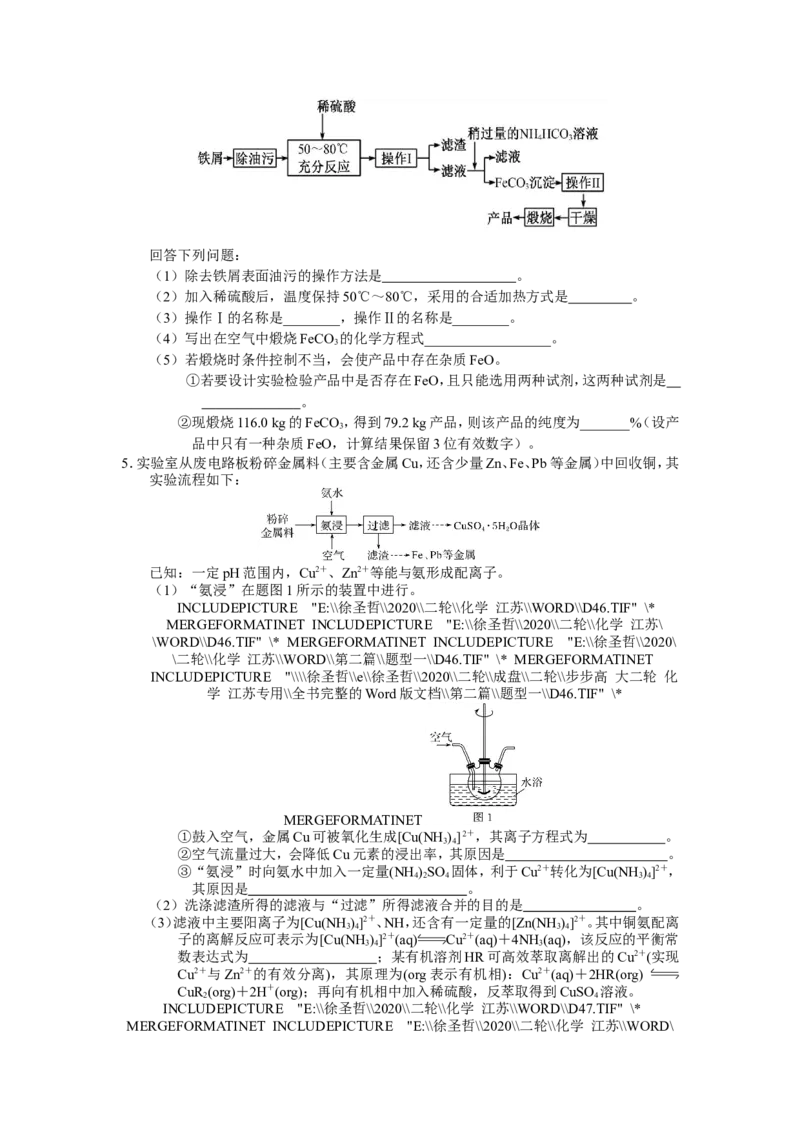
3.硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法不正确的是
A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用作净水剂
3
B.NH HCO 与FeSO 反应的离子方程式是CO2-+Fe2+===FeCO ↓
4 3 4 3 3
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.常温下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的小
4 2 4 2 4
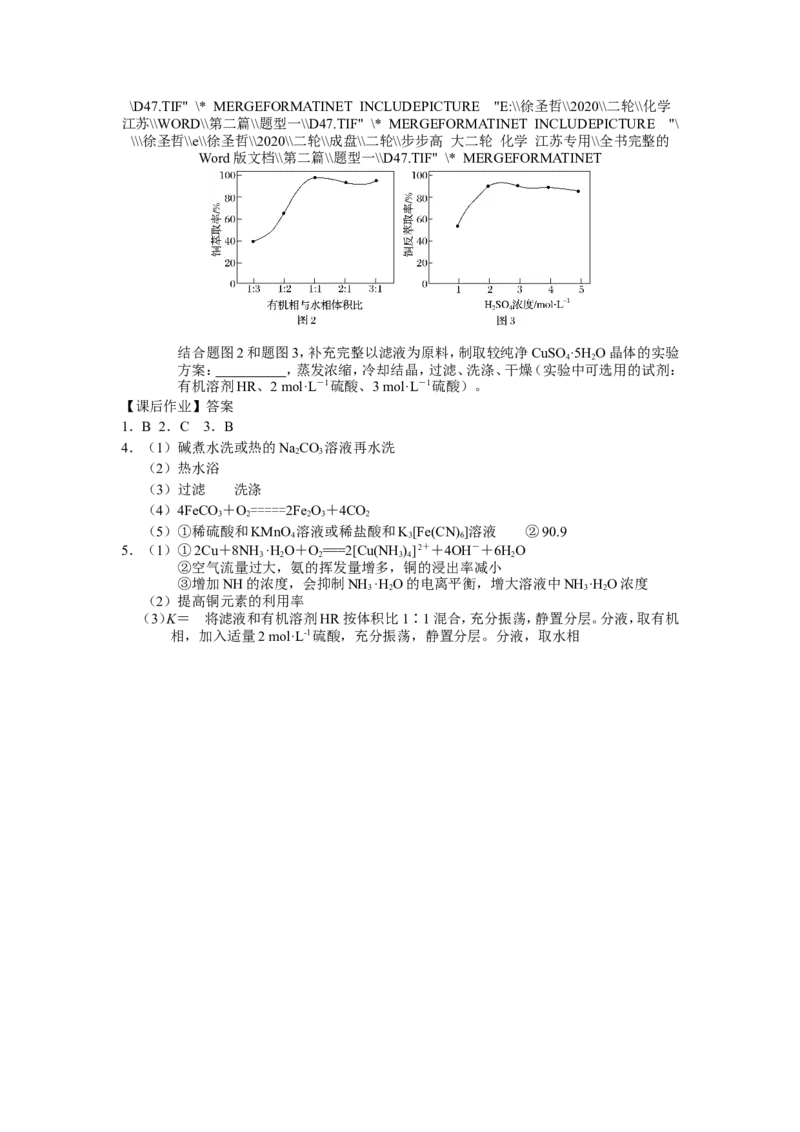
4.氧化铁工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,用废铁屑制备它的流程如下:回答下列问题:
(1)除去铁屑表面油污的操作方法是 。
(2)加入稀硫酸后,温度保持50℃~80℃,采用的合适加热方式是 。
(3)操作Ⅰ的名称是________,操作Ⅱ的名称是________。
(4)写出在空气中煅烧FeCO 的化学方程式__________________。
3
(5)若煅烧时条件控制不当,会使产品中存在杂质FeO。
①若要设计实验检验产品中是否存在FeO,且只能选用两种试剂,这两种试剂是
。
②现煅烧116.0 kg的FeCO,得到79.2 kg产品,则该产品的纯度为_______%(设产
3
品中只有一种杂质FeO,计算结果保留3位有效数字)。
5.实验室从废电路板粉碎金属料(主要含金属Cu,还含少量Zn、Fe、Pb等金属)中回收铜,其
实验流程如下:
已知:一定pH范围内,Cu2+、Zn2+等能与氨形成配离子。
(1)“氨浸”在题图1所示的装置中进行。
INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\D46.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\
\WORD\\D46.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\
\二轮\\化学 江苏\\WORD\\第二篇\\题型一\\D46.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "\\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化
学 江苏专用\\全书完整的Word版文档\\第二篇\\题型一\\D46.TIF" \*
MERGEFORMATINET
①鼓入空气,金属Cu可被氧化生成[Cu(NH )] 2+,其离子方程式为 。
3 4
②空气流量过大,会降低Cu元素的浸出率,其原因是 。
③“氨浸”时向氨水中加入一定量(NH )SO 固体,利于Cu2+转化为[Cu(NH )]2+,
4 2 4 3 4
其原因是 。
(2)洗涤滤渣所得的滤液与“过滤”所得滤液合并的目的是 。
(3)滤液中主要阳离子为[Cu(NH )]2+、NH,还含有一定量的[Zn(NH )]2+。其中铜氨配离
3 4 3 4
子的离解反应可表示为[Cu(NH )]2+(aq) Cu2+(aq)+4NH (aq),该反应的平衡常
3 4 3
数表达式为 ;某有机溶剂HR可高效萃取离解出的Cu2+(实现
Cu2+与Zn2+的有效分离),其原理为(org表示有机相):Cu2+(aq)+2HR(org)
CuR (org)+2H+(org);再向有机相中加入稀硫酸,反萃取得到CuSO 溶液。
2 4
INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\D47.TIF" \*
MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学 江苏\\WORD\\D47.TIF" \* MERGEFORMATINET INCLUDEPICTURE "E:\\徐圣哲\\2020\\二轮\\化学
江苏\\WORD\\第二篇\\题型一\\D47.TIF" \* MERGEFORMATINET INCLUDEPICTURE "\
\\\徐圣哲\\e\\徐圣哲\\2020\\二轮\\成盘\\二轮\\步步高 大二轮 化学 江苏专用\\全书完整的
Word版文档\\第二篇\\题型一\\D47.TIF" \* MERGEFORMATINET
结合题图2和题图3,补充完整以滤液为原料,制取较纯净CuSO ·5H O晶体的实验
4 2
方案: ,蒸发浓缩,冷却结晶,过滤、洗涤、干燥(实验中可选用的试剂:
有机溶剂HR、2 mol·L-1硫酸、3 mol·L-1硫酸)。
【课后作业】答案
1.B 2.C 3.B
4.(1)碱煮水洗或热的NaCO 溶液再水洗
2 3
(2)热水浴
(3)过滤 洗涤
(4)4FeCO+O=====2Fe O+4CO
3 2 2 3 2
(5)①稀硫酸和KMnO 溶液或稀盐酸和K[Fe(CN) ]溶液 ②90.9
4 3 6
5.(1)①2Cu+8NH ·H O+O===2[Cu(NH )] 2++4OH-+6HO
3 2 2 3 4 2
②空气流量过大,氨的挥发量增多,铜的浸出率减小
③增加NH的浓度,会抑制NH ·H O的电离平衡,增大溶液中NH ·H O浓度
3 2 3 2
(2)提高铜元素的利用率
(3)K= 将滤液和有机溶剂HR按体积比1∶1混合,充分振荡,静置分层。分液,取有机
相,加入适量2 mol·L-1硫酸,充分振荡,静置分层。分液,取水相